Chẳng bao lâu sau khi phát hiện ra kháng thể, người ta đã nhận thấy rằng, khả năng của kháng thể trong việc bất hoạt vật lạ còn phụ thuộc vào một yếu tố phối hợp khác, đó là bổ thể. Bổ thể bao gồm một nhóm protein mà phần lớn là các proteinase. Hệ thống enzym này hỗ trợ một cách không đặc hiệu của kháng thể trong việc opsonin hóa và ly giải các tế bào đích. Tuy nhiên, hiểu biết ban đầu này về sau đã được bổ sung với những kiến thức hiện đại về chức năng sinh học của bổ thể. Hiện nay người ta thấy bổ thể thực hiện ba chức năng sau đây:
Hoạt hóa tế bào.
Ly giải tế bào.
Opsonin hóa: chuẩn bị tế bào đích điều kiện thích hợp cho việc thực bằng cách giúp đỡ tế bào thực hành bám dính tốt vào tế bào đích.
Các protein của hệ thống bổ thể tạo thành hai chuỗi enzym mà người ta gọi là con đường cổ điển và con đường không cổ điển để tạo nên hai cách phân cách hai phân tử C3 tức phân tử trung tâm của hệ thống bổ thể. Giai đoạn cuối của hai con đườ ng này giống nhau, đó là tạo ra phức hợp protein huyết thanh gắn được lên tế bào đích, gây tổn thương màng dẫn đến hủy hoại tế bào đích.
Con đường hoạt hóa cổ điển (classical pathway)
Quá trình enzym và tấn công màng dẫn đến giết chết tế bào. Đơn vị nhận diện bổ thể hoạt động của con đường này có thể chia làm ba giai đoạn: nhận dạng, hoạt hóa là phức hợp C1.
Cố định c1 bởi immunoglobulin
Cố định C1 xảy ra khi tiểu đơn vị C1q gắn trực tiếp lên Ig. Hai tiểu đơn vị còn lại của C1 là Clr và Cls không kiên kết với Ig mà tham gia vào quá trình hoạt hóa cổ điển về sau. Phân tử kháng thể sau khi kết hợp với kháng nguyên tương ứng sẽ bị thay đổi cấu trúc không gian làm lộ các thụ thể đối với C1q. Tính chất kết hợp của bổ thể vào phức hợp kháng nguyên – kháng thể là cơ sở của phản ứng cố định bổ thể mà chúng ta thường hay sử dụng trong các xét nghiệm miễn dịch học.
Không phải tất cả các Ig có khả năng kết hợp với bổ thể. Ở người chỉ có IgG1, IgG3, và IgM là có khả năng này; ở chuột nhắt có IGg2 và IgM, và chuột lang có IgG2, .v.v. Cấu hình không gian của phức hợp kháng nguyên – kháng thể cũng có ảnh hưởng đến khả năng cố định bổ thể. Nhưng cụ thể thì chưa được biết rõ.
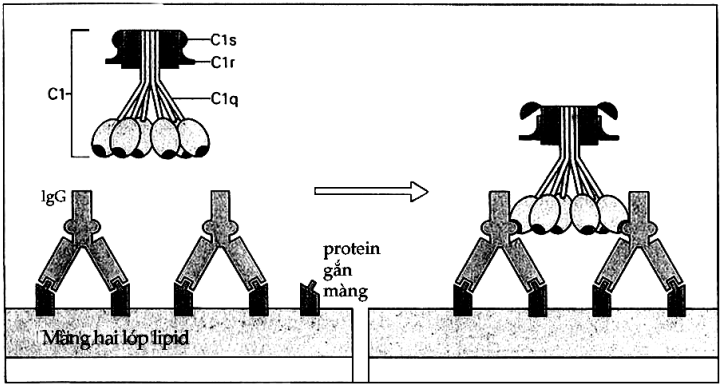
Một phân tử IgM pentamer kết hợp với kháng nguyên là có thể cố định bổ thể nhưng đối với IgG thì phải có phân tử IgG được gắn với kháng nguyên ở vị trí gần nhau mới có thể cố định được bổ thể (Hình 6.1). Để đạt được điều này trong thực nghiệm đối với hồng cầu cừu, người ta tính ra phải cần đến 600-800 phân tử IgG gắn lên hồng cầu. Do đó mà người ta thường dùng IgM hơn. Vị trí gắn của bổ thể vào Ig là lĩnh vực CH2 của IgG và CH4 của IgM. Sau khi C1q đã kết hợp với kháng thể, sự hoạt hóa sẽ đựơc truyền sang C1r và Cls. Cơ chế C1q hoạt hóa C1r vẫn còn chưa được biết. C1s sau khi được hoạt hóa C4 và C2 là hai thành phần tiếp theo của chuỗi phản ứng.
Hình 6.1. Cố định C1qrs
Một cặp phân tử IgG liên kết với các phân tử protein kháng nguyên (protein gắn màng). Mảnh C1 cố định các lĩnh vực CH2 c ủa IgG. Sự hoạt hóa C1r và C1s là do phân cắt nội bộ và do sự biến đổi của thành phần C1q tạo nên.
Cố định và hoạt hóa c4 và c2 bởi phức hợp c1qrs
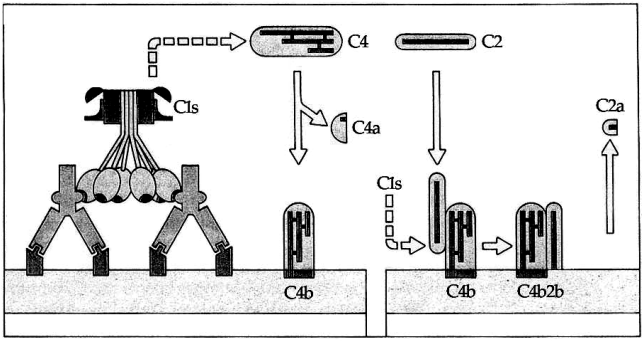
Hình 6.2. Sự hình thành C4b2b
C1s cắt C4 tạo ra C4a và C4b. C4b gắn vào màng tế bào. C2 huyết thanh đến gắn vào C4b và bị C1s cắt để giải phóng C2a. C4b2b chính là enzym cắt C3 của con đường hoạt hóa cổ điển.
Phân tử C1s sau khi được hoạt hóa nó trở thành một enzym và cắt phân tử C4 thành hai mảnh: mảnh nhỏ là C4a và mảnh lớn C4b. Mảnh C4b có một vị trí hoạt động giúp nó gắn lên thụ thể dành cho nó trên bề mặt một số tế bào. Chúng ta cần lưu ý rằng mảnh C4b không nhất thiết chỉ nằm chung quanh nơi nó được hình thành mà nó thể vào máu tuần hoàn và được lưu động, tuy nhiên khi nó vào tuần hoàn thì trở nên bị bất hoạt. Phần C4b còn lại tại chäù ( khoảng 10%) sẽ gắn lên tế bào.
C1s có tác dụng rất yếu lên C2 tự do, nhưng khi C2 tạo phức hợp với C4b thì tác dụng này mạnh hơn nhiều. Sự hấp thụ C2 lên C4b chỉ xảy ra trong điều kiện có mặt ion Mg++. C2 sẽ bị cắt làm hai mảnh, mảnh nhỏ C2a sẽ bị mất vào môi trường chung quanh còn mảnh lớn C2b thì vẫn còn bám trên C4b tạo thành phức hợp C4b2b có tính enzym không bền vững, có thời gian nửa đời sống ngắn (5 phút) vì mảnh C2b dễ bị hủy hoại hoặc tách rời khỏi C4b (Hình 6.2).
Tác động của c4b2b lên c3
Phức hợp C4b2b hoạt hóa phân tử C3 bằng cách cắt phân tử này thành hai mảnh C3a và C3b. Mảnh C3a có trọng lượng phân tử thấp, được giải phóng vào trong dịch cơ thể và có hoạt tính của một hóa chất trung gian của phản viêm. Mảnh lớn của C3b có trọng lượng phân tử khoảng 175.000 kD và có khả năng dính lên bề mặt tế bào. Tuy nhiên, chỉ có tỷ lệ nhỏ C3b dính được vào màng tế bào ở vị trí sát với phức hợp enzym C4b2b để tạo phức hợp C4b2b3b có diện tác dụng nằm trên mảnh C3b. Các phân tử C3b bám vào màng tế bào ở các vị trí xa C4b2b thì chỉ có vai trò giúp cho việc kết dính miễn dịch và làm dễ hiện tượng thực bào nhờ vào đầu kia gắn lên thụ thể dành cho C3 ở các thực bào (Hình 6.3).
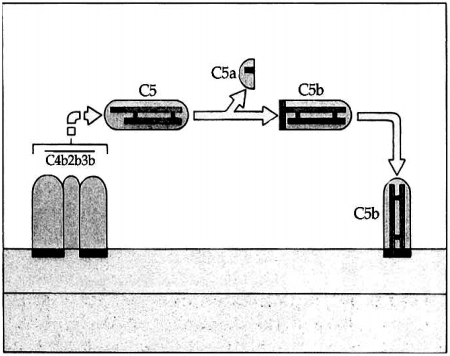
Hình 6.3. Cố định C5
C4b2b3b tách mảnh C5a từ chuỗi α của C5 ra. Mảnh còn lại là C5b sau đó gắn vào màng tế vào.
Tác động của c3b lên c5
Phức hợp C4b2b3b mà diện tác dụng là C3b cắt phân tử C5 thành ra hai mảnh. Mảnh C5a là mảnh nhỏ cũng được giải phóng vào dịch cơ thể và có tác dụng như một chất trung gian hóa học của phản ứng viêm. Mảnh C5b sẽ được cố định lên màng tế bào và bắt đầu tạo phức hợp tấn công màng.
Con đường hoạt hóa không cổ điển (alternative pathway)
Năm 1950, Pillemer nhận thấy hệ thống bổ thể có thể được hoạt hóa để làm ly giải tế bào mà không cần phải khởi đầu bằng phản ứng kháng nguyên – kháng thể, đó là con đường hoạt hóa không cổ điển. Con đường này được cho rất là quan trọng bởi vì:
Không nhất thiết phải có phản ứng kháng nguyên – kháng thể nên phản ứng có thể xảy ra tức thì, và cơ thể được bảo vệ theo cơ chế không đặc hiệu.
Có con đường khuyếch đại thông qua C3b nên cho phép tăng hiệu quả của hệ bổ thể cả trong đáp ứng đặc hiệu lẫn không đặc hiệu.
Các yếu tố tham gia trong con đường không cổ điển gồm:
Yếu tố C3 trước đây gọi là yếu tố A, nhưng sau khi đó sự khảo sát cấu trúc và chức năng đã xác nhận đó chính là C3. Như vậy, C3 có vai trò rất quan trọng vì nó là nơi gặp gỡ của hai con đường hoạt hóa bổ thể.
Yếu tố B là một β – globulin. Yếu tố B khi cùng với C3b và sự hiện diện của ion Mg++ có khả năng hoạt hóa một phần C3. Tuy nhiên, khả năng này tăng lên khi có yếu tố D để phức hợp C3bB thành C3bBb. Phức hợp C3bBb là một enzym tác dụng lên cơ chất là C3, vì vậy nó tạo ra vòng một khuyếch đại (amplifying loop) hay còn gọi là vòng phản hồi dương. Ngoài ra, so sánh với con đường C3bBb sẽ được gắn thêm C3b để tạo phức hợp C3bBb3b có tác dụng cắt C5 để tạo phân tử C5b có hoạt tính enzym cần có các bước tiếp theo của chuỗi phản ứng bổ thể.
Yếu tố D khi có sự hiện diện của C3b thì nó tác dụng như một enzym lên yếu tố B để cho ta phức hợp C3bBb và mảnh nhỏ Ba bị tách ra ngoài.
Yếu tố P hay properdin không có cấu trúc của globulin miễn dịch. P được hấp thụ cho phức hợp C3bBb làm cho phức hợp này ổn định, và người ta còn gọi con đường không cổ điển là đường properdin.
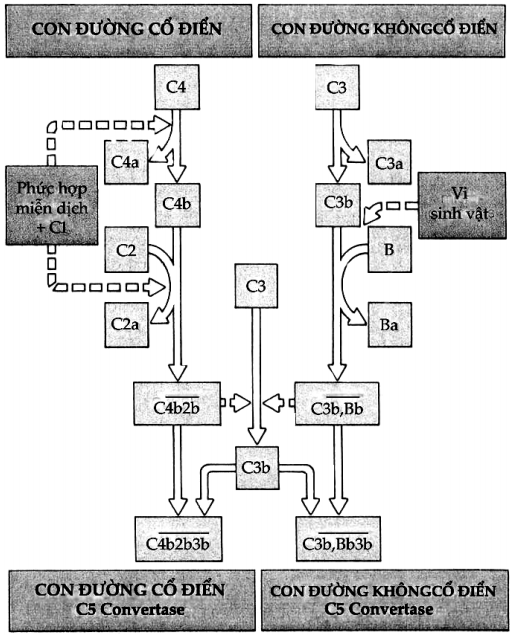
So sánh hai con đường hoạt hóa bổ thể được trình bày ở Hình 6.4.
Sự hình thành phức hợp tấn công màng c5-9
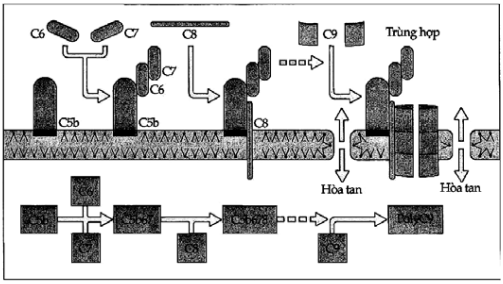
Sau khi C5b hình thành nó lập tức bám vào màng tế bào. Trên cơ sở đó các phân tử khác trong hệ bổ thể là C6, C7 và C8 sẽ đến gắn vào C5b để tạo thành phức hợp C5-9. Sau đó, phức hợp này tạo phản ứng trùng hợp (polymerize) các phân tử C9 để tạo một cấu trúc ống, đó là phức hợp tấn công màng cắm xuyên qua lớp màng tế bào (Hình 6.5). Phức hợp này có thể thấy dưới kính hiển vi điện tử.
Hình 6.4. Hoạt động giống nhau của con đường cổ điển và không cổ điển
Hình 6.5. Sự hình thành phức hợp tấn công màng C5-9
Sau khi C5b gắn màng, C6 và C7 đến gắn vào C5b để tạo C5b67. C5b67 tác động với C8 để tạo C5b678. Đơn vị này tạo phản ứng trùng hợp phân tử C9 đã tạo một ống xuyên thủng qua màng tế bào. Ống này tồn tại cùng với C5b678 và người ta gọi đó là phức hợp tấn công màng