Giải phẫu bệnh đại cương nghiên cứu về các tổn thương cơ bản, là tổn thương chung của mọi loại bệnh lý ở các cơ quan và hệ thống khác nhau.
Tổn thương cơ bản là các biến đổi hình thái của tế bào và mô gây ra bởi các nguyên nhân bệnh lý hoặc sinh lý, gồm có 7 loại là: các đáp ứng thích nghi, ứ đọng nội bào, lắng đọng ngoại bào, hoại tử, viêm, u, tổn thương huyết quản huyết do rối loạn tuần hoàn.
Các đáp ứng thích nghi
Là các biến đổi hình thái của tế bào và mô nhằm thích ứng với môi trường xung quanh đã bị thay đổi. Có 5 loại đáp ứng thích nghi sau:
Phì đại (hypertrophy)
Là hiện tượng tăng kích thước tế bào. Tế bào tăng kích thước bởi vì có sự tăng tổng hợp tất cả các thành phần cấu tạo của nó. Nhiều tế bào phì đại sẽ dẫn đến sự phì đại của 1 mô, 1 cơ quan. Nguyên nhân gây phì đại thường là do có một yêu cầu cao hơn về mặt chức năng đối với tế bào và mô hoặc do có sự kích thích của một hormôn đặc hiệu. Phì đại có liên quan mật thiết với tăng sản và cả 2 hiện tượng này thường xảy ra đồng thời với nhau. Phì đại được phân thành 2 loại: phì đại sinh lý và phì đại bệnh lý.
Phì đại sinh lý:
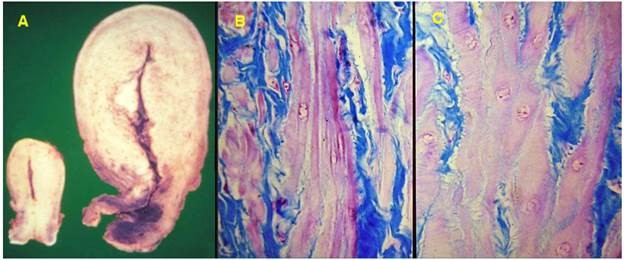
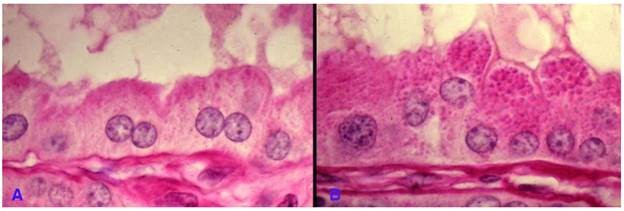
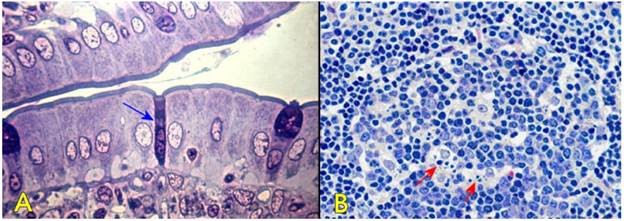
Khi mang thai, tế bào cơ trơn tử cung được estrogen kích thích sẽ phì đại gấp 10 lần bình thường. Estrogen gắn lên các thụ thể tương ứng có trong bào tương tế bào cơ trơn, đi vào trong nhân và tương tác với ADN, kích thích sự tổng hợp các ARNm; kết quả làm tăng số lượng protein của tế bào cơ trơn và làm tăng kích thước tế bào. Ở các vận động viên, các tế bào cơ vân phì đại để thích nghi với yêu cầu tăng cao về chức năng co duỗi của cơ trong quá trình tập luyện (Hình 1).
Hình 1: Phì đại sinh lý tử cung khi mang thai (A); tế bào cơ trơn bình thường (B); tế bào cơ trơn phì đại (C).
Phì đại bệnh lý:
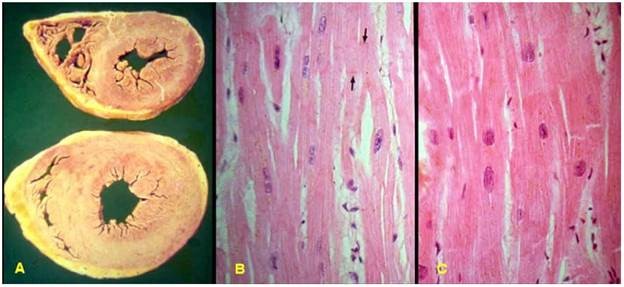
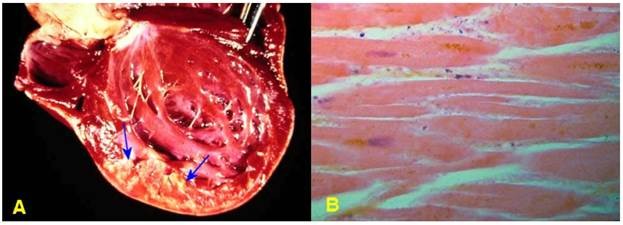
Trong bệnh cao huyết áp hoặc hẹp van động mạch chủ, tâm thất trái của tim phải co bóp mạnh hơn để thắng được sự gia tăng lực cản trong động mạch; để thích nghi tế bào cơ tim sẽ phì đại, làm vách tim dầy lên và làm tăng trọng lượng quả tim (Hình 2).
Hình 2: Phì đại bệnh lý thất trái do cao huyết áp (A); tế bào cơ tim bình thường (B); tế bào cơ tim phì đại (C).
Tăng sản (hyperplasia)
Là hiện tượng tăng số lượng tế bào bằng hoạt động phân bào. Như vậy, chỉ những tế bào còn giữ được khả năng phân bào mới có thể tăng sản. Tăng sản cũng được phân biệt thành 2 loại: tăng sản sinh lý và tăng sản bệnh lý.
Tăng sản sinh lý:
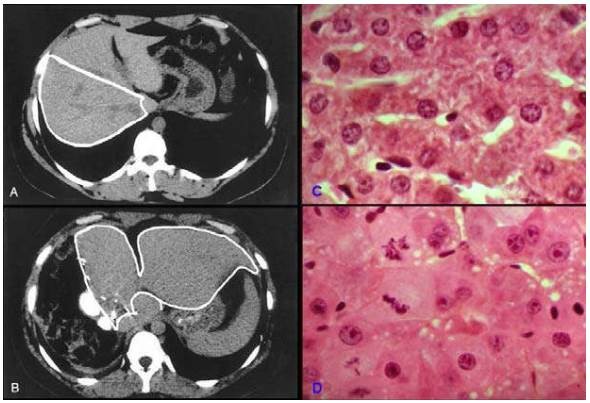
Khi mang thai, các tế bào tuyến vú vừa tăng sản vừa phì đại để chuẩn bị cho hoạt động tiết sữa, tương tự như vậy đối với các tế bào cơ trơn của tử cung. Ở gan, nếu một phần gan bị cắt bỏ, phần còn lại sẽ tăng sản nhằm bù đắp lại số tế bào gan đã mất, còn gọi là tăng sản bù trừ (Hình 3).
Hình 3: Ảnh chụp CT ở một người trước khi hiến tặng thuỳ phải gan (A); chỉ 1 tuần sau phẫu thuật, thuỳ trái gan đã to hẳn ra do hoạt động tăng sản bù trừ (B). Vi thể mô gan bình thường ít thấy hình ảnh phân bào (C); còn mô gan tăng sản bù trừ thì có tỉ lệ phân bào cao (D).
Tăng sản bệnh lý:
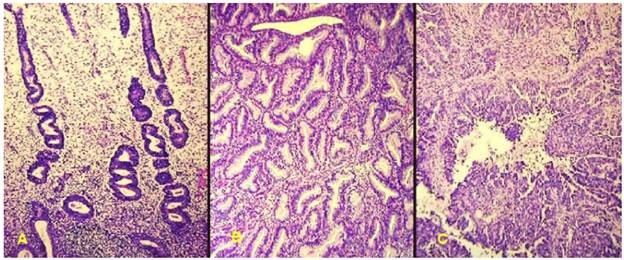
Hầu hết đều do sự kích thích quá mức của một hormôn đặc hiệu. Tăng sản bệnh lý khác với sự tăng sinh của các tế bào u ở chỗ nó sẽ biến mất khi không còn kích thích của hormôn. Thí dụ như tình trạng tăng sản nội mạc tử cung gây ra bởi sự gia tăng estrogen, khi lượng estrogen trở về bình thường, tình trạng tăng sản nội mạc sẽ biến mất. Tuy nhiên, tăng sản bệnh lý vẫn là một mảnh đất mầu mỡ cho sự phát triển của ung thư, thí dụ tình trạng tăng sản nội mạc tử cung không kiểm soát được có thể dẫn đến carcinôm tuyến nội mạc (Hình 4).
Tăng sản có thể diễn ra đồng đều hoặc không đồng đều cho tất cả các tế bào trong cùng một mô. Trường hợp tăng sản không đồng đều, chỉ xảy ra ở một số nhóm tế bào, sẽ tạo thành các cục tăng sản; do đó kiểu tăng sản này được gọi là tăng sản dạng cục, thường thấy ở tuyến tiền liệt, tuyến giáp, tuyến vú, lớp cơ trơn thân tử cung.
Hình 4: Nội mạc tử cung: bình thường (A); tăng sản bệnh lý (B); carcinôm tuyến nội mạc (C)
Teo đét (atrophy)
Là hiện tượng giảm kích thước và thể tích tế bào do các thành phần cấu tạo của nó đều bị giảm số lượng. Dưới KHVĐT, người ta thấy có sự gia tăng số lượng túi tự thực và không bào tự thực trong bào tương. Mô hoặc cơ quan sẽ teo nhỏ lại khi có nhiều tế bào bị teo đét. Các nguyên nhân gây teo đét tế bào gồm có: sự giảm yêu cầu chức năng đối với tế bào và mô, mất phân bố thần kinh, giảm tưới máu nuôi, suy dinh dưỡng, mất sự kích thích của hormôn đặc hiệu, sự già nua. Teo đét được phân thành 2 loại: teo đét sinh lý và teo đét bệnh lý.
Teo đét sinh lý:
Tử cung nhỏ lại sau sinh.
Các cơ vân ở người già bị teo lại do sự giảm hoạt động.
Các tuyến sinh dục của người già bị teo lại do mất các kích thích hormôn.
Teo đét bệnh lý:
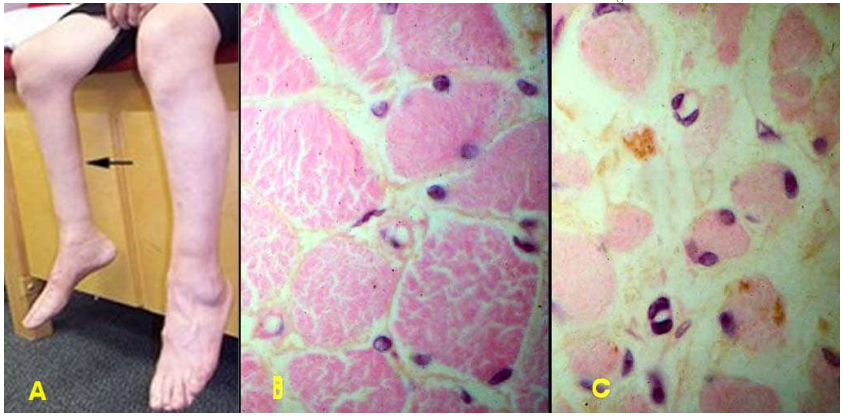
Teo cơ do bệnh bại liệt làm tổn thương các nơron vận động (Hình 5).
Teo cơ do chi bị gãy xương phải bó bột bất động.
Sự teo dần bộ não do bệnh xơ vữa động mạch làm giảm lượng máu nuôi.
Cần phân biệt sự teo đét tế bào với hiện tượng thoái triển (involution) của một số cơ quan, xảy ra trong quá trình phát triển tự nhiên của cơ thể. Trong hiện tượng này, có sự giảm số lượng tế bào bằng cơ chế tự hủy tế bào (apoptosis), kết quả cơ quan bị teo nhỏ lại; thí dụ như sự thoái triển của tuyến ức ở tuổi thiếu niên. Trong sự teo nhỏ các cơ quan sinh dục ở người già, thực ra có sự phối hợp của cả 2 hiện tượng: teo đét tế bào và thoái triển.
Hình 5: Teo cơ cẳng chân phải do bệnh bại liệt (A); Tế bào cơ vân bình thường (B); Tế bào cơ vân teo đét.
Chuyển sản (metaplasia)
Đối với một số loại thay đổi của môi trường xung quanh, tế bào chỉ có thể thích nghi tốt bằng cách thay đổi hướng biệt hoá, gọi là chuyển sản. Đây là hiện tượng chuyển dạng từ 1 loại mô đã biệt hoá thành 1 mô biệt hoá khác nhưng vẫn cùng loại (cùng là biểu mô hay trung mô). Chuyển sản là 1 tổn thương có tính khả hồi.
Thí dụ:
Ở người nghiện thuốc, biểu mô trụ giả tầng của khí phế quản thích nghi với sự kích thích kéo dài của khói thuốc bằng cách chuyển dạng thành biểu mô lát tầng, gọi là chuyển sản gai của biểu mô hô hấp.
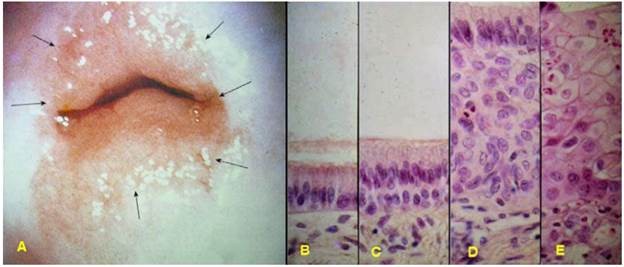
Ở cổ tử cung của người phụ nữ trưởng thành, phần biểu mô trụ đơn tiết nhầy của cổ trong thường bị lộn ra ngoài, gọi là tình trạng lộ tuyến cổ tử cung; để thích nghi với môi trường acid trong âm đạo, biểu mô trụ đơn cổ trong sẽ chuyển thành biểu mô lát tầng giống biểu mô cổ ngoài cổ tử cung, gọi là hiện tượng chuyển sản gai. (Hình 6)
Hình 6: Lộ tuyến cổ trong cổ trong cổ tử cung ( mũi tên, A); Biểu mô trụ đơn cổ trong bình thường (B); bắt đầu chuyển sản thành 2 lớp (C); nhiều lớp (D); cuối cùng trở nên biểu mô lát tầng giống giống cổ ngoài (E).
Biểu mô chuyển tiếp của bàng quang chuyển sản thành biểu mô lát tầng do bị kích thích kéo dài bởi sỏi bàng quang hoặc nhiễm trùng.
Biểu mô lát tầng ở đoạn dưới thực quản chuyển thành biểu mô trụ đơn tiết nhầy để thích ứng với axit có trong dịch vị trào ngược lên thực quản.
Biểu mô trụ đơn tiết nhầy của bề mặt niêm mạc dạ dày chuyển thành biểu mô có tề bào hình đài tiết nhầy giống biểu mô ruột, do viêm mãn tính
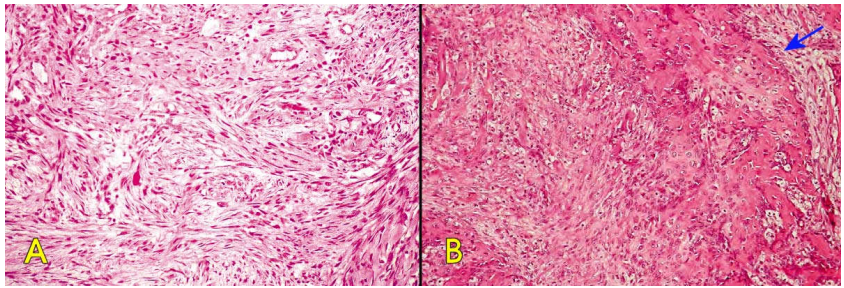
Mô sợi có thể chuyển sản thành mô sụn hoặc mô xương sau 1 chấn thương (Hình 7).
Hình 7: Mô sợi sau chấn thương (A); các bè xương (mũi tên) do mô sợi chuyển sản tạo ra.
Nghịch sản (dysplasia)
Nghịch sản là 1 rối loạn của sự tăng sinh tế bào, dẫn đến sự thay đổi hình dạng, kích thước của tế bào cũng như cách tổ chức sắp xếp của chúng trong một mô. Nghịch sản thực chất không phải là 1 đáp ứng thích nghi, nhưng do có mối liên quan mật thiết với tăng sản nên vẫn được đề cập tại đây.
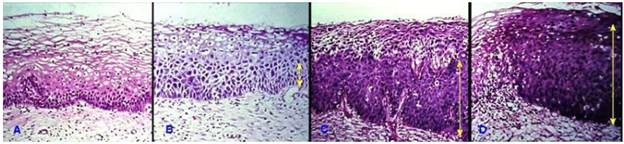
Nghịch sản xảy ra chủ yếu ở các biểu mô (thường là 1 biểu mô đã bị chuyển sản) do tác động kéo dài của 1 kích thích. Các tế bào nghịch sản có kích thước to nhỏ không đều, nhân tăng sắc và cũng có kích thước to nhỏ không đều, tỉ lệ nhân/ bào tương tăng, tỉ lệ phân bào tăng nhưng không có phân bào bất thường, định hướng sắp xếp của các lớp tế bào trong mô bị rối loạn. Đối với biểu mô lát tầng, tùy theo các hình ảnh biến đổi nói trên còn giới hạn ở 1/3 dưới, 1/3 giữa hoặc đã lên đến 1/3 trên của chiều dày biểu mô, phân biệt ra 3 mức độ nghịch sản: nhẹ, vừa và nặng. Khi hình ảnh biến đổi đã chiếm toàn bộ chiều dày biểu mô, kể cả lớp bề mặt thì tổn thương khi đó được gọi là carcinôm tại chỗ. Như vậy nghịch sản được xem là tổn thương tiền ung thư vì nghịch sản nặng có thể chuyển thành ung thư; tuy nhiên nó vẫn còn là một tổn thương khả hồi vì biểu mô nghịch sản ở mức độ nhẹ và vừa có thể trở lại bình thường khi không còn tác nhân kích thích (Hình 8).
Hình 8: Biểu mô lát tầng bình thường (A); bị nghịch sản nhẹ (B); nghịch sản vừa (C); nghịch sản nặng (D).
Thí dụ trong trường hợp cổ tử cung bị viêm nhiễm kéo dài, biểu mô trụ đơn của cổ trong chuyển sản thành biểu mô lát tầng. Nếu viêm nhiễm tiếp tục gia tăng, biểu mô lát tầng này có thể bị nghịch sản từ nhẹ đến nặng; nếu nghịch sản nặng kéo dài mà không được điều trị thì có thể chuyển thành carcinôm tại chỗ và tiếp sau đó là carcinôm tế bào gai xâm lấn.
Ứ đọng nội bào (intracellular accumulation)
Là hiện tượng ứ đọng bên trong tế bào 1 sản phẩm chuyển hoá bình thường hoặc bất thường. Tùy theo mức độ ứ đọng, hoạt động của tế bào có thể bị rối loạn từ ít đến nhiều hoặc trầm trọng đến mức gây chết tế bào.
Ứ đọng nước
Là hiện tượng ứ đọng nước trong tế bào, chủ yếu gặp ở tế bào ống thận, gan, tim.
Nguyên nhân: các tình trạng thiếu máu, thiếu oxy, ngộ độc (Chloroform, tetrachlorur carbon…), nhiễm trùng… làm giảm sự sản xuất ATP tại ty thể. Do thiếu hụt ATP, hoạt động của bơm Na+/ K+ – ATPase ở màng tế bào bị rối loạn, dẫn đến ứ đọng natri trong tế bào, kết quả nước bị kéo vào làm trương giãn các bào quan và toàn bộ tế bào.
Hình thái tổn thương:
Đại thể: các tạng ứ nước bị trương to tăng trọng lượng, vỏ bọc căng, mầu sắc lợt lạt.
Vi thể: tùy theo mức độ ứ đọng nước, có thể thấy hình ảnh:
Trương đục tế bào (cloudy swelling): do ứ nước mức độ trung bình, tế bào trương to, bào tương dạng hạt, bắt mầu kém, nhân còn ở giữa tế bào. Ở giai đoạn này, tổn thương còn khả hồi.
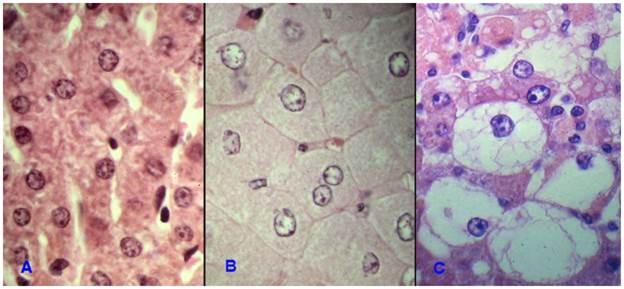
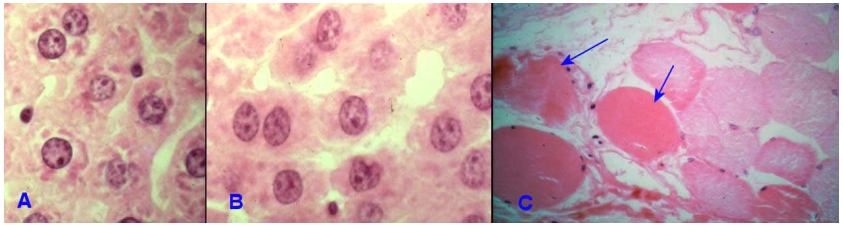
Thoái hoá nước (hydropic degeneration): do ứ nước trầm trọng, tế bào trương to, bào tương bị choán bởi các không bào lớn không mầu mà bản chất là các túi lưới nội bào bị trương to, nhân bị đẩy lệch ra ngoại vi. Tế bào có thể vỡ, chết (Hình 9).
Hình 9: Tế bào gan bình thường (A); Trương đục tế bào gan (B); Thoái hóa nước tế bào gan (C)
Ứ đọng lipid
Ứ đọng triglycerid (ứ đọng mỡ):
Thường gặp ở gan vì chuyển hoá mỡ được thực hiện chủ yếu tại đây, cũng có thể gặp ở các tạng khác như tim, thận, cơ.
Nguyên nhân gây ứ đọng mỡ đa dạng và khác nhau tùy cơ quan. Gan thường bị ứ đọng mỡ chủ yếu là do ngộ độc rượu, hoặc do suy dinh dưỡng. Tim bị ứ đọng mỡ do thiếu oxy mãn, do độc tố của vi khuẩn như trong trong bệnh viêm cơ tim do vi khuẩn bệnh bạch hầu.
Hình thái tổn thương:
Đại thể: tạng bị ứ đọng mỡ to ra, mầu vàng.
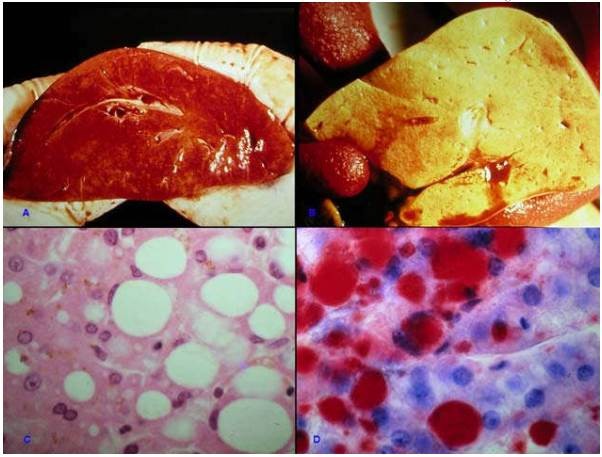
Vi thể: tuỳ mức độ ứ đọng, trong bào tương chứa nhiều không bào nhỏ không mầu hoặc một không bào lớn duy nhất, đẩy nhân lệch ra ngoại vi. Nếu ứ đọng quá nặng, tế bào bị hoại tử (Hình 10).
Hình 10: Gan bình thường (A); Gan ứ đọng mỡ (B); tế bào gan chứa một giọt mỡ lớn trong bào tương làm nhân bị đẩy lệch (C); giọt mỡ bắt mầu đỏ với phẩm nhuộm Oil Red O (D)
Cần phân biệt tổn thương ứ đọng mỡ với sự xâm nhập mỡ vào mô đệm (stromal infiltration of fat) tức là sự xâm nhập của các tế bào mỡ trưởng thành vào trong mô liên kết của các tạng (thường nhất là tim và tụy tạng), xảy ra trong quá trình lão hoá. Sự xâm nhập này không gây ảnh hưởng gì đến hoạt động bình thường của tạng bị xâm nhập.
Ứ đọng cholesterol và cholesterol ester hoá:
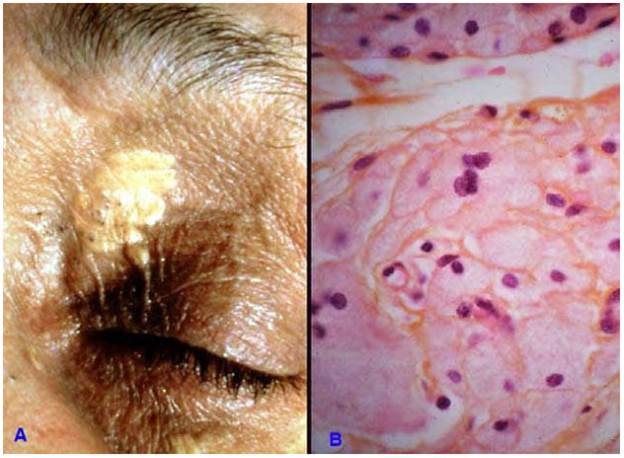
Bình thường, cholesterol được vận chuyển từ gan đến tế bào sẽ được sử dụng hết để tổng hợp các cấu trúc màng nên không bị ứ lại trong bào tương. Trong một số bệnh lý như bệnh xơ vữa động mạch, bệnh tăng cholesterol máu có tính chất gia đình; cholesterol và cholesterol ester hoá bị ứ đọng trong các đại thực bào dưới dạng những không bào rất nhỏ, làm cho đại thực bào có hình ảnh bọt bào (foam cell). Các bọt bào này có thể tập trung nhiều trong mô liên kết của da, tạo thành các đám sùi mềm mầu vàng gọi là u vàng (xanthoma) (Hình 11).
Hình 11: U vàng ở mí mắt trên (A); Các bọt bào ứ đọng cholesterol
Ứ đọng lipid phức tạp:
Gặp trong 1 số rối loạn chuyển hoá bẩm sinh gọi chung là các bệnh tích tiêu thể (lysosomal storage disease); lipid bị ứ đọng trong các tiêu thể do tiêu thể bị thiếu hụt enzym thủy phân tương ứng.
Thí dụ: trong bệnh GAUCHER, có sự thiếu hụt enzym glucocerebrosidase làm glucocerebroside bị ứ lại trong tiêu thể của các đại thực bào. Các đại thực bào này còn được gọi là tế bào Gaucher, có kích thước lớn (100mcm), bào tương có dạng sợi.
Trong bệnh NIEMANN – PICK, có sự thiếu hụt enzym sphingomyelinase làm sphingomyelin bị ứ lại trong tiêu thể của các đại thực bào. Các đại thực bào này có kích thước lớn, có dạng tế bào bọt do bào tương chứa đầy những không bào nhỏ.
Ứ đọng glucid
Ứ đọng glycogen:
Gặp trong các rối loạn chuyển hoá glucoz như bệnh tiểu đường hoặc các bệnh tích glycogen (glycogen storage disease).
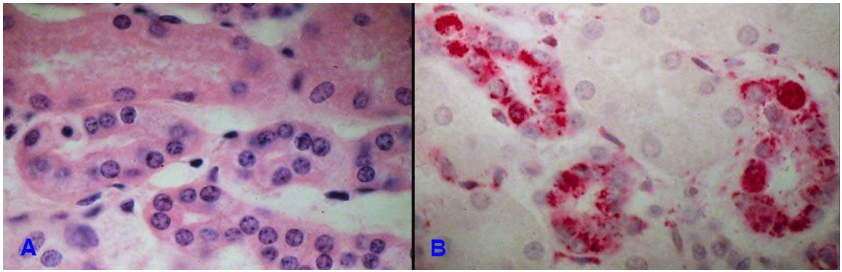
Trong bệnh tiểu đường, glucoz thoát vào ống thận gần sẽ được các tế bào biểu mô ống thận cố tái hấp thu cho hết. Kết quả là glucoz bị ứ đọng trong bào tương dưới dạng glycogen, tạo thành các không bào nhỏ khó thấy, nhiều khi phải nhuộm đặc biệt (PAS, Carmin de Best ) mới phát hiện được (Hình 12).
Hình 12: Ứ đọng glycogen trong tế bào biểu mô ống thận khó thấy với nhuộm thông thường (A); thấy rõ khi nhuộm với phẩm nhuộm Carmin de Best
Trong bệnh tích glycogen (bệnh Von Gierke, bệnh Mc Ardle, bệnh Pompe, v.v.), có sự thiếu hụt một trong các enzym liên quan đến quá trình tổng hợp hoặc giáng hoá glycogen, kết quả là glycogen bị ứ lại trong bào tương hoặc trong tiêu thể của các tế bào gan, thận, cơ tim… làm tăng kích thước và rối loạn hoạt động các cơ quan.
Ứ đọng mucopolysaccharide:
Bệnh tích mucopolysaccharide (mucopolysaccharidoses) là một nhóm bệnh rối loạn chuyển hoá bẩm sinh gây ra sự thiếu hụt 1 trong các enzym cần cho sự giáng hoá các mucopolysaccharide như heparan sulfate, keratan sulfate, chondroitin sulfate, dermatan sulfate. Kết quả là các mucopolysaccharide bị ứ lại trong tiêu thể của các đại thực bào, tế bào cơ trơn, tế bào nội mô, nguyên bào sợi trong khắp cơ thể.
Ứ đọng protein
Đặc trưng bởi sự xuất hiện trong bào tương các thể vùi hình tròn đồng nhất vô định hình, trong như kính, bắt mầu phẩm nhuộm acid, gọi là các thể vùi hyalin (Hình 13).
3 cơ chế gây ứ đọng protein nội bào:
Nhập bào quá mức: thí dụ trong các bệnh cầu thận làm thoát protein huyết tương vào dịch lọc cầu thận, các tế bào ống thận cố gắng tái hấp thu tối đa, kết quả bào tương chứa nhiều thể vùi hyalin trong tế bào.
Xuất bào quá chậm: thí dụ trong bệnh đa u tủy, các tương bào có trong bào tương các thể vùi hyalin hình tròn (thể RUSSEL), tương ứng với lưới nội bào chứa đầy globulin miễn dịch mà lẽ ra phải được xuất bào.
Tổn thương bộ xương tế bào: thí dụ trong ngộ độc rượu, tế bào gan chứa những thể vùi hyalin (thể MALLORY) do các siêu sợi trung gian cytokeratin kết tụ với ubiquitin nhau tạo thành.
Hình 13: Biểu mô ống thận bình thường (A); Biểu mô ứ đọng thể vùi hyalin (B)
Ứ đọng sắc tố
Sắc tố bị ứ đọng trong tế bào có thể có nguồn gốc ngoại sinh hoặc nội sinh.
Ngoại sinh: thí dụ ứ đọng bụi than trong các đại thực bào phế nang (công nhân mỏ than), ứ đọng mực xâm trong các đại thực bào của lớp bì (vết xâm). Sự ứ đọng các sắc tố này không kích thích phản ứng viêm.
Nội sinh: là các sắc tố do chính tế bào tổng hợp, thí dụ như :
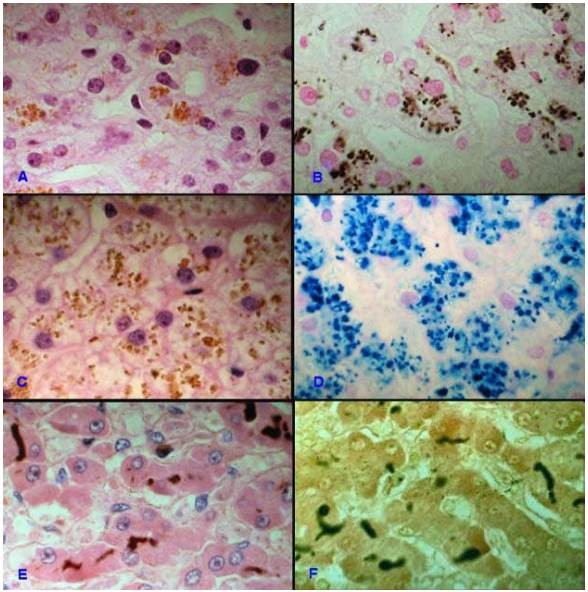
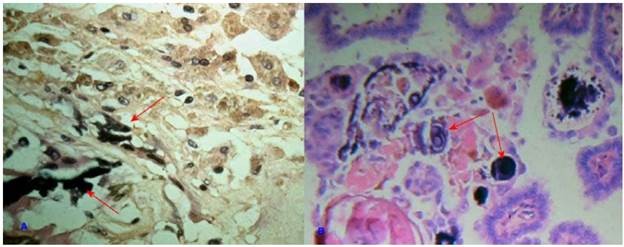
Hình 14: Tế bào gan ứ đọng các sắc tố đều có mầu nâu khi nhuộm thông thường (A, C, E); nhuộm đặc biệt để phân biệt là lipofuscin (bắt mầu đen với Fontana, B), hemosiderin (mầu xanh dương với Perls, D) và bilirubin (mầu xanh lá với Fouchet, F)
LIPOFUSCIN: ứ đọng trong tế bào gan, tim của người già hoặc người bị đói ăn lâu ngày. Dưới KHVĐT, các hạt lipofuscine tương ứng với các thể cặn bã của không bào tự thực.
MELANIN: là một sắc tố bình thường có trong các hắc bào ở lớp đáy của biểu bì. Trong các bướu lành hoặc ác xuất phát từ hắc bào, có sự ứ đọng sắc tố này bên trong bào tương.
HEMOSIDERIN: sắc tố chứa sắt được tạo thành do sự giáng hoá các phân tử hemoglobin của hồng cầu già, bình thường vẫn thấy trong bào tương của các đại thực bào ở lách. Hemosiderin bị ứ đọng trong các đại thực bào phế nang ở những người suy tim, trong các tế bào nhu mô gan, thận, tim ở những người bị bệnh ứ sắt (hemosiderosis).
BILIRUBINE: cũng được tạo thành từ sự giáng hoá hemoglobine, bị ứ đọng trong tế bào gan do các bệnh lý gây tắc mật.
Các sắc tố trên đều bắt mầu nâu khi nhuộm thông thường (Hematoxylin-Eosin); để phân biệt, có thể dùng các phương pháp nhuộm đặc biệt như Perls (nhuộm xanh dương hemosiderin), Fouchet (nhuộm xanh lá cây bilirubin), Fontana (nhuộm đen melanin và lipofuscin), PAS (nhuộm đỏ lipofuscin) (Hình 14).
Lắng đọng ngoại bào
Đặc trưng bởi sự hiện diện quá mức 1 chất hữu cơ hoặc vô cơ trong khoảng gian bào.
Lắng đọng cholesterol
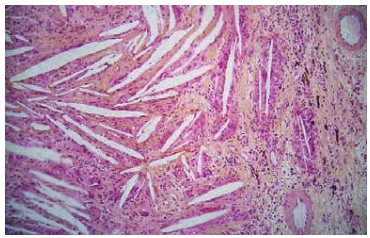
Xảy ra khi có 1 số lượng lớn cholesterol được giải phóng vào môi trường ngoại bào, thí dụ như sự giải phóng cholesterol từ màng các hồng cầu bị vỡ trong khối máu tụ. Cholesterol có thể kết tinh thành các tinh thể hình kim và sau đó bị thực bào bởi các đại thực bào (Hình 15).
Hình 15: Cholesterol lắng đọng ngoại bào dưới dạng tinh thể hình kim
Lắng đọng protein
Phân biệt 3 loại (Hình 16):
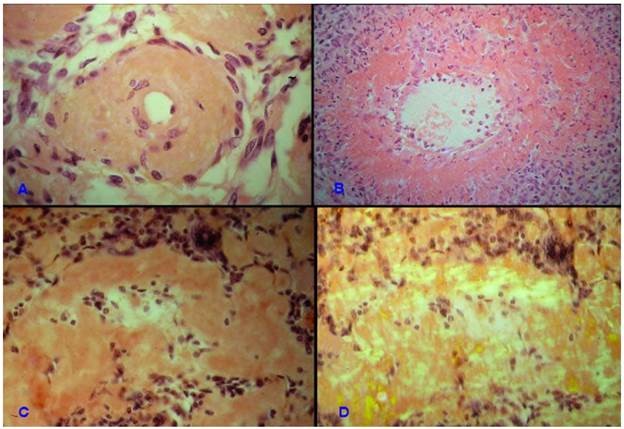
Lắng đọng hyalin: có dạng một chất vô định hình, trong như kính và ưa phẩm nhuộm acid. Có thể gặp trong thành động mạch người lớn tuổi, trong tổ chức liên kết của các sẹo cũ, trong các ổ viêm mãn tính. Cấu tạo của hyalin rất phức tạp, gồm các thành phần protein của huyết tương từ trong lòng mạch thấm ra như fibrin, globulin miễn dịch loại IgM, IgG, các lipoprotein và bổ thể. Đáng chú ý là không có phản ứng viêm đi kèm sự lắng đọng hyalin này.
Lắng đọng chất dạng fibrin (fibrinoid substances): dưới dạng sợi, rất ưa phẩm nhuộm acid. Gặp trong thành tiểu động mạch của người bị cao huyết áp ác tính, trong mô liên kết của người mắc bệnh tạo keo. Luôn có phản ứng viêm đi kèm sự lắng đọng chất dạng fibrin. Cấu tạo của chất dạng fibrin cũng tương tự như chất hyalin nhưng giàu fibrin hơn.
Lắng đọng chất dạng tinh bột (amyloid substances): có dạng các cuộn bông gòn, ưa phẩm nhuộm acid. Gặp trong thành tiểu động mạch, dọc theo thành các mao mạch dạng xoang ở gan và lách của người mắc bệnh viêm nhiễm mãn tính, u tủy (myelome); cấu tạo hoá học chủ yếu là các globulin miễn dịch. Trong bệnh ung thư tuyến giáp dạng tủy, cũng có sự lắng đọng ngoại bào chất dạng tinh bột, nhưng cấu tạo hoá học lại là chất calcitonin do tế bào ung thư tiết ra. Khi nhuộm thông thường, chất dạng tinh bột trông giống như hyalin. Để phân biệt, cho nhuộm đỏ congo (red congo), chất dạng tinh bột bắt mầu cam nhưng sẽ đổi sang mầu vàng xanh khi quan sát bằng kính hiển vi phân cực.
Hình 16: Lắng đọng hyalin trong thành động mạch (A); lắng đọng chất dạng fibrin trong thành mạch, kèm phan ứng viêm (B); Chất dạng tinh bột bắt mầu cam khi nhuộm đỏ congo (C), đổi sang vàng xanh dưới ánh sáng phân cực (D).
Lắng đọng calci
Phân biệt 2 loại:
Calci hoá nghịch dưỡng: calci bị lắng đọng trong mô chết (ổ hoại tử bã đậu, ổ máu tụ, mảng xơ vữa thành động mạch, ung thư tuyến giáp dạng nhú…); tạo thành những đám vô định hình, dạng hạt, bắt mầu kiềm hoặc những cấu trúc như thể cát (psammoma bodies) (Hình 17).
Hình 17: các đám calci vô định hình bắt mầu kiêm, trong ổ máu tụ ( mũi tên, A); hoặc tạo thành thể cát trong ung thư tuyến giáp dạng nhú (mũi tên, B).
Calci hoá di căn: calci bị lắng đọng trong các mô sống (chủ yếu là ở thành mạch máu, nhu mô thận, gan, niêm mạc dạ dày) do tình trạng tăng calci máu (trong các bệnh như cường tuyến cận giáp, u xương có hủy xương…). Hình ảnh vi thể của các đám calci cũng tương tự trong calci hoá nghịch dưỡng.
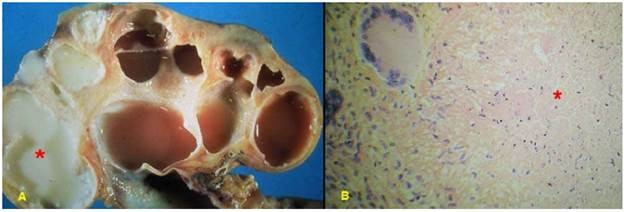
Lắng đọng urat
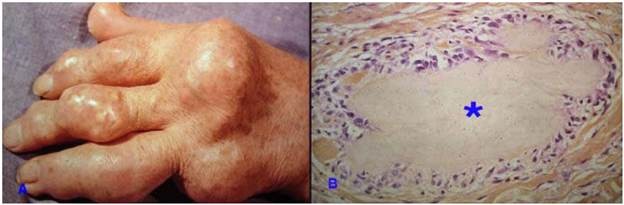
Hình 18: Nốt tophi ở khớp ngón tay (A); trên vi thể, đám urát lắng đọng (*) được bao quanh bởi các tế bào viêm.
Gặp trong bệnh gút, là một nhóm bệnh lý có đặc điểm chung là tình trạng rối loạn chuyển hoá purin, dẫn đến tình sự tăng cao acid uric trong máu (> 7mg%). Acid uric sẽ bị lắng đọng trong nhiều cơ quan khác nhau như khớp, thận, kích thích mạnh phản ứng viêm gây ra viêm khớp mãn tính, viêm thận. Sự lắng đọng urat trong mô quanh khớp tạo thành các nốt tophi, cấu tạo gồm một đám tinh thể urat có dạng sợi (có hình kim dưới kính hiển vi phân cực), được bao quanh bởi các tế bào viêm như đại thực bào, lymphô bào và đại bào ăn dị vật (Hình 18).
Sự chết tế bào (cell death)
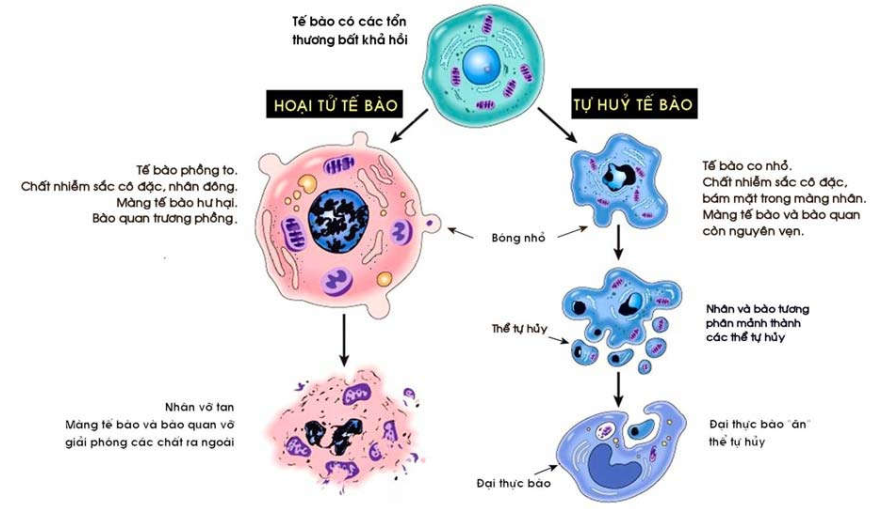
Tế bào chết khi bị các thương tổn bất khả hồi do tác động của các yếu tố độc hại từ môi trường bên ngoài, hoặc do bản thân tế bào đã trở nên không còn cần thiết đối với mô cơ thể. Dựa vào sự khác biệt về đặc điểm hình thái, nguyên nhân và cơ chế phát sinh, phân biệt 2 kiểu chết tế bào là: hoại tử tế bào và tự hủy tế bào (Hình 19) .
Hình 19: Hai kiểu chết tế bào: hoại tử tế bào và tự hủy tế bào
Hoại tử tế bào (necrosis):
Là toàn bộ các biến đổi hình thái xảy ra khi tế bào chết do các nguyên nhân bệnh lý. Các biến đổi siêu cấu trúc xuất hiện sớm, chỉ ít phút sau khi tế bào chết; nhưng phải sau vài tiếng đồng hồ mới có thể quan sát được các biến đổi vi thể.
Trong hiện tượng hoại tử tế bào, tế bào thường chết với số lượng lớn, ảnh hưởng đến chức năng của mô và luôn kích thích theo phản ứng viêm.
ĐẶC ĐIỂM HÌNH THÁI:
Biến đổi nhân:
Gồm 3 biến đổi nối tiếp nhau :
Nhân đông (pyknosis): nhân vón cục nhỏ lại, bắt mầu kiềm đậm do chất nhiễm sắc bị cô đặc.
Nhân vỡ (karyorrhexis): do chất nhiễm sắc cô đặc thành nhiều khối .
Nhân tan (karyolysis): chất nhiễm sắc bị hoà tan dần, nhân chỉ còn là 1 bóng mờ nhạt và biến mất .
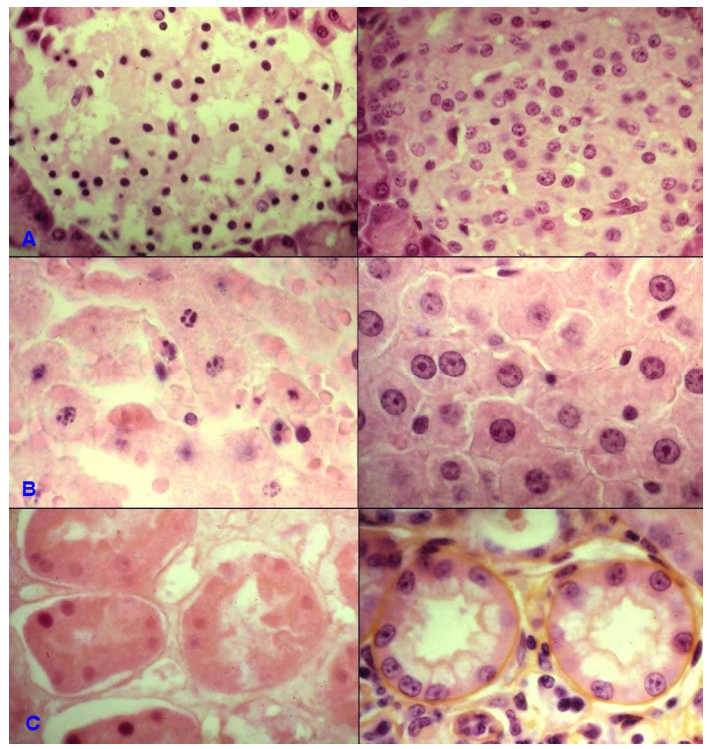
Trong mỗi tế bào hoại tử, biến đổi nhân xuất hiện theo đúng thứ tự trên, nhưng cả 3 hình ảnh có thể cùng hiện diện trong những tế bào khác nhau của 1 mẫu mô hoại tử (Hình 20).
Hình 20: Các biến đổi nhân của tế bào hoại tử, so sánh với tế bào bình thường: nhân đông ở tế bào đảo Langerhans tụy tạng (A), nhân vỡ ở tế bào gan (B), nhân tan ở tế bào ống thận (C).
Biến đổi bào tương:
Xuất hiện trước biến đổi nhân, cũng gồm 3 biến đổi nối tiếp nhau:
Giảm tính bắt mầu kiềm: thấy rõ nhất ở những tế bào có chứa nhiều ribosome trong bào tương. Cơ chế của biến đổi này là do sự giải trùng hợp ARN làm phân rã các ribosome.
Tăng tính bắt mầu acid: do protein bào tương bị biến chất, mất đi các gốc carboxyl.
Xoá mờ các cấu trúc trong bào tương: do sự phân rã các bào quan, thí dụ như mất hình ảnh các vi sợi cơ trong tế bào cơ vân, mất các vi nhung mao ở bề mặt cực đỉnh tế bào biểu mô ống thận,.. kết quả bào tương bắt mầu trong đều hoặc lỗ chỗ do chứa nhiều không bào (Hình 21).
Hình 21: Tế bào gan bình thường (A); Tế bào gan hoại tử, bào tương mất tính bắt mầu kiềm (B); bào tương tế bào cơ vân hoại tử, tăng tính bắt mầu acid, các cấu trúc trong bào tương bị xoá (mũi tên, C)
Biến đổi màng tế bào:
Màng của tế bào và các bào quan mất tính thấm chọn lọc, làm thể tích tế bào tăng và trương to các bào quan.
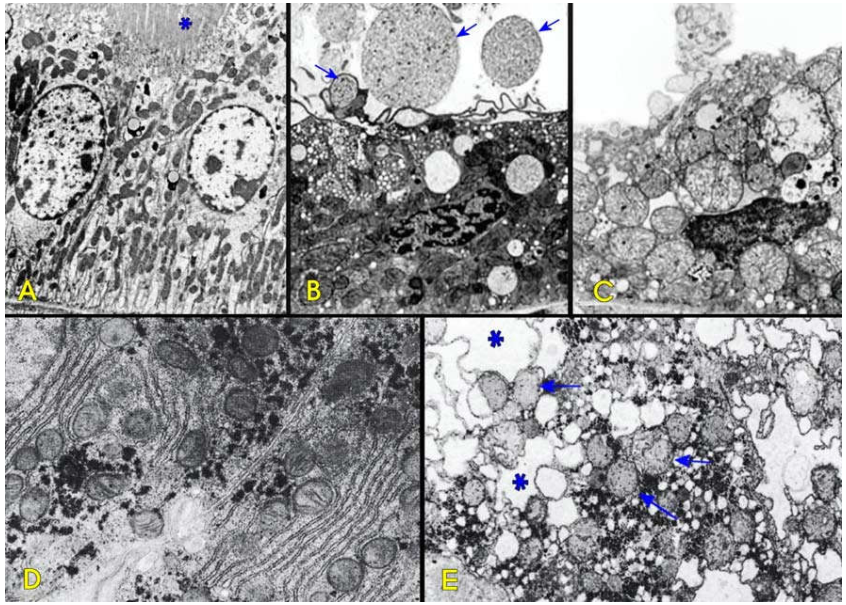
Hình 22: Tế bào biểu mô ống thận gần bình thường, có vi nhung mao cực đỉnh (*) (A); Khi bị hoại tử, màng tế bào tạo ra các bóng nhỏ (mũi tên), vi nhung mao biến mất, nhân nhỏ lại và cô đặc, bào tương có các ty thể phồng to và nhiều không bào; Tế bào hoại tử “nổ tung”, giải phóng các thành phần cấu tạo ra môi trường bên ngoài (C). Tế bào gan bình thường, bào tương có lưới nội bào hạt phát triển phong phú và nhiều ti thể (D); Khi bị hoại tử, lưới nội bào hạt phồng to và mất các hạt ribôsôm trên bề mặt (*), ty thể phồng to (mũi tên), nhân vỡ vụn (E).
Dưới KHVĐT, màng tế bào hoại tử phồng lên thành các bóng nhỏ trên bề mặt, các cấu trúc chuyên biệt ở cực đỉnh (nếu có) như vi nhung mao hoặc lông chuyển tế bào cũng bị phồng lên và biến mất. Nhân tế bào cô đặc và tan dần. Lưới nội bào hạt phồng to, các ribôsôm bám ngoài bề mặt bong vào trong dịch bào tương, ty thể và tiêu thể cũng bị phồng lên và nứt vỡ; bộ xương tế bào sụp đổ tạo thành các đám kết tủa trong bào tương. Hình ảnh cuối cùng là toàn bộ tế bào bị “nổ tung” (Hình 22).
NGUYÊN NHÂN VÀ CƠ CHẾ GÂY HOẠI TỬ TẾ BÀO
Hoại tử tế bào chỉ xảy ra trong các tình trạng bệnh lý, do các nguyên nhân sau:
Thiếu oxy: do suy tuần hoàn, thiếu máu cục bộ,…
Các tác nhân vật lý: như chấn thương cơ học, các bức xạ ion hoá, nhiệt độ, điện thế…
Tác nhân hoá học: các độc chất như cyanur, acid, baz; hoặc ngay cả các chất có vẻ vô hại như glucoz, muối, nếu tác động vào tế bào với nồng độ quá cao.
Tác nhân nhiễm trùng: như vi khuẩn, ký sinh trùng, virút, nấm mốc.
Đáp ứng miễn dịch bất thường như trong các bệnh lý quá mẫn hoặc tự miễn.
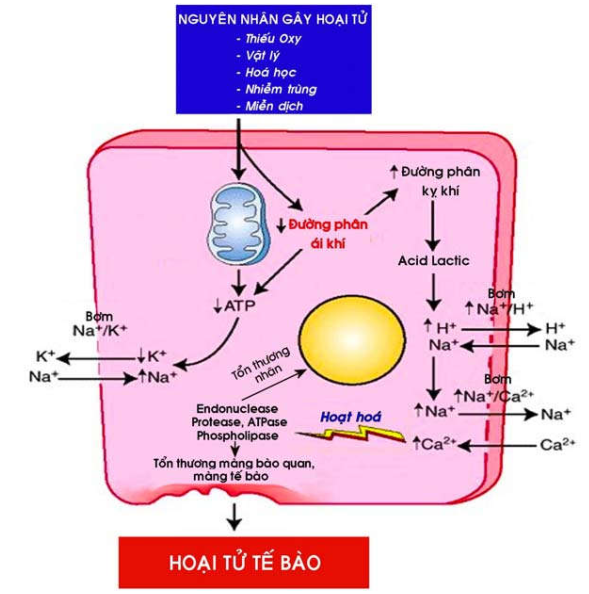
Cơ chế gây hoại tử tế bào có thể khác biệt nhiều ít tuỳ từng loại nguyên nhân, liều lượng và thời gian tác động của nó, và tuỳ theo loại tế bào nào trong cơ thể đang chịu tác động; nhưng nhìn chung, chúng đều được thực hiện thông qua các rối loạn sinh hoá riêng lẻ hay phối hợp, xảy ra trên ty thể, màng tế bào và màng các bào quan (Hình 23).
Hình 23: Cơ chế gây hoại tử tế bào
Ty thể bị tổn thương khiến màng ty thể không còn giữ được tính thấm chọn lọc; phản ứng oxy hoá-phosphoryl hoá bị đình trệ dẫn đến sự thiếu hụt ATP. Tế bào phải sử dụng con đường đường phân kỵ khí để sản xuất ATP với hệ quả là nguồn dự trữ glycogen trong bào tương bị cạn kiệt kèm ứ đọng acid lactic nội bào; pH nội bào giảm làm chất nhiễm sắc trong nhân bị cô đặc lại (hình ảnh nhân đông).
Màng tế bào không còn giữ được tính thấm chọn lọc do bơm Na+/K+- ATPase ngừng hoạt động vì thiếu hụt ATP; ion Na+ và nước từ ngoài ùa vào trong làm tăng thể tích tế bào. Do pH nội bào giảm, bơm Na+/H+ được kích hoạt để đẩy bớt H+ ra ngoài nhưng lại tăng thêm Na+ nội bào. Sự tăng Na+ nội bào sẽ kích hoạt bơm Na+/Ca2+ để đẩy Na+ ra ngoài nhưng lại làm tăng Ca2+ nội bào. Ca2+ nội bào tăng sẽ hoạt hoá hàng loạt enzym có trong bào tương, gây ra các tổn thương bất khả hồi ở nhân, màng tế bào và các bào quan, thí dụ:
Phospholipase phân hủy các phospholipid màng.
Protease làm vỡ màng của tế bào và các bào quan, làm sụp đổ bộ xương tế bào.
ATPase, gây thiếu hụt ATP trầm trọng hơn.
Endonuclease, cắt khúc ADN trong nhân (hình ảnh nhân vỡ).
Tiêu thể bị vỡ màng bao sẽ giải phóng vào trong bào tương các enzym thuỷ phân rất mạnh, sau khi được hoạt hoá bởi pH acid nội bào, có khả năng phân hủy mọi thành phần cấu tạo của tế bào, thí dụ:
Desoxyribonuclease (DNase): phân huỷ ADN (hình ảnh nhân tan dần).
Ribonuclease (RNase): phân hủy ribosome (hình ảnh bào tương giảm tính bắt mầu kiềm).
Protease: giáng hoá các protein nội bào, làm mất đi các gốc carboxyl (hình ảnh tăng tính bắt mầu acid).
Enzym tiêu thể phá vỡ các bào quan khác (hình ảnh xoá mờ các cấu trúc trong bào tương.
Kết quả cuối cùng, tế bào hoại tử bị “nổ tung”, giải phóng ra bên ngoài các thành phần nội bào, trong đó có những chất trung gian hoá học mạnh, thu hút các bạch cầu và đại thực bào.
HIỆN TƯỢNG TỰ TIÊU VÀ DỊ TIÊU (autolysis – heterolysis)
Trong cơ thể sống, các tế bào hoại tử được loại bỏ theo 2 cơ chế:
Tự tiêu: các tế bào hoại tử bị phân rã và loại bỏ bởi enzym tiêu thể của chính mình, thí dụ như các tế bào tụy tạng hoại tử sẽ bị phân rã và loại bỏ bởi chính các enzym tiêu thể của chúng.
Dị tiêu: tế bào hoại tử bị loại bỏ bằng enzym tiêu thể của các tế bào khác, thí dụ như sự tiêu hủy các tế bào cơ bị hoại tử nhờ vào hoạt động của các bạch cầu đa nhân trung tính, đại thực bào (Hình 24).
Hình 24: Tế bào tuyến tụy ngoại tiết hoại tử (A), được loại bỏ bằng cơ chế tự tiêu (B); tế bào cơ vân hoại tử
Tự huỷ tế bào (apoptosis):
Tế bào chết bằng cách khởi động chương trình tự hủy, theo đó một loạt các enzym trong tế bào sẽ được hoạt hoá để phân cắt tế bào thành những mảnh nhỏ gọi là thể tự hủy.
Trong hiện tượng tự hủy tế bào, tế bào chết riêng lẻ, số lượng ít, không ảnh hưởng đến chức năng của mô và không kích thích phản ứng viêm.
ĐẶC ĐIỂM HÌNH THÁI:
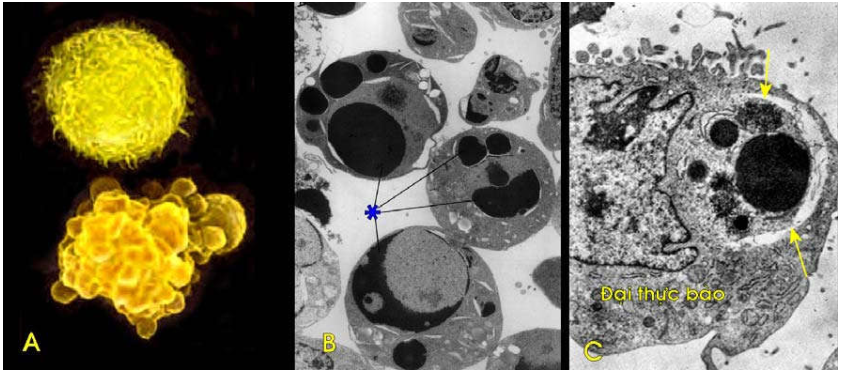
Tế bào tự hủy có thể tích giảm, kích thước thu nhỏ lại. Nhân tăng sắc bắt mầu kiềm đậm do chất nhiễm sắc cô đặc, có thể thấy nhân đã bị phân cắt thành nhiều mảnh nhỏ. Bào tương đậm đặc do các bào quan bên trong bị lèn chặt. Tế bào tự hủy cuối cùng sẽ đuợc cắt thành các thể tự hủy; mỗi thể tự hủy là 1 túi màng chứa bào tương, các bào quan và các mảnh nhân, sẽ được các đại thực bào “ăn” ngay lập tức (Hình 25).
Hình 25: Tế bào biểu mô ruột tự huỷ (mũi tên) có kích thước thu nhỏ, nhân đậm mầu, bào tương đậm đặc (A); Trong trung tâm mầm của 1 nang limphô thứ cấp, limphô bào tự hủy phân thành các thể tự hủy (mũi tên) và đã được đại thực bào “ăn” và đưa vào trong bào tương.
Dưới KHVĐT, chất nhiễm sắc cô đặc thành nhiều khối bám ngay dưới màng nhân. Màng tế bào có thể tạo ra các bóng nhỏ trên bề mặt nhưng cấu trúc của màng và các bào quan vẫn còn nguyên vẹn (Hình 26).
Hình 26: So với limphô bào bình thường ở trên, limphô bào tự huỷ ở dưới tạo ra các bóng nhỏ trên bề mặt
(A).Nhân các limphô bào tự hủy có chất nhiễm sắc cô đặc dưới màng nhân, đã tách ra thành nhiều mảnh
(*) (B).Thể tự huỷ (mũi tên) của limphô bào chết nằm trong không bào tiêu hoá của 1 đại thực bào (C).
NGUYÊN NHÂN VÀ CƠ CHẾ GÂY TỰ HỦY TẾ BÀO
Khác với hoại tử tế bào, tự hủy tế bào chủ yếu là 1 hiện tượng sinh lý bình thường, rất cần thiết trong quá trình tạo hình các mô-cơ quan trong giai đoạn phôi thai. Trong giai đoạn sau sinh, tự huỷ tế bào đảm bảo sự ổn định về cấu trúc và chức năng của nhiều loại mô khác nhau, loại bỏ những tế bào không còn cần thiết ; thí dụ:
Cấu trúc tuyến Lieberkhn được đổi mới liên tục nhờ vào sự tự hủy của các tế bào biểu mô ở bề mặt niêm mạc ruột, nhường chỗ cho các tế bào biểu mô mới sinh ra tại đáy tuyến di chuyển lên.
Ở tuyến ức, các tế bào T chống lại kháng nguyên của chính cơ thể sẽ bị loại bỏ bằng cơ chế tự huỷ tế bào. Tại trung tâm mầm các nang limphô thứ cấp trong hạch bạch huyết, các limphô bào B có đáp ứng kém với kháng nguyên sẽ tự hủy, phân cắt thành các thể tự hủy và được đại thực bào “ăn”.
Ở tuyến vú sau khi ngừng hoạt động tạo sữa, 90% tế bào biểu mô tuyến sẽ tự hủy.
Trong một số tình trạng bệnh lý, tác động của các yếu tố độc hại bên ngoài như tia xạ, gốc oxi hoá tự do, hoá chất, nhiễm virus…có thể gây tổn thương phân tử ADN trong nhân, làm cho các phân tử protein bị ứ kẹt trong lưới nội bào do gấp cuộn sai chuỗi polypéptid; tế bào sẽ tự huỷ nếu không sửa chữa được. Đây là 1 cơ chế bảo vệ giúp cơ thể loại bỏ những tế bào mang đột biến gen có tiềm năng chuyển dạng thành tế bào ung thư.
Cơ chế tự hủy tế bào đuợc thực hiện theo 2 đường, nội sinh- ty thể và ngoại sinh- thụ thể chết, trong đó đường thứ nhất xảy ra nhiều hơn (Hình 27).
Đường nội sinh-ty thể (mitochondrial-intrinsic pathway):
Tế bào tự hủy là do hoạt động của các protein điều hoà sự tự huỷ thuộc họ bcl-2 có trong dịch bào tương, phân thành 2 nhóm với tác động đối nghịch nhau:
Các protein thúc đẩy tự hủy tế bào: Bax, Bak, Bad, Bim, Bid, Bik, Nox, Puma, Noxa,..
Các protein ức chế tự hủy tế bào: Bcl-2, Bcl-XL, Bcl-X, A1, Ku70, Mcl-1,..
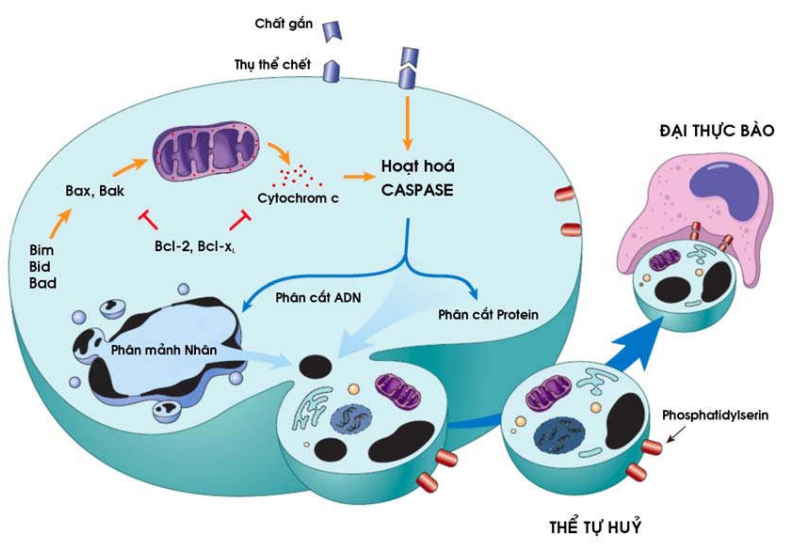
Hinh 27: Hai con đường tự hủy tế bào
Tùy theo mối cân bằng hoạt động giữa 2 nhóm này mà tế bào sẽ bị thúc đẩy đi vào tự huỷ hay là không:
Khi tế bào hoạt động bình thường, hoạt động các protein ức chế tự huỷ Bcl-2, Bcl-XL chiếm ưu thế sẽ bất hoạt Bax và Bak, ngăn cản không cho protein cytochrom c từ trong khoang gian màng của bao ti thể đi ra ngoài bào tương.
Khi tế bào trở nên không còn cần thiết trong cơ thể, hoặc có mang những tổn thương không sửa chữa được trên ADN và protein; các protein Bim, Bid, Bad sẽ ngay lập tức nhận biết tình trạng này và hoạt hoá Bax và Bak; Bax và Bak sẽ di chuyển đến màng ngoài bao ti thể, tạo thành kênh dẫn xuyên màng cho phép cytochrom c thoát vào dịch bào tương. Trong bào tương, cytochrom c sẽ hoạt hoá 1 chuỗi các enzym caspase có khả năng phân cắt đặc hiệu ADN và protein của bộ xương tế bào, khiến nhân bị phân thành nhiều mảnh nhỏ và tế bào thành các thể tự hủy. Khác với hoại tử tế bào, cấu trúc màng tế bào và màng bào quan vẫn bình thường, ty thể và tiêu thể còn nguyên vẹn, không nứt vỡ. Đại thực bào nuốt trọn thể tự hủy chỉ trong vài phút; sự nhanh nhẹn này là do đại thực bào có các thụ thể tương ứng với các phosphatidylserin trên bề mặt của thể tự hủy (ở tế bào sống, phosphatidylserin phân bố ở mặt trong màng tế bào nhưng khi tê bào tự huỷ, nó sẽ được chuyển ra mặt ngoài) và cũng nhờ thế mà không có thành phần nội bào nào của tế bào tự huỷ bị thất thoát ra bên ngoài để kích thích phản ứng viêm.
Đường ngoại sinh- thụ thể chết (death receptor-extrinsic pathway):
Các thụ thể chết có trên bề mặt tế bào, là các protein thuộc về họ thụ thể TNF, trong đó 2 loại được biết rõ nhất là thụ thể TNF týp 1 và FAS. Khi có chất gắn tương ứng là TNF-alpha và FASL đến gắn vào thụ thể thì phức hợp hình thành có khả năng hoạt hoá chuỗi các enzym caspase, dẫn đến kết cục là tế bào bị cắt thành các thể tự hủy tương tự như trên.
Bảng dưới đây tóm tắt các điểm khác biệt giữa hoại tử tế bào và tự huỷ tế bào:
|
|
Hoại tử tế bào |
Tự huỷ tế bào |
|
Nguyên nhân |
Do các tác nhân bệnh lý |
Chủ yếu do tác nhân sinh lý, có thể do 1 số tác nhân bệnh lý |
|
Mức độ |
Số lượng nhiều Ảnh hưởng chức năng mô |
Tế bào riêng lẻ, số lượng ít Không ảnh hưởng chức năng mô |
|
Hình thái: |
|
|
|
Thể tích tế bào |
Tăng |
Giảm |
|
Nhân |
Nhân đông, nhân vỡ, nhân tan |
Nhân phân thành các mảnh nhỏ |
|
Bào tương |
Giảm tính bắt mầu kiềm, tăng tính bắt mầu acid, xoá mờ cấu trúc |
Đậm đặc |
|
Bào quan |
Trương phồng |
Nguyên vẹn |
|
Màng |
Mất tính thấm chọn lọc |
Bình thường |
|
Kết quả |
Tế bào “nổ tung”, giải phóng các chất trung gian hoá học. Kích thích phản ứng viêm |
Tế bào phân thành các thể tự hủy, được đại thực bào “ăn”. Không kích thích phản ứng viêm |
Các hình thái mô học của hoại tử
Khi 1 mô có quá nhiều tế bào bị hoại tử cùng lúc thì được gọi là mô hoại tử. Mô hoại tử có thể có những hình thái riêng biệt như sau:
Hoại tử đông (coagulative necrosis):
Là dạng thường gặp nhất và đặc trưng cho hoại tử do thiếu oxy. Thí dụ: hoại tử đông trong nhồi máu cơ tim. Mô hoại tử chắc, mầu trắng đục. Dưới KHVQH, mô là 1 đám tế bào đồng nhất bắt mầu acid, nhân thường bị tan. Tuy nhiên, cấu trúc mô vẫn được bảo tồn nên còn nhận diện được (Hình 28).
Hình 28: Đại thể và vi thể của hoại tử đông trong nhồi máu cơ tim
Cơ chế của hiện tượng này có lẽ do tình trạng toan hóa nội bào trong tế bào hoại tử đã làm biến chất các protein kể cả các enzym tiêu thể do đó ức chế sự tự tiêu tế bào. Hoại tử đông chỉ tồn tại trong 1 thời gian sau đó chuyển thành hoại tử hoá lỏng do hiện tượng dị tiêu.
Hoại tử hoá lỏng (liquefactive necrosis):
Mô hoại tử mềm nhũn, mầu nhợt nhạt, thường hoá lỏng ở giữa. Hình ảnh vi thể là một đám chất vô định hình chứa đầy các mảnh vụn tế bào hoại tử. Cơ chế của hoại tử hoá lỏng là do hoạt động mạnh mẽ của các enzym tiêu thể (tự tiêu hoặc dị tiêu). Gặp trong tổn thương mô não do thiếu oxy (nhũn não), các ổ viêm do vi khuẩn sinh mủ (áp xe) (Hình 29).
Hình 29: Đại thể và vi thể của hoại tử hóa lỏng trong áp xe thành bụng
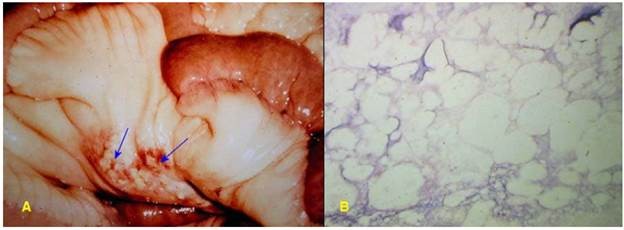
Hoại tử mỡ (fat necrosis):
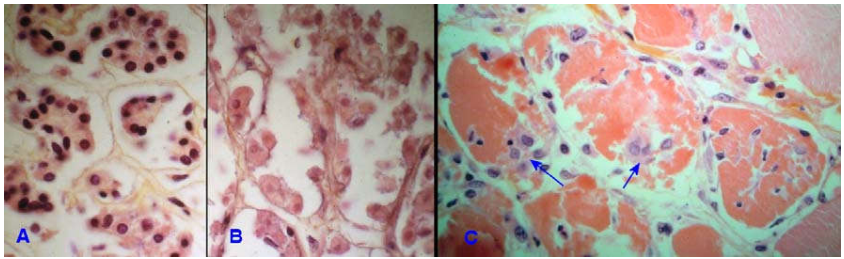
Mô mỡ bị hoại tử tạo ra các vết mầu trắng ngà chắc, thường gặp trong viêm tụy cấp. Hình ảnh vi thể là các tế bào mỡ bị hoại tử không còn thấy rõ ranh giới giữa các tế bào, thường có lắng đọng calci và thấm nhập tế bào viêm (Hình 30).
Hình 30: Đại thể và vi thể của hoại tử mỡ trong viêm tụy cấp
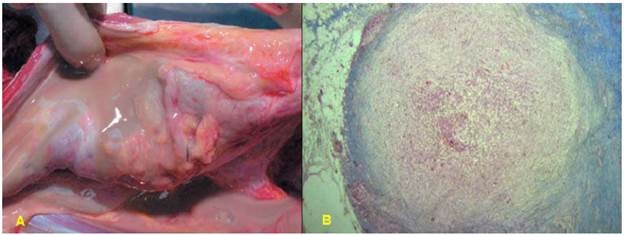
Hoại tử bã đậu (caseous necrosis):
Là 1 dạng hoại tử đặc biệt gặp trong viêm lao. Mô hoại tử là 1 chất bở mầu trắng tương tự bã đậu. Hình ảnh vi thể cho thấy cấu trúc mô bị phá hủy hoàn toàn, thay vào đó là 1 chất vô định hình dạng hạt, cấu tạo bởi các mảnh vỡ của các tế bào bị hoại tử (Hình 31).
Hoại tử hoại thư (gangrenous necrosis):
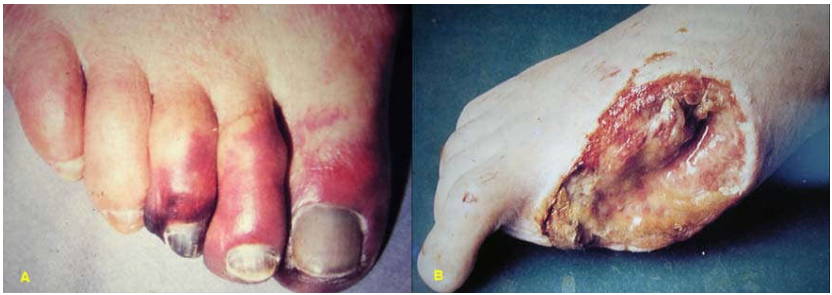
Còn gọi là hoại thư, tuy không thực sự là 1 hình thái mô học riêng biệt của hoại tử, nhưng thuật ngữ này vẫn còn được quen dùng trong lâm sàng để mô tả dạng đại thể của tổn thương chi do tắc động mạch. Phân biệt 2 loại:
Hoại thư khô: phần chi bị hoại thư có mầu tím và khô. Vi thể là hình ảnh hoại tử đông.
Hoại thư ướt: là giai đoạn tiếp sau hoại thư khô. Dưới tác động của vi khuẩn và các bạch cầu, vùng hoại thư khô bị phân hủy trở nên lầy nhầy, ướt, hôi. Hình ảnh vi thể là hoại tử hoá lỏng. (Hình 32)
Hình 31: Đại thể và vi thể của hoại tử bã đậu trong lao thận (*)
Hình 32: Hoại thư khô (A); Hoại thư ướt (B)