COVID-19 treatment combinations and associations with mortality in a large multi-site healthcare system
Dagan Coppock , Michael Baram, Anna Marie Chang, Patricia Henwood, Alan Kubey, Ross Summer, John Zurlo, Michael Li, Bryan Hess
PLoS ONE 16(6): e0252591. Published: June 11, 2021 https://doi.org/10.1371/journal.pone.0252591
Dịch bởi: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
Giới thiệu
Trong những tháng đầu của đại dịch COVID-19, tỷ lệ tử vong liên quan đến căn bệnh này đã giảm ở Hoa Kỳ. Tiêu chuẩn chăm sóc cho các can thiệp dược lý đã phát triển trong thời kỳ này khi các phương pháp điều trị mới và thay thế được sử dụng một mình và kết hợp. Mặc dù các loại thuốc này đã được nghiên cứu riêng lẻ, nhưng dữ liệu còn hạn chế về tác động tương đối của các kết hợp thuốc khác nhau. Mục tiêu của nghiên cứu này là đánh giá mối liên quan giữa tỷ lệ tử vong liên quan đến COVID-19 và sự kết hợp thuốc được quan sát và xác định xem liệu những thay đổi trong mô hình thực hành liên quan đến thuốc và các đặc điểm của bệnh nhân được đo lường, chỉ giải thích sự giảm tỷ lệ tử vong được thấy sớm trong đại dịch COVID- 19.
Phương pháp
Một nghiên cứu thuần tập hồi cứu được thực hiện tại một hệ thống chăm sóc sức khỏe đa bệnh viện khám phá mối liên quan giữa tỷ lệ tử vong và sự kết hợp của remdesivir, corticosteroid, thuốc chống đông máu, tocilizumab và hydroxychloroquine. Hồi quy logistic đa biến được sử dụng để xác định các yếu tố dự báo tử vong cho cả dân số tổng thể và dân số được phân tầng theo chăm sóc đặc biệt và nhập viện không chăm sóc đặc biệt. Một mô hình riêng biệt được tạo ra để kiểm soát sự thay đổi của các biến không được đo lường theo thời gian.
Kết quả
Đối với tất cả bệnh nhân, bốn kết hợp điều trị có liên quan đến tỷ lệ tử vong thấp hơn: Chỉ chống đông (OR 0,24, p
Kết luận
Nghiên cứu này cho thấy rằng kháng đông là phương pháp điều trị quan trọng nhất để giảm tỷ lệ tử vong liên quan đến COVID. Chỉ chống đông máu là loại điều trị duy nhất có liên quan đến việc giảm đáng kể tỷ lệ tử vong cho cả bệnh nhân chăm sóc đặc biệt và không chăm sóc đặc biệt. Kết hợp điều trị bao gồm thêm corticosteroid và/hoặc Remdesivir cũng có liên quan đến việc giảm tỷ lệ tử vong, mặc dù chỉ trong phân tầng chăm sóc không đặc biệt. Hơn nữa, chúng tôi nhận thấy rằng các yếu tố khác ngoài những thay đổi được đo lường về nhân khẩu học, đặc điểm lâm sàng hoặc can thiệp dược lý đã làm giảm thêm tỷ lệ tử vong liên quan đến COVID19 theo thời gian.
Giới thiệu
Tính đến tháng 7 năm 2020, tỷ lệ tử vong liên quan đến COVID-19 đã giảm ở Hoa Kỳ [1]. Điều này có thể do thay đổi chiến lược điều trị, thay đổi đặc điểm bệnh nhân hoặc kết hợp cả hai [2–4]. Vào thời điểm đó, các loại thuốc mới hoặc thuốc thay thế, chẳng hạn như remdesivir, corticosteroid, hydroxychloroquine và tocilizumab được sử dụng, một mình hoặc kết hợp, trong một tiêu chuẩn chăm sóc ngày càng phát triển để điều trị COVID-19 [5-9].
Khi đại dịch tiến triển, remdesivir, tocilizumab, và corticosteroid tiếp tục được chú ý vì lợi ích tiềm năng của chúng đối với tỷ lệ tử vong [5,10,11]. Tuy nhiên, dữ liệu thử nghiệm từ Tổ chức Y tế Thế giới cho thấy ít lợi ích từ việc sử dụng remdesivir trong COVID-19 [12]. Tương tự, có những thử nghiệm lâm sàng không chứng minh được lợi ích tử vong của tocilizumab [13–15]. Hơn nữa, mặc dù các thử nghiệm lâm sàng cho thấy lợi ích tử vong do dexamethasone ở những bệnh nhân bị bệnh nặng [5], các thử nghiệm đối với các corticosteroid khác, bao gồm hydrocortisone và methylprednisolone, không cho thấy lợi ích tương tự [16–18].
Ngoài những loại thuốc này, vai trò chống đông máu trong COVID-19 đã được quan tâm lâm sàng đáng kể. COVID-19 có thể khiến người bệnh mắc bệnh huyết khối do một số cơ chế [19]. Do đó, dù được dùng để dự phòng hay điều trị, kháng đông đều có liên quan đến việc giảm tỷ lệ tử vong ở bệnh nhân COVID-19 [20,21].
Giống như các tổ chức khác, hệ thống chăm sóc sức khỏe của chúng tôi đã quan sát thấy sự sụt giảm tỷ lệ tử vong liên quan đến COVID-19 trong những tháng đầu của đại dịch. Do thay đổi mô hình thực hành trong điều trị COVID-19, chúng tôi đã tìm cách khám phá tác động của các cách phối hợp thuốc khác nhau đối với tỷ lệ tử vong. Sử dụng dữ liệu thu được từ hệ thống đa bệnh viện lớn của chúng tôi, chúng tôi đã kiểm tra mối liên quan giữa tỷ lệ tử vong do COVID-19 và các phương pháp điều trị kết hợp và riêng lẻ khác nhau, bao gồm thuốc chống đông máu, remdesivir, corticosteroid, hydroxychloroquine và tocilizumab.
Phương pháp
Đạo đức
Nghiên cứu này đã được phê duyệt bởi Hội đồng Đánh giá Thể chế của Đại học Jefferson (IRB) (phê duyệt giao thức # 20E.846). Nó đã nhận được sự từ bỏ cho sự đồng ý của IRB Đại học Jefferson.
Thiết lập và dân số nghiên cứu
Nghiên cứu được thực hiện như một nghiên cứu thuần tập quan sát, hồi cứu tại Jefferson Health, một hệ thống chăm sóc sức khỏe bao gồm 11 cơ sở nội trú ở đông nam Pennsylvania và nam New Jersey. Nhóm nghiên cứu bao gồm những bệnh nhân dương tính với COVID-19 được nhập viện từ ngày 1 tháng 3 năm 2020 đến ngày 31 tháng 7 năm 2020. Tình trạng dương tính với COVID-19 được xác định bằng sự hiện diện của ít nhất một trong những điều sau: (1) xét nghiệm dương tính với COVID-19 kết quả trong hoặc trong vòng hai mươi mốt ngày kể từ ngày nhập viện; (2) Nhiễm COVID-19 được thêm vào danh sách sự cố điện tử của bệnh nhân trong hoặc trong vòng hai mươi mốt ngày kể từ ngày nhập viện; (3) mã ICD-10 U07.1 được liệt kê là một trong những chẩn đoán cuối cùng của bệnh nhân khi nhập viện.
Kết quả
Tỷ lệ tử vong trong quá trình nhập viện được đánh giá là kết quả chính. Chúng tôi khám phá điều này trong hai bối cảnh. Đầu tiên, chúng tôi đã kiểm tra mối liên quan tổng thể của tỷ lệ tử vong trong bối cảnh phơi nhiễm chính của chúng tôi — các mô hình điều trị bằng thuốc. Để thực hiện điều này, chúng tôi đã tạo ra một mô hình kiểm soát tất cả các biến số bệnh nhân có sẵn, bao gồm nhân khẩu học, thuốc men, đặc điểm nhập viện, mức độ chăm sóc, hỗ trợ hô hấp và bệnh đi kèm.
Thứ hai, chúng tôi khám phá sự thay đổi tỷ lệ tử vong theo thời gian. Đối với điều này, chúng tôi đã sử dụng mô hình, như được mô tả ở trên, để tính toán tỷ lệ tử vong dự đoán cho các giai đoạn “sớm” và “muộn” của đại dịch. Đưa vào nghiên cứu giai đoạn đầu được định nghĩa là tất cả các kỳ nhập viện diễn ra từ ngày 1 tháng 3 năm 2020 đến ngày 30 tháng 4 năm 2020, trong khi đưa vao nghiên cứu giai đoạn sau được định nghĩa là tất cả các kỳ nhập viện diễn ra từ ngày 1 tháng 5 năm 2020 đến ngày 31 tháng 7 năm 2020. Việc phân chia các giai đoạn này dựa trên Ngày 1 tháng 5 năm 2020 cấp phép sử dụng khẩn cấp của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ cho remdesivir [22].
Định nghĩa thuốc sử dụng
Đối với định nghĩa sử dụng thuốc chính, một số loại thuốc đã được đánh giá về mối liên quan của chúng với tỷ lệ tử vong. Những loại thuốc này bao gồm remdesivir, corticosteroid, tocilizumab, thuốc chống đông máu và hydroxychloroquine. Sử dụng thuốc chống đông máu và corticosteroid được định nghĩa là việc sử dụng một loại thuốc trong nhóm thuốc tương ứng trong thời gian nhập viện bất kể chỉ định. Trong trường hợp dùng thuốc chống đông máu, điều này bao gồm bất kỳ việc sử dụng thuốc chống đông máu nào, bất kể thuốc được sử dụng để dự phòng hay điều trị toàn thân.
Để mô tả phác đồ điều trị được áp dụng cho một bệnh nhân nhất định trong thời gian nhập viện, một biến số “kết hợp điều trị” được tạo ra dựa trên cách sử dụng của năm loại thuốc – thuốc chống đông máu, corticosteroid, hydroxychloroquine, remdesivir và tocilizumab. Để tránh đa cộng tuyến, mỗi bệnh nhân chỉ được chỉ định vào một loại phối hợp điều trị. Tất cả các danh mục kết hợp điều trị có số trường hợp nhỏ hơn năm mươi được nhóm vào một danh mục duy nhất, được gắn nhãn “tất cả các kết hợp khác”.
Các biến số quan tâm khác bao gồm nhân khẩu học của bệnh nhân, cụ thể là tuổi, giới tính và chủng tộc; đặc điểm nhập viện, bao gồm thời gian lưu trú và mức độ chăm sóc; hỗ trợ hô hấp/oxy hóa, bao gồm thở máy, sử dụng áp lực đường thở dương liên tục – áp lực đường thở dương 2 mức áp lực, sử dụng ống thông mũi lưu lượng cao (HFNC), và oxy hóa màng ngoài cơ thể; và, các bệnh đi kèm, bao gồm bệnh mạch vành/nhồi máu cơ tim, suy tim sung huyết, bệnh mạch máu ngoại vi, bệnh mạch máu não, sa sút trí tuệ, bệnh phổi mãn tính, bệnh gan nhẹ, bệnh gan vừa hoặc nặng, bệnh tiểu đường có biến chứng, bệnh tiểu đường không có biến chứng, bệnh thận, ung thư, ung thư biểu mô di căn và nhiễm vi rút suy giảm miễn dịch ở người.
Để ước tính tác động của các biến không đo lường được theo thời gian, một biến “khoảng thời gian” nhị phân đã được tạo. Biến số bao gồm hai loại – nhập viện trong thời kỳ đầu và nhập viện trong thời kỳ sau, với các khoảng thời gian được xác định như trên.
Phân tích thống kê
Thống kê mô tả (phương tiện và tỷ lệ) được sử dụng để đánh giá các đặc điểm của bệnh nhân trong giai đoạn nghiên cứu. Phân tích lưỡng biến được thực hiện để kiểm tra mối liên hệ giữa tỷ lệ tử vong với các biến quan tâm bằng cách sử dụng kiểm định Chi-square cho các biến phân loại và kiểm định t cho các biến liên tục.
Hồi quy logistic đa biến được sử dụng để xác định các yếu tố dự báo tử vong cho toàn bộ dân số. Để đánh giá tỷ lệ tử vong cho bệnh nhân theo mức độ nghiêm trọng của bệnh tật, chúng tôi đã chạy mô hình hậu cần cho cả trường hợp nhập viện không chăm sóc đặc biệt (ICU) và nhập viện ICU. Các mô hình được tạo bằng cách sử dụng quy trình lựa chọn ngược cho các hiệp biến. Tất cả các loại kết hợp điều trị đều được đưa vào mô hình, bất kể ý nghĩa thống kê. “Không điều trị” được sử dụng làm giá trị tham chiếu cho biến kết hợp điều trị. Độ mạnh liên kết của tất cả các biến độc lập được biểu thị dưới dạng ước lượng tỷ lệ chênh lệch (OR), khoảng tin cậy (CI) 95% và giá trị p. Để giải quyết các ý nghĩa sai từ nhiều thử nghiệm, chúng tôi đã tính toán các giá trị p đã điều chỉnh bằng cách sử dụng phương pháp Bonferroni giảm dần và phương pháp Benjamini và Hochberg theo từng bước. Ý nghĩa thống kê được đặt ở mức p
Kết quả
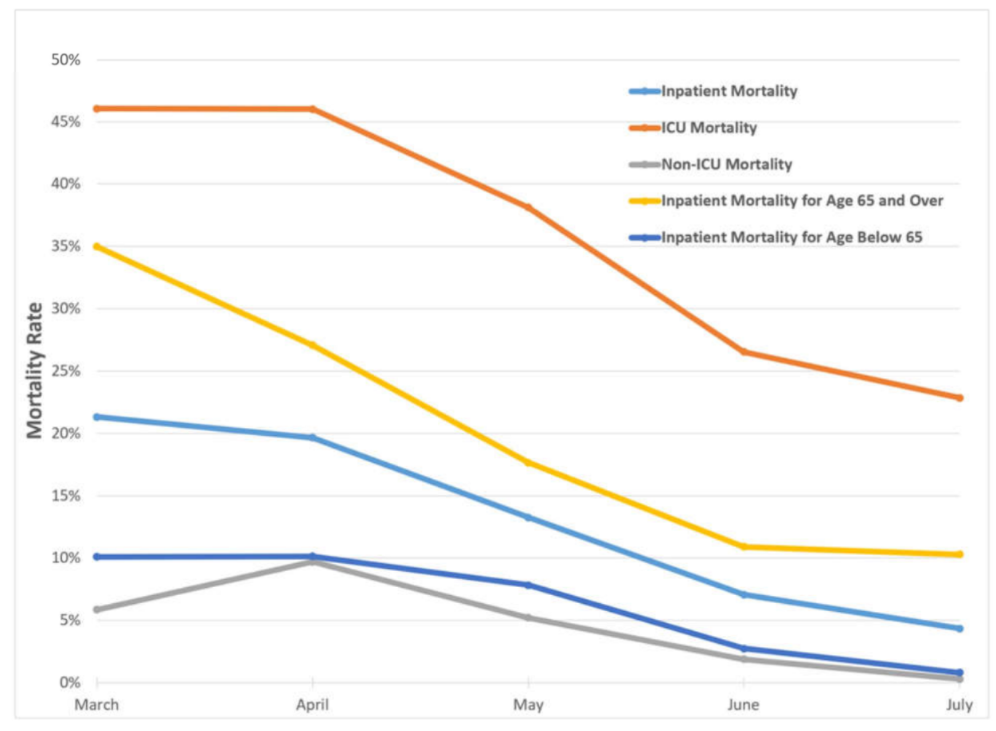
Trong thời gian nghiên cứu, 4.351 bệnh nhân nhập viện với COVID-19, trong đó 664 bệnh nhân tử vong và 3.687 bệnh nhân xuất viện còn sống. Tỷ lệ tử vong nội trú trung bình trong cả giai đoạn là 15,3%. Tuy nhiên, tỷ lệ tử vong chung đã giảm đáng kể từ 21,3% vào tháng 3 năm 2020 xuống 8,8% vào tháng 7 năm 2020 (Hình 1). Tỷ lệ giảm cho cả bệnh nhân ICU và không nhận ICU và bệnh nhân dưới sáu mươi lăm tuổi và sáu mươi lăm tuổi trở lên.
Trong suốt thời gian nghiên cứu, tỷ lệ tử vong nói chung trong hệ thống chăm sóc sức khỏe đã giảm. Sự suy giảm cũng được nhìn thấy bất kể phân tầng theo độ tuổi hoặc mức độ chăm sóc.
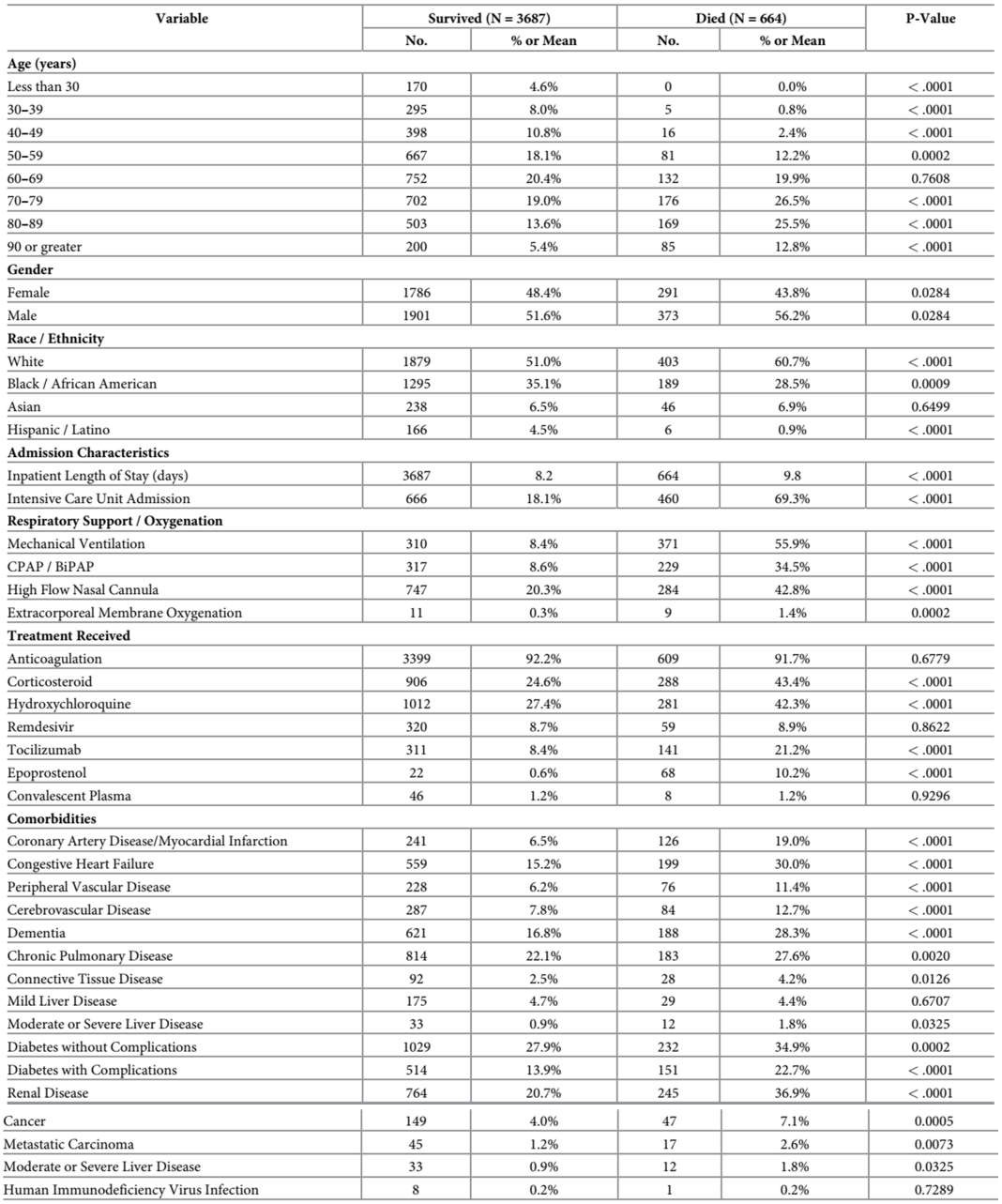
Bảng 1 cung cấp sự so sánh giữa những bệnh nhân sống sót và những người đã chết. Một phân tích lưỡng biến về tỷ lệ tử vong được thực hiện dựa trên các biến số nhân khẩu học và lâm sàng chính. Tuổi trung bình của bệnh nhân sống sót là 62,5, trong khi tuổi trung bình của bệnh nhân tử vong là 74,3 tuổi (p-value
Hình 1. Xu hướng tử vong khi nhập viện COVID-19.
Nhìn chung, những bệnh nhân tử vong có tỷ lệ bệnh tim, phổi, gan và mạch máu cao hơn. Về điều trị, việc sử dụng kháng đông và sử dụng remdesivir không có sự khác biệt đáng kể giữa những người đã chết và những người sống sót. Tuy nhiên, việc sử dụng corticosteroid, hydroxychloroquine, và tocilizumab cao hơn đáng kể trong nhóm bệnh nhân tử vong.
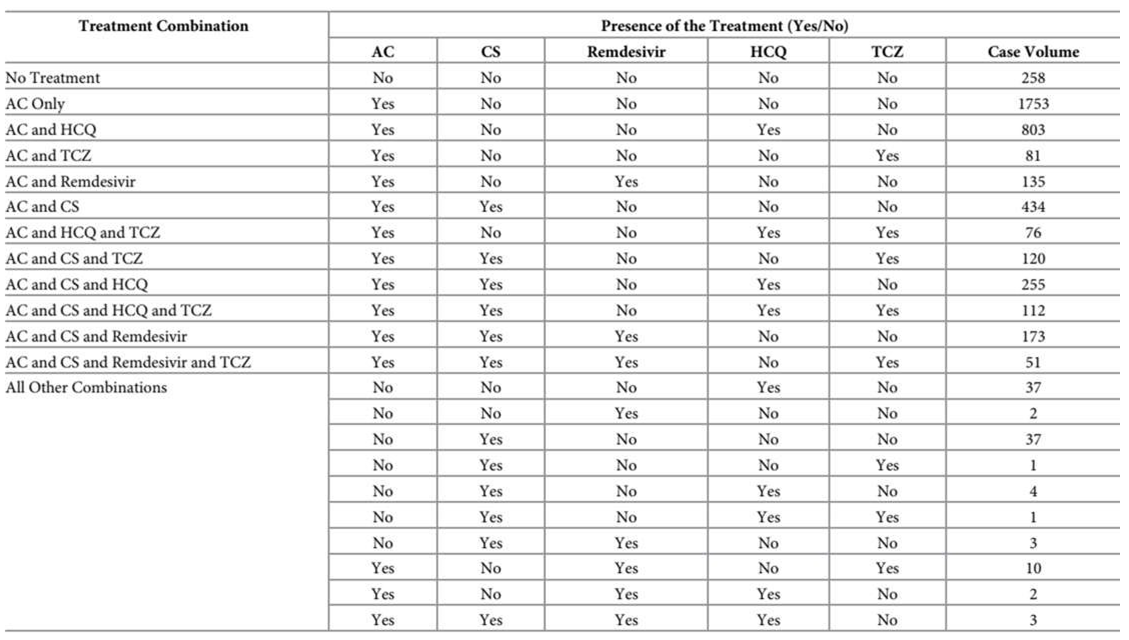
Đối với phân tích đa biến, mười ba loại điều trị được tạo dựa trên các mô hình điều trị quan sát được như trong Bảng 2. Theo số lượng trường hợp, ba kết hợp điều trị hàng đầu là “chỉ chống đông máu” với 1.753 trường hợp (40,3%), “chống đông máu và Hydroxychloroquine” với 803 ca (18,5%) và “chống đông và Corticoid” với 434 ca (10,0%). Mười kết hợp điều trị chứa ít hơn năm mươi bệnh nhân và được thu gọn vào một danh mục duy nhất— “Tất cả các kết hợp khác”. Nhóm “Không điều trị” có 258 trường hợp bệnh nhân (5,9%). Mười ba hạng mục điều trị là độc quyền và chứa một khối lượng đủ để phân tích.
Các giả định chính của hồi quy logistic đa biến đã được đáp ứng, dựa trên các biến phụ thuộc nhị phân và thiếu đa cộng tuyến giữa tất cả các biến độc lập. Các yếu tố lạm phát phương sai đều dưới 2. Thống kê C, giống với diện tích bên dưới đường ROC và đo lường khả năng phân biệt của mô hình, ở mức cao là 0,921. Các thử nghiệm của Hosmer và Lemeshow đã chứng minh rằng mô hình tử vong của bệnh nhân nội trú có Chi-bình phương là 11,4 và giá trị p cao là 0,183, cho thấy rằng mô hình đã được hiệu chỉnh tốt và phù hợp với dữ liệu.
Bảng 1. Đặc điểm nhân khẩu học và lâm sàng của bệnh nhân dương tính với COVID theo tình trạng tử vong.
Bảng 2. Các phối hợp thuốc được sử dụng để điều trị COVID-19.
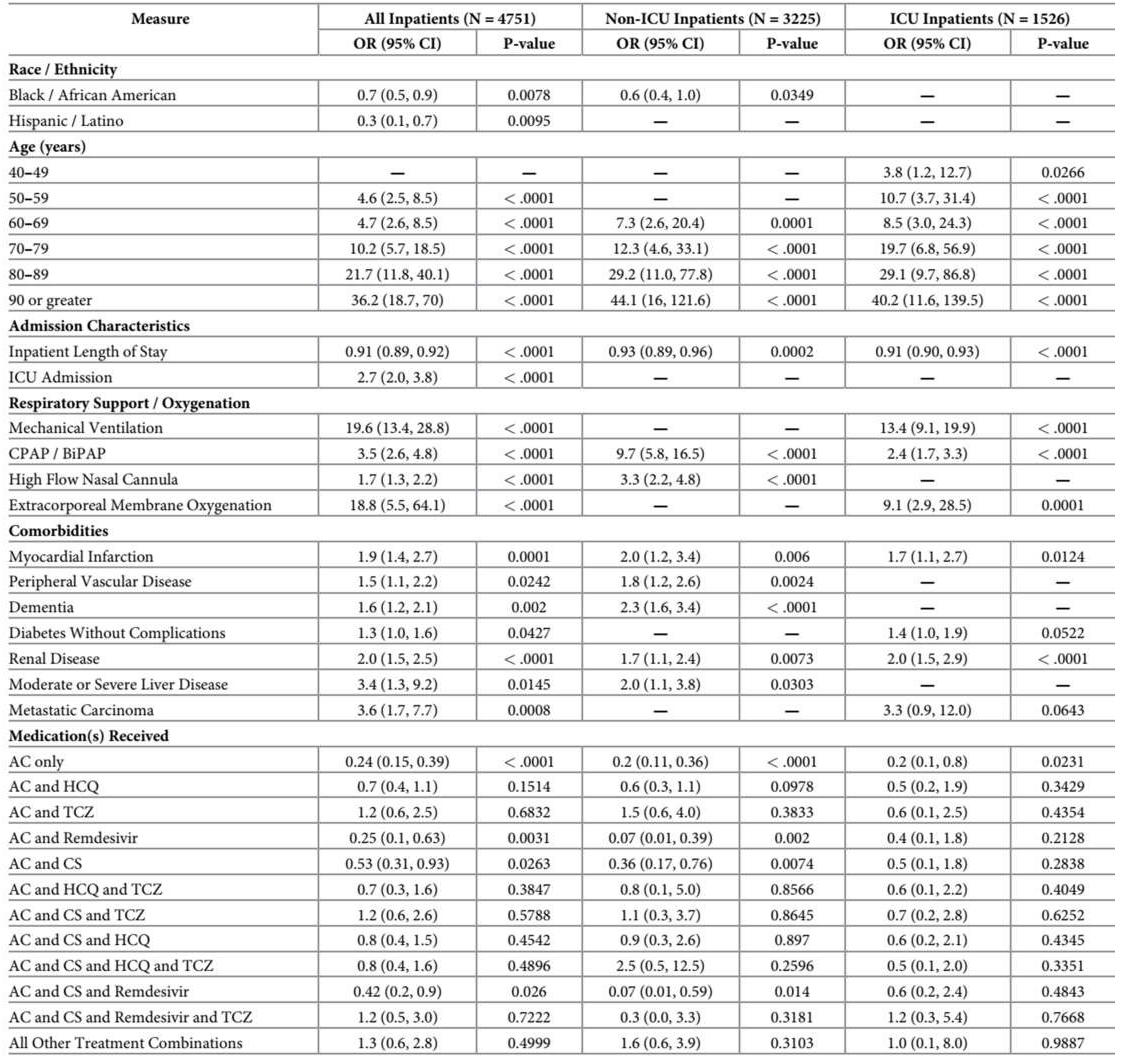
Dân số nghiên cứu được đánh giá, cả tổng thể và phân tầng theo mức độ chăm sóc, cho các yếu tố dự báo tử vong (Bảng 3). Đối với dân số tổng thể, bốn loại thuốc có ước tính tương quan nghịch đáng kể về tỷ lệ tử vong: chỉ chống đông (OR 0,24, p
Tỷ lệ tử vong cũng được đánh giá dựa trên mức độ chăm sóc – bệnh nhân không ICU so với bệnh nhân ICU (Bảng 3). Tỷ lệ tử vong ở bệnh nhân ICU cao hơn nhiều so với bệnh nhân không ICU – tương ứng là 40,9% so với 6,3%. Như trong mô hình của tất cả bệnh nhân nội trú, mô hình không ICU cho thấy rằng bốn sự kết hợp điều trị giống nhau có liên quan đến tỷ lệ tử vong thấp hơn: chỉ chống đông (OR 0,2, p
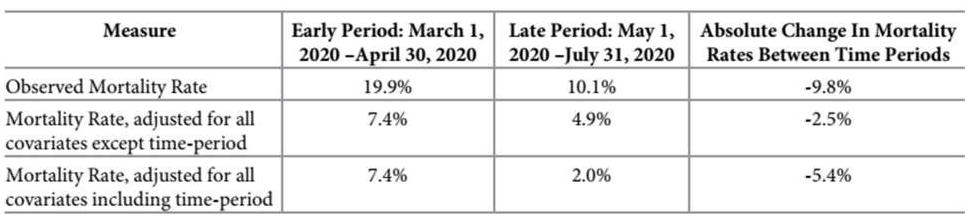
Bảng 4 đưa ra đánh giá định lượng về tác động của các yếu tố không giải thích được đối với sự giảm tỷ lệ tử vong theo thời gian. Sử dụng các thông số ước tính của mô hình và dữ liệu bệnh nhân trong hai khoảng thời gian, chúng tôi đã tính toán tỷ lệ tử vong dự đoán cho các khoảng thời gian sớm và muộn. Trong hàng một của Bảng 4, tỷ lệ tử vong quan sát được được báo cáo trong khoảng thời gian sớm và muộn mà không cần điều chỉnh rủi ro cho bất kỳ hiệp biến quan tâm nào.
Bảng 3. Phân tích đa biến các yếu tố dự báo tử vong ở bệnh nhân COVID-19.
Tỷ lệ tử vong quan sát được giảm từ 19,9% xuống 10,1%. Trong hàng hai, tỷ lệ tử vong được dự đoán trong hai khoảng thời gian dựa trên mô hình đa biến sau khi điều chỉnh cho tất cả các hiệp biến quan tâm, bao gồm nhân khẩu học, đặc điểm lâm sàng và kết hợp điều trị. Tỷ lệ tử vong được điều chỉnh theo rủi ro trong hai giai đoạn lần lượt là 7,4% và 4,9%, thể hiện mức giảm tuyệt đối 2,5% so với tỷ lệ tử vong dự đoán. Khi thêm biến khoảng thời gian vào mô hình đa biến, tỷ lệ tử vong được dự đoán giữa hai khoảng thời gian giảm tuyệt đối là 5,4%.
Bảng 4. Thay đổi tỷ lệ tử vong được điều chỉnh giữa các khoảng thời gian.
Thảo luận
Kể từ khi đại dịch COVID-19 đến Hoa Kỳ, các nhà cung cấp dịch vụ chăm sóc sức khỏe và các nhà nghiên cứu đã tiến hành một phản ứng nhanh chóng [23]. Trong một môi trường lâm sàng luôn thay đổi, việc đo lường kết quả, chẳng hạn như tỷ lệ tử vong, và các yếu tố dự báo của chúng có thể là một thách thức, đặc biệt là trước sự phát triển nhanh chóng của các chiến lược điều trị [24,25]. Thông qua nghiên cứu này, chúng tôi đã điều tra tỷ lệ tử vong bằng cách sử dụng dữ liệu từ một hệ thống chăm sóc sức khỏe lớn được thu thập trong những tháng đầu của đại dịch. Dữ liệu có sẵn không chỉ bao gồm nhân khẩu học và đặc điểm lâm sàng của bệnh nhân mà còn bao gồm các chi tiết liên quan đến các mô hình điều trị bằng thuốc.
Dựa trên quan sát của chúng tôi, thuốc chống đông máu, dù được sử dụng để dự phòng hay điều trị, là những loại thuốc quan trọng nhất để giảm tỷ lệ tử vong ở COVID-19. Điều này phù hợp với cách hiểu hiện tại về COVID-19 là trạng thái tăng đông – một trạng thái có liên quan đến huyết khối, do đó, có thể trực tiếp dẫn đến tử vong [26,27]. Trong nghiên cứu này, chỉ chống đông là loại điều trị duy nhất có liên quan đến việc giảm tỷ lệ tử vong ở cả bệnh nhân ICU và không nhập viện ICU. Hơn nữa, trong khi các kết hợp bao gồm remdesivir và/hoặc corticosteroid có liên quan đến tỷ lệ tử vong thấp hơn trong dân số chung, các ước tính điểm về tỷ lệ tử vong kém hơn so với chỉ dùng kháng đông. Khi dùng tocilizumab và/hoặc hydroxychloroquine trong phác đồ, bất kể sự kết hợp nào, không có lợi ích thống kê đối với tỷ lệ tử vong.
Giống như các tổ chức khác, chúng tôi đã quan sát thấy sự thay đổi trong mô hình điều trị và nhân khẩu học bệnh nhân trong đại dịch COVID-19. Trong nghiên cứu này, chúng tôi đã điều chỉnh ước tính tỷ lệ tử vong của mình không chỉ đối với các mô hình điều trị và đặc điểm của bệnh nhân mà còn cả về khoảng thời gian. Khi được điều chỉnh rủi ro cho tất cả các yếu tố nhân khẩu học và lâm sàng sẵn có, mô hình của chúng tôi dự đoán tỷ lệ tử vong giảm tuyệt đối là 2,5%. Tuy nhiên, chúng tôi lo ngại rằng có những yếu tố khác có thể góp phần vào sự thay đổi tỷ lệ tử vong. Để giải quyết mối lo ngại này, chúng tôi đã đưa một biến khoảng thời gian vào mô hình đã điều chỉnh theo rủi ro. Khi thêm biến khoảng thời gian vào mô hình, tỷ lệ tử vong được dự đoán tuyệt đối giảm thêm 2,9%. Biến khoảng thời gian có ý nghĩa thống kê, cho thấy rằng có những yếu tố khác, không được đo lường trong nghiên cứu của chúng tôi, đã thay đổi trong suốt đại dịch và đã ảnh hưởng đến tỷ lệ tử vong.
Những yếu tố không được đo lường này ảnh hưởng đến tỷ lệ tử vong có thể lấy bệnh nhân làm trung tâm, nhà cung cấp dịch vụ làm trung tâm hoặc liên quan đến những thay đổi của vi rút theo thời gian. Về yếu tố bệnh nhân, dân số nhập viện sớm trong đại dịch có thể khác với dân số nhập viện muộn trong đại dịch. Không rõ sự khác biệt nào là đáng kể, mặc dù các khía cạnh không thể đo lường được của sức khỏe, đặc biệt là những khía cạnh liên quan đến tình trạng kinh tế xã hội hoặc năng lực chức năng, có thể góp phần, tất cả hoặc một phần, làm giảm tỷ lệ tử vong. Về yếu tố nhà cung cấp dịch vụ, đã có một số thay đổi trong tiêu chuẩn chăm sóc, những thay đổi này không được đưa vào làm biến số trong nghiên cứu của chúng tôi. Ví dụ, các phác đồ xử trí ủng hộ HFNC và thông khí không xâm lấn hơn là đặt nội khí quản sớm có thể đã góp phần cải thiện tỷ lệ tử vong [28,29]. Tư thế nằm sấp của bệnh nhân, cả khi sử dụng và không sử dụng máy thở, cũng có thể là một yếu tố [30,31]. Trong khi nghiên cứu của chúng tôi đánh giá nghiêm ngặt sự hiện diện hoặc không có của các phương pháp điều trị, có những thành phần khác của việc quản lý điều trị đã thay đổi theo tiến trình của đại dịch. Ví dụ, các thuật toán cải tiến về chống đông máu [32] có thể góp phần làm giảm tỷ lệ tử vong. Hơn nữa, sự sẵn lòng gia tăng của các nhà cung cấp dịch vụ vào phòng bệnh nhân có thể dẫn đến việc chú ý nhiều hơn đến các chi tiết, phát hiện sớm hơn sự suy giảm lâm sàng và dẫn đến những thay đổi trong điều trị.
Có một số hạn chế trong nghiên cứu của chúng tôi. Mặc dù chúng tôi đã cố gắng nắm bắt gián tiếp các yếu tố gây nhiễu không được đo lường, nhưng đây là một nghiên cứu quan sát không bao gồm một số biến số bệnh nhân quan trọng. Đáng chú ý, tập dữ liệu của chúng tôi không bao gồm dữ liệu nhân khẩu học chi tiết như nghề nghiệp, thu nhập hộ gia đình, cư trú trong môi trường tập trung như viện dưỡng lão hoặc tình trạng kinh tế xã hội. Hơn nữa, nó không bao gồm các biến số lâm sàng như thời gian bệnh nhân có các triệu chứng tại thời điểm xuất hiện, mức độ thiếu oxy của họ hoặc các giá trị xét nghiệm của họ, chẳng hạn như protein phản ứng C hoặc D-dimer, tất cả đều có thể dự đoán tỷ lệ tử vong ở Tuyển sinh liên quan đến COVID [33–36].
Hơn nữa, phân tích của chúng tôi về các kết hợp điều trị rất rộng. Nó chỉ chứa giá trị nhị phân của điều trị ít nhất một lần trong quá trình nhập viện. Trong bộ dữ liệu của chúng tôi, không có thông tin nào liên quan đến liệu trình điều trị, liều lượng hoặc thời gian. Có những hạn chế đặc biệt liên quan đến phân tích của chúng tôi về việc sử dụng thuốc chống đông máu và corticosteroid. Theo nghiên cứu của chúng tôi, chống đông máu bao gồm nhiều loại thuốc và liều lượng. Hơn nữa, thuốc kháng đông được kê đơn theo sự kết hợp của các hướng dẫn của cơ sở và sự tùy ý của người kê đơn, điều này có thể góp phần làm thay đổi liều lượng. Các chiến lược dùng thuốc chống đông máu quốc gia vẫn đang được hoàn thiện dựa trên dữ liệu thử nghiệm hiện có [37]. Tương tự như vậy, việc sử dụng corticosteroid, theo định nghĩa của nghiên cứu của chúng tôi, cũng chứa các corticosteroid khác nhau với các hiệu lực khác nhau. Liều corticosteroid được sử dụng cho những bệnh nhân cụ thể có thể không tương đương với liều dexamethasone đã trở thành tiêu chuẩn chăm sóc cho COVID-19. Các nghiên cứu trong tương lai sẽ cần khám phá các phương pháp điều trị riêng lẻ chi tiết hơn.
Tóm lại, chúng tôi đã trình bày một phân tích hồi cứu về tỷ lệ tử vong liên quan đến COVID-19 ở những bệnh nhân nhập viện trong một hệ thống chăm sóc sức khỏe lớn ở đông bắc Hoa Kỳ. Trong giai đoạn đầu của đại dịch, tỷ lệ tử vong ở Hoa Kỳ, nói chung và trên toàn Jefferson Health, cụ thể là đã giảm. Để hiểu được sự suy giảm này, chúng tôi đã tạo ra các mô hình để kiểm tra các yếu tố dự đoán tỷ lệ tử vong ở bệnh nhân nhập viện. Nghiên cứu này phát hiện ra rằng chống đông máu là một đóng góp quan trọng vào sự sống còn của những bệnh nhân nhập viện với COVID-19. Hơn nữa, nghiên cứu này gợi ý rằng việc bổ sung remdesivir và corticosteroid, dù đơn lẻ hoặc kết hợp, để chống đông máu có thể làm tăng tỷ lệ tử vong ở những bệnh nhân nhập viện ICU. Hơn nữa, việc bổ sung tocilizumab vào thuốc chống đông máu dường như làm vô hiệu hóa lợi ích có ý nghĩa thống kê của thuốc kháng đông đối với tỷ lệ tử vong trong nhóm thuần tập của chúng tôi. Điều này hỗ trợ các thử nghiệm lâm sàng chống lại hiệu quả của phương pháp điều trị này. Mặc dù sự sụt giảm tỷ lệ tử vong của hệ thống chăm sóc sức khỏe của chúng tôi một phần có thể liên quan đến các yếu tố nhân khẩu học và lâm sàng được khám phá trong nghiên cứu này, nhưng có nhiều yếu tố bổ sung đã góp phần làm giảm tỷ lệ tử vong. Những điều này sẽ cần được khám phá thông qua các phân tích trong tương lai về dân số bệnh nhân của chúng tôi.
References
1.Centers for Disease Control and Prevention: NCHS Mortality Surveillance Data. https://wwwcdcgov/coronavirus/2019ncov/covid-data/covidview/07102020/nchs-mortality-reporthtml. Accessed 3/29/2021.
2.Asch DA, Sheils NE, Islam MN, Chen Y, Werner RM, Buresh J, et al. Variation in US Hospital Mortality Rates for Patients Admitted With COVID-19 During the First 6 Months of the Pandemic. JAMA internal medicine. 2020:e208193. pmid:33351068.
3.Boehmer TK DJ, Caruso E, et al. Changing Age Distribution of the COVID-19 Pandemic—United States, May–August 2020. MMWR Morbidity and mortality weekly report. ePub: 23 September 2020.
4.Rosenthal N, Cao Z, Gundrum J, Sianis J, Safo S. Risk Factors Associated With In-Hospital Mortality in a US National Sample of Patients With COVID-19. JAMA Network Open. 2020;3(12):e2029058–e. pmid:33301018
5.Dexamethasone in Hospitalized Patients with Covid-19—Preliminary Report. New England Journal of Medicine. 2020. pmid:32678530
6.Radbel J, Narayanan N, Bhatt PJ. Use of Tocilizumab for COVID-19-Induced Cytokine Release Syndrome: A Cautionary Case Report. Chest. 2020;158(1):e15–e9. Epub 2020/04/25. pmid:32343968.
7.Beigel JH, Tomashek KM, Dodd LE, Mehta AK, Zingman BS, Kalil AC, et al. Remdesivir for the Treatment of Covid19—Preliminary Report. N Engl J Med. 2020. Epub 2020/05/24. pmid:32445440; PubMed Central PMCID: PMC7262788.
8.Geleris J, Sun Y, Platt J, Zucker J, Baldwin M, Hripcsak G, et al. Observational Study of Hydroxychloroquine in Hospitalized Patients with Covid-19. The New England journal of medicine. 2020;382(25):2411–8. Epub 2020/05/08. pmid:32379955; PubMed Central PMCID: PMC7224609.
9.Li M, Yoo EJ, Baram M, McArthur M, Skeehan C, Awsare B, et al. Tocilizumab in the Management of COVID-19: A Preliminary Report. Am J Med Sci. 2021;361(2):208–15. Epub 2020/12/29. pmid:33358502; PubMed Central PMCID: PMC7649658.
10.Beigel JH, Tomashek KM, Dodd LE, Mehta AK, Zingman BS, Kalil AC, et al. Remdesivir for the Treatment of Covid19—Preliminary Report. New England Journal of Medicine. 2020. pmid:32445440
11.Tocilizumab in patients admitted to hospital with COVID-19 (RECOVERY): preliminary results of a randomised, controlled, open-label, platform trial. https://wwwmedrxivorg/content/101101/2021021121249258v1. Accessed 3/29/21.
12.Repurposed antiviral drugs for COVID-19 –interim WHO SOLIDARITY trial results. https://wwwmedrxivorg/content/101101/2020101520209817v1. Accessed 10/25/2020.
13.Stone JH, Frigault MJ, Serling-Boyd NJ, Fernandes AD, Harvey L, Foulkes AS, et al. Efficacy of Tocilizumab in Patients Hospitalized with Covid-19. The New England journal of medicine. 2020;383(24):2333–44. Epub 2020/10/22. pmid:33085857; PubMed Central PMCID: PMC7646626.
14.Hermine O, Mariette X, Tharaux PL, Resche-Rigon M, Porcher R, Ravaud P. Effect of Tocilizumab vs Usual Care in Adults Hospitalized With COVID-19 and Moderate or Severe Pneumonia: A Randomized Clinical Trial. JAMA internal medicine. 2021;181(1):32–40. Epub 2020/10/21. pmid:33080017; PubMed Central PMCID: PMC7577198.
15.Salvarani C, Dolci G, Massari M, Merlo DF, Cavuto S, Savoldi L, et al. Effect of Tocilizumab vs Standard Care on Clinical Worsening in Patients Hospitalized With COVID-19 Pneumonia: A Randomized Clinical Trial. JAMA internal medicine. 2021;181(1):24–31. Epub 2020/10/21. pmid:33080005; PubMed Central PMCID: PMC7577199.
16.Angus DC, Derde L, Al-Beidh F, Annane D, Arabi Y, Beane A, et al. Effect of Hydrocortisone on Mortality and Organ Support in Patients With Severe COVID-19: The REMAP-CAP COVID-19 Corticosteroid Domain Randomized Clinical Trial. Jama. 2020;324(13):1317–29. Epub 2020/09/03. pmid:32876697.
17.Dequin PF, Heming N, Meziani F, Plantefève G, Voiriot G, Badié J, et al. Effect of Hydrocortisone on 21-Day Mortality or Respiratory Support Among Critically Ill Patients With COVID-19: A Randomized Clinical Trial. Jama. 2020;324(13):1–9. Epub 2020/09/03. pmid:32876689.
18.Jeronimo CMP, Farias MEL, Val FFA, Sampaio VS, Alexandre MAA, Melo GC, et al. Methylprednisolone as Adjunctive Therapy for Patients Hospitalized With COVID-19 (Metcovid): A Randomised, Double-Blind, Phase IIb, Placebo-Controlled Trial. Clinical infectious diseases: an official publication of the Infectious Diseases Society of America. 2020. Epub 2020/08/14. pmid:32785710; PubMed Central PMCID: PMC7454320.
19.Bikdeli B, Madhavan MV, Jimenez D, Chuich T, Dreyfus I, Driggin E, et al. COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-Up: JACC State-of-the-Art Review. J Am Coll Cardiol. 2020;75(23):2950–73. Epub 2020/04/21. pmid:32311448; PubMed Central PMCID: PMC7164881.
20.Tang N, Bai H, Chen X, Gong J, Li D, Sun Z. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Thromb Haemost. 2020;18(5):1094–9. Epub 2020/03/29. pmid:32220112.
21.Paranjpe I, Fuster V, Lala A, Russak AJ, Glicksberg BS, Levin MA, et al. Association of Treatment Dose Anticoagulation With In-Hospital Survival Among Hospitalized Patients With COVID-19. J Am Coll Cardiol. 2020;76(1):122–4. Epub 2020/05/11. pmid:32387623; PubMed Central PMCID: PMC7202841.
22.Fact Sheet for Patients And Parents/Caregivers: Emergency Use Authorization (EUA) Of Veklury® (remdesivir) For Coronavirus Disease 2019 (COVID-19). https://wwwfdagov/media/143190/download Accessed 11/2/2020.
23.Collins FS, Stoffels P. Accelerating COVID-19 Therapeutic Interventions and Vaccines (ACTIV): An Unprecedented Partnership for Unprecedented Times. Jama. 2020;323(24):2455–7. pmid:32421150
24.Zylke JW, Bauchner H. Mortality and Morbidity: The Measure of a Pandemic. Jama. 2020;324(5):458–9. pmid:32609308
25.Characterisation WHOWGotC, Management of C-i. A minimal common outcome measure set for COVID-19 clinical research. The Lancet Infectious diseases. 2020;20(8):e192–e7. Epub 2020/06/12. pmid:32539990.
26.Menter T, Haslbauer JD, Nienhold R, Savic S, Hopfer H, Deigendesch N, et al. Postmortem examination of COVID-19 patients reveals diffuse alveolar damage with severe capillary congestion and variegated findings in lungs and other organs suggesting vascular dysfunction. Histopathology. 2020. Epub 2020/05/05. pmid:32364264.
27.Wichmann D, Sperhake JP, Lütgehetmann M, Steurer S, Edler C, Heinemann A, et al. Autopsy Findings and Venous Thromboembolism in Patients With COVID-19: A Prospective Cohort Study. Ann Intern Med. 2020;173(4):268–77. Epub 2020/05/07. pmid:32374815; PubMed Central PMCID: PMC7240772.
28.Schünemann HJ, Khabsa J, Solo K, Khamis AM, Brignardello-Petersen R, El-Harakeh A, et al. Ventilation Techniques and Risk for Transmission of Coronavirus Disease, Including COVID-19: A Living Systematic Review of Multiple Streams of Evidence. Ann Intern Med. 2020;173(3):204–16. Epub 2020/05/23. pmid:32442035; PubMed Central PMCID: PMC7281716.
29.Update Alert: Ventilation Techniques and Risk for Transmission of Coronavirus Disease, Including COVID-19. Annals of Internal Medicine. 2020;173(6):W122. pmid:32735446
30.Sartini C, Tresoldi M, Scarpellini P, Tettamanti A, Carcò F, Landoni G, et al. Respiratory Parameters in Patients With COVID-19 After Using Noninvasive Ventilation in the Prone Position Outside the Intensive Care Unit. Jama. 2020;323(22):2338–40. Epub 2020/05/16. pmid:32412606; PubMed Central PMCID: PMC7229533.
31.Pan C, Chen L, Lu C, Zhang W, Xia JA, Sklar MC, et al. Lung Recruitability in COVID-19-associated Acute Respiratory Distress Syndrome: A Single-Center Observational Study. American journal of respiratory and critical care medicine. 2020;201(10):1294–7. Epub 2020/03/24. pmid:32200645; PubMed Central PMCID: PMC7233342.
32.Thachil J, Tang N, Gando S, Falanga A, Cattaneo M, Levi M, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. J Thromb Haemost. 2020;18(5):1023–6. Epub 2020/04/28. pmid:32338827.
33.Tenforde MW, Kim SS, Lindsell CJ, Billig Rose E, Shapiro NI, Files DC, et al. Symptom Duration and Risk Factors for Delayed Return to Usual Health Among Outpatients with COVID-19 in a Multistate Health Care Systems Network— United States, March-June 2020. MMWR Morbidity and mortality weekly report. 2020;69(30):993–8. Epub 2020/07/31. pmid:32730238.
34.Gupta S, Hayek SS, Wang W, Chan L, Mathews KS, Melamed ML, et al. Factors Associated With Death in Critically Ill Patients With Coronavirus Disease 2019 in the US. JAMA internal medicine. 2020. pmid:32667668
35.Vidali S, Morosetti D, Cossu E, Luisi MLE, Pancani S, Semeraro V, et al. D-dimer as an indicator of prognosis in SARS-CoV-2 infection: a systematic review. ERJ Open Res. 2020;6(2). Epub 2020/07/21. pmid:32685436.
36.Luo X, Zhou W, Yan X, Guo T, Wang B, Xia H, et al. Prognostic Value of C-Reactive Protein in Patients With Coronavirus 2019. Clinical Infectious Diseases. 2020. pmid:32445579
37.Cuker A, Tseng EK, Nieuwlaat R, Angchaisuksiri P, Blair C, Dane K, et al. American Society of Hematology 2021 guidelines on the use of anticoagulation for thromboprophylaxis in patients with COVID-19. Blood Adv. 2021;5(3):872– 88. Epub 2021/02/10. pmid:33560401; PubMed Central PMCID: PMC7869684.