Đại cương
Thuốc bảo vệ phóng xạ (BVPX) là những thuốc khi đưa vào cơ thể (trước khi chiếu xạ) có tác dụng tăng đề kháng chống PX của cơ thể, hạn chế hoặc giảm nhẹ các tổn thương do phóng xạ gây ra và tăng cường khả năng phục hồi các tổn thương đó.
Tình huống sử dụng:
Trong chiến tranh: có sử dụng VKHN, thuốc được sử dụng:
Khi có báo động chiến tranh hạt nhân
Trước khi vào hoạt động trong khu vực nhiễm xạ
Khi làm việc ở các bãi, trạm xử lý VS, tiếp nhận thương binh từ khu vực nhiễm xạ trở về.
Trong thời bình: thuốc được sử dụng trong các ngành công nghiệp, nông nghiệp, KHKT vũ trụ, y học mà con người bắt buộc phải tiếp xúc với PX. Người ta thường chia thành 3 nhóm ngành nghề phải tiếp xúc với PX:
Những người làm ở các cơ sở sản xuất chất PX như: mỏ uran, nhà máy xử lý quặng và tách ĐVPX, các lò phản ứng nguyên tử hay trung tâm nghiên cứu về PX, điện hạt nhân, đơn vị vận chuyển và chứa chất PX.
Những người sử dụng các tia bức xạ ion hoá từ những ĐVPX:
Trong công nghiệp:
Đo độ dày, độ ẩm, tỷ trọng… kỹ thuật dựa vào tính đâm xuyên của tia phóng xạ
Chụp bằng tia gamma để xác định cấu trúc bên trong của vật thể như kim loại, gỗ, beton… để tìm khuyết tật.
Dùng PX làm chất chỉ thị đánh dấu… tìm đường đi của mạch nước ngầm, chỗ hở của đường ống nước…
Trong sinh học và sinh hoá:
Làm chất chỉ điểm để nghiên cứu hiện tượng sinh lý động vật hay thực vật (C14; S-35; I-131)
Khử trùng bảo quản thực phẩm, dụng cụ, nước…
Trong y học:
Dùng trong chẩn đoán, thăm dò chức năng, đánh giá tình trạng một số cơ quan. Các cơ quan này giữ lại một cách chọn lọc các nguyên tố PX…
Tia xạ trong, xạ ngoài điều trị bệnh
Xác định thành phần các chế phẩm dược
Trong nông nghiệp:
Nghiên cứu cáchiện tượng sinh lý thực vật, triệt sản
Nghiêncứu biến dị, kích thích tăng trưởng, diệt nấm…
Những người sử dụng máy phát tia X.
Tình hình nc thuốc bvpx trên thế giới và trong nước
Giai đoạn 1: từ 1942-1951 là giai đoạn của việc tìm kiếm các thuốc BVPX, từ việc phát hiện tác dụng bảo vệ trên men, trên vi khuẩn, trên động vật, năm 1949 Patt H.M. và CS. thuộc phòng thí nghiệm Argoone (Chicago) cho thấy Cystein có tác dụng BVPX, chuột nhắt được uống cystein sống nhiều hơn nhóm chứng. Đây được coi như công trình nghiên cứu đầu tiên về thuốc BVPX. Năm 1951 Bacq Z.M và CS. chứng minh cysteamin và cystamin là 2 loại thuốc có tác dụng BVPX về sau được ứng dụng trên lâm sàng.
Giai đoạn 2: từ 1952-1961 hàng loạt thuốc mới được thí nghiệm, ngoài thành tựu của Doherty D. và Burnett W. (1955) công bố tác dụng BVPX của aminoethylisothiouronium – (AET), các chất khác có hiệu lực thấp hơn cystein và cysteamin. AET khi áp dụng thử trên người thấy có nhiều tai biến .
Giai đoạn 3: Từ năm 1962 trở lại đây, trong những năm 60 phát hiện thêm những thuốc mới có tác dụng bảo vệ khá mạnh thuộc nhóm Thiophosphat. Nói chung, những thuốc BVPX đầu tiên được nghiên cứu thường chỉ có tác dụng ngắn hạn. Những năm 70 đã nghiên cứu được một số thuốc có tác dụng bảo vệ kéo dài như Thiazolidine (duy trì tác dụng khoảng 6 giờ).
Các tác giả thường nghiên cứu kết hợp các thuốc với nhau chẳng hạn như Cystamin với Etiron, Cystamin với Gutimin, Cystein với Mexamin…
Các thuốc BVPX còn có những nhược điểm, chưa đáp ứng được yêu cầu, đó là:
Thuốc mới có hiệu lực với thể bệnh phóng xạ cấp tính mức độ vừa và nhẹ. Với bệnh phóng xạ cấp tính mức độ nặng (thể não, thể ruột) thì thuốc không đạt hiệu quả. Chưa có thuốc cho bệnh phóng xạ mạn tính.
Các thuốc BVPX hiện có hầu như không có tác dụng trong trường hợp vị chiếu bởi chùm neutron.
Thuốc BVPX hầu như không có hiệu lực bảo vệ, ngăn chặn những hậu quả xa của tổn thương do phóng xạ.
Các thuốc BVPX hoá học nói chung đều có độc tính, dùng nhiều lần không có lợi. Đôi khi thuốc BVPX hoá học còn làm tăng độc tính của một số thuốc và hoá chất khác.
tình hình nghiên cứu thuốc bvpx trên thế giới
Xu hướng nghiên cứu trong những năm gần đây là tìm các chất có hiệu lực cao, một mặt tìm thêm thuốc BVPX mới, mặt khác vẫn phải sử dụng những thuốc tốt hiện có nhưng phối hợp với những chất khác để tăng hiêụ lực, giảm độc tính. Hướng thứ hai hiện nay là nghiên cứu các thuốc có khả năng điều biến đáp ứng sinh học (Biological Response Modifier – BRM). Theo hướng này có hàng trăm các chế phẩm sinh học được thử, có nhiều chất có hiệu lực BVPX tốt. Phần lớn các thuốc này là các chất sinh thích nghi, có khả năng tăng cường miễn dịch của cơ thể, tăng sức đề kháng, chống lại các tác nhân độc hại nói chung và đề kháng chống phóng xạ nói riêng. Các thuốc BRM thông thường là những thuốc bổ, không độc hại, có tác dụng chậm hơn nhưng lại duy trì được lâu hơn .
Các BRM có tác dụng giúp cho cơ thể tăng cường sức đề kháng, chống lại bệnh tật. Các nhà nghiên cứu tìm kiếm nhiều BRM dùng trong điều trị ung thư, nhất là kết hợp với xạ trị và hoá trị liệu. BRM tăng cường khả năng hồi phục các tế bào bị tổn thương do ung thư, do tia xạ…
Nghiên cứu về thuốc BVPX có nguồn gốc tự nhiên đang được các nhà khoa học trên thế giới quan tâm, nhất là ở Nga.
Ogrưzov thấy dịch chiết của cây Salsolapestyera và Tamarixra-mosisima, Crostachus spinosa có tác dụng tăng tỷ lệ sống sót của chuột lên từ 35-100% sau chiếu xạ 7Gy.
Goncharenko E.N., Kudriasov, Antonova, Mazhul (1995) đã nghiên cứu chất MIGI-K (Mytilis Galloprovincialis) thu được bằng thuỷ phân thịt một loài nhuyễn thể trong môi trường axit. Trong MIGI-K có các axit amin, melanoidin, một số nguyên tố vi lượng: Co, Cu, Zn, Mn, Fe… Các axit amin có khả năng tăng kháng xạ của cơ thể, melanoidin có hoạt tính chống oxy hoá, còn các nguyên tố vi lượng cần thiết để thực hiện các chức năng miễn dịch, tạo máu và một số chức năng quan trọng khác của cơ thể .
Vasin và Antipov cho biết Indraline tăng khả năng kháng xạ của các tế bào hệ tạo máu, giảm sự rối loạn nhiễm sắc thể của tuỷ xương, tăng khả năng hồi phục tuỷ xương và lách, tái tạo BC, HC và TC nhanh hơn. HS giảm liều >1,5 .
Trong mươi năm gần đây, sự ô nhiễm phóng xạ ở một số nước như Ucraina sau thảm hoạ Chernobyl đã đặt ra nhiệm vụ: tìm biện pháp BVPX cho những người bị chiếu xạ liều thấp, trường diễn trong điều kiện tự nhiên .
Quan trọng là làm sao có được những chất có nguồn gốc tự nhiên (động vật, thực vật) có thể dùng trong điều kiện bị chiếu xạ liều thấp, trường diễn. Các chất này phải không độc, có khả năng duy trì hiệu lực tác dụng tương đối lâu và dùng dưới dạng “ăn, uống” được. Chúng làm tăng các phản ứng không đặc hiệu của cơ thể, tăng sức đề kháng, có tính giải độc và sinh thích nghi, có khả năng kích thích hệ tạo máu, hệ miễn dịch, tác dụng lên hệ thần kinh nội tiết, tăng các amin sinh học, các thiol, giảm các chất cảm xạ nội sinh- sản phẩm của quá trình oxy hoá lipit (các peroxit) .
Gần đây, còn có một hướng mới nữa là dùng các chất có nguồn gốc vi sinh để nâng cao tính kháng xạ của cơ thể. Các chất có nguồn gốc vi sinh thường có hoạt tính sinh học cao, chúng kích thích tạo kháng thể, tăng cường chức năng thực bào của bạch cầu, kích thích tái tạo tế bào máu, tăng số lượng tiểu cầu, hồng cầu lưới, tăng các quần thể tạo huyết ở lách, tuỷ xương…
Tác dụng có lợi của các sản phẩm vi sinh lên hệ tạo máu có thể được thực hiện thông qua hệ miễn dịch. Điều hoà hệ tạo máu bởi các cơ chế miễn dịch nhờ các lympho bào T và đại thực bào. Các tế bào này khi được kích thích sẽ tiết một số yếu tố chủ yếu điều khiển quá trình tạo máu GM-CSF, M-CSF và G-CSF, hoặc tiết các yếu tố tác động lên quá trình tăng sinh và biệt hoá cũng như chức năng của nhiều loại tế bào miễn dịch như interleukin-1, g-interferon.
Vladimirov [64] sử dụng vacxin và các chất có nguồn gốc vi khuẩn tiêm vào cơ thể trước khi chiếu xạ để tăng sức đề kháng cho cơ thể đồng thời tăng khả năng kháng xạ của cơ thể. Dupliseva và một số tác giả nhận thấy polysaccarit của vi khuẩn thương hàn, các kháng nguyên nội độc tố phó thương hàn nhóm B đều có tác dụng BVPX. Hàng loạt các nghiên cứu theo hướng này cho thấy các polysaccarit tách từ vi khuẩn đường ruột, từ nấm men Sacharomyces cerevisiae hoặc một số độc tố của một số vi khuẩn đều có hiệu lực BVPX tương đối tốt. Stelnikov đã tổng kết được có khoảng 80 loại vacxin và các sản phẩm vi sinh có khả năng BVPX thể hiện qua tỷ lệ động vật sống sót sau chiếu xạ được tăng lên.
Một số thuốc khác có nguồn gốc thực vật và động vật đã được các tác giả nước ngoài quan tâm nghiên cứu như: antoxian tách chiết từ cánh hoa hồng Bungari, mật ong, nọc rắn, lách rùa Trung Á…
Khalikov, Rakhimov nghiên cứu tác dụng của nọc rắn Naja naja axiana, với các liều 50, 100, 150, 250 microgam/kg thấy chúng có tác dụng tăng tỷ lệ sống sót của chuột sau chiếu xạ lên 40-65% so với nhóm chứng .
Akhmadieva công bố antoxan (pelapronidin 3,5-diglucozit) đạt HSGL =1,7. Krasilnikov [80] thấy vikanin thuộc nhóm alcaloit, dẫn xuất của lindol, là một phomat thực vật, tăng tỷ lệ sống sót ở chuột cống trắng sau chiếu xạ liều 7,5Gy lên từ 24-65%.
Turdiev, Prus đã tách protein từ lách rùa Trung Á thấy chúng có tác dụng BVPX, tăng tỷ lệ sống sót của chuột, HSGL =1,46. Xeverin và CS nhận thấy cacnozin (một chất nội sinh có hàm lượng lớn trong cơ, xương của động vật có xương sống) có tác dụng tăng tỷ lệ sống sót của chuột nhắt lên 55%.
Lee và Yang (1999) nghiên cứu 2 bài thuốc cổ truyền Trung Quốc si-wu-tang và si-jun-zi-tang thấy si-wu-tang tăng cường tạo máu, si-jun-zi-tang là bài thuốc tăng lực. si-wu-tang có khả năng kéo dài thời gian sống thêm, hình thành quần thể lách nội sinh. Tác dụng BVPX của si-wu-tang có thể là chất chiết từ Danggui và Baishaoyao. Si-wu-tang có tác dụng BVPX rõ hơn, chúng lại là chế phẩm tự nhiên không độc
Kim K.C cho biết nước quả (dịch thân cây) của Ganoderma lucidum được dùng dự phòng và điều trị một số bệnh ở Á Đông. Chúng có khả năng chống ung thư, tăng cường miễn dịch, không gây độc mô, do đó có thể dự phòng chống oxy hoá. Polysaccharide tách từ Ganoderma lucidum có tác dụng tương tự, như vậy hỗn hợp polysaccharide có tác dụng chống PX.
Hai loại flavonoids orientin và vicentin chiết từ một loại lá cây ở Ấn Độ tiêm tĩnh mạch 50microg/kg 30 phút trước chiếu xạ. Vicentin khá hơn (không nhiều) orientin kéo dài thời gian sống thêm của chuột. Hệ số giảm liều (Dose modification factors -DMF) với vicentin là 1,37, orientin là 1,30. Cơ chế quét gốc tự do được bàn đến. So sánh với aminothiol (WR-2721) thấy có tác dụng tương đương, giảm tổn thương biến loạn nhiễm sắc thể tế bào tuỷ xương. Liều sử dụng cách xa liều độc, do đó có thể ocimum flavonoid sẽ là một thuốc BVPX ứng dụng cho người. Jagetia và Aruna nghiên cứu một loại chế phẩm thảo mộc abana thấy rằng nếu cho chuột uống trước khi chiếu xạ với liều 20mg/kg có thể giảm tần suất nhiễm sắc đa nhân khoảng 4 lần so với nhóm chứng.
Aminothiol (ký hiệu WR-1065) có tác dụng giảm tần suất biến loạn nhiễm sắc thể do chiếu xạ khi thử nghiệm in vitro đối với các lympho bào người với liều chiếu 3Gy tia gamma của nguồn Cs-137. Dùng bổ sung WR-1065 3 giờ sau chiếu xạ còn tăng thêm khả năng chống biến loạn nhiễm sắc thể. WR-1065 và các aminothiol tương tự có khả năng chống lại tác động gây biến loạn nhiễm sắc thể của bức xạ ion hoá giống như polyamine, tức là ổn định cấu trúc chromatin, ức chế phân chia tế bào, tác dụng tích cực đến quá trình tái thiết DNA.
Dùng các chất chống oxy hoá để hạn chế tổn thương nội bào do gốc tự do gây ra đang là sự quan tâm của nhiều nhà nghiên cứu. Dung dịch 2′, 7′ – dichlorofluorescin diacetate (DCFH-DA) khi bị chiếu xạ 10Gy nguồn Co-60 đã tăng vận tốc chuyển thành 2′,7′ dichlorofluorescein (DCF).
Ganasoundari, Devi và Rao cho biết dịch chiết một loại lá Ocimum sanctum thử nghiệm trên chuột chiếu xạ 1-6Gy, dùng 10mg/kg trong 5 ngày, lần cuối 30 phút trước chiếu xạ đã giảm các biến loạn nhiễm sắc thể (cả dicentric, chuỗi) hiệu ứng giảm liều đạt 2,63 đối với liều chiếu 2Gy. Liều chiếu dưới 3Gy, thuốc có tác dụng hồi phục các biến đổi nhiễm sắc thể trong 2 ngày. Dịch chiết Ocimum giảm gốc tự do hydroxyl.
Indomethafen (IM) có khả năng kích thích tổng hợp DNA, RNA và các protein ở chuột. IM giảm nhẹ tổn thương do phóng xạ, kích thích tổng hợp protein và DNA bù đắp lại sự suy giảm hoạt tính RNA-reductase ở lách, tăng hàm lượng Fe-transferrin, cytochrome-C, cytochrome P-450, kích thích tổng hợp ATP, tăng các phản ứng bù trừ ở lách .
Spencer và Goa công bố Amifostine (ký hiệu WR-2721) có khả năng chống lại các tổn thương phóng xạ trên động vật. Chiu S., Oleinick N.L cho biết Spesmine là chất BVPX có hiệu quả của plasmid hoặc của axit nhân virus với cơ chế quét gốc tự do.
Akiyama M. nghiên cứu hậu quả muộn của bom A lên hệ miễn dịch 20 năm sau vụ nổ bom nguyên tử 1945 ở Nhật. Hầu hết phát hiện thấy có sự bất thường chức năng của tế bào T và B ở những người nằm trong vùng bị chiếu xạ >1Gy. Với lympho T: Giảm CD3 ở máu ngoại vi, giảm CD4, CD8, giảm chức năng tế bào T trong đáp ứng với mytogens và alloantigens. Với lympho B: tăng số lượng lympho B ở máu ngoại vi; trong huyết thanh thấy tăng immunoglobulin A ở nữ và immunoglobulin M, tăng yếu tố Rh ở cả 2 giới, tăng kháng thể virus anti-epstein-Barr .
Tình hình nghiên cứu thuốc bvpx ở trong nước
Trong nước, việc nghiên cứu thuốc BVPX được đề cầp đầu tiên với công trình tổng hợp về lý luận và phương pháp của Nguyễn Xuân Phách (1962). Một số cây thuốc, con thuốc được nghiên cứu như Hoàng kỳ, Hoàng hoa. Hoàng kỳ là một thuốc bổ đông y có nhiều tác dụng, có khả năng tăng sức bền mao mạch, tăng sức đề kháng cho cơ thể, HSGL = 1,3. Từ 1982- 1985 Nguyễn Xuân Phách cùng nhóm NCđã nghiên cứu một số chế phẩm có tác dụng BVPX như chè đen Việt Nam, tảo Spirulina platensis thuộc họ tảo lam (Cyanophyta), RPM (Radix polygoni multiflovi) là cao mềm chế từ rễ hà thủ ô đỏ. Phân tích thành phần bán định lượng RPM có các chất như Flavon, Catechic tannin, Anthraquinon, Amino-acid, Starch, Protein và rất nhiều nguyên tố vi lượng có hàm lượng cao như K, Fe, Zn, Br, Zr, Cu, Rb…RPM có tác dụng tăng hàm lượng các chất bảo vệ nội sinh như catecholamin, dopamin, hàm lượng nhóm SH phi protein trong gan và lách. PX là hỗn hợp của RPM với cao xương động vật, có HSGL = 1,41. RPM có tác dụng BVPX tốt khi dùng đường uống liều 1g/kg trong 3 ngày liên tiếp. RPM còn có tác dụng làm tăng ESC rất rõ so với nhóm đối chứng.
Năm 1990, Nguyễn Xuân Phách và CS nghiên cứu cho thấy Protein từ gan và lách rùa dùng khoảng 20mg/kg thể trọng có tác dụng hồi phục hệ tạo huyết tốt, cao quy bản chế từ yếm rùa cũng có tác dụng BVPX.
Hỗn hợp tinh chất rùa và hà thủ ô đỏ được chế thành viên quy hà, ứng dụng trên nhóm bệnh nhân liên quan đến vụ tai nạn Chernobyl và kết quả rất tốt: chỉ sau 1 tuần dùng thuốc (3-4 viên/ngày) nhịp tim trở lại bình thường, sau 2 tuần giảm triệu chứng suy giáp…
Một số thuốc BVPX chế từ nguồn gốc động- thực vật được nghiên cứu và ứng dụng trong những năm qua tại Học viện Quân y, bệnh viện 103, bệnh viện Hai Bà Trưng Hà Nội như bột Phylamin, bột Spirulina, cao quy bản, KT1 (dùng tẩm gạc đắp tại chỗ).
Nguyễn Thị Kim Ngân và CS. [11] nghiên cứu khả năng BVPX của một số chất như cepharanthin tách chiết từ củ bình vôi, gacavit- một chế phẩm từ quả gấc vừa có tác dụng điều trị ung thư, vừa có tác dụng BVPX.
Nhiều tác giả sử dụng chỉ tiêu hàm lượng acid nucleic trong các mô để đánh giá ảnh hưởng của thuốc. PG-2 hạn chế giảm ADN sau chiếu xạ và sau 3 ngày tốc độ phục hồi nhóm PG-2 + 7Gy cao hơn nhóm ĐCCX. Tác giả cho rằng có thể do hệ enzym phục hồi trong các tế bào lách. A.V Popov (1987) đã biết rõ 5 enzym tham gia quá trình phục hồi ADN: endonucleaza I (nhận biết vị trí tổn thương); endonucleaza II…Khi chiếu xạ, các tính chất lý hoá của ADN, ARN và các enzym bị biến đổi mạnh. PG-2 tăng cường phục hồi hệ enzym này, nhất là trong các mô tạo máu. Tác giả cho thấy ADN-aza II trong lisosom tế bào 12 giờ sau chiếu xạ đã tăng lên rất mạnh (250% so với ĐCSH), tiếp tục tăng cao đến ngày thứ 3 (700%). PG-2 tăng ít hơn. Cơ chế BVPX của PG-2 có lẽ ức chế tạm thời sinh tổng hợp ADN trong mô lách chuột cống, giống như Cystamin, gammaphos, thiazolizin…, tăng phông kháng xạ nội sinh bằng cách tăng các chất Serotonin, histamin, cetecholamin, các chất chứa nhóm SH, các acid amin, giảm phông cảm xạ nội sinh: giảm các sản phẩm quá trình oxy hoá lipit: dialdehyd malonic, các chất dien, hydroperoxyt lipit .
Ngô Văn Thành, Triệu Duy Điệt nghiên cứu Catechin tách chiết từ vỏ cây xoan trà, thấy có tác dụng BVPX với hệ số giảm liều 1,205; dùng 400mg/kg tiêm phúc mạc 15 phút trước khi chiếu xạ. Hệ số alpha = 0,51 và beta = 0,49.
Mai Văn Điển nghiên cứu flavonoid chiết xuất từ vỏ đậu xanh có tác dụng BVPX với hệ số giảm liều 1,218. Tác giả đã giải thích một số cơ chế tác dụng như ảnh hưởng lên hệ tạo huyết, kích thích tạo quần thể lách nội sinh, giảm tổn thương hệ miễn dịch (lách, hạch, tuyến ức), ức chế các phản ứng peroxit hoá lipid màng, giảm MDA trong mô gan, lách, ruột non chuột nhắt trắng.
Đoàn Suy Nghĩ nghiên cứu nấm linh chi và thấy Linh chi có tác dụng kích thích hệ tạo huyết ở mô lách, ức chế hoạt tính enzym peroxydaza, hạn chế tốc độ giảm nhóm SH trong máu tuần đầu sau chiếu xạ, giảm nhẹ tổn thương cấu trúc mô một số cơ quan như ruột non, gan, lách, tinh hoàn…Hệ số giảm liều của linh chi đạt 1,278.
Đặng Trần Trung cho biết tắc kè được ngâm chiết trong dung dịch cồn 20 độ có tác dụng BVPX với hệ số giảm liều 1,25.
Phạm Mạnh Kiên và CS nghiên cứu tác dụng của artesunat có tác dụng BVPX trên chuột nhắt trắng qua các chỉ tiêu như hệ số giảm liều, số lượng quần thể tạo huyết nội sinh ở lách. artemisinin với liều 20mg/kg, artesunat với liều 10mg/kg thể trọng chuột có tác dụng giảm mức độ nhiễm khuẩn nội sinh ở chuột được chiều xạ liều 7Gy.
Nguyễn Xuân Phách thăm dò tác dụng bảo vệ phóng xạ của một số dạng chế phẩm từ củ hà thủ ô đỏ và nhận thấy chế phẩm hà thủ ô đỏ có tác dụng BVPX: alpha = 0,42, beta = 0,44. phục hồi chức năng hệ tạo huyết: ESC = 6,2.
PG-2 có hiệu lực BVPX rõ khi tiêm phúc mạc 15 phút trước chiếu xạ, liều 1200mg/kg hiệu lực BVPX cao nhất, HSGL đạt tốt nhất (1,45).
Hoàng Công Minh cho biết Hapatin- một chế phẩm trong thành phần có cao quy hà, hà thủ ô đỏ và tam thất – nếu cho động vật uống trước khi chiếu xạ 7Gy, có tác dụng giảm độ hấp thu I-131 ở tuyến giáp. Tác giả cho rằng Hapatin gây giảm chức năng tuyến giáp, gián tiếp làm giảm oxy ở tổ chức và có khả năng làm giảm tổn thương phóng xạ.
Trần Văn Hanh, Lê Thế Trung, Nguyễn Minh Thông cho biết cao lỏng và viên phylamin có tác dụng BVPX (1985, 1987), kích thích hồi phục các tế bào lympho bị huỷ hoại sau chiếu xạ. Phylamin có tác dụng hạn chế sự phát triển ung thư. Tác giả đã nêu vấn đề có thể do trong phylamin có 9 axit amin, đặc biệt là methionin có thể là có tác dụng phòng chống hậu quả lâu dài của phóng xạ, chứa một số flavonoid có tác dụng điều hoà miễn dịch, một số vitamin và nguyên tố vi lượng giúp nâng cao thể trạng của cơ thể.
Thuốc thải xạ do nhiễm xạ trong
Hiện nay, tình trạng ô nhiễm phóng xạ do các sự cố hạt nhân vẫn xảy ra. Hoặc trong chiến tranh ở Côsôvô, Mỹ đã sử dụng uran nghèo. Do đó ngoài việc bị chiếu xạ ngoài, có thể còn xảy ra nhiễm xạ trong. Chất phóng xạ có thể xâm nhập vào cơ thể qua da, qua hô hấp và qua đường tiêu hoá.
Khi chất phóng xạ vào bên trong cơ thể, sẽ qua các giai đoạn hấp thu, tích đọng, tồn lưu và bài tiết. Khi chất phóng xạ thâm nhập vào đường tiêu hoá, đầu tiên phải ngăn ngừa chúng hấp thu vào máu và tích tụ ở các tổ chức, cơ quan. Muốn phong bế hấp thu, cần đưa vào đường tiêu hoá các chất hấp thu chất phóng xạ, biến chúng thành những hợp chất mới không hoà tan, không qua được nhung mao, không thâm nhập vào máu. Phong bế có hiệu quả nếu được dùng sớm mang tính dự phòng hoặc dùng ngay sau khi bị NX trong, 15 phút đầu có hiệu lực tốt.
Cần phải rút ngắn thời gian tồn tại chất phóng xạ trong cơ thể. Các thuốc sử dụng phải làm sao có tác dụng tăng thải chất phóng xạ ra khỏi đường tiêu hoá, hô hấp và vị trí chất phóng xạ tích tụ lại. Có thể dùng các chất chelateurs – là những phức chất dễ dàng kết hợp với kim loại và thải ra chủ yếu theo đường niệu. Trước đấy, năm 1981, Lâm Xuân Hải đã thăm dò tác dụng thải xạ Sr-85 của Natrialginat. Trần Cẩm Vinh nghiên cứu thực nghiệm trên thỏ cho thấy chế phẩm xoan trà với liều 0,5g/kg dùng ngay sau khi bị nhiễm xạ trong đã tăng tốc độ đào thải uran ở thỏ, chu kỳ bán thải sinh học từ 43 giờ rút xuống còn 13 giờ. Một số nghiên cứu tại Học viện Quân y còn cho thấy thuốc B76 có tác dụng thải xạ Strontium-85 và uranium U3O8 khi gây nhiễm độc thực nghiệm ở thỏ. Kết quả có so sánh với nhóm chứng, qua các chỉ tiêu lâm sàng, huyết học, mô bệnh học, xác định liều tích đọng bằng đo xạ toàn thân .
Phân loại thuốc bvpx
Các thuốc BVPX rất đa dạng về cấu tạo hoá học, hiệu lực bảo vệ, đặc điểm cũng như cơ chế tác dụng. Có nhiều cách phân loại khác nhau .
Thuốc bvpx có tác dụng ngắn hạn
Thuốc có tác dụng BVPX khi đưa vào cơ thể trước chiếu xạ một thời gian tương đối ngắn.
Các hợp chất có chứa lưu huỳnh
Cystein
Aminothiol và các dẫn chất của chúng: Cysteamin, Cystamin (dẫn chất của disulphua), AET, Cystaphos và Gammaphos
Các amin có hoạt tính sinh học cao
Các dẫn chất của indolylalkylamin: adrenalin, noradrenalin, ephedrin, mexamin, serotonin
Histamin, axetylcolin…
Các chất gây thiếu oxy tổ chức:
Amylnitrit, Natri nitrit, PAPP (Para-aminopropiophenol)
Oxyt cacbon
Muối xyanua
Morphin, heroin
Thuốc bvpx có tác dụng dài hạn
Thuốc có tác dụng chậm, kéo dài, có khi tới vài ngày
Hormon (Oestrogen)
Các hợp chất cao phân tử: axit nucleic, polysaccarit; Polyvinylsulphat, polyglutamat…
Vitamin E
Các chế phẩm có nguồn gôc sinh học chưa tinh chế: mật ong, nọc rắn, lách rùa Trung Á, nấm men và một số vi khuẩn, nhân sâm, đương quy, hà thủ ô đỏ ngũ vị tử, nấm linh chi, tam thất, phylamin, flavonoid…
Thuốc có tác dụng điều trị
Những chất có tác dụng chống phóng xạ sau khi đã bị chiếu xạ.
Có thể có những chất thuộc 1 nhóm, nhưng cũng có những chất có cả 2, 3 tác dụng khác nhau.
Đánh giá tác dụng của thuốc bvpx
Hiện nay có rất nhiều phương pháp khác nhau để đánh giá hiệu lực của thuốc BVPX, tuỳ theo đối tượng và mục đích nghiên cứu mà chọn những phương pháp thích hợp nhất.
Đánh giá tác dụng bvpx trên cơ thể toàn vẹn – các chỉ tiêu chung
Đây là phương pháp cơ bản. Động vật thường dùng là chuột nhắt trắng, cho dùng thuốc BVPX (uống hoặc tiêm màng bụng) 15-30 phút trước khi chiếu xạ toàn thân. Có thể sử dụng các chỉ tiêu đánh giá sau:
Tỷ lệ động vật sống sót và thời gian sống trung bình sau chiếu xạ 30 ngày, hệ số giảm liều, hệ số bảo vệ anpha, beta, gamma.
a = [p(D) – p(DA)]/ p(D)
Trong đó p(D): xác suất chết của động vật bị chiếu xạ liều D, không dùng thuốc
p(DA): xác suất chết của động vật bị chiếu xạ liều D, dùng thuốc A.
Hệ số anpha cho thấy khả năng tăng tỷ lệ động vật sống sót của thuốc, không đề cập đến thời gian sống trung bình. a càng gần 1 thì thuốc càng tốt.
b = [Tth – Tc]/ [Ts – Tc]
Tth: thời gian sống trung bình sau chiếu xạ của động vật được dùng thuốc
Tc: TG sống trung bình của động vật bị chiếu xạ
Ts: TG sống trung bình của nhóm đối chứng sinh học.
Hệ số beta đánh giá được cả tỷ lệ sống chết và thời gian sống. Có thể tỷ lệ sống chết không chênh nhưng kéo dài thời gian sống thì thuốc vẫn có ý nghĩa. Hệ số beta càng gần 1 càng tốt.
g = [Gt – Gc]/ [Gs – Gc]
Gt, Gc, Gs: trọng lượng trung bình của các nhóm động vật có dùng thuốc trước chiếu xạ, chiếu xạ và nhóm ĐCSH.
Hệ số gamma đánh giá sự biến đổi trọng lượng cơ thể sau chiếu xạ.
Hệ số giảm liều (HSGL) (DRF – Dose Reduction Factor): Đó là tỷ lệ giữa 2 liều chiếu cùng gây một hiệu quả như nhau ở nhóm có dùng thuốc và nhóm không dùng thuốc. HSGL ³ 1,3 có thể coi là thuốc có hiệu lực tốt. Qua nghiên cứu HSGL có thể nhận định được thuốc BVPX có tác dụng đến liều chiếu nào. Đây là chỉ tiêu bắt buộc phải tiến hành đối với các công trình nghiên cứu về thuốc BVPX.
LD50/30 nhóm thí nghiệm
Hệ số giảm liều (HSGL) = ———————————–
LD50/30 nhóm chứng
Các chỉ tiêu về máu và cơ quan tạo máu
Không có tổn thương phóng xạ nào không liên quan tới bệnh lý máu và hệ tạo máu. Do đó các chỉ tiêu huyết học là rất phong phú.
Đánh giá sự thay đổi số lượng tế bào máu ngoại vi (HC, BC, tiểu cầu, hồng cầu lưới…Có thể theo dõi động học của quá trình hồi phục. Số lượng hồng cầu máu ngoại vi giúp đánh giá và tiên lượng bệnh phóng xạ cấp. Bạch cầu nhạy cảm nhất với PX, nhất là BC lympho, do đó giảm mạnh, nhất là từ ngày thứ 3-7 sau chiếu xạ.
Đánh giá sự thay đổi số lượng tế bào tuỷ xương
Đánh giá chỉ số quần thể tế bào lách nội sinh (ESC- Endogenous Spleen Colonies) Thường tiến hành vào ngày thứ 9 sau chiếu xạ, mổ lấy lách chuột, ngâm trong dung dịch Bouin 4 giờ, đếm các đốm nốt sần kích thước >1mm xuất hiện trên bề mặt lách.
Biến đổi đường huyết sau chiếu xạ: giảm tiêu thụ glucose nên gây tăng đường huyết, rõ nhất ở thời điểm 2 giờ sau chiếu xạ.
Đánh giá sự sinh sản hồng cầu bằng Fe-59: Sau khi tiêm Fe-59 sẽ từ huyết tương vào tuỷ xương để sử dụng cho quá trình tổng hợp huyết sắc tố. Sau khi tạo thành hồng cầu ở tuỷ xương, phần lớn HC sẽ ra máu ngoại vi. Tốc độ đưa HC ra máu ngoại vi là chỉ tiêu quan trọng của động thái hồng cầu. Nếu bị chiếu xạ, tuỷ xương bị tổn thương, do đó sự xuất hiện các hồng cầu đánh dấu Fe-59 trong máu ngoại vi sẽ giảm.
Tính đời sống hồng cầu bằng Cr-51: Theo dõi độ phóng xạ Cr-51 trong máu ta thấy giảm dần. Thời gian độ phóng xạ giảm xuống còn 1/2 ta gọi là thời gian sống 1/2 của hồng cầu. Sự thực thời gian đó không phải hoàn toàn sinh lý hoặc bệnh lý, nó bao gồm quá trình thoát bình thường của Cr-51 ra khỏi hồng cầu do thẩm thấu và do HC bị phá huỷ màng (chết). Giảm T1/2 có thể do giảm sự sinh sản hồng cầu của tuỷ xương, hoặc do tan huyết nhanh nên mất cân bằng.
Biến đổi adn và chromosomes
Đánh giá các biến loạn thể nhiễm sắc: tăng, giảm, đứt gãy đơn, đứt gãy đôi, multinuclei… Thuận tiện nhất là nghiên cứu trên những tế bào lympho ở máu ngoại vi. Tế bào được nuôi cấy và dùng hoá chất để kích thích sự phân chia in vitro. Sai lệch nhiễm sắc thể có thể ghi nhận được ở metaphase của phân bào (mytosis). Sai lệch nhiễm sắc thể xảy ra khi 2 nhánh của DNA bị đứt gãy. Đầu đứt gẫy này có thể được nối lại với một đầu đứt gãy khác không tương ứng. Hiện tượng này thường gặp khi tế bào bị chiếu trong pha G1 của chu kỳ tế bào. Nếu tế bào bị chiếu ở pha G2, thì sẽ thấy có sai lệch nhiễm sắc tử (chromatid aberrations). Tần số sai lệch nhiễm sắc thể của tế bào lympho máu ngoại vi tương quan thuận với liều chiếu xạ trong một giới hạn nào đó.
Hàm lượng axit nucleic, hoạt tính ADN-ase, ARN-ase trong lách chuột. Thuốc có tác dụng BVPX khi có khả năng tăng cường sự hồi phục ADN, ARN; ức chế sự tăng hoạt tính ADN-ase và ARN-ase.
Các chỉ tiêu về hình thái, chức năng một số cơ quan và tb md
Các cơ quan miễn dịch quan trọng như lách, hạch, tuyến ức là những cơ quan đặc biệt có nhiều tế bào non đang trong quá trình biệt hoá. Dưới tác động của bức xạ, các cơ quan này biến đổi rất mạnh. Có thể xác định:
Sự thay đổi trọng lượng của các cơ quan miễn dịch: lách, hạch, tuyến ức
Sự biến đổi hình thái, mô học của tế bào các cơ quan miễn dịch: các tiêu bản lách, hạch, tuyến ức nhuộm HE hoặc Carnoy được quan sát dưới kính hiển vi điện tử để phân tích hình ảnh vi thể: xung huyết, hoại tử, thoái hoá tế bào, mức độ tan rã, đông vón nhân của tế bào, sự đảo lộn cấu trúc vùng vỏ/vùng tuỷ. Các tế bào lympho giảm nhiều về số lượng ở vùng tuỷ trắng cũng như vùng tuỷ đỏ, giãn các xoang tĩnh mạch, trong các xoang tĩnh mạch ứ đầy hồng cầu.
Sử dụng kỹ thuật miễn dịch huỳnh quang gián tiếp để xác định các tiểu quần thể lympho T: TCD4, TCD8
Chức năng đại thực bào: kỹ thuật tạo hoa hồng của đại thực bào để đánh giá màng tế bào của đại thực bào: E, Ea của lympho T, EAC của lympho B.
Kỹ thuật thực bào (Killing test) đánh giá khả năng thực bào của bạch cầu trung tính máu ngoại vi. Đánh giá qua:
Số ĐTB có thực bào vi khuẩn
%Thực bào =——————————— x100%
Tổng số ĐTB đếm được
Tổng số VK có trong ĐTB
Chỉ số thực bào = ————————————- x100%
Số ĐTB có thực bào
Tổng số VK chết
Tỷ lệ giết = ————————————- x100%
Tổng số VK đếm được
Đánh giá sự thay đổi tỉ lệ Th1/Th2: có một số công bố cho rằng bức xạ ion hoá tác dụng lên sự hình thành thụ cảm thể của tế bào T, làm biến đổi cân bằng Th1 và Th2. Bức xạ gây tổn thương Th2 nhiều hơn Th1. Tuy nhiên theo dõi xa sau chiếu xạ Th1 lại thiếu nhiều hơn vì Th1 chỉ sản sinh ở một vùng nhỏ cuả tuyến ức. Như vậy tỉ số Th1/Th2 lúc đầu tăng và sau đó lại giảm.
Về khả năng chống peroxit hoá lipid
Quá trình peroxit hoá lipid là quá trình chuyển hoá bình thường, điều hoà tính thấm của màng. Nếu xảy ra mạnh, kéo dài sẽ xuất hiện phân tử lipoperoxit làm thay đổi tính thấm của màng. Các lipoperoxit phản ứng với các nhóm -SH của enzym gây khóa hoạt động các enzym chuyển hoá năng lượng ở màng làm thay đổi quá trình phosphoryl hoá, các bơm canxi, natri, kali không hoạt động, dẫn tới tích tụ canxi ở bào tương.
MDA là một axit malolic dialdehyt sản phẩm cuối cùng của quá trình peroxit hoá lipit. MDA hình thành sẽ tiếp tục gây tổn thương các đại phân tử, đặc biệt với các axit nhân, có thể gây nên sự nối bắt chéo DNA trong hệ thống khuôn mẫu. Hiệu lực thuốc BVPX tốt khi có khả năng giảm MDA trong các tổ chức của động vật thí nghiệm.
Xác định in vitro khả năng ức chế phản ứng peroxit hoá lipit trong một số dịch nghiền đồng thể, trong ty thể tế bào gan chuột nhắt trắng. Tốc độ quá trình oxy hoá xác định bằng cách đo hàm lượng MDA hình thành.
Hệ thống chống oxy hoá có bản chất enzym:
SOD: Superoxit dimustase có mặt trong tất cả các tế bào có chuyển hoá oxy. Chức năng là xúc tác quá trình phân huỷ anion gốc superoxyl (O2–)
Bản chất enzym này là một protein có 2 đồng phân là MnSOD ở ty lạp thể và CuZnSOD ở bào tương. Hoạt độ CuZn SOD ở gan chuột là 122UI/mg protein và hoạt độ MnSOD là 35UI/mg protein.
Hiện nay đã chế tạo được SOD từ máu bò hoặc SOD tái tổ hợp bằng công nghệ gien và áp dụng trong các trường hợp viêm, giảm tác hại của PX. Tuổi thọ của các loài đều có quan hệ chặt chẽ với tỷ số hoạt độ SOD và chuyển hoá cơ bản. SOD giảm, tế bào mất khả năng chống đỡ với ngay các dạng oxy hoạt động nội sinh do hô hấp tế bào tạo nên.
Enzym catalase: là một chất chống oxy hoá vì nó xúc tác phản ứng phân huỷ hydrogen peroxit:enzym này chỉ được hoạt hoá khi H2O2 có nồng độ cao.
Enzym Glutathion peroxidase: xúc tác phản ứng loại bỏ các peroxit hữu cơ và vô cơ. Khi H2O2 có nồng độ cao sẽ ức chế glutathiol peroxidase, khi đó catalase sẽ hoạt động.
Cơ chế tác dụng của thuốc bvpx
Mặc dù đã tìm được một số thuốc BVPX có giá trị từ 30-40 năm trước đây, nhưng cơ chế tác dụng của thuốc vẫn đang là vấn đề phức tạp. Có thể nêu một số thuyết sau:
Thuyết “lý – hoá”
Theo Bacq và Alecxander (1955): hiệu lực BVPX của một số chất đạt được là do chúng có khả năng kết hợp với gốc tự do- sinh ra do bức xạ ion hoá, làm cho các gốc tự do này mất hoạt tính, cắt đứt phản ứng chuỗi tạo gốc tự do. Đặc biệt các gốc tự do tạo ra do quá trình peroxit hoá lipid- những chất có khả năng gây ra hàng loạt các phản ứng hoá học bất bình thường, làm rối loạn quá trình trao đổi chất trong tế bào.
GTD sinh ra trong cơ thể do quá trình hô hấp tế bào, do tác nhân phóng xạ. Hô hấp tế bào sinh GTD ở nội bào, còn do tác dụng của tia xạ gốc tự do sinh ra ở cả nội và ngoại bào. Các tia xạ tác động bẻ gãy 1 phân tử thành 2 gốc tự do. Trong cơ thể nước (H2O) chiếm gần 80% nên chủ yếu phân tử nước bị phân ly:
Tia xạ
H2O ——-> H. + OH.
Tia xạ
R1 – R2 ———> R1. + R2.
H.O2HO2. H. + O2.
Ngoài ra gốc tự do hình thành do hiện tượng thực bào, do thiếu máu cục bộ và tưới máu lại, do tác nhân hoá học ngoại lai, ô nhiễm môi trường, do các stress, do tia tử ngoại, do phản ứng Fenton, do phản ứng oxy hoá lipid màng.
Bản thân cơ thể có hệ thống enzym chống GTD như men SOD (superoxyde Dimustase) phân huỷ các O2. ; có 2 đồng phân:
MnSOD ở mitochondrie chống gốc O2. do hô hấp TB; CuZn SOD ở bào tương, chống O2. lọt ra bào tương.
SOD
2O2. + 2H+ ———> H2O2 + O2
Peskova và Goncharenko (1982) thấy E.coli bền vững hơn với phóng xạ khi hoạt tính SOD tăng lên. Chủng vi khuẩn nào có hoạt tính SOD cao thì kháng xạ tốt hơn.
Men Catalase, không phân huỷ được peroxit hữu cơ, phân huỷ H2O2 ở nồng độ cao >108 mol/l
Catalaza
2 H2O2 ——–> 2H2O + O2
Men GSH-PO (Glutation Peroxydase) loại bỏ peroxit hữu cơ và vô cơ, dọn triệt để H2O2 ở nồng độ thấp 8 mol/l + các peroxyt ở màng. Có sự phối hợp của Vitamin E, Selen, Glutation.
Glutation peroxidase
ROOH + 2GSH —————–> GSSG + ROH + H2O
GSH: Glutation dạng khử; GSSG: Glutation dạng oxy hoá; R là gốc hữu cơ hoặc là H.
Các nghiên cứu cho thấy glutation cần thiết để các chất nội sinh như serotonin phát huy tác dụng, Glutation không tham gia vào các quá trình ban đầu sau chiếu xạ, mà tham gia vào giai đoạn muộn hơn, ảnh hưởng đến đặc trưng diễn biến các quá trình tổn thương và hồi phục sau chiếu xạ.
Ngoài ra còn có các chất chống oxy hoá không enzym: nhóm poliphenol-ancol; nhóm các thiol, muối selen, nhóm chất chứa nhiều nối đôi liên hợp.
Nhóm OH phenol và ancol: Coenzym Q10, vitamin E bioflavonit, vitamin C. Các diphenol (đồng phân octo) có khả năng tạo phức Chelat với Fe2+ và Cu2+ làm mất khả năng xúc tác của 2 ion này để tạo phản ứng Fenton, một trong những nguồn gốc gây ra các gốc tự do độc hại.
Ubiquinone Q9 có tác dụng phục hồi tổn thương màng mitôchndrie do tác dụng của bức xạ ion hoá.
Vitamin E là chất chống oxy hoá vì nó ngăn cản quá trình oxy hoá các axit chưa no của màng tế bào.
Vitamin C đưa Vitamin E từ dạng oxy hoá về dạng khử.
Các hợp chất có chứa nhóm thiol: do có tính khử mạnh nên chúng có thể cùng vitamin C chuyển vitamin E từ dạng oxy hoá về dạng khử nhằm phục hồi chức năng dập tắt mạch peroxit hoá lipit do các gốc tự do độc hại sinh ra.
Graevski và Taraxenko (1972) thấy có sự phụ thuộc của độ nhạy cảm phóng xạ của cơ thể với hàm lượng SH. SH càng tăng cao càng có khả năng kháng xạ, ngược lại, SH giảm gây tăng độ nhạy cảm phóng xạ.
Nhóm chất có nhiều nối đôi liên hợp: beta-caroten là chất bẫy gốc tự do, chủ yếu là oxy đơn bội.
Ben-Amotz A., Yativ S. Sela M. (1998) theo dõi trên 709 chấu bè bị ảnh hưởng của thảm hoạ Chernobyl đã được đưa tới Israel 1990-1994, tất cả được kiểm tra xác định các triệu chứng lâm sàng, chia làm 3 nhóm: bị chiếu xạ 2; >5Ci/m2 và có liên quan. 57 bé trai và 42 bé gái được dùng thêm 40mg 9 cis và trans beta-caroten dạng viên nén trong 3 tháng. Kiểm tra các chỉ tiêu huyết thanh trước khi dùng, sau khi dùng 1 và 3 tháng. Kết quả cho thấy các sản phẩm oxy hoá lipid giảm, trong khi các chỉ tiêu về carotenoid, retinol hay alpha-tocopherol thay đổi không đáng kể. Các chỉ tiêu sinh hoá khác nằm trong giới hạn bình thường. Bằng phương pháp phân tích sắc ký lỏng cao áp với carotenoid trong máu thấy chủ yếu là oxycarotenoid, beta-carotene dạng trans, alpha-carotene, không thấy 9-cis beta-carotene. Từ đó có giả thiết rằng trẻ em bị chiếu xạ làm tăng oxy hoá lipid và beta-carotene có thể tác dụng như một chất chống oxy hoá lipid và như một chất BVPX.
Konopacka M., Widel M., Wolny J. (1998) cho biết, nếu cho động vật uống vitamin 5 ngày liên tục trước khi chiếu xạ hoặc uống ngay sau khi chiếu xạ liều 2Gy với liều 100-200mg/kg/ngày vitamin E và 3-12mg/kg/ngày beta-carotene có hiệu quả chống lại việc hình thành đa nhân (micronucleus) trong tế bào. Vitamin C với liều khác nhau có thể gây hiệu quả khác nhau: 400mg/kg/ngày tăng hiệu ứng của bức xạ, còn 50-100mg/kg/ngày có tác dụng giảm hình thành các hồng cầu đa nhân. In vitro các tác giả cho thấy sự có mặt của vitamin trong dung dịch nuôi cấy có ảnh hưởng tốt đến tốc độ hồi phục tổn thương DNA của bạch cầu.
Có thể chống GTD bằng giảm sinh GTD, tăng phản ứng phân huỷ gốc superoxyt bằng tăng tạo SOD, tăng tạo men GSH-PO (tăng bổ sung Selen), trung hoà GTD ở ngoại bào: tăng glutation, beta caroten, Flavonoid. Dùng các thuốc antioxydant.
Trong thiên nhiên có rất nhiều chất có khả năng chống oxy hoá, chống GTD, chúng nằm trong các loại thực phẩm, rau quả, dược liệu cây con thuốc. Thuốc BVPX gây phản ứng với các GTD trước khi các GTD tác động vào phân tử sống. Thuốc có thể khôi phục lại hoạt tính sinh học của các đại phân tử đã bị tổn thương. Chính vì vậy trong đánh giá khả năng chống oxy hoá của một chế phẩm, có thể đánh giá qua khả năng thuốc đó có hạn chế được tác dụng của tia bức xạ làm giảm hoạt tính enzym SOD hay không.
Pericova E.G., Goncharenko E.N. (1982) cho thấy SOD có tác dụng BVPX. Tiêm SOD cho chuột có thể bảo vệ được tế bào gốc tuỷ xương với hệ số giảm liều 2,1. Khi chiếu xạ làm hoạt tính SOD ở gan giảm khoảng 20%, SOD biến đổi ngay sau chiếu xạ 15 phút, giảm từ 1 giờ và giảm rõ nhất vào 4 giờ sau chiếu xạ (còn 70-75% hoạt tính ban đầu). Chính những sản phẩm peroxit lipid màng đã ức chế hoạt tính của SOD.
Nguyễn Liêm, Triệu Duy Điệt, Đỗ Văn Bình khi nghiên cứu tác dụng chống oxy hoá của một số cây thuốc Việt Nam đã tìm thấy 4 cây có tác dụng chống oxy hoá mạnh: lá đỏ ngọn, chè xanh, lá bụt mọc, vỏ cây xoan trà.
Malonic dialdehyd (MDA) là một radiotoxin đặc biệt, có hoạt tính hoá học cao, có phản ứng mạnh với các nhóm amin của bazơ nitơ trong ADN, khi tạo búi với ADN, sẽ làm đứt sự nhân đôi ADN, gây sai lạc nhiễm sắc thể và gây chết tế bào. Ngô Văn Thành nghiên cứu ảnh hưởng của chế phẩm Panpsegin (PG-2) tới hàm lượng malonic dialdehyd trong các mô lách, ruột non, gan của chuột cống trắng bị chiếu xạ liều 7Gy thấy PG-2 liều 0,5g/kg có tác dụng giảm MDA, mạnh nhất ở lách: còn 60% so với chứng .
Mai Văn Điển cũng cho thấy flavonoid chiết xuất từ vỏ đậu xanh có thể giảm lượng MDA trong lách còn 69,94%, trong gan còn 75,23% trong ruột non 74,83% so với nhóm chứng.
Thuyết hiệu ứng oxy
Các thuốc BVPX gây thiếu oxy bằng cách:
Gây co mạch: adrenalin, noradrenalin, mexamin
Ngăn cản vận chuyển oxy bằng cách tạo MetHb (Amylnitrit, natri nitrit)
Ức chế chuỗi hô hấp tế bào (muối xyanua)
Ức chế trung khu hô hấp: Morphin, heroin…
Một số lớn thuốc BVPX tác dụng theo cơ chế gây thiếu oxy tổ chức. Chúng làm giảm quá trình vận chuyển oxy tới tế bào và giảm phân áp oxy trong nguyên sinh chất. Trạng thái đó làm tăng khả năng kháng xạ của tế bào và cơ thể. Qua thực nghiệm thấy rõ tuỷ xương ở chỗ thiếu oxy giảm số tế bào chết theo dạng phân bào, giảm số tế bào có sai lệch nhiễm sắc thể.
Các công trình nghiên cứu trên động vật thực nghiệm nhằm tìm hiểu và làm sáng tỏ cơ chế tác dụng của thuốc BVPX. Các tác giả nhận thấy hiệu ứng BVPX được thể hiện thông qua các thụ cảm thể tế bào như a- adrenoreceptor, D-serotonin, H1- histamin. Một số chất có tác dụng BVPX như indraline đã gây thiếu oxy trong mô, giảm tiêu thụ oxy 10% sau 2 phút trên chuột được tiêm màng bụng 0,01ml/g thể trọng 5 phút trước khi chiếu xạ, có thể giảm 30% sau 40 phút, gây giảm dòng máu tới gan, tác dụng giống mercamin. Hiệu ứng BV giảm khi dùng chất chẹn anpha như aminasine và theophyline. Các chất BVPX tuy có tác dụng giảm tiêu thụ oxy nhưng lại tăng sản phẩm trao đổi nhiệt.
Vai trò của oxy làm tăng tác dụng của tia phóng xạ được nghiên cứu khá nhiều. Gọi N là tổng số tế bào nuôi cấy, Ns là số tế bào sống sót sau chiếu xạ liều D, ta có biểu thức: Ns/N = exp (-Ks – Kox1 – Kox2)D
Ks ứng với điều kiện không có oxy. Kox1 là phần tác dụng tăng cường khi có oxy do tạo gốc tự do và không còn tác dụng khi ngừng chiếu xạ. Kox2 là tác dụng tăng cường khi có oxy nhưng đã ngừng chiếu xạ. Phần này do các gốc oxy tác dụng với các phân tử xung quanh tạo gốc thứ cấp.
Như vậy để bảo vệ phóng xạ, việc giảm Ks rất khó, có thể dùng các chất chống oxy hoá có nguồn gốc nội sinh cũng như ngoại sinh để giảm Kox1 và Kox2. Ngược lại, khi nghiên cứu điều trị ung thư bằng tia phóng xạ thì phải tăng Kox1 và Kox2, tăng mức độ cảm xạ của tế bào khối u. Tế bào u hô hấp yếm khí, pO2 trong tế bào u tăng dẫn tới Kox1 và Kox2 trong tế bào u tăng. Đó là cơ sở để điều trị ung thư bằng tia xạ. Tuy nhiên, dù liều chiếu cao vẫn còn tế bào u sống sót, đó là những tế bào thiếu oxy hay tế bào kháng xạ. Khi đó phải dùng những chất có tác dụng như oxy và tập trung nhiều ở tế bào u làm tăng tính nhạy cảm phóng xạ của chúng. Các chất này được gọi là thuốc gây cảm xạ kiểu oxy (oxygen – likeradiosensitizing drugs).
Saskov và Anaskin (1971) đã nhận thấy Serotonin, Mexamin, AET, Cystamin có tác dụng BVPX đều có cơ chế dược lý gần giống nhau làm co mạch, giảm nồng độ oxy.
Svedlov A.G. nhận thấy Mexamin gây giảm pO2 rất nhanh, với liều 25, 50mg/kg, sau 12-15 phút giảm 50-60%, duy trì ở mức thấp trong khoảng thời gian 60-90 phút.
Cho chuột dùng caffeine (1,3,7-trimethylxanthine) thành phần chủ yếu của cà phê, liều 80 hoặc 100mg/kg, 60 phút trước khi chiếu toàn thân 7.5Gy có 70% và 63% chuột sống sót, trong khi nhóm CX chết 100%. Tiền điều trị với liều thấp 50mg/kg không có tác dụng chống PX. Có hiệu ứng BVPX khi liều đạt 80mg/kg. Liều 80mg/kg dùng 3 phút sau chiếu xạ cũng không có tác dụng. Chứng tỏ caffeine là chất có khả năng quét GTD, chống oxy hoá, là chất BVPX, chống lại hiệu ứng oxy của tổn thương PX trong tế bào. Kabakova cũng nhận thấy, sau chiếu xạ, nếu nuôi cấy tế bào trong dung dịch có thêm 0,1; 0,2; 0,3; 0,4% caffeine thì nồng độ caffeine càng tăng, số tế bào sống càng giảm.
Thuyết oxy hoá – khử
Vladimirov (1982) [63,65] cho biết nếu điện thế oxy hoá khử giảm trong thời gian dài thì hiệu lực tác dụng của thuốc cũng tồn tại trong thời gian dài. Dưới tác dụng của bức xạ ion hoá, các gốc tự do H. , OH., O2. tác dụng lên màng tế bào, phá huỷ cấu trúc màng, thay đổi tính thấm của màng, và do đó thay đổi điện thế màng, phá huỷ quá trình vận chuyển chất và ion qua màng, gia tăng sự oxy hoá, làm tăng điện thế oxy hoá khử. Khi sử dụng chất BVPX có khả năng trung hoà điện tích, ngăn chặn phản ứng sinh gốc tự do mới, dọn sạch các sản phẩm phân huỷ phóng xạ, phục hồi cấu trúc màng và tính phân cực của màng, nghĩa là thuốc BVPX có tác dụng giảm điện thế oxy hoá khử , ngăn chặn sự tấn công của GTD.
Một số chất chống oxy hoá có nguồn gốc từ cây cỏ Tocopherol vitamin E, vitamin C, caroten vitamin A; bioflavonoid tham gia tích cực trong quá trình vận chuyển các điện tử, giảm tính thấm, làm bền thành mạch.
Iarmonenko và CS. (1984) nhận thấy nhiều chất BVPX có đặc điểm chung là đều có khả năng chống oxy hoá, tuy nhiên không phải chất chống oxy hoá nào cũng có tác dụng BVPX. Ngược lại, có những chất không gây biến đổi rõ sự cân bằng điện thế oxy hoá khử nhưng tạo được những chất nội sinh, tăng sức đề kháng chống phóng xạ, đó là những chất bảo vệ nội sinh .
Thuyết “sốc sinh hoá”
Bacq và Alecxander [32] đưa ra thuyết này cho rằng: các chất bảo vệ hoá học, nhất là những chất có lưu huỳnh, có khả năng làm biến đổi sâu sắc các phản ứng hoá sinh dẫn tới thay đổi các quá trình sinh lý trong tế bào giai đoạn trước chiếu xạ theo hướng tăng khả năng kháng xạ của cơ thể. “Sốc sinh hoá” có đặc trưng là ức chế các quá trình trao đổi hydratcacbon, thay đổi tính nhạy cảm phóng xạ của cơ thể theo hướng bền vững với phóng xạ hơn. Các tác giả nhận thấy chỉ vài phút sau khi các chất BVPX được đưa vào cơ thể, chúng đã liên kết với protein và số lượng nhóm thiol phi protein tăng dần nhờ tích tụ các sulfhydryl nội sinh.
Eidus (1977) cho rằng “sốc hóa sinh” chỉ là một trường hợp riêng của phản ứng chung không đặc hiệu của tế bào đối với các tác nhân bên ngoài. Khi chất BVPX vào cơ thể sẽ làm cho sự vận chuyển chất qua màng bị thay đổi, dẫn tới biến đổi gradien nồng độ các chất hữu cơ giữa bên trong và bên ngoài màng. Các chất hữu cơ có phân tử lượng thấp ở trong tế bào hoạt tính sinh học bị yếu đi. Cuối cùng xuất hiện trạng thái “cận hoại tử” và trạng thái này sẽ bình phục nếu tổn thương do tia phóng xạ không nặng.
Thuyết quyết định thể sinh hoá
Zexchianikov (1968) cho rằng một trong những cơ chế chống lại các yếu tố gây tổn thương là quá trình hồi phục ADN, bảo vệ gen tránh được các yếu tố gây đột biến. Tính bền vững ở mức độ cơ thể thông qua sự hồi phục ADN được xác định bởi cơ chế đặc hiệu và không đặc hiệu của hệ miễn dịch. Tế bào máu nguyên thuỷ được xem như là yếu tố quyết định sự sống sót của động vật khi bị chiếu xạ (quyết định thể sinh hoá). Để thực hiện chức năng tạo máu sau chiếu xạ, vấn đề quan trọng không chỉ là sự sống sót của tế bào tạo máu mà còn là chức năng của lympho baò, đại thực bào tham gia vào sự tác động tương hỗ giữa các tế bào nhờ tiết hỗn hợp các yếu tố nội tiết chủ yếu điều khiển quá trình tạo máu như interleukin -1, prostaglandin E, g -interferon… Khi đưa chất BVPX vào cơ thể nó tác động tới thành phần sinh hoá của tế bào, tăng cường tính kháng xạ của cơ thể.
Thuyết tạo phức chất với phân tử sinh học dễ bị tổn thương
Có loại chất BVPX không “bắt” gốc tự do nhưng lại có khả năng tham gia vào phản ứng trực tiếp tạo phức với các đại phân tử sinh học. Như vậy chúng sẽ bảo vệ được các đại phân tử khỏi sự tấn công của các gốc tự do, các peroxit và các sản phẩm độc hình thành do chiếu xạ. Các hợp chất có chứa lưu huỳnh khi đưa vào cơ thể sẽ kết hợp với đại phân tử sinh học tạo các liên kết disulfit (S-S), nhờ đó khi chiếu xạ, năng lượng bức xạ chủ yếu tập trung vào liên kết tạm thời này, phá vỡ liên kết và giải phóng thiol. Các đại phân tử ít bị tổn thương hơn.
Thuyết sulfhydryl
Các chất thiol đóng vai trò quan trọng trong hoạt động sống của tế bào. Thiol góp phần đảm bảo tính thấm của màng nội bào và là một trong những yếu tố cần cho tạo cấu trúc bậc ba của protein. Thiol là chất chống oxy hoá mạnh nên giảm được các quá trình oxy hoá nguyên phát của tổn thương phóng xạ. Khi bị tổn thương phóng xạ, trong cơ thể các chất chứa nhóm thiol là cấu trúc duy nhất bị tổn thương làm cho men mất hoạt tính và những cấu trúc nội bào có liên quan tới thiol cũng bị tổn thương. Khi có chất BVPX có chứa lưu huỳnh (S) nó đóng vai trò phân giải gốc tự do hay độc tố phóng xạ và bổ sung những axid amin không thay thế, tham gia vào quá trình tổng hợp enzym, hormon… nâng cao tính chống phóng xạ của cơ thể. Thuyết này chưa lý giải được vì sao nhiều chất trong phân tử có chứa thiol song lại không có tác dụng BVPX.
Simonhenkova và Sverdlov (1971) cho biết Mexamin, Cystaphos có tác dụng tăng hàm lượng nhóm -SH trong bạch cầu ở lách chuột, hạch lympho và cho rằng cơ chế bào vệ của thuốc có liên quan đến tăng -SH.
Nhiều ý kiến lại cho rằng vai trò BVPX không thuộc về các thiol đưa từ ngoài vào mà chính là các thiol nội sinh. Chỉ có các thiol nội sinh loại SH phi protein mới có khả năng tăng đề kháng chống phóng xạ cho cơ thể…
Thuyết “phông nội sinh”
Chất bảo vệ nội sinh là một tập hợp gồm nhiều chất trong đó có thiol phi protein, serotonin, histamin, dopamin, adrenalin, noradrenalin, đồng thời cũng có những chất khác có tác dụng ngược lại: tăng tổn thương PX của cơ thể. Một thuốc BVPX muốn đạt được tác dụng phải làm tăng được các chất BVPX nội sinh, giảm hoạt tính các chất cảm xạ (sản phẩm oxy hoá của các acid béo không no). Các chất BVPX như AET, cystaphos, cystamin… đều có tác dụng tăng hàm lượng serotonin ở ruột non, dạ dày và lách. Các chất BVPX tác dụng hoạt hoá men, tăng cường hình thành serotonin.
Qua nghiên cứu Goncharenko nhận thấy ở những động vật có sức đề kháng chống phóng xạ tốt thì hàm lượng serotonin, histamin đều cao hơn nhiều so với động vật không kháng xạ. Loài vật nào có độ mẫn cảm cao với phóng xạ thì trong cơ thể có nhiều chất tăng tổn thương phóng xạ.
Một số tác giả lại chú ý đến hệ GMP vòng, đó là hệ đối kháng với AMP vòng trong nhiều quá trình của hoạt động tế bào, nhất là quá trình tổng hợp ADN. Vladimirov cho rằng chất BVPX phong bế men guanylatcyclaza, ảnh hưởng đến hệ GMP vòng và ảnh hưởng tới sự kháng xạ của tế bào. Tuy vậy luận điểm này chưa được chứng minh đầy đủ.
Thuyết tác động trên hệ apud
APUD (Amine Precursor Uptake and Decarboxylation) là một hệ thống tế bào gồm hơn 50 loại khác nhau ở rải rác khắp cơ thể. Các tế bào của hệ APUD tiết ra nhiều chất thuộc loại nội tiết tố và chất dẫn truyền thần kinh. Đáng chú ý là các chất serotonin, dopamin, catecholamin…
Hệ APUD tạo nên một nền kháng xạ nội sinh. Vì ở rải rác khắp nơi, nên có khả năng đáp ứng nhanh chóng, sản sinh kịp thời các nội tiết tố, các amin quan trọng để chống lại tác hại của phóng xạ. Chất có tác dụng BVPX là chất có khả năng kích thích hệ APUD, tăng cường hoạt động của hệ APUD.
Khi chuột bị chiếu xạ hàm lượng serotonin trong lách giảm ngay giai đoạn đầu tiên sau chiếu xạ (2-20 phút), giảm mạnh nhất vào thời điểm 1-3 giờ, nguyên nhân do giảm tiết từ ruột non và từ lách. Dưới tác động của các chất BVPX như Cystein, Mexamin đã có tác dụng tăng cường sự huy động serotonin. Các amin ở dạng kết hợp không hoạt động, chúng có thể tham gia vào phản ứng bảo vệ khi được chuyển thành dạng tự do. Chiếu xạ đã ngăn cản quá trình này. Còn các chất BVPX như Cystein, Mexamin đã làm tăng tích luỹ serotonin ở lách lên 1300-2400ng/g, tăng tính kháng xạ của cơ quan này.
Như vậy, tồn tại rất nhiều thuyết khác nhau về cơ chế tác dụng của thuốc BVPX, mỗi thuyết đều mới giải thích được một phần, chưa có thuyết nào giải thích đầy đủ cơ chế tác dụng của thuốc BVPX. Việc nghiên cứu cơ chế tác dụng của thuốc còn khó khăn, cần được tiếp tục.
Thuốc thải xạ do nhiễm xạ trong
Động học của chất px khi vào cơ thể:
Chất PX có thể thâm nhập vào cơ thể qua da, hô hấp và qua đường tiêu hoá. Khi vào trong cơ thể, nói chung chúng trải qua những giai đoạn sau:
Hấp thu: là giai đoạn từ khi chất PX vào qua các con đường trên đến khi chúng vào tới dịch lỏng ngoại bào.Chất PX có thể khuếch tán khắp cơ thể lúc đó gọi là nhiễm xạ hệ thống và cơ thể có thể hấp thu nhiều và nhanh (iôt), có thể hấp thu ít và chậm, kéo dài hàng năm (oxyt plutoni).
Tích đọng: sau khi hấp thu, chất PX có thể tích đọng ở một số bộ phận (iôt ở tuyến giáp, P-32, Radium ở xương…)
Tồn lưu: Khi đã vào trong cơ thể, dù tích đọng ở bộ phận nào, chất PX cũng bị tác động của các quy luật vật lý và sinh học. Chất PX giảm dần theo thời gian do bán thải vật lý và sinh học. Phần còn lại ở một thời điểm nhất định gọi là tồn lưu.
Bài tiết: qua nước tiểu và phân (không hapá thu và đã qua hấp thu).
Biện pháp phòng ngừa cơ bản tổn thương PX do nhiễm xạ trong là phải rút ngắn thời gian tồn tại chất PX trong cơ thể. Để đạt điều đó cần sử dụng các thuốc phong bế sự hấp thu và làm tăng thải chất PX ra khỏi đường tiêu hoá, hệ hô hấp và vị trí chất PX tích tụ lại.
Phong bế sự hấp thu:
Đưa vào đường tiêu hoá các chất làm kết dính chất PX, biến chúng thành những chất mới không hoà tan, không qua được nhung mao, không thâm nhapạ vào máu mà chỉ qua đường tiêu hoá rồi thải theo phân. Chúng chỉ có ý nghĩa khi được sử dụng sớm: dùng trước khi bị nhiễm xạ trong (dự phòng) hay dùng ngay sau khi bị nhiễm xạ trong (trong 15 phút đầu có hiệu lực tốt, sau 30 phút hiệu lực đã giảm và sau 2 giờ hầu như không còn ý nghĩa.
Thuốc tăng thải chất px ra khỏi đường tiêu hoá:
Khi chất PX thâm nhập vào đường tiêu hoá đầu tiên phải ngăn ngừa chúng hấp thu vào máu và tích tụ ở các tổ chức, cơ quan. Do đó cần phải cho BN uống chất hấp phụ được coi như là đặc hiệu (antidos) đối với chất PX. Chất hấp phụ không phải là đa năng đối với các chất PX mà chỉ hấp phụ một số chất riêng biệt hoặc một nhóm chất PX nhất định.
Khi chất PX là Stronti và Bari nhập vào cơ thể qua đường tiêu hoá, cần dùng các chất hấp phụ như barisulphat, polysurmin, anginat canxi. Nếu là I-131 thì dùng iôt có cấu trúc ổn định, còn nếu là xeri thì dùng pherosin, bermiculit.
Một số chất hấp phụ phổ biến như than hoạt, cao lanh thực tế ít có hiệu quả hấp phụ chất PX.
Để tăng thải chất PX ra khỏi cơ thể có hiệu quả sử dụng các chất trao đổi ion. Chất ở trạng thái cation (Sr-90, Ba-140, Pu-210) hoặc anio (Mo-99, U-238) trao đổi với ion tương ứng làm giảm 1,5-2 lần lượng PX hấp thu vào máu.
Đánh giá thuốc bằng cách đo các chất thải và đo tồn đọng. Đo tồn đọng phải dùng đến phương pháp đo xạ toàn thân.
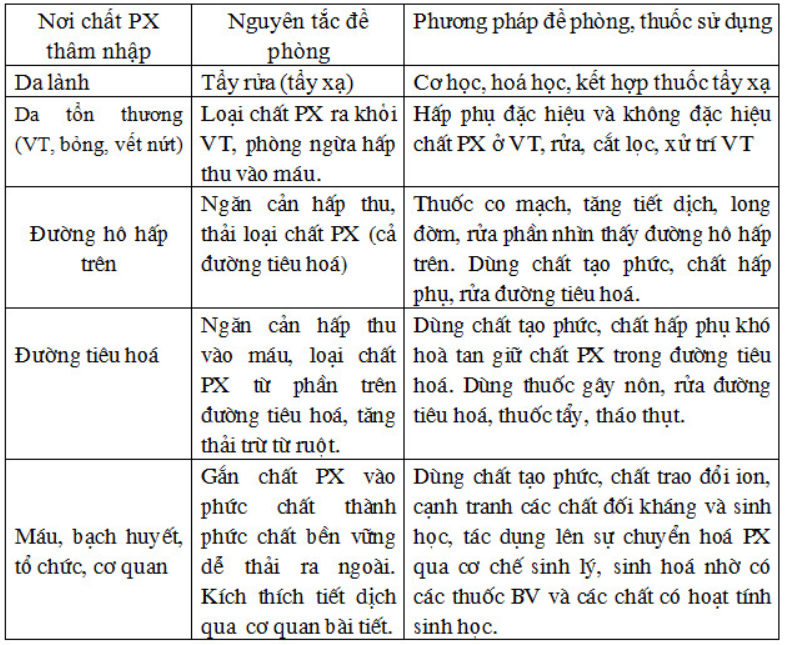
Tổng quát về đề phòng tổn thương do nhiễm xạ trong như sau:
Phòng chống tổn thương da do px:
Biện pháp có hiệu quả nhất khi bị bụi xạ bám vào da là xử lý về sinh. Phải tiến hành càng sớm càng tốt ngay sau khi bị nhiễm xạ. Rửa kỹ bằng nước và xà phòng.
Sản phẩm phân hạch loại hoà tan khi vũ khí hạt nhân nổ trên mặt nước hay dưới nước loại khỏi da rất khó, cần phải sử dụng axit chlohydric 1-3% hoặc xitrat natri. Làm sạch da bằng giẻ, bàn chải… ít có hiệu quả.
Trong điều kiện chiến đấu có thể bụi phóng xạ rơi vào vết thương, vết bỏng. Chất PX dễ hoà tan ngấm vào máu nhanh chóng, lượng hấp thụ có thể đạt tới vài chục % số lượng chất PX rơi vào vết thương. Sự hấp thu chất PX qua bề mặt da bị bỏng độ I-II cao hơn 2-20 lần so với da lành.
Để giảm hấp thu chất PX từ vết thương, vết bỏng vào máu, sử dụng các chất hapá phụ khác nhau. Bông băng bình thường cũng có khả năng hấp phụ tốt chất PX (tới 60%). Xử lý ngoại khoa là tốt nhất, khi đó đến 90% bụi phóng xạ được loại ra.
Phương pháp xử lý ngoại khoa vết thương, vết bỏng có nhiễm bụi xạ được tiến hành bình thường nhưng trước đó phải làm sạch phần da lành quanh vết thương khỏi bụi PX. Ngoài ra còn chỉ định rửa vết thương, vết bỏng nhiều lần bằng nước đun sôi để nguội, nước muối sinh lý, dung dịch loãng thuốc sát trùng.