(Tài liệu sử dụng tập huấn cho cán bộ y tế)
Danh mục từ viết tắt
|
BYT |
Bộ Y tế |
|
BKT |
Bơm kim tiêm |
|
COVID-19 |
Bệnh do vi-rút corona 2019 |
|
HAT |
Hộp an toàn |
|
5K |
Khẩu trang, Khử khuẩn, Khoảng cách, Không tụ tập, Khai báo y tế |
|
HIV |
Vi rút gây suy giảm miễn dịch ở người (Human Immunodeficiency Virus) |
|
SARS-CoV-2 |
Hội chứng hô hấp cấp tính nghiêm trọng do viruts corona 2 gây ra. |
|
TCMR |
Tiêm chủng mở rộng |
Phần i: thông tin về vắc xin phòng covid-19 moderna
Giới thiệu về vắc xin phòng covid-19 moderna
Vắc xin phòng COVID-19 Moderna là vắc xin RNA thông tin (mRNA). Vắc xin mRNA giúp các tế bào cơ thể tạo ra một loại protein vô hại. Sau đó, protein vô hại này sẽ kích hoạt phản ứng miễn dịch của cơ thể tạo kháng thể chống lại vi rút SARS-CoV2 là tác nhân gây bệnh COVID-19. Vắc xin mRNA:
Không làm thay đổi hoặc tương tác với DNA của người được tiêm chủng theo bất kỳ cách nào.
Không sử dụng vi rút sống gây bệnh COVID-19.
Không thể gây bệnh COVID-19 cho người được tiêm chủng.
Vắc xin phòng COVID-19 Moderna của hãng Moderna đã được Cục Quản lý Thực phẩm và Dược phẩm (FDA) cấp Giấy phép Sử dụng Khẩn cấp (EUA) vào ngày 18 tháng 12 năm 2020 và được Tổ chức Y tế thế giới thông qua chấp thuận sử dụng vắc xin trong trường hợp khẩn cấp ngày 30 tháng 4 năm 2021. Vắc xin này đã được nhiều quốc gia trên thế giới cấp phép lưu hành và sử dụng.
Tại Việt Nam, vắc xin phòng COVID-19 Moderna đã được Bộ Y tế phê duyệt có điều kiện vắc xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh COVID-19 tại Quyết định số 3122/QĐ-BYT ngày 28 tháng 6 năm 2021 và quyết đinh 3291/QĐ-BYT ngày 02/07/2021 về việc bổ sung nội dung Điều 1 Quyết định số 3122/QĐ-BYT ngày 28 tháng 6 năm 2021.
Tên vắc xin:
Moderna COVID-19 Vaccine
Moderna mRNA-1273 Vaccine
COVID-19 mRNA Vaccine (nucleiside modified)
Vắc xin SPIKEVAX
Cơ sở sản xuất/nước sản xuất:
Moderna TX-Mỹ
Catalent Indiana, LLC-Mỹ
Lonza Biologics, Inc-Mỹ
Baxter-Mỹ
Rovi Pharma Industrial Services, SA-Tây Ban Nha
Moderna Biotech-Tây Ban Nha
Racipharm Monts-Pháp
Dạng trình bày của vắc xin phòng COVID-19 Moderna:
Mỗi liều 0.5 ml vắc xin phòng COVID-19 Moderna chứa 100 mcg mRNA (được nhúng trong các lipid nanoparicle SM-102)
Ở nhiệt độ bảo quản -50°C đến -15°C: Vắc xin ở dạng dung dịch cô đặc đông lạnh.
Ở nhiệt độ bảo quản +2°C đến +8°C vắc xin ở dạng dung dịch màu từ trắng đến trắng ngà.
Vắc xin đóng lọ nhiều liều:
Lọ đa liều chứa nhiều nhất 11 liều/lọ: trong khoảng 10-11 liều, mỗi liều 0,5ml.
Lọ đa liều chứa nhiều nhất 15 liều/lọ: trong khoảng 13-15 liều, mỗi liều 0,5ml.
Hộp thứ cấp đóng gói: 10 lọ/hộp
Hiệu lực của vắc xin phòng COVID-19 Moderna:
Vắc xin đã được chứng minh là có hiệu quả tới 94,1% (dao động từ 89,3% đến 96,8% với độ tin cậy 95%). Hiệu quả được duy trì trên tất cả các nhóm tuổi (trên 18 tuổi) và không bị ảnh hưởng bởi giới tính hoặc dân tộc.
Theo một số nghiên cứu về vắc xin phòng COVID-19 Moderna, hiệu quả sau liều đầu tiên đạt 91,9% bắt đầu từ 14 ngày sau tiêm với thời gian theo dõi trung bình là 28 ngày và thông tin về việc kháng thể tồn tại đến 6 tháng sau liều thứ hai đã được ghi nhận.
Bảo quản vắc xin, vận chuyển
Điều kiện bảo quản vắc xin phòng COVID-19 Moderna
Bảo quản ở nhiệt độ âm -50°C đến -15°C trong tủ lạnh âm
Vắc xin có thể bảo quản ở nhiệt độ từ -50°C đến -15°C cho đến ngày hết hạn sử dụng được ghi trên nhãn của lọ vắc xin (7 tháng kể từ ngày sản xuất).
Không bảo quản vắc xin phòng COVID-19 Moderna ở nhiệt độ dưới -50oC, sử dụng đá khô để bảo quản có thể làm nhiệt độ hạ dưới -50oC.
Trong quá trình bảo quản vắc xin cần để lọ vắc xin thẳng đứng trong hộp và hạn chế tiếp xúc với ánh sáng. Vắc xin đã rã đông sẽ không bảo quản trở lại nhiệt độ đông băng do vậy không lấy lọ vắc xin ra khỏi tủ lạnh âm cho đến khi sẵn sàng rã đông và sử dụng vắc xin hoặc vận chuyển vắc xin.
Bảo quản ở nhiệt độ +2°C đến +8°C
Vắc xin có thể bảo quản ở nhiệt độ từ 2°C đến 8°C trong thời gian tối đa 30 ngày. Ghi lại thời gian bắt đầu bảo quản vắc xin ở nhiệt độ từ 2°C đến 8°C. Không được để đông băng lại vắc xin đã rã đông.
Nhiệt độ bảo quản khác:
Lọ vắc xin chưa mở có thể bảo quản ở nhiệt độ từ +8°C đến +25°C trong thời gian tổng cộng là 24 giờ.
Lọ vắc xin đã mở có thể bảo quản ở nhiệt độ từ +2°C đến +25°C trong tối đa 12 giờ.
Điều kiện vận chuyển vắc xin phòng COVID-19 Moderna
Nếu không thực hiện vận chuyển vắc xin phòng COVID-19 Moderna ở nhiệt độ âm. Khuyến cáo vận chuyển lọ vắc xin ở nhiệt độ từ 2°C đến 8°C trong tối đa 12 giờ. Phương tiện và đóng gói vận chuyển cần đảm bảo duy trì nhiệt độ từ 2°C đến 8°C trong suốt thời gian di chuyển và hạn chế tối đa sự rung lắc.
Sau khi rã đông và vận chuyển ở nhiệt độ +2°C đến +8°C, vắc xin sẽ tiếp tục được bảo quản ở 2°C đến 8°C cho đến khi sử dụng. KHÔNG làm đông băng lại vắc xin đã được làm rã đông.
Rã đông vắc xin
Nếu vắc xin bảo quản ở nhiệt độ âm từ -50°C đến -15°C cần rã đông vắc xin trước khi sử dụng. Thời gian rã đông phụ thuộc vào liều đóng lọ và nhiệt độ rã đông:
Lọ đa liều chứa nhiều nhất 11 liều/lọ: thời gian rã đông là 2 giờ 30 phút ở nhiệt độ 2°C đến 8°C hoặc 1 giờ ở nhiệt độ phòng 15°C đến 25°C.
Lọ đa liều chứa nhiều nhất 15 liều/lọ: thời gian rã động 3 giờ ở nhiệt độ 2°C đến 8°C hoặc 1 giờ 30 phút ở nhiệt độ phòng 15°C đến 25°C.
Lịch tiêm chủng
Vắc xin phòng COVID-19 Moderna được chỉ định tiêm phòng cho người từ 18 tuổi trở lên.
Lịch tiêm gồm 2 mũi, khoảng cách giữa mũi 2 và mũi 1 là 1 tháng (28 ngày).
Nếu mũi 2 được tiêm cách mũi 1 ít hơn 28 ngày, không cần tiêm lại mũi đó. Nếu hoãn tiêm so với lịch tiêm chủng nên tiêm càng sớm càng tốt sau đó. Hiện tại, nhà sản xuất khuyến cáo mỗi đối tượng tiêm tối đa 2 mũi.
Liều lượng, đường tiêm:
0,5ml, tiêm bắp.
Chỉ định, chống chỉ định:
Tiêm chủng vắc xin phòng COVID-19 Moderna cho nhóm đối tượng đặc biệt:
Nhóm người mắc bệnh kèm theo: Người có bệnh nền, bệnh mãn tính là đối tượng có nguy cơ cao mắc bệnh COVID-19 và cần được tiêm vắc xin phòng bệnh. Một số bệnh đi kèm đã được xác định làm tăng nguy cơ mắc bệnh COVID-19 nghiêm trọng và tử vong. Thử nghiệm lâm sàng giai đoạn 3 đã chứng minh vắc xin an toàn và hiệu quả ở những người có tình trạng sức khỏe khác nhau, bao gồm cả những người có nguy cơ cao mắc COVID-19 nặng. Các bệnh đi kèm được nghiên cứu trong thử nghiệm lâm sàng giai đoạn 3 bao gồm bệnh phổi mãn tính, bệnh tim nghiêm trọng, béo phì nặng, tiểu đường, bệnh gan và nhiễm vi rút suy giảm miễn dịch ở người (HIV). Tuy nhiên trước khi tiêm chủng, những đối tượng mắc bệnh kèm theo cần được khám sàng lọc, đánh giá bởi các chuyên gia và chỉ định tiêm chủng khi bệnh đã ổn định, nên được tiêm chủng tại bệnh viện.
Nhóm phụ nữ mang thai: Dữ liệu hiện có chưa đầy đủ để cung cấp thông tin về tiêm vắc xin cho phụ nữ mang thai. Tuy nhiên, khuyến cáo tiêm chủng vắc xin cho phụ nữ mang thai nếu lợi ích của việc tiêm chủng lớn hơn các rủi ro tiềm ẩn của vắc xin. Không khuyến cáo phải thử thai trước khi tiêm chủng, trì hoãn mang thai hoặc bỏ thai vì tiêm vắc xin.
Nhóm phụ nữ cho con bú: Tiêm vắc xin nếu các đối tượng thuộc nhóm nguy cơ. Không cần tạm ngừng cho con bú sau khi tiêm vắc xin.
Nhóm người bị suy giảm miễn dịch: Có thể tiêm vắc xin nếu đối tượng thuộc nhóm nguy cơ, các thông tin, hồ sơ về suy giảm miễn dịch cần được cung cấp cho nhân viên y tế để tư vấn về lợi ích và rủi do cũng như theo dõi, đánh giá sau tiêm chủng.
Nhóm người có tình trạng tự miễn dịch: có thể được tiêm chủng nếu đối tượng không thuộc diện chống chỉ định tiêm vắc xin.
Nhóm người bị HIV: Có thể tiêm vắc xin nếu đã kiểm soát tốt bằng điều trị bằng thuốc kháng vi rút và thuộc nhóm nguy cơ khuyến cáo tiêm vắc xin…
Nhóm người có tiền sử sử dụng kháng thể kháng COVID-19 điều trị trước đó: Khuyến cáo tiêm chủng vắc xin ít nhất 90 ngày sau điều trị kháng thể kháng COVID-19.
Chống chỉ định:
Có tiền sử phản ứng phản vệ nặng với bất kỳ thành phần nào của vắc xin phòng COVID-19 Moderna.
Những đối tượng có phản ứng phản vệ nặng sau mũi 1, không tiêm mũi 2 của vắc xin phòng COVID-19 Moderna hoặc bất kỳ vắc xin COVID-19 mRNA nào khác.
Tiêm chủng đồng thời cùng các vắc xin khác:
Chưa có đầy đủ dữ liệu về khả năng sử dụng thay thế cho nhau của vắc xin phòng COVID-19 Moderna với các vắc xin phòng COVID-19 khác. Khuyến cáo tiêm đủ 2 liều của cùng một loại vắc xin phòng COVID-19.
Nên tiêm vắc xin phòng COVID-19 Moderna cách tối thiểu 14 ngày với các vắc xin phòng bệnh khác.
Phản ứng sau tiêm chủng:
Rất phổ biến (≥1 / 10): Nhức đầu, buồn nôn, nôn, đau cơ, đau khớp và cứng khớp, đau tại chỗ tiêm, mệt mỏi, ớn lạnh, sốt, nổi hạch, sưng đỏ vị trí tiêm
Phổ biến (≥1/100 đến Phát ban, mẩn đỏ hoặc sưng tại chỗ tiêm, nôn, tiêu chảy
Không phổ biến (≥1/1000 đến ˂1/100): Ngứa chỗ tiêm
Hiếm (≥1/10000 đến ˂ 1/1000): Sưng mặt, liệt mặt ngoại biên cấp tính
Không có số liệu: Sốc phản vệ, quá mẫn tuy nhiên phản ứng phản vệ sau tiêm vắc xin là rất hiếm gặp.
Viêm cơ tim và viêm màng ngoài tim
Các báo cáo cho thấy nguy cơ viêm cơ tim và viêm màng ngoài tim tăng lên, đặc biệt là sau khi sử dụng vắc xin phòng COVID-19 Moderna liều thứ hai. Thông thường, các triệu chứng khởi phát trong vòng vài ngày sau tiêm chủng. Cần thận trọng khi chỉ định tiêm chủng vắc xin phòng COVID-19 Moderna cho các đối tượng có tiền sử viêm cơ tim hoặc viêm màng ngoài tim.
Phần ii: hướng dẫn thực hành tiêm chủng vắc xin phòng covid-19
Chuẩn bị trước buổi tiêm chủng
Lập danh sách đối tượng đến tiêm chủng không quá 100 đối tượng/điểm tiêm chủng/buổi tiêm chủng. Thông báo cho các đối tượng đến tiêm theo khung giờ để đảm bảo không tập trung quá đông trong cùng một thời điểm.
Lưu ý: Nếu đủ nhân lực y tế và diện tích có thể bố trí nhiều bàn tiêm chủng tại 1 điểm tiêm chủng
Dự trù vắc xin, BKT, HAT và trang thiết bị sử dụng cho buổi tiêm chủng.
Chuẩn bị dụng cụ cần thiết cho buổi tiêm chủng
Thiết bị bảo quản vắc xin (tủ lạnh/hòm lạnh/phích vắc xin)
Nhiệt kế theo dõi nhiệt độ bảo quản vắc xin.
Các dụng cụ khác (bông, panh, khay men, săng chải bàn…)
Thùng đựng rác, túi hoặc hộp đựng vỏ lọ vắc xin riêng.
Giấy bút, bàn, ghế, biển chỉ dẫn.
Nhiệt kế đo thân nhiệt, ống nghe, máy đo huyết áp.
Phiếu khám sàng lọc trước tiêm chủng vắc xin phòng COVID-19; Phiếu đồng ý tham gia tiêm vắc xin phòng COVID-19; Giấy xác nhận tiêm chủng vắc xin phòng COVID-19.
Xà phòng, nước rửa tay, dung dịch sát khuẩn.
Hộp chống sốc có đầy đủ cơ số thuốc còn hạn sử dụng, dụng cụ cần thiết theo Thông tư 51/2017/TT-BYT ngày 29/12/2017 về Hướng dẫn phòng, chẩn đoán, xử trí phản vệ.
Đối với các điểm tiêm chủng tại các cơ sở điều trị bệnh nhân COVID-19 nhân viên tiêm chủng cần được trang bị phòng hộ cá nhân.
Phân công nhân lực:
Đối với điểm tiêm cố định: Tối thiểu phải có 3 nhân viên y tế, trong đó có ít nhất 01 nhân viên có trình độ chuyên môn từ y sỹ trở lên. Các nhân viên Y tế phải được tập huấn về tiêm chủng vắc xin phòng COVID-19.
Điểm tiêm lưu động: Có tối thiểu 02 nhân viên y tế, nhân viên thực hiện khám sàng lọc, tư vấn, theo dõi, xử trí phản ứng sau tiêm chủng có trình độ chuyên môn từ y sỹ trở lên; Các nhân viên Y tế phải được tập huấn về tiêm chủng vắc xin COVID-19.
Tại mỗi điểm tiêm chủng phải có bảng phân công nhiệm vụ cụ thể cho từng nhân viên.
Người hỗ trợ đón tiếp, đo thân nhiệt, khai báo y tế, hướng dẫn và sắp xếp đối tượng tại điểm tiêm, ghi chép vào danh sách đối tượng, giấy xác nhận đã tiêm chủng vắc xin phòng COVID-19.
Nhân viên y tế đảm nhiệm khám sàng lọc, tư vấn trước tiêm chủng và xử lý tai biến nặng sau tiêm chủng (nếu có).
Nhân viên y tế tiêm chủng vắc xin.
Nhân viên y tế theo dõi đối tượng sau tiêm chủng.
Tại điểm tiêm chủng phải có số điện thoại người/đội cấp cứu lưu động/ cơ sở điều trị hỗ trợ cấp cứu, xử trí các trường hợp tai biến nặng.
Bố trí điểm tiêm chủng:
Bố trí điểm tiêm chủng theo quy tắc 1 chiều, đảm bảo giãn cách giữa các bàn/vị trí tiêm chủng.
Bố trí đủ diện tích ở khu vực chờ trước tiêm chủng và khu vực ở lại theo dõi sau tiêm chủng để đảm bảo giãn cách giữa các đối tượng.
Có sơ đồ hướng dẫn để người đến tiêm chủng dễ dàng thực hiện.
Đón tiếp, hướng dẫn khai báo y tế →Khu vực chờ trước tiêm chủng →Bàn khám sàng lọc và tư vấn trước tiêm chủng → Bàn tiêm chủng, ghi chép, vào sổ tiêm chủng →Khu vực ở lại theo dõi sau tiêm chủng.
Có tài liệu hướng dẫn chuyên môn về Hướng dẫn thực hành tiêm chủng vắc xin phòng COVID-19, các tài liệu truyền thông cho người dân.
Sắp xếp bàn tiêm chủng
Sắp xếp các dụng cụ trong tầm tay và thuận tiện cho cán bộ y tế khi thao tác.
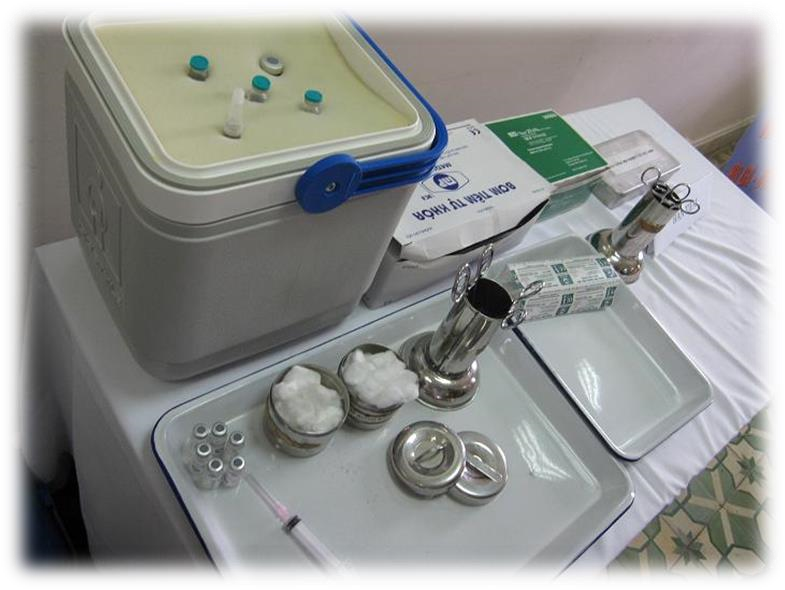
Trên bàn tiêm chủng gồm có các thiết bị cần thiết: Phích bảo quản vắc xin, bơm kim tiêm, khay đựng panh, panh, lọ đựng bông khô và lọ đựng bông có cồn, hộp chống sốc…..
Hộp an toàn, túi hoặc hộp đựng vỏ lọ vắc xin đặt phía dưới bàn.
Thùng rác đặt phía dưới bàn.
Hình 2. Hình ảnh bàn tiêm chủng
Trước khi thực hiện buổi tiêm chủng, các cơ sở tổ chức tiêm chủng thực hiện rà soát, đánh giá công tác chuẩn bị, sẵn sàng đáp ứng xử trí cấp cứu các sự cố bất lợi sau tiêm chủng vắc xin phòng COVID-19 sử dụng Bảng kiểm an toàn tiêm chủng vắc xin phòng COVID-19 (Phụ lục 9)
Đón tiếp và khai báo y tế
Yêu cầu đối tượng tiêm chủng, người nhà khi đến tiêm chủng đều phải đeo khẩu trang.
Hướng dẫn, kiểm tra đối tượng đến tiêm chủng và người đi cùng thực hiện khai báo y tế.
Thực hiện đo nhiệt độ, sàng lọc các trường hợp nghi ngờ có bệnh đường hô hấp và có các yếu tố dịch tễ.
Khám sàng lọc trước tiêm chủng
Khám sàng lọc trước tiêm chủng cho mỗi đối tượng đến tiêm chủng để đảm bảo chỉ định đúng đối tượng và an toàn tiêm chủng.
Nhân viên y tế thực hiện khám sàng lọc phải có trình độ từ Y sĩ trở lên và đã được tập huấn chuyên môn về triển khai vắc xin phòng COVID-19.
Chuẩn bị trang thiết bị bao gồm nhiệt kế, ống nghe, máy đo huyết áp, máy đo SpO2 (nếu có), phiếu sàng lọc trước tiêm chủng vắc xin phòng COVID-19 (Phụ lục 3).
Các bước thực hiện khám sàng lọc trước tiêm chủng và điền vào phiếu
Sử dụng phiếu khám sàng lọc cho mỗi đối tượng/mỗi lần tiêm chủng .
Bước 1: Xác định tên, tuổi địa chỉ đối tượng tiêm chủng trong danh sách đối tượng.
Bước 2: Hỏi tiền sử và các thông tin có liên quan
Hỏi tình hình sức khoẻ hiện tại. Lưu ý đang sử dụng thuốc, kháng sinh, thuốc kháng nấm, thuốc điều trị HIV (ARV).
Hỏi tiền sử bệnh tật, bệnh nền, tiền sử suy giảm miễn dịch, ung thư, đang dùng thuốc corticoid, ức chế miễn dịch. Lưu ý các đối tượng có tiền sử viêm cơ tim và viêm màng ngoài tim.
Tiền sử dị ứng/phản vệ với bất kỳ căn nguyên nào, lưu ý thành phần của vắc xin phòng COVID-19 Moderna.
Hỏi các phản ứng sau tiêm ở liều tiêm chủng trước (nếu tiêm liều thứ 2).
Hỏi về tiền sử tiêm chủng vắc xin khác gần đây trong vòng 14 ngày?
Hỏi tiền sử mắc COVID-19 trong vòng 6 tháng qua?
Nếu người đã mắc COVID-19 hỏi tiền sử được điều trị bằng huyết tương của người đã điều trị khỏi COVID-19 trong vòng 90 ngày qua?
Đang mang thai, phụ nữ đang nuôi con bằng sữa mẹ.
Bước 3: Đánh giá tình trạng sức khỏe hiện tại
Đo thân nhiệt, huyết áp, đếm mạch cho tất cả các đối tượng đến tiêm.
Đếm nhịp thở và đo SpO2 ở những người có bệnh nền hô hấp và khám thực thể từng trường hợp cho phù hợp.
Bước 4: Kết luận
Chỉ định tiêm vắc xin: Khi đủ điều kiện sức khỏe, không có điểm bất thường cần hoãn tiêm hoặc chống chỉ định
Mũi 1: Tiêm cho người từ 18 tuổi trở lên.
Mũi 2: áp dụng lịch tiêm sau 1 tháng (28 ngày) sau mũi 1.
Chống chỉ định tiêm chủng với các trường hợp:
Có tiền sử phản ứng nặng phản vệ độ 2 trở lên với bất kỳ dị nguyên nào + Các trường hợp chống chỉ định khác theo hướng dẫn của nhà sản xuất:
Những đối tượng có phản ứng phản vệ nặng hoặc phản vệ độ 2 trở lên sau mũi 1, không tiêm mũi 2 của vắc xin phòng COVID-19 Moderna hoặc bất kỳ vắc xin COVID-19 mRNA nào khác.
Phản ứng phản vệ nặng với hoạt chất hoặc với bất kỳ tá dược nào có trong thành phần của vắc xin.
Tạm hoãn tiêm chủng
Người đang mắc các bệnh cấp tính, các bệnh nhiễm trùng hay mãn tính tiến triển.
Phụ nữ mang thai, phụ nữ đang nuôi con bằng sữa mẹ.
Những người bị suy giảm khả năng đáp ứng miễn dịch, ung thư giai đoạn cuối, xơ gan mất bù.
Trong vòng 14 ngày trước có điều trị corticoid liều cao (tương đương prednisolon ≥ 2 mg/kg/ngày trong ≥ 7 ngày), hoặc điều trị hóa trị, xạ trị.
Đã mắc COVID-19 trong vòng 6 tháng qua.
Trong vòng 90 ngày trước có điều trị immunoglobulin hoặc điều trị huyết tương của người bệnh COVID-19.
Tiền sử tiêm vắc xin khác trong vòng 14 ngày trước.
Các đối tượng cần được khám sàng lọc và tiêm chủng trong bệnh viện:
Người có tiền sử dị ứng với các dị nguyên khác.
Người có bệnh nền nặng, bệnh mạn tính chưa được điều trị ổn định.
Người mất tri giác, mất năng lực hành vi.
Người có bệnh mạn tính có phát hiện thấy bất thường dấu hiệu sống:
Mạch: 100 lần/phút
Huyết áp: Huyết áp tối thiểu 90 mmHg
Huyết áp tối đa 140 mmHg
Nhịp thở > 25 lần/phút và/hoặc SpO2
Các đối tượng có tiền sử viêm cơ tim và viêm màng ngoài tim.
Tư vấn trước tiêm chủng
Nhân viên y tế thực hiện tư vấn cho đối tượng tiêm chủng đọc thông tin và ký Phiếu đồng ý tham gia tiêm chủng vắc xin phòng COVID-19 (Phụ lục 2).
Các nội dung cần tư vấn
Nhân viên y tế thực hiện tư vấn cho đối tượng tiêm chủng đọc thông tin và ký Phiếu đồng ý tham gia tiêm chủng vắc xin phòng COVID-19 (Phụ lục 2).
Các nội dung cần tư vấn:
Thông báo về loại vắc xin phòng COVID-19 được tiêm chủng lần này.
Thông báo về những phản ứng có thể xảy ra sau tiêm vắc xin.
Hướng dẫn người được tiêm chủng theo dõi 30 phút tại điểm tiêm chủng và tự theo dõi sau tiêm chủng trong vòng 28 ngày, đặc biệt trong vòng 7 ngày đầu.
Dặn đối tượng tiêm chủng đến ngay bệnh viện/cơ sở y tế khi thấy một trong các dấu hiệu sau:
Ở miệng thấy có cảm giác tê quanh môi hoặc lưỡi;
Ở da thấy có phát ban hoặc nổi mẩn đỏ hoặc tím tái hoặc đỏ da hoặc chảy máu, xuất huyết dưới da;
Ở họng có cảm giác ngứa, căng cứng, nghẹn họng, nói khó;
Về thần kinh có triệu chứng đau đầu kéo dài hoặc dữ dội, li bì; ngủ gà, lú lẫn, hôn mê, co giật;
Về tim mạch có dấu hiệu đau tức ngực, hồi hộp đánh trống ngực kéo dài, ngất;
Đường tiêu hóa dấu hiệu nôn, đau quặn bụng hoặc tiêu chảy;
Đường hô hấp có dấu hiệu khó thở, thở rít, khò khè, tím tái;
Toàn thân:
Chóng mặt, choáng, xây xẩm, cảm giác muốn ngã, mệt bất thường.
Đau dữ dội bất thường tại một hay nhiều nơi không do va chạm, sang chấn.
Sốt cao liên tục trên 39 độ C mà không đáp ứng thuốc hạ sốt.
Lưu ý:
Luôn có người hỗ trợ bên cạnh 24/24 giờ, ít nhất là trong 3 ngày đầu sau tiêm chủng vắc xin phòng COVID-19.
Không nên uống rượu bia và các chất kích thích ít nhất là trong 03 ngày đầu sau tiêm chủng.
Bảo đảm dinh dưỡng đầy đủ.
Nếu thấy sưng, đỏ, đau, nổi cục nhỏ tại vị trí tiêm: Tiếp tục theo dõi, nếu sưng to nhanh thì đi khám ngay, không bôi, chườm, đắp bất cứ thứ gì vào chỗ sưng đau.
Thường xuyên đo thân nhiệt, nếu có:
Sốt dưới 38,5 độC: Cởi bớt, nới lỏng quần áo, chườm/lau bằng khăn ấm tại trán, hố nách, bẹn, uống đủ nước. Không để nhiễm lạnh. Đo lại nhiệt độ sau 30 phút.
Sốt từ 38,5 độ C trở lên: Sử dụ ng thuốc hạ sốt theo chỉ dẫn của nhân viên y tế. Nếu không cắt được sốt hoặc sốt lại trong vòng 2 tiếng cần thông báo ngay cho nhân viên y tế và đến cơ sở y tế gần nhất.
Hướng dẫn các đối tượng tiêm chủng sau khi tiêm vắc xin vẫn phải thực hiện các biện pháp phòng chống dịch COVID-19 (Thông điệp 5K).
Nhắc đối tượng tiêm chủng giữ phiếu xác nhận đã tiêm chủng, tải phần mềm Sổ sức khỏe điện tử và đăng ký tài khoản trên ứng dụng để theo dõi lịch sử tiêm chủng vắc xin COVID-19 và chủ động khai báo về sự cố bất lợi sau tiêm chủng.
Tiêm vắc xin
Chuẩn bị vắc xin.
Thực hiện theo kỹ thuật vô trùng. Thực hiện vệ sinh tay trước khi chuẩn bị vắc xin và bất cứ lúc nào tay bị bẩn.
Nếu vắc xin bảo quản ở nhiệt độ 2oC đến 8oC: lấy vắc xin ra khỏi tủ lạnh dương hòm lạnh hoặc phích.
Kiểm tra vắc xin
Kiểm tra nhãn lọ vắc xin. Nếu lọ vắc xin không có nhãn phải hủy bỏ.
Kiểm tra hạn sử dụng của vắc xin. Ngày hết hạn của vắc xin được ghi trên nhãn các lọ vắc xin. Nếu quá hạn sử dụng phải hủy bỏ. KHÔNG sử dụng vắc xin đã hết hạn.
Kiểm tra nhãn ghi thời gian bảo quản vắc xin trong tủ lạnh dương ở nhiệt độ 2°C đến 8°C: thời gian tối đa là 30 ngày. KHÔNG sử dụng vắc xin bảo quản quá thời gian trên.
Kiểm tra cảm quan vắc xin: dung dịch có màu từ trắng đến trắng ngà, có thể chứa các hạt màu trắng hoặc trong mờ liên quan đến sản phẩm. Không sử dụng các lọ vắc xin có chất dạng hạt khác và/hoặc đổi màu.
Thực hành tiêm vắc xin:
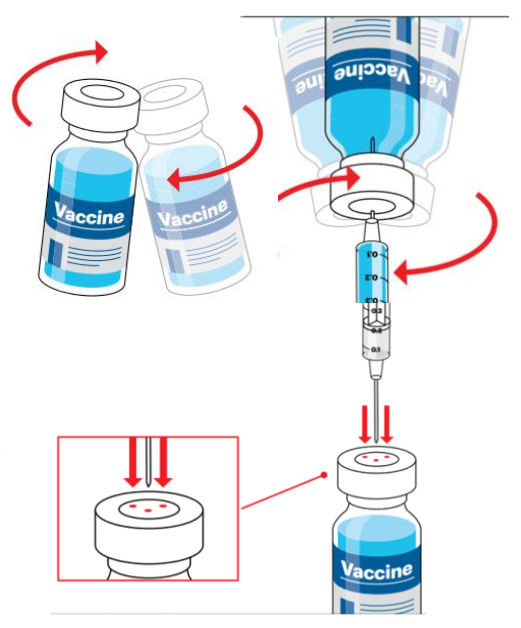
Sát trùng nút lọ vắc xin bằng một miếng bông cồn mới, vô trùng.
Xoay nhẹ lọ vắc xin mỗi lần lấy vắc xin. KHÔNG lắc lọ vắc xin. Với mỗi lần lấy vắc xin, thay đổi điểm cắm của kim qua các vị trí khác nhau của nắp lọ vắc xin để giảm nguy cơ rò rỉ vắc xin.
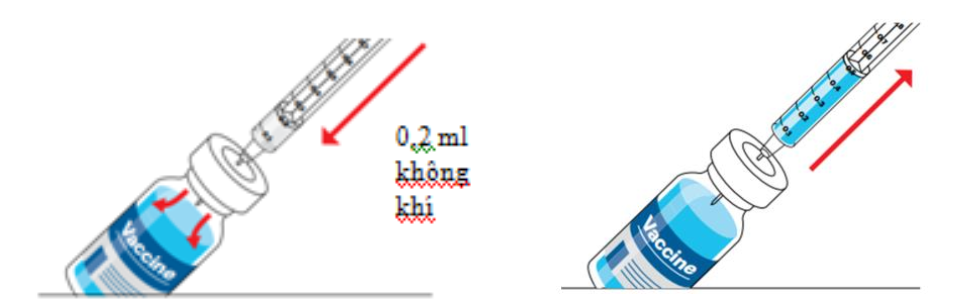
Nếu sử dụng bơm kim tiêm dùng một lần: Lấy 0,2 ml không khí và bơm vào lọ vắc xin trước khi lấy vắc xin. KHÔNG áp dụng bước này khi sử dụng bơm kim tiêm tự khóa.
Lấy 0,5 ml vắc xin vào bơm tiêm.
Sử dụng cùng một kim tiêm để rút và tiêm vắc xin. Đảm bảo lượng vắc xin trong bơm tiêm là 0,5 ml. Nếu lượng vắc xin còn lại trong lọ không đủ liều 0,5 ml, hãy bỏ số vắc xin còn lại trong lọ vắc xin. KHÔNG dồn vắc xin từ nhiều lọ với nhau để có được một liều 0,5ml.
Đề nghị người được tiêm ngồi xuống. Lưu ý cán bộ y tế không ngồi trực diện với đối tượng tiêm chủng để phòng lây nhiễm SARS-CoV-2. 2) Để lộ vùng vai và đặt cánh tay ra sau lưng hoặc chống tay vào hông. Cơ ở cánh tay sẽ được thả lỏng và khi tiêm sẽ đỡ đau hơn.
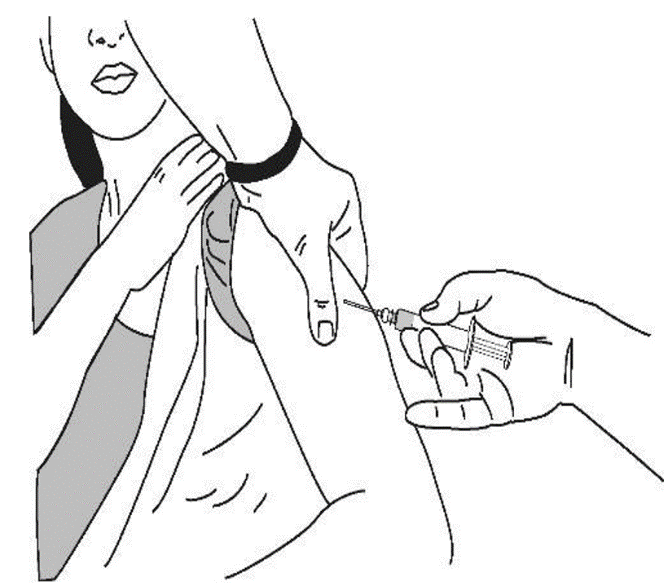
Cán bộ y tế đặt các ngón tay và ngón cái ở phần ngoài phía trên cánh tay của đối tượng tiêm chủng, bóp nhẹ vào cơ cánh tay của người được tiêm.
Đâm nhanh và thẳng kim xuyên qua da giữa các ngón tay làm cữ của bạn. Đâm sâu vào bắp thẳng góc 90 độ.
Ấn pít tông bằng ngón cái đẩy vắc xin vào.
Rút kim nhanh, nếu nơi tiêm bị chảy máu sử dụng bông khô vô khuẩn ấn vào chỗ tiêm.
Hình 3 : Kỹ thuật tiêm bắp
Ghi chép thông tin sau khi tiêm vắc xin:
Ghi các thông tin (số liều, ngày tiêm) vào danh sách/phần mềm quản lý đối tượng được tiêm chủng vắc xin phòng COVID-19 tích hợp trên Hệ thống thông tin tiêm chủng Quốc gia hoặc Ứng dụng Hồ sơ sức khỏe điện tử.
Ghi đầy đủ các thông tin vào Giấy xác nhận đã tiêm vắc xin phòng COVID-19 (Phụ lục 4) trả lại cho đối tượng tiêm chủng và hẹn lần tiêm chủng sau.
Kết thúc buổi tiêm chủng
Bảo quản những lọ vắc xin chưa mở trong hộp riêng trong dây chuyền lạnh ở nhiệt độ từ +2 độ C đến + 8 độ C, ưu tiên sử dụng trước trong buổi tiêm chủng sau.
Những bơm kim tiêm chưa sử dụng bảo quản theo qui định để dùng lần sau.
Các lọ vắc xin đã mở không được sử dụng nữa và để trong túi/hộp đựng rác riêng.
Bỏ bơm tiêm và kim tiêm vào hộp an toàn ngay sau khi tiêm, hủy hộp an toàn sau khi đầy.
Quản lý chất thải y tế trong tiêm phòng vắc xin phòng COVID-19 theo qui định tại Văn bản số 102/MT-YT ngày 04/3/2021 của Cục Quản lý Môi trường Y tế.
Giám sát phản ứng sau tiêm chủng
Theo dõi, xử trí phản ứng sau tiêm chủng tại điểm tiêm chủng.
Tại các điểm tiêm chủng cần phân công nhân viên y tế chịu trách nhiệm theo dõi, xử trí các trường hợp phản ứng sau tiêm chủng sẵn sàng các phương tiện cấp cứu tại chỗ, hộp thuốc phòng chống sốc.
Chuẩn bị sẵn 01 Bơm tiêm có chứa dung dịch Adrenalin 1mg/1ml (rút sẵn 1ml thuốc Adrenalin 1mg/1ml vào bơm tiêm gắn sẵn kim, đậy kín kim tiêm bằng nắp). Kết thúc buổi tiêm chủng nếu không sử dụng đến cần phải hủy bỏ bơm tiêm có chứa dung dịch Adrenalin 1mg/1ml
Có sẵn phương án phân công cụ thể người hỗ trợ cấp cứu, đội cấp cứu lưu động, phương tiện vận chuyển bệnh nhân khi cần thiết.
Yêu cầu đối tượng tiêm chủng ở lại theo dõi 30 phút để phát hiện sớm các trường hợp phản ứng sau tiêm chủng.
Khi đang triển khai tiêm chủng mà xảy ra tai biến nặng sau tiêm chủng, thì cần:
Tạm dừng buổi tiêm chủng.
Xử trí cấp cứu, trường hợp vượt quá khả năng thì phải chuyển người bị tai biến nặng sau tiêm chủng đến cơ sở khám bệnh, chữa bệnh gần nhất.
Thống kê đầy đủ thông tin liên quan đến trường hợp tai biến nặng và báo cáo theo quy định.
Ghi nhận, báo cáo phản ứng sau tiêm chủng
Ghi nhận phản ứng sau tiêm chủng thông qua thông tin phản hồi từ đối tượng tiêm chủng hoặc khi đối tượng đến cơ sở tiêm chủng, khám chữa bệnh.
Tổng hợp thực hiện báo cáo hàng ngày về số trường hợp phản ứng sau tiêm chủng bao gồm phản ứng thông thường và các trường hợp tai biến nặng.
Các trường hợp tai biến nặng sẽ được báo cáo và điều tra ngay trong vòng 24 giờ.
Thực hiện báo cáo “0” ngay cả không ghi nhận phản ứng sau tiêm chủng.
Thống kê, báo cáo
Trong thời gian tới sẽ có thêm nhiều loại vắc xin phòng COVID-19 được đưa vào triển khai tại Việt Nam, do vậy các địa phương cần quản lý hiệu quả việc triển khai theo từng đợt (Quyết định phân bổ vắc xin của Bộ Y tế) và theo từng loại vắc xin COVID-19. Để công khai minh bạch thông tin và tạo điều kiện thuận lợi cho các cá nhân, tổ chức, đơn vị, địa phương trong quá trình triển khai chiến dịch tiêm vắc xin phòng COVID-19, các đơn vị, địa phương sử dụng Nền tảng quản lý tiêm chủng COVID-19 để triển khai chiến dịch. Thông qua việc sử dụng Hệ thống quản lý Thông tin tiêm chủng Quốc gia (https://tiemchung.vncdc.gov.vn) hoặc Ứng dụng Sổ sức khỏe điện tử (https://hssk.kcb.vn), các đơn vị triển khai thực hiện như sau:
Quản lý đối tượng tiêm chủng COVID-19
Nhập trực tiếp từng đối tượng tiêm chủng COVID-19 trên Hệ thống
Tải danh sách các đối tượng gồm có thông tin cá nhân, lịch sử tiêm chủng vắc xin COVID-19 lên Hệ thống thông qua tính năng Import trong mục quản lý đối tượng.
Lập kế hoạch tiêm chủng vắc xin COVID-19 cho những đối tượng đã được quản lý trên Hệ thống
Thực hiện quy trình tiêm chủng 4 bước trên Hệ thống gồm: Đón tiếp → Khám sàng lọc → Tiêm chủng → Theo dõi sau tiêm.
Quản lý vắc xin, vật tư tiêm chủng vắc xin COVID-19 trên Hệ thống
Báo cáo tiêm chủng COVID-19
Việc thực hiện báo cáo kết quả triển khai tiêm chủng văc xin phòng COVID-19
được triển khai từ khi đơn vị bắt đầu tiêm cho đến khi kết thúc đợt tiêm chủng, gồm các báo cáo sau:
Báo cáo hàng ngày:
Tổng hợp báo cáo hàng ngày kết quả triển khai tiêm chủng (phụ lục 6)
Tổng hợp danh sách trường hợp tai biến nặng sau tiêm (phụ lục 7);
Báo cáo kết thúc đợt tiêm: được thực hiện trong vòng 5 ngày sau khi kết thúc triển khai (phụ lục 8).
Các đơn vị thực hiện báo cáo tiêm chủng COVID-19 như sau:
Với các đơn vị triển khai tiêm chủng: Sử dụng tính năng Báo cáo tiêm chủng COVID để báo cáo Kết quả tiêm chủng hàng ngày và Danh sách các trường hợp tai biến nặng sau tiêm chủng. Thực hiện báo cáo theo từng đơn vị, từng đợt triển khai (theo Quyết định của Bộ Y tế) và từng loại vắc xin triển khai.
Với các đơn vị không thực hiện tiêm chủng: Quản lý đối tượng tiêm (danh sách tại phụ lục 1) và Báo cáo kết thúc đợt tiêm chủng trong vòng 5 ngày sau ngày tiêm cuối (phụ lục 8).
Lưu ý với các đơn vị:
Lựa chọn vào báo cáo đúng đợt triển khai tại đơn vị, tương ứng với Quyết định phân bổ vắc xin của Bộ Y tế đã ban hành.
Thực hiện đúng thời gian quy định việc nhập báo cáo hàng ngày trên Hệ thống:
Đối với đơn vị triển khai tiêm chủng (Tuyến xã, bệnh viện, cơ sở triển khai tiêm chủng…): Thực hiện rà soát và báo cáo trước 17 giờ 00.
Đối với tuyến quận/huyện (Trung tâm Y tế quận/huyện): Rà soát báo cáo của tuyến dưới, thực hiện gửi báo cáo trước 17 giờ 30.
Đối với tuyến tỉnh/thành phố (CDC tỉnh/TP): Rà soát báo cáo của tuyến dưới, thực hiện gửi báo cáo trước 18 giờ 00.
Văn phòng TCMR Khu vực (Viện Vệ sinh dịch tễ/Pasteur): Rà soát báo cáo của các tuyến, thực hiện báo cáo trước 18 giờ 30.
Các đơn vị thực hiện báo cáo Tổng hợp kết quả tiêm vắc xin phòng COVID-19 sau khi kết thúc đợt tiêm chủng trong vòng 5 ngày cho Văn phòng TCMR Quốc gia và Khu vực (Phụ lục 8).
PHỤ LỤC
|
STT |
Nội dung |
|
Phụ lục 1 |
Danh sách đối tượng tiêm vắc xin phòng COVID-19 |
|
Phụ lục 2 |
Phiếu đồng ý tham gia tiêm chủng vắc xin COVID-19 |
|
Phụ lục 3 |
Phiếu sàng lọc trước tiêm chủng vắc xin phòng COVID-19 |
|
Phụ luc 4 |
Giấy xác nhận đã tiêm vắc xin phòng COVID-19 |
|
Phụ lục 5 |
Báo cáo hàng ngày kết quả triển khai kế hoạch tiêm chủng vắc xin COVID19 |
|
Phụ lục 6 |
Báo cáo tổng hợp hàng ngày của tuyến tỉnh |
|
Phụ lục 7 |
Báo cáo tổng hợp biến cố bất lợi của tuyến tỉnh |
|
Phụ lục 8 |
Báo cáo kết thúc chiến dịch tiêm vắc xin phòng COVID-19 |
|
Phụ lục 9 |
Bảng kiểm an toàn tiêm chủng vắc xin phòng COVID-19 |
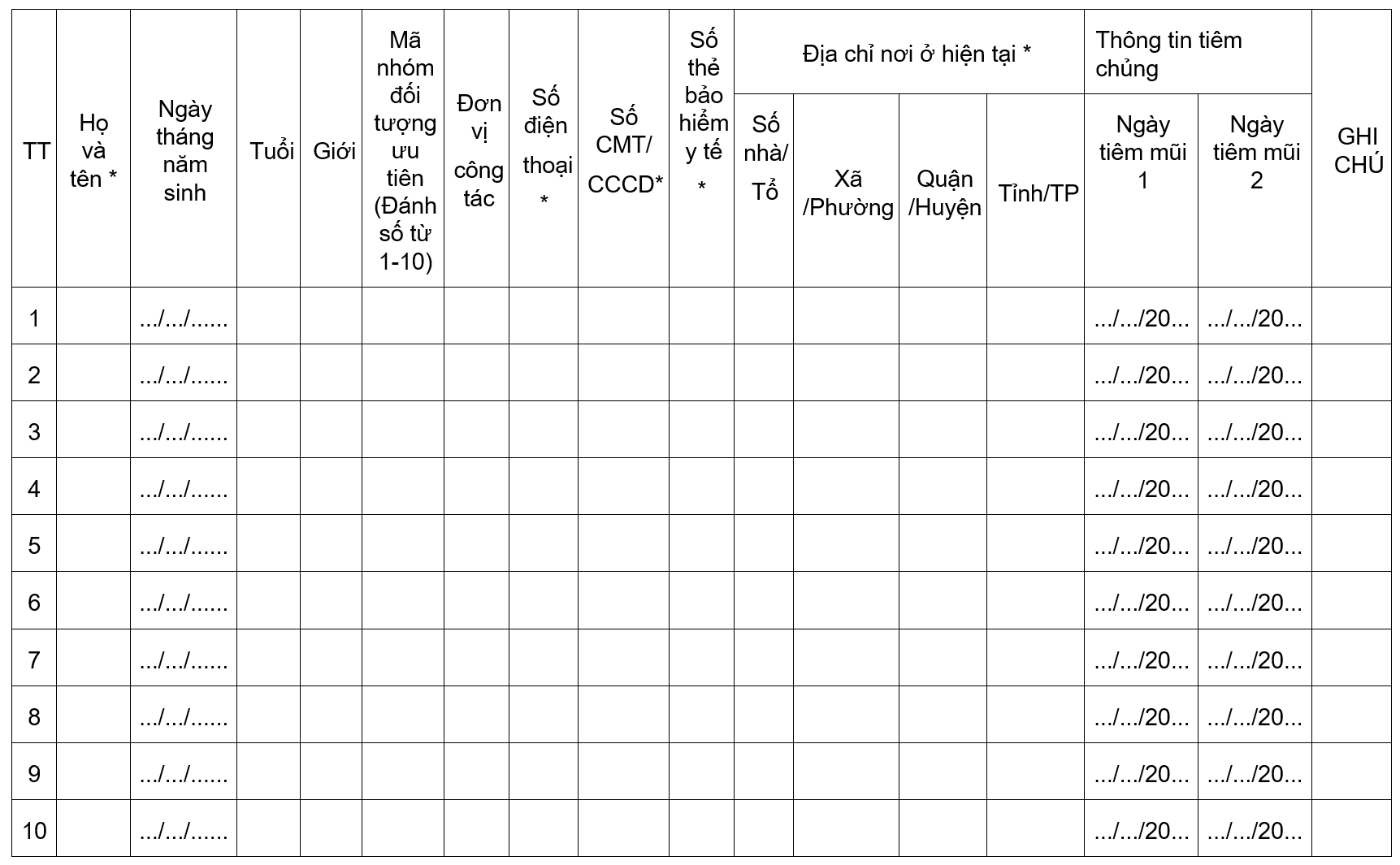
Phụ lục 1
DANH SÁCH ĐỐI TƯỢNG TIÊM VẮC XIN PHÕNG COVID-19
Tỉnh:…………….. Huyện:……………………………..
Xã:……………….. Điểm tiêm chủng:……………….
*: BẮT BUỘC PHẢI ĐIỀN
Mã nhóm đối tượng ưu tiên: (1) Lực lượng tuyến đầu phòng chống dịch; (2) Nhân viên, cán bộ ngoại giao của Việt Nam được cử đi nước ngoài; hải quan, cán bộ làm công tác xuất nhập cảnh; (3) Người cung cấp dịch vụ thiết yếu: hàng không, vận tải, du lịch; cung cấp dịch vụ điện, nước…; (4) Giáo viên, người làm việc tại các cơ sở giáo dục, đào tạo; người làm việc tại các cơ quan, đơn vị hành chính thường xuyên tiếp xúc với nhiều người; (5) Người mắc các bệnh mạn tính, người trên 65 tuổi; (6) Người sinh sống tại các vùng có dịch; (7) Người nghèo, các đối tượng chính sách xã hội; (8) Người được cơ quan nhà nước có thẩm quyền cử đi công tác, học tập, lao động ở nước ngoài; (9) Các đối tượng khác do Bộ Y tế quyết định căn cứ yêu cầu phòng chống dịch; (10) Nhóm khác, ghi rõ………
………., Ngày……..tháng ….năm 202…
|
Người lập danh sách |
Lãnh đạo đơn vị |
Phụ lục 2:
(Ban hành kèm theo văn bản số 1734/BYT-DP ngày 17/03/2021)
|
PHIẾU ĐỒNG Ý THAM GIA TIÊM CHỦNG VẮC XIN COVID-19
1.Tiêm chủng vắc xin là biện pháp phòng bệnh hiệu quả, tuy nhiên vắc xin phòng COVID-19 có thể không phòng được bệnh hoàn toàn. Người được tiêm chủng vắc xin phòng COVID-19 đủ liều có thể phòng được bệnh hoặc giảm mức độ nặng nếu mắc COVID-19. Sau khi được tiêm vắc xin phòng COVID-19 cần thực hiện đầy đủ Thông điệp 5K phòng, chống dịch COVID19.
2.Tiêm chủng vắc xin phòng COVID-19 có thể gây ra một số biểu hiện tại chỗ tiêm hoặc toàn thân như sưng, đau chỗ tiêm, nhức đầu, buồn nôn, sốt, đau cơ….hoặc tai biến nặng sau tiêm chủng.
3.Khi có triệu chứng bất thường về sức khỏe, người được tiêm chủng cần liên hệ với cơ sở y tế gần nhất để được tư vấn, khám và điều trị kịp thời.
Sau khi đã đọc các thông tin nêu trên, tôi đã hiểu về các nguy cơ và:
Đồng ý tiêm chủng ☐ Không đồng ý tiêm chủng ☐
Họ tên người được tiêm chủng:……………………………………………………………….
Số điện thoại: ……………………………………….
…………, ngày……tháng…..năm 202… (Ký, ghi rõ họ tên)
|
Phụ lục 3
(Ban hành kèm theo Quyết định số 3445/QĐ-BYT ngày 15/7/2021)
|
CƠ SỞ TIÊM CHỦNG ……………………….. |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hạnh phúc ————— |
PHIẾU SÀNG LỌC TRƯỚC TIÊM CHỦNG VẮC XIN PHÒNG COVID-19
Họ và tên:…………………………………………..………………………… …. Nam □ Nữ □
Ngày tháng năm sinh……………….…………………………………………………………………
Nghề nghiệp:…………………………………………………………………………………………………………….
Đơn vị công tác: ……………………………………………………………………………………………………………………….
Địa chỉ: ………………………………………………………………………..Số điện thoại: ……………………………………..
I.Sàng lọc:
|
1. Tiền sử phản vệ từ độ 2 trở nên ( Nếu có, loại tác nhân dị ứng………………………………) |
Không □ |
Có □ |
|
2.Tiền sử bị COVID-19 trong vòng 6 tháng |
Không □ |
Có □ |
|
3.Tiền sử tiêm vắc xin khác trong vòng 14 ngày qua ( Nếu có, loại vắc xin …………………………………….) |
Không □ |
Có □ |
|
4.Tiền sự bệnh mạn tính, đang tiến triển ( Nếu có, loại bệnh………………………………………….) |
Không □ |
Có □ |
|
5.Đang bị suy giảm khả năng đáp ứng miễn dịch nặng, ung thư giai đoạn cuối đã cắt lách, đang dùng thuốc ức chế miễn dịch, corticoid liều cao (tương đương hoặc hơn 2 mg prednisolon/kg/ngày trong ít nhất 7 ngày) |
Không □ |
Có □ |
|
6.Bệnh cấp tính ( Nếu có, loại bệnh mắc:………………….) |
Không □ |
Có □ |
|
7.Đang mang thai, phụ nữ đang nuôi con bằng sữa me |
Không □ |
Có □ |
|
8.Tiền sử dị ứng với bất kỳ dị nguyên nào |
Không □ |
Có □ |
|
9.Tiền sử bệnh nền, bệnh mạn tính được điều trị ổn định ( Nếu có, loại bệnh:……………………………………………) |
Không □ |
Có □ |
|
10.Tiền sử rối loạn đông máu/cầm máu hoặc đang sử dụng thuốc chống đông |
Không □ |
Có □ |
|
11.Độ tuổi > 65 tuổi |
Không □ |
Có □ |
|
12.Bất thường dấu hiệu sống (Ghi rõ) Nhiệt độ °C Mạch lần/phút Huyết áp mmHg Nhịp thở lần/phút, SpO2 % (nếu có) |
Không □ |
Có □ |
|
13.Dấu hiệu bất thường khi nghe tim phổi |
Không □ |
Có □ |
|
14.Rối loạn tri giác |
Không □ |
Có □ |
|
15.Đã tiêm mũi 1 vắc xin phòng COVID-19 □ Chưa tiêm □ Đã tiêm, loại vắc xin |
|
|
II.Kết luận
Đủ điều kiện tiêm chủng ngay (Tất cả đều KHÔNG có điểm bất thường)
Chống chỉ định tiêm chủng vắc xin cùng loại ( Khi CÓ điểm bất thường tại mục 1)
Trì hoãn tiêm chủng ( Khi CÓ bất kỳ điểm bất thường tại mục 2, 3, 4, 5, 6, 7 )
Chuyển tiêm chủng và theo dõi tại bệnh viện ( Khi CÓ tại mục 8, 9, 10, 11, 12, 13, 14 )
Đề nghị chuyển đến……………………………….
Lý do:…………………………………………………
|
|
Thời gian:……giờ………phút, ngày……tháng…..năm 202… Người thực hiện sàng lọc (Ký, ghi rõ họ tên)
|
Phụ lục 4
(Ban hành kèm theo văn bản số 1734/ BYT-DP ngày 17/03/2021)
 |
CỘNG HOÀ XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hạnh phúc
|
|
|
GIẤY XÁC NHẬN ĐÃ TIÊM VẮC XIN PHÒNG COVID-19
Họ và tên: …………………………………………………………………………………………………… Sinh ngày: ……………..tháng ……………..năm …………………. Số điện thoại: …………………………………………………………………………………… Địa chỉ: ………………………………………………………………………………………………………… ……………………………………………………………………………………………… Đã được tiêm vắc xin phòng COVID-19: |
||
|
Mũi 1: ngày …….tháng ……năm 202….. Loại vắc xin sử dụng: …………….. … .. …………………………………………….. |
Mũi 2: ngày …….tháng ……năm 202….. Loại vắc xin sử dụng: …………….. … .. .…………………………………………….. |
|
|
Đơn vị tiêm chủng (Ký, đóng dấu) |
Đơn vị tiêm chủng (Ký, đóng dấu) |
|
Phụ lục 5
(Ban hành kèm theo Quyết định số 1734/QĐ-BYT ngày 17/03/2021)
Mẫu
BÁO CÁO HÀNG NGÀY KẾT QUẢ TRIỂN KHAI KẾ HOẠCH TIÊM CHỦNG VẮC XIN COVID-19
(Dành cho cơ sở thực hiện tiêm chủng báo cáo)
Tỉnh/TP………………………… Quận/huyện ……………………….
Cơ sở tiêm chủng……………
Tổng số đối tượng đăng kí tiêm chủng: ………., Ngày ……../……./……..
|
Số đối tượng tiêm chủng |
Số vắc xin nhận |
Số vắc xin sử dụng |
Số vắc xin hủy |
Số vắc xin còn lại |
Số trường hợp hoãn tiêm chủng1 |
Số TH phản ứng thông thường2 |
Số TH tai biến nặng3 |
|
|
|
|
|
|
|
|
|
Ghi chú: Nếu 1 cơ sở tổ chức tiêm cho nhiều đơn vị thì sử dụng bảng dưới đây:
|
Tên đơn vị |
Số đối tượng tiêm chủng |
Số vắc xin nhận |
Số vắc xin sử dụng |
Số vắc xin hủy |
Số vắc xin còn lại |
Số trường hợp hoãn tiêm chủng1 |
Số TH phản ứng thông thường2 |
Số TH tai biến nặng3 |
|
Đơn vị đăng ký tiêm 1 |
|
|
|
|
|
|
|
|
|
Đơn vị đăng ký tiêm 2 |
|
|
|
|
|
|
|
|
Báo cáo trường hợp hoãn tiêm chủng
Số trường hợp hoãn tiêm: …………………..
Lý do khác:…………………………………………
Báo cáo cụ thể các trường hợp phản ứng thông thường
|
|
Phản ứng thông thường |
||
|
Đơn vị |
Sốt ≤39 °C |
Sưng, đau tại chỗ tiêm |
Triệu chứng khác |
|
Đơn vị đăng kí tiêm 1 |
|
|
|
|
Đơn vị đăng kí tiêm 2 |
|
|
|
Báo cáo trường hợp tai biến nặng sau tiêm chủng:
Liệt kê các trường hợp và mô tả ngắn gọn từng trường hợp:
|
STT |
Đơn vị |
Họ và tên |
Ngày sinh |
Mô tả (triệu chứng, diễn biến, cách xử trí, kết quả… ) |
|
|
|
|
|
|
|
|
|
|
|
|
Từng trường hợp được báo cáo chi tiết theo phiếu điều tra tai biến nặng sau tiêm chủng tại thông tư 34/2018/TT – BYT ngày 12 tháng 11 năm 2018.
Ngày ………..tháng ……..năm 2021
|
Người tổng hợp (Ký, ghi rõ họ tên)
|
Thủ trưởng cơ quan (Ký tên, đóng dấu)
|
Phụ lục 6: báo cáo tổng hợp hàng ngày của tuyến tỉnh
|
Đơn vị ………………………………………… |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hạnh phúc |
TỔNG HỢP BÁO CÁO HÀNG NGÀY KẾT QUẢ TRIỂN KHAI TIÊM CHỦNG VẮC XIN PHÒNG COVID-19
Thời gian bắt đầu triển khai: Ngày ……../……/2021
Ngày báo cáo: ……/……../2021
*: Đợt tiêm: Tính theo Quyết định của Bộ Y tế (Đơt 5: QĐ 2971/QĐ-BYT ngày 17/6/2021; Đợt 6: QĐ 3020/QĐ-BYT ngày 23/6/2021)
**: Số vắc xin sử dụng nguyên lọ (liều) (VD1: lọ vắc xin 10 liều đã mở, sử dụng để tiêm chủng cho 9 người, còn 1 liều trong lọ sau buổi tiêm chủng thì số sử dụng báo cáo là 10 liều. VD2: lọ vắc xin 10 liều đã mở, sử dụng để tiêm chủng cho 11 người thì số sử dụng báo cáo là 10 liều)
***: Số ca phản ứng nhẹ được ghi nhận trong ngày nhưng có thể bao gồm các ca được tiêm chủng trước ngày báo cáo. Một người có nhiều triệu chứng chỉ ghi nhận 1 trường hợp ở cột này
****: Trường hợp xác định là phản ứng nặng thì bắt buộc phải có thông tin báo cáo để nhập vào danh sách “PL 2”. Đề nghị Hội đồng chuyên môn cấp tỉnh tổ chức họp và đánh giá, xác định, phân loại ca phản ứng sớm trong vòng 5 ngày kể từ khi nhận báo cáo theo quy định.
|
Người làm báo cáo |
Ngày……..tháng ….năm 2021 Lãnh đạo đơn vị |
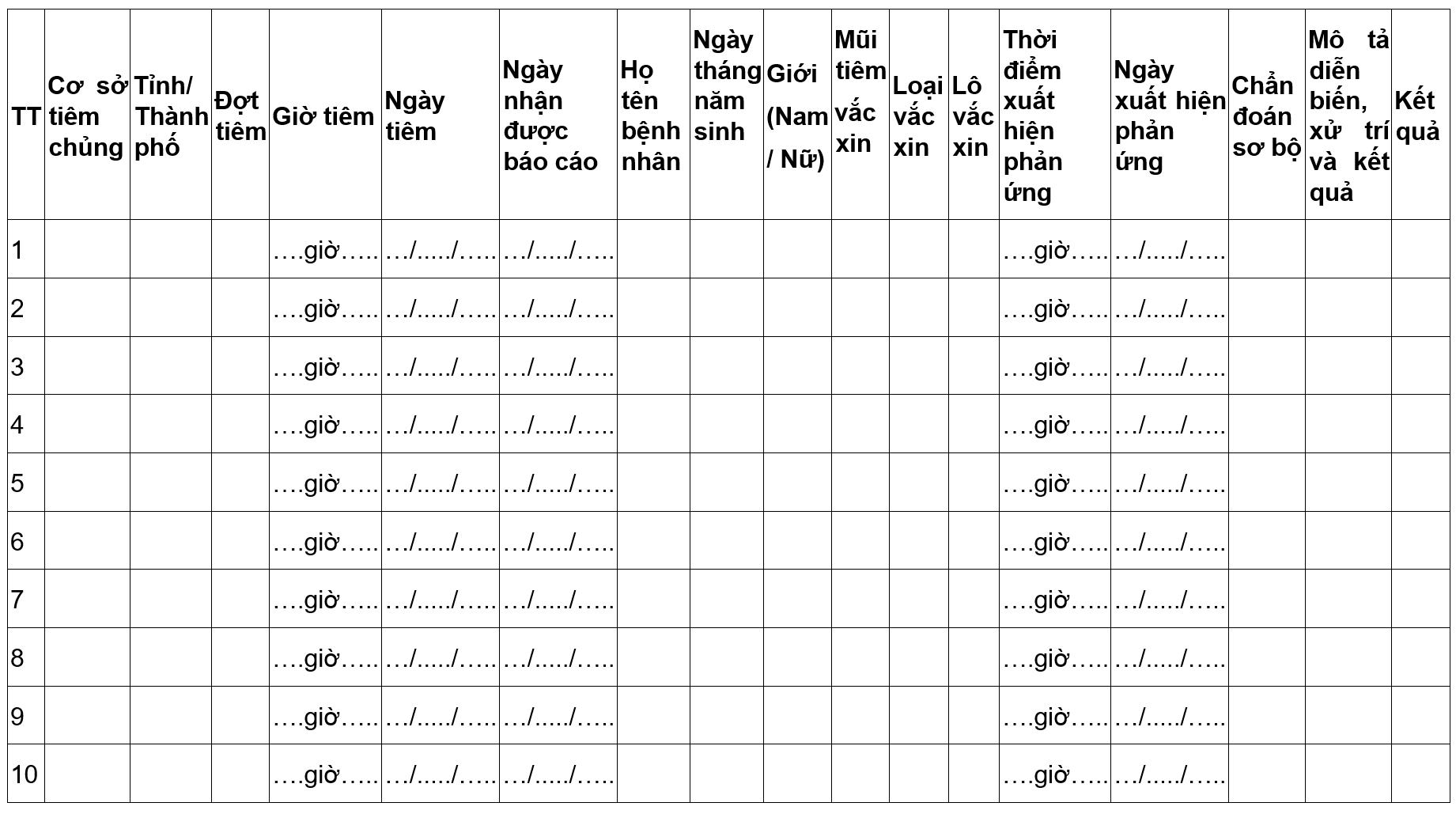
Phụ lục 7: tổng hợp biến cố bất lợi của tuyến tỉnh
Phụ lục 2:
|
ĐƠN VỊ ………………………………………… |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hạnh phúc |
TỔNG HỢP BÁO CÁO HÀNG NGÀY TRƯỜNG HỢP TAI BIẾN NẶNG SAU TIÊM CHỦNG VẮC XIN PHÒNG COVID-19
Thời gian bắt đầu triển khai: Ngày ……../………/2021
Ngày báo cáo: ………/………./2020
|
Người làm báo cáo |
Ngày……..tháng ….năm 2021 Lãnh đạo đơn vị
|
Phụ lục 8:
|
TỈNH: ………………………………… |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hanh phúc ——————— |
Ngày tháng năm 2021
BÁO CÁO KẾT QUẢ TRIỂN KHAI TIÊM CHỦNG VẮC XIN PHÒNG COVID-19
ĐỢT ……..
I.KẾT QUẢ
Kết quả chung:
|
Nhóm đối tượng ưu tiên |
Các đợt trước đây |
|
Đợt này |
|
Ghi chú |
||
|
Số đối tượng |
Số đã tiêm |
Số đối tượng |
Số đã tiêm |
Tỷ lệ (%) |
|||
|
Mũi 1 |
Mũi 2 |
||||||
|
Nhóm 1 |
|
|
|
|
|
|
|
|
Nhóm 2 |
|
|
|
|
|
|
|
|
Nhóm 3 |
|
|
|
|
|
|
|
|
Nhóm 4 |
|
|
|
|
|
|
|
|
Nhóm 5 |
|
|
|
|
|
|
|
|
Nhóm 6 |
|
|
|
|
|
|
|
|
Nhóm 7 |
|
|
|
|
|
|
|
|
Nhóm 8 |
|
|
|
|
|
|
|
|
Nhóm 9 |
|
|
|
|
|
|
|
|
Khác ………….. |
|
|
|
|
|
|
|
|
Cộng |
|
|
|
|
|
|
|
Kết quả theo đơn vị:
|
TT |
Đơn vị |
Số đối tượng |
Số đã tiêm |
Tỷ lệ (%) |
Ghi chú |
|
|
Mũi 1 |
Mũi 2 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tổng |
|
|
|
|
|
II.PHẢN ỨNG SAU TIÊM VẮC XIN PHÒNG COVID-19.
|
1. Liệt kê những dấu hiệu thường gặp sau khi tiêm vắc xin phòng Covid-19 |
Số trường hợp |
|
Số trường hợp phản ứng thông thường (Nếu 1 người có nhiều triệu chứng thì chỉ tính 1 trường hợp ở dòng này. Đối với các dòng PƯST thông thường dưới đây thì tính cho từng dấu hiệu) |
………. |
|
Đau/sưng tại chỗ tiêm |
|
|
Nôn/buồn nôn |
|
|
Tiêu chảy/đau bụng |
|
|
Sốt |
|
|
Sốt ≥39⁰ C |
|
|
Đau họng/chảy nước mũi |
|
|
Ớn lạnh |
|
|
Đau đầu |
|
|
Phát ban |
|
|
Các triệu chứng khác (ghi rõ) |
|
|
Số trường hợp tai biến nặng: |
|
|
2. Số trường hợp chống chỉ định: |
|
|
3. Số trường hợp tạm hoãn (ghi lý do tạm hoãn) |
|
|
– |
|
|
– |
|
|
– |
|
|
– |
|
|
4. Số trường hợp không đồng ý tiêm chủng |
|
|
|
|
|
5. Số trường hợp vắng mặt tại thời điểm tiêm chủng |
|
|
|
|
III.TỔ CHỨC THỰC HIỆN
1.Công tác chỉ đạo
–
–
–
2.Tổ chức thực hiện
2.1. Thời gian triển khai
Thời gian chung triển khai trên địa bàn: Từ ngày … tháng … năm 2021 đến ngày … tháng … năm 2021
Tổng số điểm tiêm chủng: ……….., trong đó:
Số điểm tiêm chủng tại trạm: ……..;
Số điểm tiêm chủng tại Bệnh viện: ……..;
Số điểm tiêm chủng lưu động: …..…; –
Số cơ sở tiêm chủng:
Bệnh viện tuyến TW/Khu vực/Tỉnh/Bộ ngành/ĐHY: ……. cơ sở;
Bệnh viện/Trung tâm Y tế huyện …………. cơ sở;
Phòng khám đa khoa… …………. cơ sở;
Trạm Y tế …………. cơ sở;
Cơ sở tiêm chủng dịch vụ …………. cơ sở;
Cơ sở khám chữa bệnh tư nhân …………. cơ sở; o
Điểm tiêm chủng lưu động …………. cơ sở;
Khác (ghi rõ)…………………………………..……………. cơ sở;
2.2. Hoạt động truyền thông
|
Nội dung |
Số lượng |
|
Tổng số lượt tuyên truyền trên báo, đài địa phương |
|
|
Số buổi phát thanh trên loa truyền thanh xã/thị trấn |
|
|
Tổng số lớp tập huấn đã mở tại địa phương |
|
|
Tổng số người tham dự |
|
|
Các tài liệu do địa phương phát hành |
|
|
Các hình thức tuyên truyền khác |
|
|
Số người đã sử dụng ứng dụng Hồ sơ sức khỏe |
|
|
Số người đã khai báo Phản ứng sau tiêm văc xin Covid-19 |
|
2.3. Cung cấp vắc xin, vật tư
|
Vật tư, vắc xin |
Có sẵn/ Tồn |
Được cấp trong TCMR |
Tự mua |
Sử dụng* |
Hủy |
Tồn |
|
Vắc xin (liều) |
|
|
|
|
|
|
|
– …… |
|
|
|
|
|
|
|
– …… |
|
|
|
|
|
|
|
Hộp an toàn (chiếc) |
|
|
|
|
|
|
|
BKT 0,5ml (cái) |
|
|
|
|
|
|
|
Vật tư khác: |
|
|
|
|
|
|
*: Số liều vắc xin đã tiêm cho đối tượng và số liều còn lại trong các lọ đã mở nhưng không sử dụng hết được tính vào số sử dụng.
2.4. Kinh phí
|
Nguồn kinh phí |
Số kinh phí (đồng) |
|
1. Ngân sách Trung ương cấp |
|
|
2. Ngân sách địa phương cấp |
|
|
– Tỉnh: |
|
|
– Huyện: |
|
|
– Xã: |
|
|
Các nguồn khác (ghi cụ thể) |
|
|
Các hình thức hỗ trợ khác (ghi cụ thể) |
|
|
Tổng cộng |
|
2.5. Công tác giám sát và nhân lực triển khai
a.Công tác giám sát
Tuyến tỉnh: Số lượt giám sát: ………lượt; Số người giám sát: ……. người; số điểm giám sát: ……. điểm
Tuyến huyện: Số lượt giám sát: ……. lượt; Số người giám sát: …… người; số điểm giám sát: …….. điểm
Các vấn đề phát hiện trong quá trình giám sát:
+
+
+
Các vấn đề đã được giải quyết:
+
+
+
b.Nhân lực trực tiếp tham gia
|
Cán bộ y tế |
Lượt người |
|
Người tình nguyện |
Lượt người |
|
Khối cơ quan quản lý |
|
Giáo dục |
|
|
|
Khối bệnh viện |
|
Hội chữ Thập đỏ |
|
|
|
Khối trường Y |
|
Hội phụ nữ |
|
|
|
Khối Y học Dự phòng |
|
Mặt trận Tổ quốc |
|
|
|
Quân Y và Y tế các ngành khác |
|
Đoàn Thanh niên |
|
|
|
Ban, Ngành, đoàn thể khác |
|
|||
|
Tổng số |
|
Tổng số |
|
IV.NHỮNG THUẬN LỢI VÀ KHÓ KHĂN
Thuận lợi
–
–
–
Khó khăn
–
–
–
V.nhận xét và đề nghị
–
–
–
|
Người tổng hợp (ký ghi rõ họ tên) |
LÃNH ĐẠO ĐƠN VỊ (ký ghi rõ họ tên, đóng dấu) |
Phụ lục 9:
Bảng kiểm an toàn tiêm chủng vắc xin phòng COVID-19
(Theo phụ lục văn bản số 5488/BYT-KCB ngày 09/7/2021)

Tài liệu tham khảo
Chính phủ Việt Nam (2021) Nghị quyết số 21/NQ-CP ngày 26 tháng 02 năm 2021 của Thủ tướng Chính phủ về mua và sử dụng vắc xin phòng COVID-19.
Chính phủ Việt Nam (2017) Nghị định số 104/NĐ-CP ngày 1/7/2016 của Thủ tướng Chính phủ qui định về hoạt động tiêm chủng.
Chính phủ Việt Nam (2018) Nghị định 155/2018/NĐ-CP ngày 12/11/2018 sửa đổi bổ sung một số qui định của Nghị định 104/NĐ-CP ngày 1/7/2016.
Bộ Y tế (2021), Quyết định số 3355/QĐ-BYT ngày 08 tháng 07 năm 2021 về việc phê duyệt kế hoạch triển khai chiến dịch tiêm vắc xin phòng COVID-19 năm 20212022.
Bộ Y tế (2021), Quyết định số 1464/QĐ-BYT ngày 05 tháng 03 năm 2021 về việc ban hành Hướng dẫn tiếp nhận, bảo quản, phân phối và sử dụng vắc xin phòng COVID-19.
Bộ Y tế (2021), Văn bản số 1734/BYT-DP ngày 17/3/2021 Hướng dẫn tổ chức buổi tiêm chủng vắc xin phòng COVID-19
Bộ Y tế (2021), Quyết định số 2995/QD-BYT ngày 18/6/2021 Hướng dẫn tạm thời Khám sàng lọc trước tiêm chủng vắc xin phòng COVID-19.
Bộ Y tế (2021), Quyết định số 3445/QD-BYT ngày 15/7/2021 Hướng dẫn sửa đổi, bổ sung Hướng dẫn tạm thời khám sàng lọc trước tiêm chủng vắc xin phòng COVID-19.
Bộ Y tế (2021), Quyết đinh số 1966/QĐ-BYT ngày 22/4/2021 về Hướng dẫn chẩn đoán và điều trị Hội chứng giảm tiểu cầu, huyết khối sau tiêm vắc xin phòng COVID-19
Văn bản số 3886/BYT-DP ngày 11/05/2021 “Hướng dẫn giám sát sự cố bất lợi sau tiêm vắc xin phòng COVID-19”
Văn bản số 4198/BYT-KCB ngày 22/05/2021 về việc Triển khai công tác an toàn tiêm chủng vắc xin phòng COVID-19”
Quyết định 3348/QĐ-BYT ngày 08/7/2021 Hướng dẫn chẩn đoán và điều trị viêm cơ tim sau tiêm chủng vắc xin phòng COVID-19
Văn bản số 5488/BYT-KCB ngày 09/7/2021 về Hướng dẫn đảm bảo an toàn tiêm chủng vắc xin phòng COVID-19
Bộ Y tế (2020) Thông tư 24/2018/TT-BYT ngày 18/9/2018 và Thông tư 05/TTBYT ngày 3/4/2020 qui định về tổ chức hoạt động của Hội đồng Tư vấn chuyên môn đánh giá tai biến nặng sau tiêm chủng.
Bộ Y tế (2017), Thông tư 34/2018/TT-BYT ngày 12/11/2018 qui định một số điều của Nghị định 104/NĐ-CP ngày 1/7/2016.
Bộ Y tế (2017), Thông tư 51/2017/TT-BYT ngày 29 tháng 12 năm 2017 Hướng dẫn phòng, chẩn đoán, xử trí phản vệ.
Dự án Tiêm chủng mở rộng Quốc gia (2017), Thực hành tiêm chủng, Tài liệu hướng dẫn cán bộ y tế (dựa theo hướng dẫn của Tổ chức Y tế Thế giới).
Thông tin từ US CDC https://vietnamese.cdc.gov/coronavirus/2019ncov/vaccines/different-vaccines/Pfizer-BioNTech.html
COVID-19 mRNA Vaccines – Immunization Action Coalition • Saint Paul, Minnesota • 651-647-9009 www.vaccineinformation.org
Fact sheet for healthcare providers administering vaccine (vaccination providers) emergency use authorization (EUA) of the Moderna COVID-19 vaccine to prevent coronavirus disease 2019 (COVID-19) updated 24 June 2021.
Extraordinary meeting of the Strategic Advisory Group of Experts on Immunization (SAGE) – 21 January 2021. Geneva: World Health Organization; 2021
WHO Prequalification – Guidance Document 23 April 2021; Status of COVID-19 Vaccines within WHO EUL/PQ evaluation process
World Health Organization, Interim recommendations for use of the Moderna mRNA-1273 vaccine against COVID-19, First issued 25 January 2021, Updated 15 June 2021.
Hill EM, Keeling MJ. Comparison between one and two dose SARS-CoV-2 vaccine prioritisation for a fixed number of vaccine doses.
Moghadas SM, Vilches TN, Zhang K, Nourbakhsh S, Sah P, Fitzpatrick MC et al. Evaluation of COVID-19 vaccination strategies with a delayed second dose.
Nam A, Ximenes R, Yeung MW, Mishra S, Wu J, Tunis M et al. Modelling the impact of extending dose intervals for COVID-19 vaccines in Canada.
Matrajt L, Eaton J, Leung T, Dimitrov D, Schiffer JT, Swan DA et al. Optimizing vaccine allocation for COVID-19 vaccines: potential role of single-dose vaccination.
Doria-Rose N, Suthar MS, Makowski M, O’Connell S, McDermott AB, Flach B et al. Antibody Persistence through 6 Months after the Second Dose of mRNA-1273 Vaccine for Covid-19. New England Journal of Medicine.