Denise Battaglini1,2, Chiara Robba1, Adriana Lopes da Silva3, Cynthia dos Santos Samary3,4, Pedro Leme Silva3, Felipe Dal Pizzol5, Paolo Pelosi1,2† and Patricia Rieken Macedo Rocco3,6*†
Tóm tắt
Việc phát hiện sớm các rối loạn chức năng tim mạch trực tiếp gây ra bởi đột quỵ thiếu máu cục bộ cấp tính (AIS) đã trở thành điều tối quan trọng. Các nhà nghiên cứu hiện nay thường đồng ý về sự tồn tại của tương tác hai chiều giữa não và tim. Ủng hộ lý thuyết này, bệnh nhân AIS rất dễ bị các biến chứng tim nặng. Tăng hoạt động giao cảm, trục hạ đồi – tuyến yên – thượng thận, các phản ứng miễn dịch và viêm, và rối loạn vi khuẩn đường ruột đã được xác định là các cơ chế bệnh lý chính liên quan đến rối loạn điều hòa trục não – tim sau AIS. Hơn nữa, bằng chứng đã xác nhận rằng các nguyên nhân chính gây tử vong sau AIS bao gồm nhồi máu cơ tim, suy tim sung huyết, huyết động không ổn định, rối loạn chức năng tâm thu thất trái, rối loạn chức năng tâm trương, tâm thu, loạn nhịp tim, dị thường điện tâm đồ và ngừng tim, tất cả đều ít nhiều liên quan đến kết cục kém và tử vong. Do đó, việc nhập viện chăm sóc đặc biệt với theo dõi huyết động liên tục đã được đề xuất như là tiêu chuẩn chăm sóc cho bệnh nhân AIS có nguy cơ phát triển các biến chứng tim mạch cao. Các thử nghiệm gần đây cũng đã nghiên cứu các liệu pháp có thể để ngăn ngừa các tai biến tim mạch thứ phát sau AIS. Labetalol, nicardipine và nitroprusside đã được khuyến cáo để kiểm soát tăng huyết áp trong thời kỳ AIS, trong khi thuốc chẹn beta được đề xuất cho cả việc ngăn ngừa tái cấu trúc mãn tính và điều trị loạn nhịp tim. Ngoài ra, sự mất cân bằng điện giải cần được xem xét và nhịp điệu bất thường phải được điều trị. Tuy nhiên, các mục tiêu điều trị vẫn còn nhiều thách thức và các cuộc điều tra thêm có thể là điều cần thiết để hoàn thành câu đố đa lĩnh vực phức tạp này. Tổng quan này nhằm làm nổi bật các cơ chế sinh lý bệnh liên quan đến sự tương tác giữa não và tim và các hậu quả lâm sàng của chúng ở bệnh nhân AIS, cũng như đưa ra các khuyến nghị cụ thể về quản lý tim mạch sau AIS.
Từ khóa: Tai biến mạch máu não cấp do thiếu máu cục bộ, Tim, Rối loạn nhịp tim,
Mạch máu não, Tim mạch, Viêm thần kinh
Giới thiệu
Bệnh tim mạch được coi là yếu tố nguy cơ chính gây đột quỵ do thiếu máu cục bộ cấp tính (AIS) [1]. Rối loạn chức năng tim vừa có thể làm trầm trọng thêm tình trạng tổn thương não đã có từ trước, vừa gây ra một tổn thương não mới. Tỷ lệ mắc AIS tăng gấp đôi ở bệnh nhân bệnh mạch vành và tăng gấp năm lần ở những người bị rung nhĩ [1]. Ngoài ra, vì tổn thương não có thể thay đổi các con đường điều hòa tự động và thần kinh liên quan đến việc kiểm soát chức năng tim, bệnh nhân bị đột quỵ rất dễ bị ảnh hưởng bởi các tác dụng phụ nghiêm trọng về tim [2]. Đặc biệt, AIS có thể góp phần làm suy giảm khả năng tự điều hòa của não, do đó làm cho lưu lượng máu não phụ thuộc hoàn toàn vào chức năng tim [3]. Trong bối cảnh này, khái niệm tương tác hai chiều giữa não và tim đã được đề xuất [4, 5]. Mục đích của tổng quan hệ thống này là làm nổi bật các cơ chế sinh lý bệnh liên quan đến tương tác giữa não và tim và các hậu quả lâm sàng của chúng ở bệnh nhân AIS, cũng như đưa ra các khuyến nghị cụ thể về quản lý tim mạch sau AIS.
Dịch tễ học về rối loạn chức năng tim trong đột quỵ do thiếu máu cục bộ
Tỷ lệ biến chứng tim mạch sau AIS dao động từ 3% đối với nhồi máu cơ tim đến > 50% đối với hẹp mạch vành không triệu chứng [6]. Các biến chứng nghiêm trọng nhất sau AIS đã được xác định trong giai đoạn cấp tính [5], và nguy cơ phát triển các biến chứng tim tỷ lệ thuận với mức độ nghiêm trọng của AIS [7]. Tương tự như vậy, suy giảm chức năng tim sau AIS làm tăng nguy cơ mắc các kết cục thần kinh tồi tệ hơn và tàn tật 90 ngày [8]. Sau AIS, 24% bệnh nhân bị rối loạn chức năng tự chủ [9], 28% cho thấy suy giảm phân suất tống máu thất trái, và 13–29% bị rối loạn chức năng tâm thu [5]. Các bất thường về điện tim được quan sát thấy ở 60–85% bệnh nhân AIS trong vòng 24 giờ đầu tiên [10, 11] (Bảng S1, Tập tin bổ sung 1).
Cơ chế sinh lý bệnh liên quan đến tương tác đột quỵ-tim
Các cơ chế chính liên quan đến cái gọi là tương tác chéo tim – não của đột quỵ bao gồm trục hạ đồi-tuyến yên-thượng thận (HPA) [12], các phản ứng miễn dịch và viêm [13], và rối loạn sinh học ruột [14], cũng như các yếu tố nguy cơ ( tuổi, giới tính, chủng tộc, tăng huyết áp, hút thuốc, ăn kiêng, và lười vận động) chủ yếu liên quan đến bệnh sinh của AIS [15]. Bất kể cơ chế nào, biến chứng tim làm tăng nguy cơ phát triển AIS và ngược lại; AIS gây ra rối loạn chuyển hóa máu và tăng viêm, do đó khiến bệnh nhân dễ bị rối loạn chức năng tim [16].
Hoạt động tự chủ không được kiểm soát sau ais
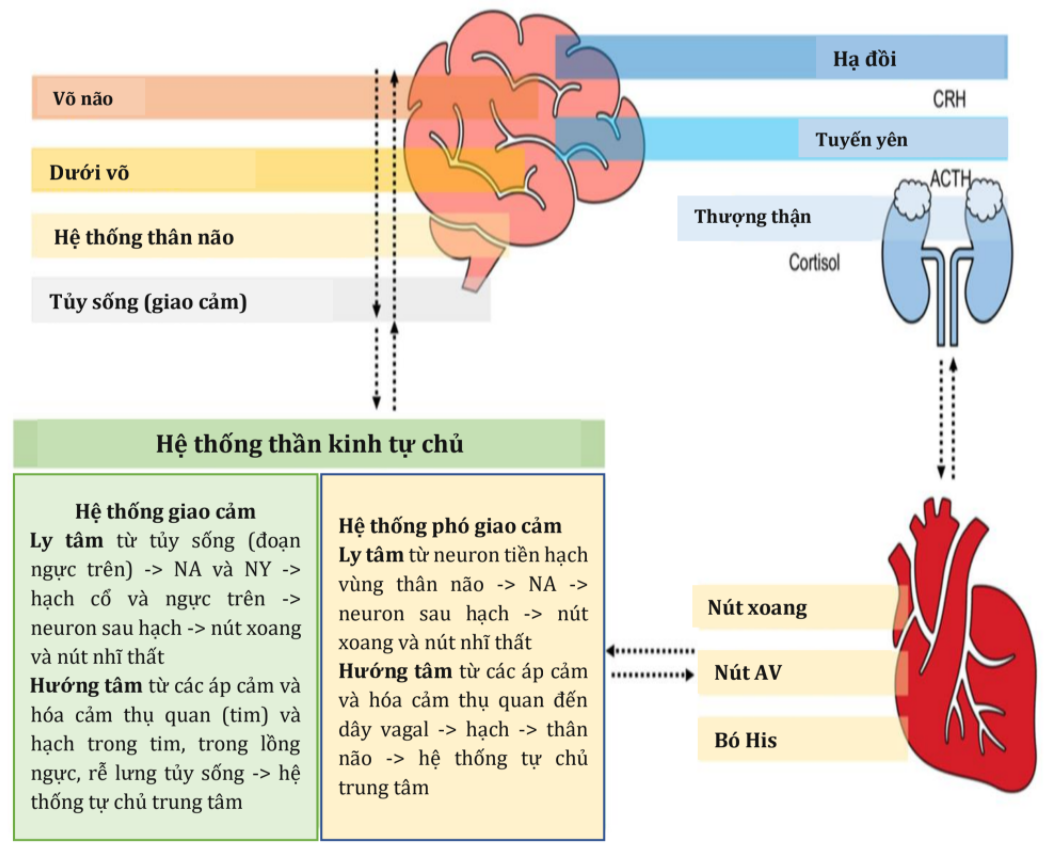
Hệ thống tự chủ trung tâm: từ não đến tim Các con đường trung tâm điều chỉnh các phản ứng tự trị từ não đến tim liên quan đến các cấu trúc liên quan đến các phản ứng sinh lý, bệnh lý và cảm xúc [17] (Hình 1). Khi tổn thương não xảy ra, mỗi vùng điều hòa trung tâm sẽ kích hoạt các con đường khác nhau phụ thuộc vào vùng bị thương liên quan và mức độ tổn thương (Hình 2). Ví dụ, sự kích thích bề mặt của thùy trán và hệ viền, làm thay đổi huyết áp và kiểm soát nhịp tim; các tổn thương do thiếu máu cục bộ của vỏ não trong ảnh hưởng đến việc kiểm soát huyết áp và gây ra các biến chứng tim nghiêm trọng, chẳng hạn như loạn nhịp tim và rối loạn chức năng tự chủ [9, 18]. Hơn nữa, nhồi máu bán cầu não trái có liên quan đến nguy cơ mắc các kết cục bất lợi về tim và tăng tỷ lệ tử vong lâu dài [19].
Tăng hoạt động giao cảm
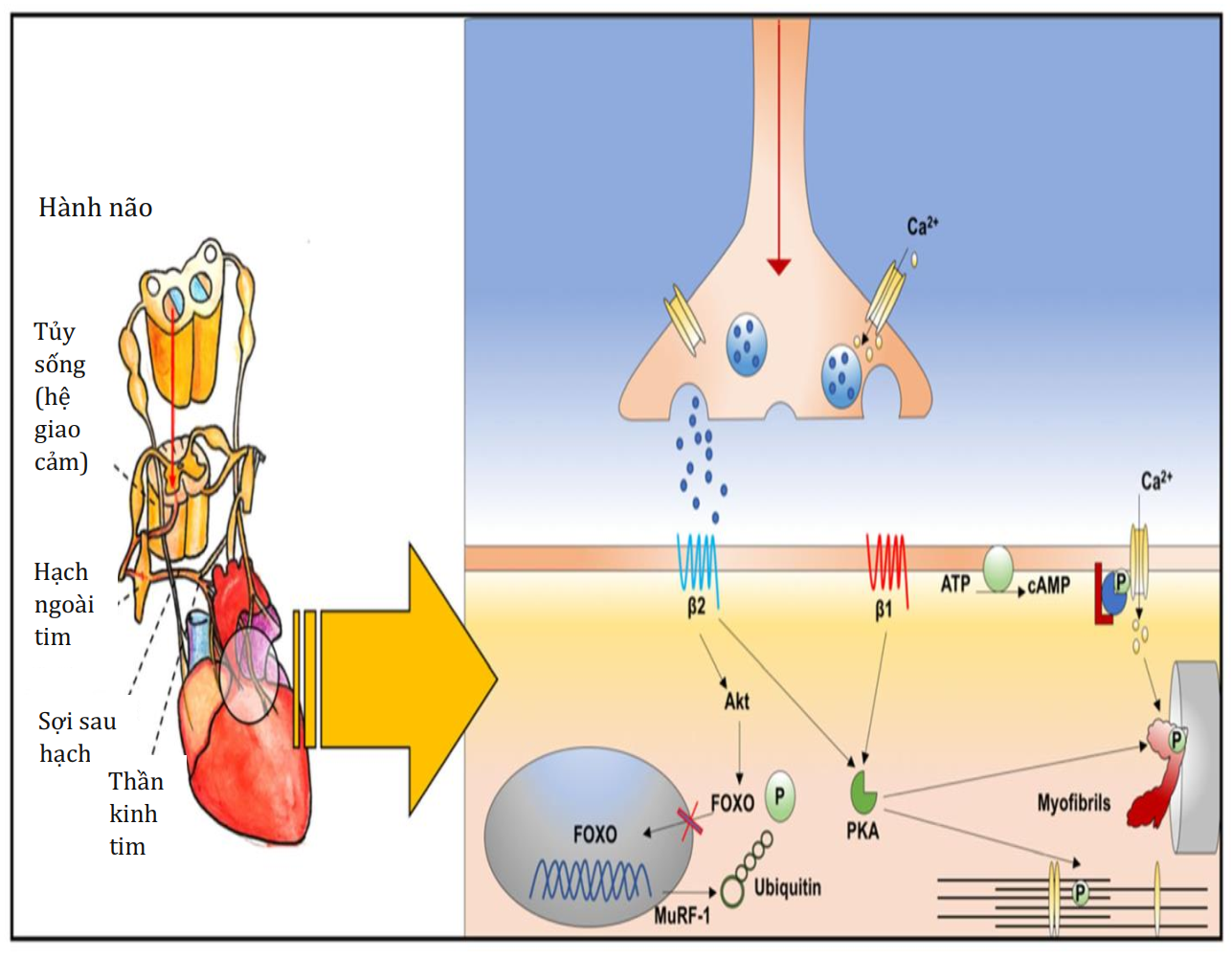
Các kết nối giao cảm giữa các nhân trung tâm và tim được trung gian bởi các tế bào thần kinh giao cảm trước hạch ở đoạn ngực trên của tủy sống, các kết nối tiếp hợp ở hạch cổ và ngực trên, và các tế bào thần kinh giao cảm sau hạch [17]. Phản ứng “chiến đấu hoặc bỏ chạy” của cơn bão catecholaminergic sau trục HPA và quá trình hoạt hóa tự trị được theo sau ở cấp độ phân tử bằng cách kích hoạt các gen đầu hộp O (FOXO). Các gen FOXO gần đây đã được xác định là mục tiêu phân tử mới tiềm năng gây rối loạn chức năng tim và có liên quan đến tăng nguy cơ nhồi máu cơ tim [20]. Noradrenaline kích hoạt thụ thể β1; đến lượt nó, kích hoạt tín hiệu adenosine monophosphate-protein kinase A vòng, do đó giải phóng canxi từ lưới cơ chất để tế bào co lại. Đồng thời, noradrenaline kích hoạt các thụ thể β2, hoạt động thông qua con đường protein kinase B (Akt) -FOXO, làm giảm sự phân hủy protein bởi ubiquitin, do đó điều chỉnh trạng thái cân bằng protein của tế bào cơ tim và duy trì khối lượng cơ tim với cơ ring finger-1, một loại protein được điều chỉnh trong tim bị thiếu hụt [20]. Hậu quả của việc tăng catecholamine này là hoại tử tế bào cơ tim, phì đại, xơ hóa và rối loạn nhịp tim [20] (Hình 3).
Hình 1. Các kết nối thần kinh: từ não đến tim và từ tim đến não. Hệ thống giao cảm đi từ tủy sống (NA và NY) đến hạch cổ và ngực trên, do đó đến nút xoang nhĩ và nút tâm nhĩ. Các liên kết hướng tâm từ các tế bào thần kinh hóa học và cơ học trong tim đến hạch rễ trong lồng ngực và rễ lưng của tủy sống, đến mạng lưới tự chủ trung ương. Hệ phó giao cảm tác động từ hành não (noradrenaline) đến nút xoang và nút nhĩ thất. Các liên kết hướng tâm từ các tế bào thần kinh hóa học và cơ học đến dây thần kinh phế vị, hạch nốt, hành não, và mạng lưới tự trị trung ương. Các hoạt động ly tâm từ vùng dưới đồi (CRH) đến tuyến yên (ACTH) đến tuyến thượng thận (cortisol). NA, noradrenaline; NY, đipeptit Y; CRH, hormone giải phóng corticotropin; ACTH, hormone vỏ thượng thận
Tăng hoạt động phó giao cảm
Các kết nối phó giao cảm bao gồm các tế bào thần kinh tiền hạch noradrenergic trong hành não, dây thần kinh phế vị và sự hệ thống lưới [17]. Các nhân này kết nối với đám rối hạch thượng tâm mạc, thông với nhau thông qua các sợi hậu hạch liên kết giải phóng acetylcholin và peptit có hoạt hóa mạch ở ruột [17]. Bằng cách liên kết với các thụ thể muscarinic type 2, acetylcholine làm giảm mức adenosine monophosphate vòng trong tế bào, do đó làm chậm tốc độ khử cực. Kích hoạt con đường này dẫn đến kéo dài thời gian dẫn truyền nhĩ thất và làm giảm sức co bóp của tâm thất [17] (Hình 1).
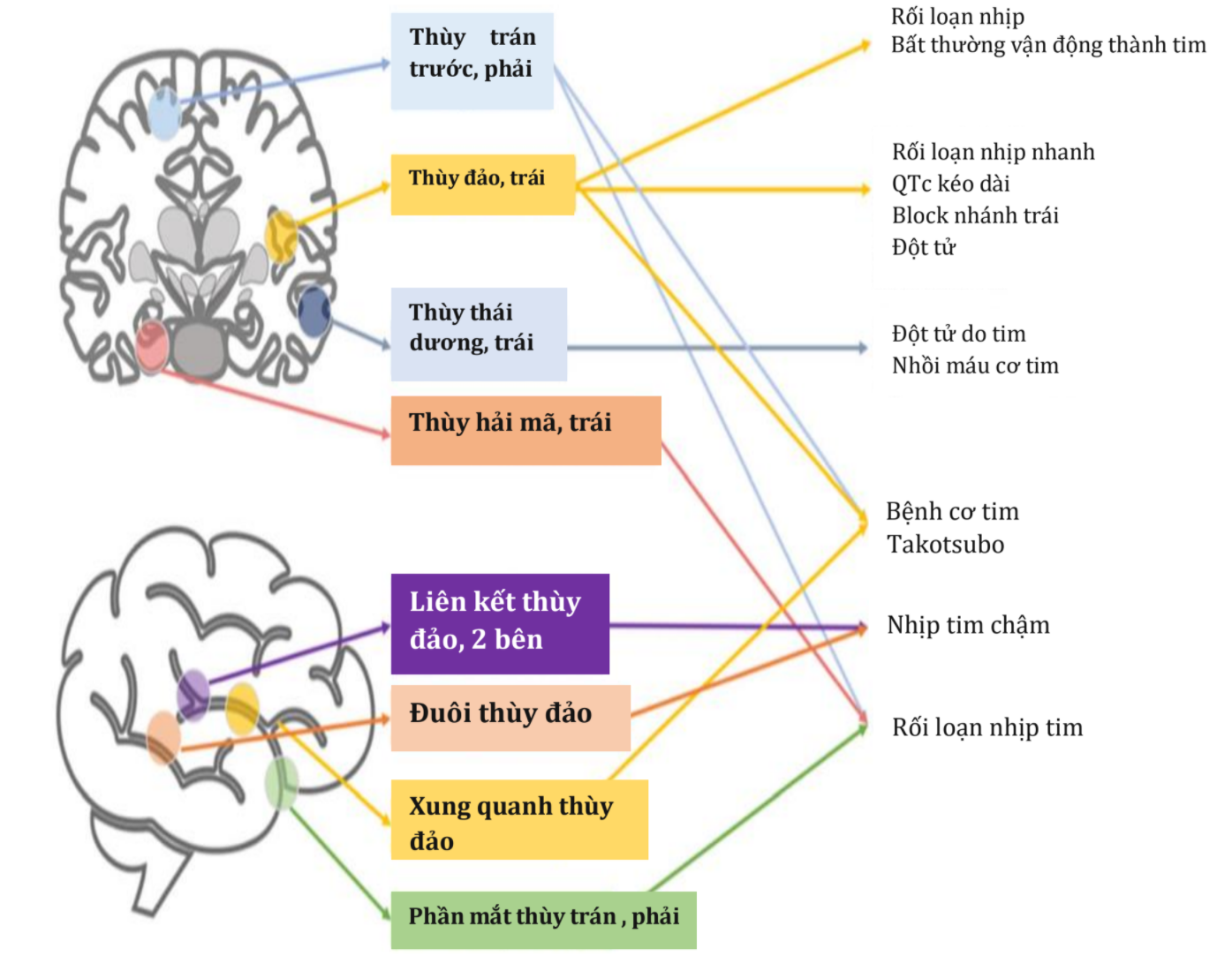
Hình 2 Kích hoạt các vùng não khác nhau trong đột quỵ sau đó là các biến chứng tim mạch cụ thể. Tùy thuộc vào mức độ tổn thương não sau đó, đột quỵ kích hoạt các vùng điều hòa trung tâm khác nhau, do đó kích hoạt các con đường tương ứng phụ thuộc vào vùng bị thương. Do đó, rối loạn chức năng tim sau đột quỵ có thể được chuyển đến các vùng não cụ thể. Đột quỵ bên phải thường liên quan đến nhiều biến chứng tim hơn đột quỵ bên trái. QTc, khoảng QT đã hiệu chỉnh
Kích hoạt phản xạ các dây thần kinh tự chủ của tim: từ tim đến não
Tế bào thần kinh hướng tâm của thụ thể hóa cảm và áp cảm thụ quan đến được nhân đơn độc, và tín hiệu được truyền đến tế bào thần kinh tim (qua tế bào thần kinh glutamatergic), đến tủy bụng bên đuôi (thông qua tế bào thần kinh GABAergic) hoặc đến tủy bụng ngực. Sau khi tích hợp đầu vào, mạng lưới tự chủ trung tâm truyền lại tín hiệu đến tim qua phó giao cảm và hệ giao cảm [17] (Hình 1).
Hình 3 Đường giao cảm não – tim ở cấp độ phân tử. Phản ứng “chiến đấu hoặc bỏ chạy” của cơn bão catecholaminergic, tiếp theo là trục hạ đồi – tuyến yên – thượng thận và sự hoạt hóa tự động, được thể hiện ở cấp độ phân tử. Kết nối synap thông qua các tế bào thần kinh và các tế bào cơ được biểu hiện. Noradrenaline kích hoạt các thụ thể β1, từ đó kích hoạt tín hiệu adenosine monophosphate-protein kinase A (cAMP-PKA) vòng, do đó giải phóng Ca2 + từ lưới cơ chất để co tế bào. Đồng thời, noradrenaline kích hoạt các thụ thể β2, hoạt động thông qua con đường protein kinase B (Akt) -FOXO, làm giảm sự phân hủy protein bởi ubiquitin, do đó điều chỉnh trạng thái cân bằng protein của tế bào cơ tim và duy trì khối lượng cơ tim với cơ đeo nhẫn-1 (MuRF-1 ), được điều hòa lên ở tim bị thiếu. FOXO, forkhead box O; Akt, protein kinase B; PKA, protein kinase A; cAMP, adenosine monophosphate mạch vòng, ATP, adenosine triphosphate; MuRF-1, cơ đeo nhẫn -1. Được điều chỉnh từ “Martini FH. Các nguyên lý cơ bản của giải phẫu và sinh lý học. Xuất bản lần thứ 8 năm 2006. Chương 20”
Phóng thích catecholamine
Hormone vỏ thượng thận kích hoạt tuyến thượng thận giải phóng cortisol, tiếp theo là catecholamine, bằng cách liên kết với thụ thể tuyến β1, điều chỉnh nồng độ canxi nội bào, gây ra stress oxy hóa, giảm tổng hợp adenosine triphosphate và dẫn đến phù nề thẩm thấu, gây chết tế bào cơ tim [21].
Phản ứng viêm tại chỗ và toàn thân đối với đột quỵ do thiếu máu cục bộ
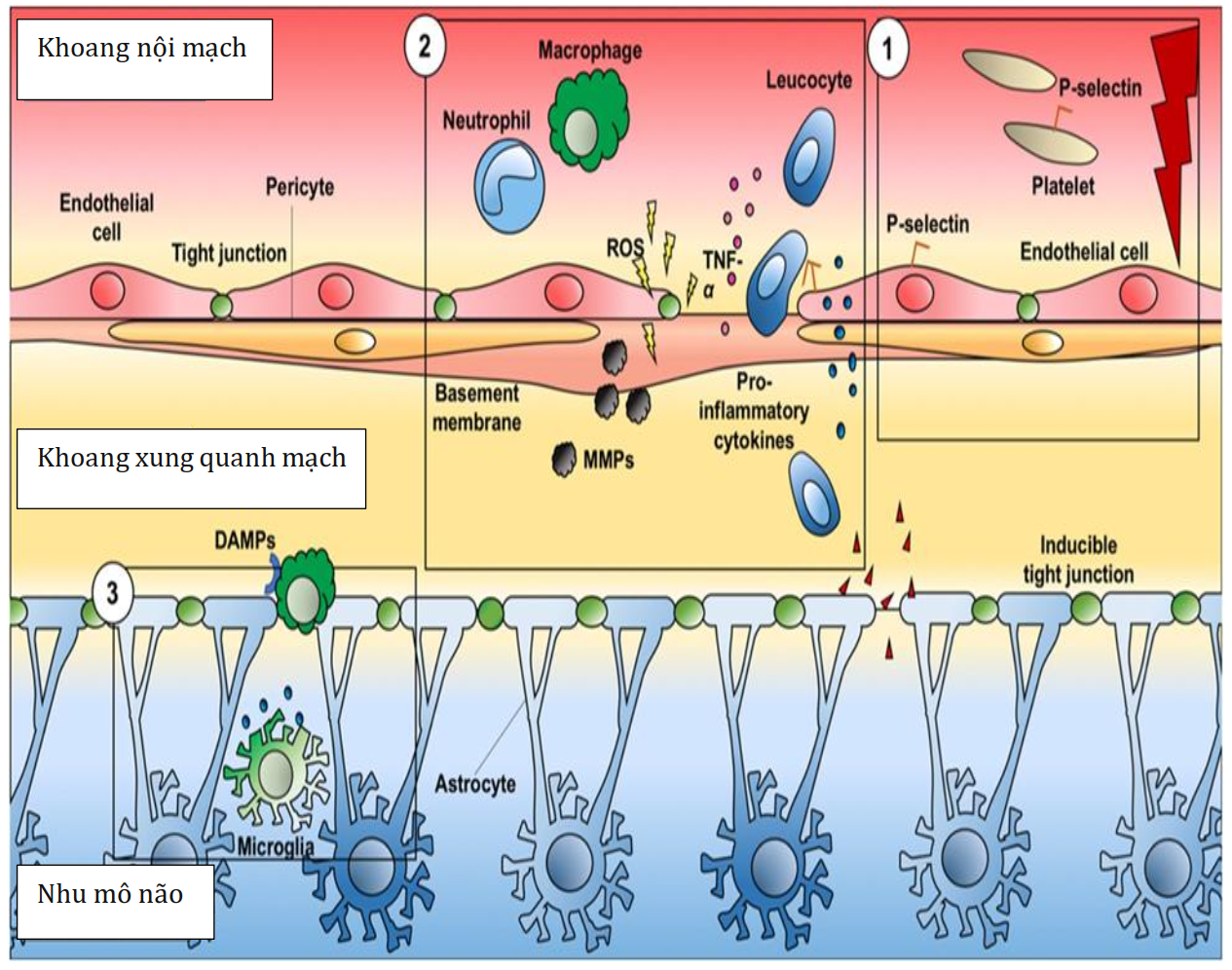
Phản ứng viêm miễn dịch đóng một vai trò nổi bật ngay sau AIS, và có liên quan chặt chẽ với tiến triển đột quỵ do thiếu máu cục bộ [22]. Trong giai đoạn đầu của AIS, các yếu tố của cả miễn dịch bẩm sinh và miễn dịch thích ứng đều tham gia vào các đợt viêm tại chỗ và toàn thân [22]. Quá trình viêm tại chỗ bắt đầu bằng việc kích hoạt các dòng thác tiền viêm (pro – inflammatory) và tiền đông máu (pro – coagualtive) vào khoang nội mạch sau khi tắc mạch, trong vòng vài phút do thiếu máu cục bộ. P-selectin, một phân tử kết dính tế bào, có trong tiểu cầu và tế bào nội mô (Hình 4, giai đoạn 1). Sau đó, các macrovesicle và liên kết với P-selectin, gây ra sự hình thành tiểu cầu và hình thành huyết khối. Sự gián đoạn hàng rào máu não (BBB) cho phép sự xâm nhập của đại thực bào ngoại vi và bạch cầu trung tính vào vùng tổn thương do thiếu máu cục bộ, đi qua không gian quanh mạch [23] (Hình 4, giai đoạn 2). Điều này dẫn đến phản ứng viêm cục bộ tăng cường trong nhu mô não, bao gồm cytokine và chemokine, thâm nhiễm microglia, thoái hóa tế bào hình sao và kích hoạt tế bào nội mô. Các microglia (tế bào có chức năng thực bào tại mô não) và đại thực bào thường trú được chuyển đổi thành kiểu hình M1 và bị thu hút vào tổn thương, đi qua BBB bị tổn thương. Các tế bào nội mô cũng bị tổn thương do tăng oxy hóa do stress và bởi các metalloproteinase được sản xuất bởi bạch cầu trung tính [24], do đó gây ra tổn thương BBB [23]. Do đó, nồng độ adenosine triphosphate tăng lên, tạo ra sự tăng phân cực của tế bào thần kinh đệm và tăng cường phản ứng viêm. Ở giai đoạn này, các cytokine tiền viêm được kích hoạt. Do đó, các tế bào miễn dịch ngoại vi khác được thu hút vào não thiếu máu cục bộ và vi tuần hoàn não, sau đó vượt qua BBB bị tổn thương và đi vào tuần hoàn hệ thống [23] (Hình 4, giai đoạn 2). Não sau thiếu máu cục bộ giải phóng các “dạng phân tử liên quan đến nguy hiểm” có khả năng kích hoạt các thụ thể giống Toll và thụ thể dọn dẹp được biểu hiện trên các đại thực bào quanh mạch, microglia và tế bào não nội mô. Các thành phần này chịu trách nhiệm cho sự trình bày kháng nguyên của các tế bào đuôi gai [23] (Hình 4, giai đoạn 3). Phản ứng viêm tại chỗ được mở rộng vào hệ tuần hoàn, gây ra tổn thương tim thứ phát. Một thử nghiệm in vitro trên tế bào tim của chuột đã chứng minh rằng, sau 90 phút thiếu oxyglucose, các tế bào tiếp xúc với tổn thương do thiếu máu cục bộ – tái tưới máu. Tương tự như vậy, một nghiên cứu in vivo đã tìm thấy biểu hiện của các dấu hiệu hoại tử, chết theo chương trình và tự thực bào trong các tế bào này [25]. Sự chết của tế bào thần kinh và tế bào tim gần đây đã được tìm thấy trong các môi trường thí nghiệm khác, cho thấy mối tương quan tiềm tàng giữa tình trạng viêm sau AIS và rối loạn chức năng tim [26]. Viêm mãn tính và chết theo chương trình được tìm thấy ở tiểu não và tim của các loài linh trưởng không phải người 6 tháng sau khi gây thiếu máu cục bộ não toàn bộ thoáng qua [27].
Rối loạn vi sinh đường ruột sau ais
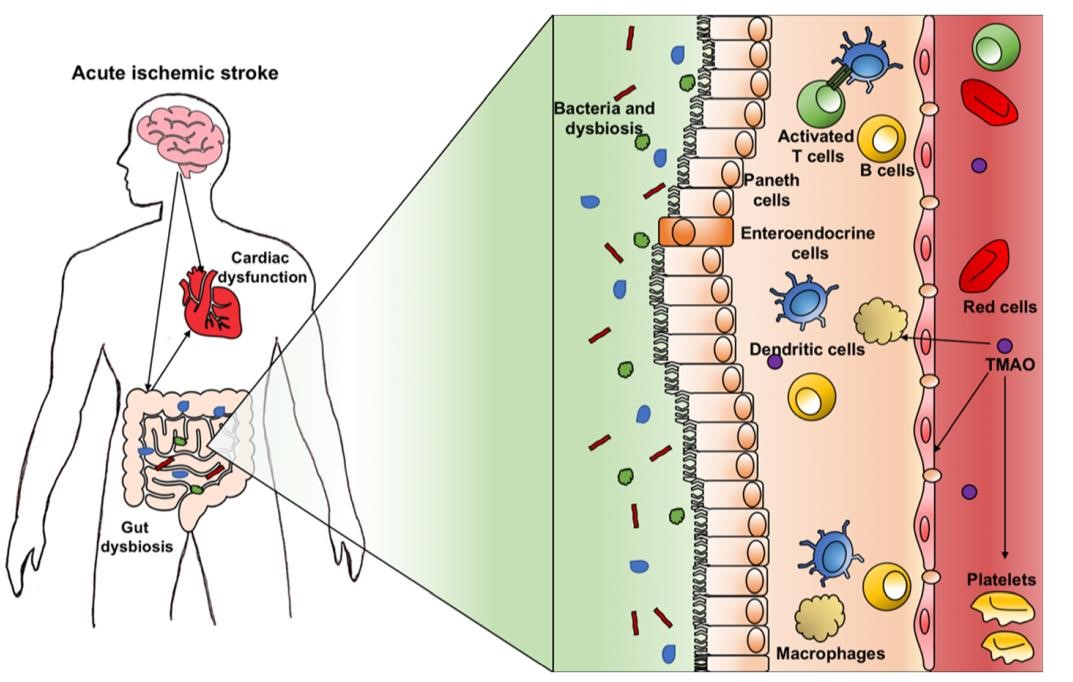
Sau khi não bị tổn thương, có tới 50% bệnh nhân AIS phát triển các biến chứng tiêu hóa như khó nuốt, xuất huyết tiêu hóa và liệt ruột, có thể ảnh hưởng lớn đến kết quả thần kinh và tử vong [28]. Hàng rào máu – ruột chịu trách nhiệm hấp thụ nước và chất dinh dưỡng đồng thời ngăn chặn sự di chuyển của chất độc và mầm bệnh vào máu [14]. Một số cơ chế gây tổn thương có thể làm thay đổi tính thẩm thấu của ruột và gây ra sự phá vỡ hàng rào máu-ruột, do đó làm tăng tính thấm của nó và điều hòa hệ vi sinh vật đường ruột [28]. Sự thay đổi tính thấm ruột càng lớn khi mức độ nghiêm trọng của đột quỵ càng lớn [14]. Sau AIS, hệ vi sinh vật trong ruột bị mất cân bằng theo hướng có lợi cho các mầm bệnh, điều này có thể ảnh hưởng đến kết quả sau AIS [29]. Tương tự như vậy, số lượng mầm bệnh trong ruột sau khi AIS có liên quan đến mức độ nghiêm trọng của phản ứng viêm [29]. Các tác nhân gây bệnh đường ruột góp phần vào phản ứng viêm thông qua tăng hoạt động tiểu cầu và huyết khối, qua trung gian chuyển đổi choline và Lcarnitine thành trimethylamine-N-oxide (TMAO). TMAO gây ra sự tăng hoạt động tiểu cầu và hình thành tế bào bọt, thay đổi sự trao đổi chất của mật và sterol, tăng yếu tố nhân kappa-B, và giảm oxit nitric. Nó cũng tăng cường phản ứng viêm bằng cách tác động lên các tế bào đuôi gai, đại thực bào và tiểu cầu. Các cơ chế này là nguyên nhân gây ra suy tim, tái cấu trúc tim, nhồi máu cơ tim, huyết khối và xơ vữa động mạch [30]. Một số thử nghiệm lâm sàng đã xác định TMAO như một chất chỉ điểm và dự báo bệnh tim mạch [29]. Mức độ của nó có liên quan đến suy giảm chức năng tim, nhồi máu cơ tim và suy tim [31] (Hình 5).
Hình 4 Phản ứng viêm cục bộ sau đột quỵ. Quá trình viêm tại chỗ bắt đầu với việc kích hoạt các dòng thác tiền viêm và tiền tích tụ vào không gian nội mạch. Sự phá vỡ hàng rào máu não cho phép sự xâm nhập của đại thực bào và bạch cầu trung tính ngoại vi vào tổn thương do thiếu máu cục bộ. Điều này dẫn đến tăng cường phản ứng viêm cục bộ trong nhu mô não. Do đó, các tế bào miễn dịch ngoại vi khác được thu hút vào não thiếu máu cục bộ và vi tuần hoàn não, sau đó vượt qua hàng rào máu não bị tổn thương và đi vào hệ tuần hoàn. ROS, các loại oxy phản ứng; TNF-α, yếu tố hoại tử khối u alpha; MMPs, metalloproteinase ma trận; DAMP, các mẫu phân tử liên quan nguy hiểm.
Ais và các yếu tố nguy cơ tim mạch
Việc xác định các yếu tố nguy cơ của AIS rất phức tạp vì cả rối loạn chức năng tim và AIS đều có chung các yếu tố. Tăng huyết áp có thể góp phần vào bệnh xơ vữa động mạch, đây là điểm nổi bật trong sinh lý bệnh của AIS [15]. Hơn nữa, nó có thể góp phần vào các biến cố tim mạch, dẫn đến tăng khó khăn khi giải thích liệu AIS hoặc các yếu tố nguy cơ có sẵn có phải là nguyên nhân gây ra rối loạn chức năng tim sau AIS hay không [32]. Nhiều điểm số đã được xác định để phát hiện những bệnh nhân có thể có nguy cơ mắc AIS hoặc bệnh tim mạch, vì họ có các yếu tố nguy cơ tương tự. Chúng bao gồm Điểm rủi ro Framingham và Pooled Cohort Equations [15, 32]. Một trong những nguyên nhân chính của AIS có thể là do tắc mạch máu não, bắt nguồn từ một mảng xơ vữa bị loét do xơ vữa, thường xuyên nằm trong động mạch cảnh trong [33]. Không rõ liệu AIS, với hậu quả viêm của nó, có phải là yếu tố chính gây ra rối loạn chức năng tim sau AIS hay liệu khuynh hướng tim trước AIS có ảnh hưởng đến các biến cố tim mạch sau đột quỵ hay không. Liên quan đến các mảng xơ vữa động mạch, bệnh mạch máu nhỏ trong các động mạch nhỏ và tiểu động mạch của não có thể thúc đẩy AIS tuyến lệ, xuất huyết não và bệnh leukoaraiosis (giảm tỷ trọng mạch máu trong chất trắng, giảm tưới máu). Sự tiếp xúc của các mạch nhỏ với áp suất cao có thể gây ra lipohyalinosis sau đó là nhồi máu dưới vỏ não [33].
Hình 5 Rối loạn vi sinh vật ruột và rối loạn chức năng tim. Rối loạn vi khuẩn đường ruột làm tăng tính thấm của hàng rào máu-ruột và chuyển vị mầm bệnh, có thể gây xơ vữa động mạch và huyết khối. Các tác nhân gây bệnh đường ruột góp phần tăng cường phản ứng viêm thông qua tăng cường tiểu cầu và hình thành huyết khối, qua trung gian chuyển đổi choline và L-carnitine thành trimethylamine N-oxide (TMAO). TMAO gây ra sự tăng hoạt động tiểu cầu và hình thành tế bào bọt, thay đổi sự trao đổi chất của mật và sterol, đồng thời kích hoạt các đại thực bào, tế bào đuôi gai và tiểu cầu. TMAO, trimetylamin N-oxit
Clinical implications
Các vấn đề về tim có thể liên quan đến AIS bao gồm rung tâm nhĩ, còn lỗ bầu dục, có vùng giảm động lực với huyết khối thành, viêm nội tâm mạc nhiễm khuẩn và bệnh lý huyết học (ví dụ, bệnh đa hồng cầu) [33]. Dựa trên các bằng chứng thực nghiệm và lâm sàng, bệnh nhân bị ảnh hưởng bởi AIS rất dễ bị các biến cố nghiêm trọng về tim [6], vì họ đã thường xuyên bị rối loạn chức năng tim [33]. Các nghiên cứu cho thấy suy tim sau AIS xảy ra tới 17% các trường hợp, ngay cả ở những bệnh nhân không có bệnh tim từ trước [34]. Tử vong do tim và các biến cố tim nghiêm trọng được báo cáo lần lượt ở 4% và 19% bệnh nhân trong vòng 3 tháng đầu sau AIS [35]. Rối loạn nhịp tim [18], bệnh cơ tim Takotsubo [7], nhồi máu cơ tim [36], rối loạn chức năng tự chủ [37], và tăng huyết áp kịch phát [38] là những đặc điểm lâm sàng thường gặp nhất (Bảng S1, Tập tin bổ sung 1). Ngoài ra, việc xác định vị trí của khu vực đột quỵ liên quan là một yếu tố dự báo cơ bản về các hậu quả tim có thể xảy ra (Hình 2). Trong hình này, nhồi máu thùy đỉnh trái là một yếu tố nguy cơ độc lập của nhồi máu cơ tim [39]. Mặc dù vỏ não có vai trò chính trong việc kiểm soát hệ thống tự chủ, nhưng đột quỵ xảy ra ở khu vực này không phổ biến lắm [40]. Tuy nhiên, khi tổn thương thùy đảo bên phải sẽ làm tăng nguy cơ loạn nhịp nhanh, kéo dài khoảng QTc và block bó trái [41]. Đột quỵ bên phải có nhiều khả năng liên quan đến điều biến phó giao cảm hơn đột quỵ bên trái [38, 42]; một mối liên quan tương tự đã được mô tả với rối loạn nhịp tim [43]. Bệnh cơ tim Takotsubo cũng có liên quan đến các vùng thiếu máu cục bộ cụ thể, chẳng hạn như vỏ não trán và vỏ não dưới thùy đảo, các khu vực trong và ngoài vỏ ngoài, và đường sau đuôi thùy đảo [44].
Rối loạn chức năng tim cấp và mãn tính trước AIS nhu rung và cuồng nhĩ gây ứ đọng máu trong tâm nhĩ trái, do đó dễ dẫn đến huyết khối và tắc mạch não [45]. Rung nhĩ do van tim làm tăng nguy cơ AIS gấp 17 lần, trong khi rung nhĩ không do van tim làm tăng nguy cơ gấp 5 lần [45]. Không có sự phân biệt nào về tỷ lệ nguy cơ mắc AIS giữa rung nhĩ kịch phát, vĩnh viễn hoặc dai dẳng, do đó làm cho chiến lược theo dõi tích cực hơn trở nên khó khăn, đặc biệt ở những bệnh nhân được chẩn đoán ban đầu là rối loạn nhịp tim khác ngoài rung nhĩ [45]. Huyết áp tâm thu cao hơn 140 mmHg là nguyên nhân gây ra 1,5 triệu ca tử vong liên quan đến AIS [46]. Hơn nữa, huyết áp cao có liên quan đến tăng nguy cơ rung nhĩ, bản thân nó là một yếu tố nguy cơ nổi tiếng của AIS [47]. Suy tim mãn tính cũng được coi là một yếu tố nguy cơ quan trọng đối với AIS, vì nó liên quan đến hình thành huyết khối, giảm động thất trái, tăng độ nhớt của máu, giảm phân suất tống máu thất trái, rối loạn chức năng nội mô, rối loạn chức năng tim tâm thu hoặc tâm trương, và tắc mạch nhỏ, với hậu quả là kết cục kém và tỷ lệ tử vong cao hơn [48].
Rối loạn chức năng tim cấp tính và mãn tính sau ais
Rối loạn chức năng tim cấp sau ais
Cả thay đổi điện tim do thiếu máu cục bộ và loạn nhịp đều phổ biến sau AIS trong vòng 24 giờ đầu tiên [18]. Ngoài ra, nhồi máu cơ tim cấp tính hoặc các bất thường giống như nhồi máu cơ tim rất phổ biến sau AIS [36] và có liên quan đến việc tăng nguy cơ dẫn đến các kết cục thần kinh chức năng không thuận lợi và các biến cố tim mạch lớn [38].
Rối loạn nhịp tim: thay đổi điện tim xảy ra ở 60–90% bệnh nhân AIS [10, 11]. Các đặc điểm chung bao gồm đảo ngược sóng T (35%), ST chênh xuống (33%), kéo dài khoảng QTc (29%), và sóng U (28%) [49]. Rung nhĩ, nhịp nhanh trên thất, ngoại tâm thu thất, nhịp nhanh thất và nhịp nhanh xoang là những rối loạn nhịp thường gặp nhất sau AIS [41]. Các bất thường về dẫn truyền thường đi đôi với sự mất ổn định huyết động cấp tính, có liên quan đến tăng tỷ lệ mắc bệnh và tử vong sau AIS [5]. Hơn nữa, tiền sử suy tim, mức độ nặng AIS, khoảng QTc, và ngoại tâm thu thất là những yếu tố nguy cơ độc lập đối với các biến cố tim nghiêm trọng sau AIS [35].
Tổn thương cơ tim do thiếu máu cục bộ và các bất thường về điện tâm đồ: các yếu tố nguyên nhân chính của rối loạn chức năng cơ tim do đột quỵ có thể là rối loạn điều hòa tự động và phản ứng căng thẳng sinh lý [41]. Các nghiên cứu đã chỉ ra rằng 18–70% bệnh nhân mắc AIS chính sẽ bị bệnh mạch vành, bất kể tiền sử tim mạch trước đó [50, 51]. Tỷ lệ cao này có thể được giải thích là do các yếu tố nguy cơ của bệnh tim mạch và mạch máu não là tương tự nhau [52]. Ngoài ra, tổn thương cơ tim do thiếu máu cục bộ xảy ra chủ yếu trong vòng 24 giờ đầu tiên sau AIS [53]. Liên quan đến những thay đổi điện tâm đồ, rung nhĩ, block nhĩ thất, ST chênh lên, ST chênh xuống và sóng T đảo ngược không liên quan đến kết cục, trong khi nhịp tim nhanh dự báo đáng kể tử vong trong 3 tháng [10]. Sóng T thẳng và sóng T đảo ngược phổ biến hơn gấp 4 lần, và đoạn ST chênh xuống phổ biến hơn 7 đến 10 lần ở bệnh nhân AIS so với những bệnh nhân cùng tuổi không bị đột quỵ [54]. Tóm lại, việc theo dõi điện tâm đồ sớm và phân tích các dấu ấn sinh học tim là cần thiết trong vòng 24 giờ đầu tiên — và có thể sau đó — để xác định những bệnh nhân có nguy cơ mắc các biến cố tim cấp tính, có liên quan đến kết cục thần kinh lâm sàng kém (Bảng S2 và S3, Tập tin bổ sung 1 ). Do đó, chúng tôi khuyên bạn nên theo dõi điện tâm đồ liên tục, tối ưu hóa cân bằng điện giải, và rối loạn chức năng tim cấp và mãn tính sau AIS
Rối loạn chức năng tim mãn tính sau ais
Rối loạn chức năng tim mãn tính sau AIS được kích hoạt bởi tình trạng viêm nội mạc, stress oxy hóa và giải phóng catecholamine dẫn đến tái cấu trúc cơ tim. Kích thích giao cảm kích hoạt sự tăng catecholamine, gây co mạch ngoại vi và động mạch vành, sau đó là thiếu máu cục bộ cấp tính. Tác động gây độc trực tiếp của catecholamine trên cơ tim và tăng huyết áp thần kinh sau đó cũng góp phần vào rối loạn chức năng cơ tim mãn tính và tái cấu trúc [55].
Rối loạn chức năng tâm thu và tâm trương thất trái: Sự hiểu biết hiện tại về bệnh tim chứng thực rằng việc tái cấu trúc lại tim là hậu quả phổ biến của rối loạn chức năng cơ tim mãn tính hoặc loạn nhịp [56]. Một nghiên cứu tiền lâm sàng đã chứng minh rằng AIS khu trú và giải phóng catecholamine tiếp theo kéo theo rối loạn chức năng tim lâu dài và tái cấu trúc [56, 57]. Trong bối cảnh này, metoprolol đã được thử nghiệm và phát hiện có tác dụng làm chậm quá trình tái cấu trúc tim và ức chế hoạt động giao cảm [57]. Các nghiên cứu lâm sàng là cần thiết để xác nhận công dụng và khả năng ứng dụng của nó như một chất bảo vệ trong AIS. Một nghiên cứu gần đây cho thấy bệnh nhân rung nhĩ không xác định gây phát triển xơ hóa tâm nhĩ thường xuyên hơn so với những bệnh nhân rung nhĩ có nguyên nhân đã được biết, ủng hộ giả thuyết rằng việc tái cấu trúc tâm nhĩ mãn tính có thể liên quan đến AIS [58]. Bệnh cơ tim Takotsubo là một ví dụ về rối loạn chức năng thất trái liên quan đến vùng mỏm và có liên quan đến những thay đổi về dấu ấn sinh học tim và theo dõi điện tâm đồ. Bởi vì nó được gây ra bởi sự hoạt hóa thần kinh, nó phần lớn có thể đảo ngược và thường tự giới hạn; quản lý lâm sàng chỉ dựa vào chăm sóc hỗ trợ [44]. Rối loạn chức năng cơ tim giống – Takotsubo ảnh hưởng đến hầu hết phụ nữ và có liên quan đến kết quả chức năng kém trong thời gian ngắn, tỷ lệ tử vong cao và suy giảm chức năng thần kinh [44]. Rối loạn chức năng thất tâm trương và tâm thu cũng là một trong những biến chứng chính của AIS [59, 60]. Rối loạn chức năng tim và mối liên quan của nó với kết quả được mô tả trong Bảng S2, Tập tin bổ sung 1. Tóm lại, theo dõi điện tâm đồ và siêu âm tim sớm có thể giúp xác định bệnh nhân AIS có nguy cơ cao bị rối loạn chức năng tim mãn tính.
Sự tự điều hòa của não: giữa huyết áp và huyết động. Sự tự điều hòa của não đóng một vai trò thiết yếu trong việc duy trì lưu lượng máu não và áp lực tưới máu não trong phạm vi không đổi để đảm bảo não được tưới đầy đủ [61]. Tuy nhiên, AIS có thể làm rối loạn điều hòa hệ thống dễ bị tổn thương này, dẫn đến tổn thương não thứ phát [61]. Kiểm soát huyết áp đóng một vai trò quan trọng trong việc ngăn ngừa cả AIS và tổn thương não thứ phát sau AIS [46, 61]. Các cơ chế chính liên quan đến tăng huyết áp sau AIS vẫn chưa rõ ràng, mặc dù các cơ chế tương tự gây ra các biến chứng tim khác đã được đề xuất và có thể giải thích cho việc tăng huyết áp tâm thu (> 140 mmHg) [61]. Trong số các phân nhóm AIS, nhồi máu lỗ khuyết có liên quan chặt chẽ nhất với tăng huyết áp, cho thấy vai trò quan trọng của các mạch máu nhỏ [62]. Vấn đề chính ở những bệnh nhân này không phải là tự điều hòa mà là đạt được sự cân bằng giữa nhu cầu tưới máu và nguy cơ xuất huyết. Vì vậy, các bác sĩ lâm sàng nên tìm kiếm các mục tiêu huyết động tốt, mặc dù trong trường hợp tim suy. Kiểm soát huyết áp là điều cần thiết ở bệnh nhân AIS, đặc biệt là ở những người đã có tăng huyết áp nặng từ trước. Một số nghiên cứu đã điều tra vai trò của việc kiểm soát huyết áp trong AIS (Bảng S3, Tập tin bổ sung 1). Theo phát hiện đó, cả huyết áp tâm thu thấp hơn (120–150 mmHg) và cao hơn (150–200 mmHg) đều có liên quan đến tăng nguy cơ tử vong [63]; thực sự, các hướng dẫn mới nhất đề nghị giữ huyết áp dưới 180/105 mmHg ở bệnh nhân AIS đủ điều kiện để điều trị tái tưới máu khẩn cấp và trong giai đoạn sau tiêu huyết khối [64]. Thuốc hạ huyết áp được phát hiện làm giảm sự xuất hiện của AIS tái phát và các biến cố tim mạch, nhưng chúng không ảnh hưởng đến tỷ lệ nhồi máu cơ tim hoặc tử vong [65]. Hơn nữa, sự thay đổi huyết áp tâm thu lớn hơn có liên quan đến tăng nguy cơ tái phát đột quỵ [38], suy giảm chức năng thần kinh [66] và kết quả chức năng lâu dài kém [67]. Một phân tích tổng hợp trên 12.703 bệnh nhân cho thấy hạ huyết áp trong giai đoạn đầu của AIS không ngăn ngừa tử vong [68] và không được khuyến cáo [69]. Một số lý do đã được đưa ra để quản lý huyết áp, cho thấy rằng can thiệp hạ huyết áp được đảm bảo trong AIS nếu huyết áp tâm thu > 180–230 mmHg hoặc huyết áp tâm trương > 105–120 mmHg, do đó tránh được sự thay đổi huyết áp quan trọng [64]. Tóm lại, việc kiểm soát huyết áp nên được cá nhân hóa, dựa trên tình trạng lâm sàng và phản ứng sinh lý của bệnh nhân. Không có bằng chứng liên quan đến loại thuốc tốt nhất để sử dụng [64].
Cardiovascular monitoring and treatment options
Theo dõi tim mạch ở những bệnh nhân có nguy cơ mắc AIS.
Do thực tế là các bệnh tim mạch và mạch máu não có các yếu tố nguy cơ tương tự nhau, nên xem xét Điểm nguy cơ Framingham và Pooled Cohort Equations [15, 32] khi theo dõi bệnh nhân có nguy cơ mắc AIS và các biến cố tim mạch. Hơn nữa, một tỷ lệ giữa huyết áp tâm thu động mạch ở mắt cá chân và động mạch cánh tay (được gọi là chỉ số mắt cá chân – cánh tay) cao hơn 0,9 cho thấy bệnh động mạch ngoại vi [32]. Ở những bệnh nhân bị rung nhĩ, điểm CHADS2 và CHA2DS2-VASc đã được xác nhận để xác định nguy cơ mắc AIS [45].
Theo dõi tim mạch ở những bệnh nhân bị AIS.
Quản lý chung AIS thường phức tạp vì có thể có rối loạn chức năng tim mạch và một số biến chứng y tế, chẳng hạn như nuốt khó, suy hô hấp do thần kinh, viêm phổi do đột quỵ, rối loạn vi sinh đường ruột, viêm hệ thống và cần phải mở khí quản hoặc thở máy [41]. Thang/ Điểm Đột quỵ của Viện Y tế Quốc gia (NIHSS) nên được sử dụng để phân tầng nguy cơ, nhờ vào tiện ích đã được chứng minh của nó trong việc phát hiện bệnh nhân AIS có nguy cơ tim mạch cao; các nghiên cứu đã phát hiện ra rằng những bệnh nhân có NIHSS > 10 có mức troponin cao hơn và có nhiều thay đổi về thiếu máu cục bộ hơn khi so sánh với những bệnh nhân có điểm
Theo dõi sinh hiệu
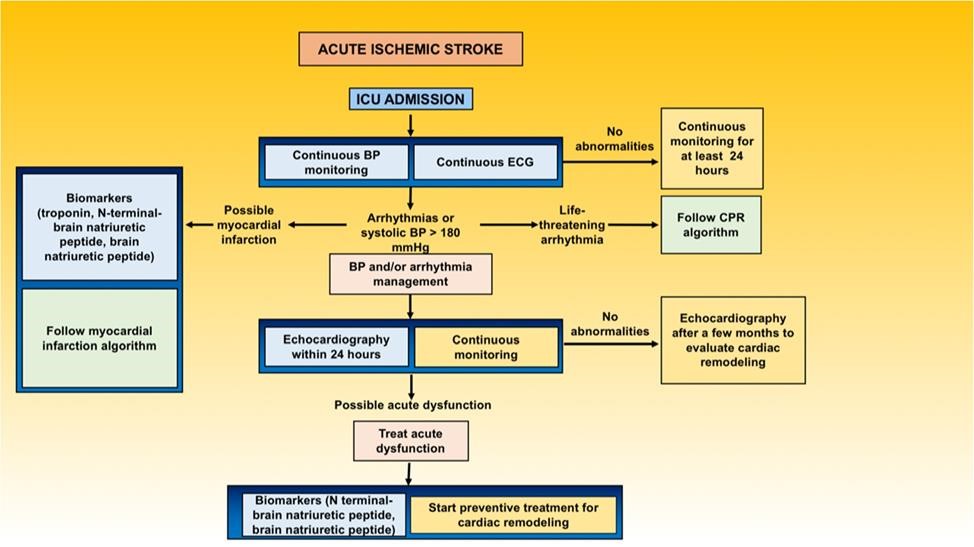
Các tiêu chí để nhận vào ICU khác nhau đáng kể giữa các quốc gia và trung tâm. Trong những trường hợp nghiêm trọng hơn, việc nhập viện ICU của bệnh nhân AIS có thể là điều cần thiết để đảm bảo theo dõi thần kinh và tim mạch xâm lấn và phát hiện sớm bất kỳ biến chứng đa cơ quan nào [71]. Theo dõi tim liên tục là điều cần thiết để phát hiện các rối loạn nhịp tim nặng và ngăn ngừa đột tử do tim. Hơn nữa, trong vòng 24 giờ đầu tiên sau khi AIS, nó có thể ngăn ngừa các biến chứng tim mạch (Hình 6).
Các dấu ấn sinh học
Các men tim có thể tăng sau AIS, nhưng thường ít hơn trong nhồi máu cơ tim nguyên phát [72]. Troponin T có liên quan đến mức độ nghiêm trọng của AIS, liên quan đến thùy đảo, và tiên lượng ngắn hạn xấu hơn [73, 74] (Bảng S4, Tập tin bổ sung 1). Peptide natri lợi niệu (BNP) trong huyết tương cũng có liên quan đến kết quả xấu hơn ở bệnh nhân AIS [75-77]. Đo men tim có thể là điều tối quan trọng để xác định sớm hơn những bệnh nhân có nguy cơ cao mắc các biến cố tim mạch sau AIS. Protein phản ứng C (CRP) có liên quan đến các phản ứng viêm và miễn dịch. Mức CRP có độ nhạy cao lớn hơn 2 hoặc 3 mg/ L có thể là ngưỡng hữu ích để phát hiện bệnh nhân có nguy cơ tim mạch cao hơn [32].
Các xem xét khác
Cắt đốt qua ống thông đã được coi là một giải pháp thay thế hiệu quả hơn các loại thuốc chống loạn nhịp tim để đảo ngược tình trạng rung nhĩ về nhịp xoang [78]. Phần tiểu nhĩ trái được coi là nguồn chính của các biểu hiện tắc mạch sau rung nhĩ. Thật vậy, nó đã được xác định là một mục tiêu quan trọng để cắt bỏ [79] ở những bệnh nhân có chống chỉ định với thuốc chống đông uống dài hạn, mặc dù khuyến cáo này vẫn cần được làm rõ [80]. Tuy nhiên, cách ly điện học tiểu nhĩ trái có liên quan đến sự xuất hiện AIS [81]. Thuốc chống co giật, thuốc an thần kinh và nhiều loại thuốc khác thường được sử dụng trong ICU có thể kéo dài khoảng QTc [82]; đặc biệt chú ý đến tác dụng ngoại ý có thể xảy ra này ở bệnh nhân AIS. Người ta thường đồng ý rằng thuốc chẹn beta là nền tảng của liệu pháp y khoa để giảm cường giao cảm và ngăn chặn sự tái cấu trúc của tim sau nhồi máu cơ tim [83], nhưng các tài liệu vẫn chưa kết luận về việc sử dụng chúng ở bệnh nhân AIS. Thuốc chẹn beta và thuốc đối kháng alpha-2 cho thấy kết quả tích cực trong điều trị tăng huyết áp cấp tính, trong khi thuốc ức chế men chuyển và thuốc chẹn thụ thể angiotensin II là những lựa chọn tốt để kiểm soát huyết áp mãn tính sau AIS [82].
Kết luận
Mặc dù có những bước tiến lớn trong sự hiểu biết của chúng ta về tương tác qua lại não-tim sau AIS, vai trò của kiểm soát giao cảm, rối loạn sinh học ruột và phản ứng viêm hệ thống vẫn còn đang được nghiên cứu. Tương tác đột quỵ-tim hiện đang là chủ đề quan tâm của các nhà nghiên cứu, và các cơ chế gây bệnh của rối loạn chức năng tim liên quan đến đột quỵ là mục tiêu mới hấp dẫn cho các chiến lược điều trị trong tương lai. Các nghiên cứu sâu hơn được đảm bảo để khám phá những lý thuyết và cơ chế hấp dẫn này cũng như chuyển kiến thức sinh lý bệnh vào thực hành lâm sàng.
Hình 6. Sơ đồ xử trí đột quỵ sau khi nhập viện chăm sóc đặc biệt. Tóm tắt các bước đầu tiên để phát hiện và xử trí các biến chứng tim có thể xảy ra ở bệnh nhân đột quỵ sau khi nhập viện chăm sóc đặc biệt. Do thiếu dữ liệu kết luận, không có khuyến nghị cụ thể về liệu pháp dược phẩm được đưa ra; độc giả được khuyến cáo thực hiện theo các giao thức địa phương và hướng dẫn quốc tế. Điện tâm đồ, điện tâm đồ; HA, huyết áp; ICU, đơn vị chăm sóc đặc biệt; CPR, hồi sức tim phổi
Supplementary information
Supplementary information accompanies this paper at https://doi.org/10. 1186/s13054-020-02885-8. Additional file 1: Table S1. Incidence and prevalence of all cardiac dysfunctions after ischemic stroke; Table S2. Cardiac dysfunctions after ischemic stroke and their association with outcome; Table S3. Blood pressure control in ischemic stroke and its association with outcome; Table S4. Troponin T as acute biomarker of cardiovascular complications after ischemic stroke. Abbreviations
AIS: Acute ischemic stroke; Akt: Protein kinase; BBB: Blood–brain barrier;
FOXO: Forkhead box O; HPA: Hypothalamic–pituitary–adrenal axis;
ICU: Intensive care unit; NIHSS: National Institutes of Health Stroke Scale; CRP: C-reactive protein;
TMAO: Trimethylamine N-oxide
Acknowledgements
The authors thank Mr. Filippe Vasconcellos (São Paulo), Brazil, for his assistance in editing the manuscript.
Authors’ contributions
DB wrote the manuscript. DB, CR, CSS, PLS, FDP, PP, and PRM designed the study. DB, CR, AV, CSS, PLS, FDP, PP, and PRMR revised the manuscript. All authors read and approved the final version. Authors’ information Not applicable.
Funding
Brazilian Council for Scientific and Technological Development (CNPq) and Rio de Janeiro State
Research Foundation (FAPERJ)
Availability of data and materials Not applicable.
Ethics approval and consent to participate Not applicable.
Consent for publication Not applicable.
Competing interests
The authors declare that they have no competing interests.
Author details
1Anesthesia and Intensive Care, San Martino Policlinico Hospital, IRCCS for Oncology and Neurosciences, Genoa, Italy. 2Department of Surgical Sciences and Integrated Diagnostics, University of Genoa, Genoa, Italy. 3Laboratory of Pulmonary Investigation, Carlos Chagas Filho Institute of Biophysics, Federal University of Rio de Janeiro, Rio de Janeiro, Brazil. 4Department of Physiotherapy, Faculty of Medicine, Federal University of Rio de Janeiro, Rio de Janeiro, Brazil. 5Unidade Acadêmica de Ciências da Saude, Universidade do Extremo Sul Catarinense (UNESC), Criciúma, Santa Catarina, Brazil. 6Rio de Janeiro
Network on Neuroinflammation, Carlos Chagas Filho Foundation for Supporting Research in the State of Rio de Janeiro (FAPERJ), Rio de Janeiro, Brazil.
Received: 17 January 2020 Accepted: 13 April 2020
References
Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk factor for stroke: the Framingham study. Stroke. 1991;22:983–8.
Chen Z, Venkat P, Seyfried D, Chopp M, Yan T, Chen J. Brain-heart interaction: cardiac complications after stroke. Circ Res. 2017;121:451–68.
Fuhrer H, Reinhard M, Niesen WD. Paradigm change? Cardiac output better associates with cerebral perfusion than blood pressure in ischemic stroke. Front Neurol. 2017;8:706.
Sposato LA, Cipriano LE, Saposnik G, Vargas ER, Riccio PM, Hachinski V. Diagnosis of atrial fibrillation after stroke and transient ischaemic attack: a systematic review and meta-analysis. Lancet Neurol. 2015;14:377–87.
Prosser J, MacGregor L, Lees KR, Diener HC, Hacke W, Davis S. Predictors of early cardiac morbidity and mortality after ischemic stroke. Stroke. 2007;38: 2295–302.
Gunnoo T, Hasan N, Khan MS, Slark J, Bentley P, Sharma P. Quantifying the risk of heart disease following acute ischaemic stroke: a meta-analysis of over 50,000 participants. BMJ Open. 2016;6:e009535.
Yoshimura S, Toyoda K, Ohara T, Nagasawa H, Ohtani N, Kuwashiro T, et al. Takotsubo cardiomyopathy in acute ischemic stroke. Ann Neurol. 2008;64: 547–54.
Li Y, Fitzgibbons TP, McManus DD, Goddeau RP, Silver B, Henninger N. Left ventricular ejection fraction and clinically defined heart failure to predict 90day functional outcome after ischemic stroke. J Stroke Cerebrovasc Dis. 2019;28:371–80.
Xiong L, Tian G, Leung H, Soo YOY, Chen X, Ip VHL, et al. Autonomic dysfunction predicts clinical outcomes after acute ischemic stroke: a prospective observational study. Stroke. 2018;49:215–8.
Christensen H, Fogh Christensen A, Boysen G. Abnormalities on ECG and telemetry predict stroke outcome at 3 months. J Neurol Sci. 2005; 234:99–103.
Adeoye AM, Ogah OS, Ovbiagele B, Akinyemi R, Shidali V, Agyekum F, et al. Prevalence and prognostic features of ECG abnormalities in acute stroke: findings from the SIREN study among Africans. Glob Heart. 2017;12:99–105.
Barugh AJ, Gray P, Shenkin SD, MacLullich AMJ, Mead GE. Cortisol levels and the severity and outcomes of acute stroke: a systematic review. J Neurol. 2014;261:533– 45.
Iadecola C, Anrather J. The immunology of stroke: from mechanisms to translation. Nat Med. 2011;17:796–808.
Kelly JR, Kennedy PJ, Cryan JF, Dinan TG, Clarke G, Hyland NP. Breaking down the barriers: the gut microbiome, intestinal permeability and stressrelated psychiatric disorders. Front Cell Neurosci. 2015;9:392.
Boehme AK, Esenwa C, Elkind MSV. Stroke risk factors, genetics, and prevention. Circ Res. 2017;120:472–95.
Guan L, Collet JP, Mazowita G, Claydon VE. Autonomic nervous system and stress to predict secondary ischemic events after transient ischemic attack or minor stroke:
possible implications of heart rate variability. Front Neurol. 2018;9:90.
Silvani A, Calandra-Buonaura G, Dampney RAL, Cortelli P. Brain-heart interactions: physiology and clinical implications. Philos Trans A Math Phys Eng Sci. 2016;374:(2067).
Fernández-Menéndez S, García-Santiago R, Vega-Primo A, González Nafría N, LaraLezama LB, Redondo-Robles L, et al. Arritmias cardiacas en la unidad de ictus: Análisis de los datos de la monitorización cardiaca. Neurologia. 2016;31:289–95.
Laredo C, Zhao Y, Rudilosso S, Renú A, Pariente JC, Chamorro Á, et al. Prognostic significance of infarct size and location: the case of insular stroke. Sci Rep. 2018;8:9498.
Xin Z, Ma Z, Jiang S, Wang D, Fan C, Di S, et al. FOXOs in the impaired heart: new therapeutic targets for cardiac diseases. Biochim Biophys Acta Mol basis Dis. 1863;2017:486–98.
Gopinath R, Ayya S. Neurogenic stress cardiomyopathy: what do we need to know. Ann Card Anaesth. 2018;21:228.
Fu Y, Liu Q, Anrather J, Shi FD. Immune interventions in stroke. Nat Rev Neurol. 2015;11:524–35.
Samary CS, Pelosi P, Leme Silva P, Rocco PRM. Immunomodulation after ischemic stroke: potential mechanisms and implications for therapy. Crit Care. 2016;20:391.
Turner RJ, Sharp FR. Implications of MMP9 for blood brain barrier disruption and hemorrhagic transformation following ischemic stroke. Front Cell Neurosci. 2016;10:56.
Ishikawa H, Tajiri N, Vasconcellos J, Kaneko Y, Mimura O, Dezawa M, et al. Ischemic stroke brain sends indirect cell death signals to the heart. Stroke. 2013;44:3175–82.
Gonzales-Portillo C, Ishikawa H, Shinozuka K, Tajiri N, Kaneko Y, Borlongan CV. Stroke and cardiac cell death: two peas in a pod. Clini Neurol Neurosurg. 2016;10:145–7.
Acosta SA, Mashkouri S, Nwokoye D, Lee JY, Borlongan CV. Chronic inflammation and apoptosis propagate in ischemic cerebellum and heart of non-human primates. Oncotarget. 2017;8:102820–34.
Wen SW, Wong CHY. An unexplored brain-gut microbiota axis in stroke. Gut Microbes. 2017;8:601–6.
Nam HS. Gut microbiota and ischemic stroke: the role of trimethylamine Noxide. J Stroke. 2019;21:151–9.
Yang S, Li X, Yang F, Zhao R, Pan X, Liang J, et al. Gut microbiotadependent marker TMAO in promoting cardiovascular disease: inflammation mechanism, clinical prognostic, and potential as a therapeutic target. Front Pharmacol. 2019;10:1360.
Zhu W, Gregory JC, Org E, Buffa JA, Gupta N, Wang Z, et al. Gut microbial metabolite TMAO enhances platelet hyperreactivity and thrombosis risk. Cell. 2016;165:111–24.
Curry SJ, Krist AH, Owens DK, Barry MJ, Caughey AB, Davidson KW, et al. Risk assessment for cardiovascular disease with nontraditional risk factors: US preventive services task force recommendation statement. JAMA. 2018;320:272–80.
Campbell BCV, De Silva DA, Macleod MR, Coutts SB, Schwamm LH, Davis SM, et al. Ischaemic stroke. Nat Rev Dis Prim. 2019;5:1–22.
Burkot J, Kopec G, Pera J, Slowik A, Dziedzic T. Decompensated heart failure is a strong independent predictor of functional outcome after ischemic stroke. J Card Fail. 2015;21:642–6.
Kallmünzer B, Breuer L, Kahl N, Bobinger T, Raaz-Schrauder D, Huttner HB, et al. Serious cardiac arrhythmias after stroke: incidence, time course, and predictors–a systematic, prospective analysis. Stroke. 2012;43:2892–7.
Alqahtani F, Aljohani S, Tarabishy A, Busu T, Adcock A, Alkhouli M. Incidence and outcomes of myocardial infarction in patients admitted with acute ischemic stroke. Stroke. 2017;48:2931–8.
Nayani S, Sreedharan SE, Namboodiri N, Sarma PS, Sylaja PN. Autonomic dysfunction in first ever ischemic stroke: prevalence, predictors and short term neurovascular outcome. Clin Neurol Neurosurg. 2016;150:54–8.
de Havenon A, Stoddard G, Saini M, Wong KH, Tirschwell D, Bath P. Increased blood pressure variability after acute ischemic stroke increases the risk of death: a secondary analysis of the Virtual International Stroke Trial Archive. JRSM Cardiovasc Dis. 2019;8:204800401985649.
Rincon F, Dhamoon M, Moon Y, Paik MC, Boden-Albala B, Homma S, et al. Stroke location and association with fatal cardiac outcomes: Northern Manhattan Study (NOMAS). Stroke. 2008;39:2425–31.
Smith JR, Lee GP, Fountas K, King DW, Jenkins PD. Intracranial stimulation study of lateralization of affect. Epilepsy Behav. 2006;8:534–41.
Kumar S, Selim MH, Caplan LR. Medical complications after stroke. Lancet Neurol. 2010;9:105–18.
Hrishi A, Lionel KR, Prathapadas U. Head rules over the heart: cardiac manifestations of cerebral disorders. Ind J Crit Care Med. 2019;23:329–35.
Colivicchi F, Bassi A, Santini M, Caltagirone C. Prognostic implications of right-sided insular damage, cardiac autonomic derangement, and arrhythmias after acute ischemic stroke. Stroke. 2005;36:1710–5.
Jung JM, Kim JG, Kim JB, Cho KH, Yu S, Oh K, et al. Takotsubo-like myocardial dysfunction in ischemic stroke: a hospital-based registry and systematic literature review. Stroke. 2016;47:2729–36.
Best JG, Bell R, Haque M, Chandratheva A, Werring DJ. Atrial fibrillation and stroke: a practical guide. Pract Neurol. 2019;19:208–24.
Forouzanfar MH, Liu P, Roth GA, Ng M, Biryukov S, Marczak L, et al. Global burden of hypertension and systolic blood pressure of at least 110 to 115 mm Hg, 1990-2015. JAMA. 2017;317:165–82.
Bryan W, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: the task force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH). Eur Heart J. 2018;39:3021–104.
Haeusler KG, Laufs U, Endres M. Chronic heart failure 2010 guidelines. Stroke. 2010;108:1–222.
Purushothaman S, Salmani D, Prarthana KG, Bandelkar SMG, Varghese S. Study of ECG changes and its relation to mortality in cases of cerebrovascular accidents. J Nat Sci Biol Med. 2014;5:434–6.
Bhatia R, Sharma G, Patel C, Garg A, Roy A, Bali P, et al. Coronary artery disease in patients with ischemic stroke and TIA. J Stroke Cerebrovasc Dis. 2019:28(12):104400.
Cha MJ, Lee HS, Kim YD, Nam HS, Heo JH. The association between asymptomatic coronary artery disease and CHADS2 and CHA2DS2-VASc scores in patients with stroke. Eur J Neurol. 2013;20:1256–63.
Wachter R, Gröschel K, Gelbrich G, Hamann GF, Kermer P, Liman J, et al. Holterelectrocardiogram-monitoring in patients with acute ischaemic stroke (FindAFRANDOMISED): an open-label randomised controlled trial. Lancet Neurol. 2017;16:282–90.
Alkhachroum AM, Miller B, Chami T, Tatsuoka C, Sila C. A troponin study on patients with ischemic stroke, intracerebral hemorrhage and subarachnoid hemorrhage: type II myocardial infarction is significantly associated with stroke severity, discharge disposition and mortality. J Clin Neurosci. 2019;64: 83–8.
Dimant J, Grob D. Electrocardiographic changes and myocardial damage in patients with acute cerebrovascular accidents. Stroke. 1977;8(4):448-55.
Kinoshita K. Traumatic brain injury: pathophysiology for neurocritical care. J Intensive Care. 2016.
Masci A, Barone L, Dedè L, Fedele M, Tomasi C, Quarteroni A, et al. The impact of left atrium appendage morphology on stroke risk assessment in atrial fibrillation: a computational fluid dynamics study. Front Physiol. 2019;9:1936.
Bieber M, Werner RA, Tanai E, Hofmann U, Higuchi T, Schuh K, et al. Strokeinduced chronic systolic dysfunction driven by sympathetic overactivity. Ann Neurol. 2017;82:729–43.
Fonseca AC, Alves P, Inácio N, Marto JP, Viana-Baptista M, Pinho-E-Melo T, et al. Patients with undetermined stroke have increased atrial fibrosis: a cardiac magnetic resonance imaging study. Stroke. 2018;49:734–7.
Kuznetsova T, Herbots L, López B, Jin Y, Richart T, Thijs L, et al. Prevalence of left ventricular diastolic dysfunction in a general population. Circ Heart Fail. 2009;2:105–12.
Kim WJ, Nah HW, Kim DH, Cha JK. Association between left ventricular dysfunction and functional outcomes at three months in acute ischemic stroke. J Stroke Cerebrovasc Dis. 2016;25:2247–52.
Ko SB, Yoon BW. Blood pressure management for acute ischemic and hemorrhagic stroke: the evidence. Semin Respir Crit Care Med. 2017;38:718–25.
Fischer U, Cooney MT, Bull LM, Silver LE, Chalmers J, Anderson CS, et al. Acute poststroke blood pressure relative to premorbid levels in intracerebral haemorrhage versus major ischaemic stroke: a populationbased study. Lancet Neurol. 2014;13:374–84.
Bangalore S, Schwamm L, Smith EE, Hellkamp AS, Suter RE, Xian Y, et al. Blood pressure and in-hospital outcomes in patients presenting with ischaemic stroke. Eur Heart J. 2017;38:2827–35.
Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, et al. Guidelines for the early management of patients with acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2018;49(3):e46-e110.
Lakhan SE, Sapko MT. Blood pressure lowering treatment for preventing stroke recurrence: a systematic review and meta-analysis. Int Arch Med. 2009;2:30.
Kang J, Hong JH, Jang MU, Choi NC, Lee JS, Kim BJ, et al. Change in blood pressure variability in patients with acute ischemic stroke and its effect on early neurologic outcome. PLoS One. 2017;12:e0189216.
Manning LS, Rothwell PM, Potter JF, Robinson TG. Prognostic significance of shortterm blood pressure variability in acute stroke: systematic review. Stroke. 2015;46:2482–90.
Lee M, Ovbiagele B, Hong KS, Wu YL, Lee JE, Rao NM, et al. Effect of blood pressure lowering in early ischemic stroke: meta-analysis. Stroke. 2015;46: 1883–9.
Liu S, Li C, Li T, Xiong J, Zhao X. Effects of early hypertension control after ischaemic stroke on the outcome: a meta-analysis. Cerebrovasc Dis S Karger AG. 2015;40:270–8.
Wira CR, Rivers E, Martinez-Capolino C, Silver B, Iyer G, Sherwin R, et al. Cardiac complications in acute ischemic stroke. West J Emerg Med. 2011;12: 414–20.
Smith M, Reddy U, Robba C, Sharma D, Citerio G. Acute ischaemic stroke: challenges for the intensivist. Intensive Care Med. 2019;45:1177–89.
Ay H, Koroshetz WJ, Benner T, Vangel MG, Melinosky C, Arsava EM, et al. Neuroanatomic correlates of stroke-related myocardial injury. Neurology. 2006;66:1325–9.
Song HS, Back JH, Jin DK, Chung PW, Moon HS, Suh BC, et al. Cardiac troponin T elevation after stroke: relationships between elevated serum troponin T, stroke location, and prognosis. J Clin Neurol. 2008;4:75–83.
He L, Wang J, Dong W. The clinical prognostic significance of hs-cTnT elevation in patients with acute ischemic stroke. BMC Neurol. 2018;18(1):118.
Maisel AS, Krishnaswamy P, Nowak RM, McCord J, Hollander JE, Duc P, et al. Rapid measurement of B-type natriuretic peptide in the emergency diagnosis of heart failure. N Engl J Med. 2002;347:161–7.
Rost NS, Biffi A, Cloonan L, Chorba J, Kelly P, Greer D, et al. Brain natriuretic peptide predicts functional outcome in ischemic stroke. Stroke. 2012;43: 441–5.
Montaner J, Perea-Gainza M, Delgado P, Ribó M, Chacón P, Rosell A, et al. Etiologic diagnosis of ischemic stroke subtypes with plasma biomarkers. Stroke. 2008;39:2280–7.
Calkins H, Kuck KH, Cappato R, Brugada J, John Camm A, Chen SA, et al. 2012 HRS/EHRA/ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation: recommendations for patient selection, procedural techniques, patient management and follow-up, definitions, endpoints, and research trial design. J Interv Card Electrophysiol. 2012;33:171–257.
Di Biase L, Natale A. Left atrial appendage after electrical isolation: to occlude or not to occlude, that is the question. Circulation. 2016;9(7):e004372.
Tzikas A, Holmes DR, Gafoor R, Ruiz CE, Blomström-Lundqvist C, Diener HC, et al. Percutaneous left atrial appendage occlusion: the Munich consensus document on definitions, endpoints, and data collection requirements for clinical studies. Europace. 2017;19:4–15.
Di Biase L, Santangeli P, Anselmino M, Mohanty P, Salvetti I, Gili S, et al. Does the left atrial appendage morphology correlate with the risk of stroke in patients with atrial fibrillation? Results from a multicenter study. J Am Coll Cardiol. 2012;60:531–8.
Ibrahim MS, Samuel B, Mohamed W, Suchdev K. Cardiac dysfunction in neurocritical care: an autonomic perspective. Neurocrit Care. 2019;30: 508–21.
Ibanez B, Macaya C, Sánchez-Brunete V, Pizarro G, Fernández-Friera L, Mateos A, et al. Effect of early metoprolol on infarct size in ST-segmentelevation myocardial infarction patients undergoing primary percutaneous coronary intervention: the effect of Metoprolol in Cardioprotection During an Acute Myocardial Infarction (METOCARDCNIC) trial. Circulation. 2013;128: 1495–503.
Publisher’s Note
Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.