Alexander P J Vaar, Nicole P Juffermans
Dịch: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Ba thập kỷ trước, tổn thương phổi cấp do truyền máu (TRALI) được coi là một biến chứng hiếm gặp của truyền máu. Ngày nay, Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ công nhận hội chứng này là nguyên nhân hàng đầu gây tử vong do truyền máu. Sự hiểu biết về sinh bệnh học của TRALI đã dẫn đến việc thiết kế các chiến lược phòng ngừa từ quan điểm của ngân hàng máu. Một bước đột phá quan trọng trong việc giảm tỷ lệ TRALI là loại trừ các người hiến máu nữ với sản phẩm có lượng huyết tương cao, dẫn đến giảm khoảng 2/3 tỷ lệ mắc bệnh. Tuy nhiên, chiến lược này đã không loại trừ được hoàn toàn sự phức tạp. Trong vài năm gần đây, nghiên cứu đã xác định các yếu tố nguy cơ liên quan đến bệnh nhân khi bắt đầu TRALI, trong đó có quyền cho các bác sĩ tiếp cận theo từng cá nhân với những bệnh nhân cần truyền máu.
Giới thiệu
Tổn thương phổi cấp liên quan đến truyền máu (TRALI), được xác định là khởi phát suy hô hấp sau khi truyền máu, từ lâu đã được coi là biến chứng hiếm gặp của truyền máu. [1] Tuy nhiên, trong thập kỷ qua, quan điểm đã thay đổi. Sự phát triển của một định nghĩa đồng thuận quốc tế đã giúp cho nghiên cứu TRALI, mang lại tỷ lệ cao hơn ở các quần thể bệnh nhân cụ thể hơn so với trước đây. [2,3] Bệnh nhân mang bệnh lý lâm sàng như nhiễm khuẩn huyết ngày càng được công nhận là có nguy cơ biểu hiện TRALI. Do đó, từ chẩn đoán loại trừ, TRALI đã trở thành nguyên nhân hàng đầu gây tử vong do truyền máu. [2,3,5,6] Tuy nhiên, hội chứng này vẫn còn ở dưới mức chẩn đoán và dưới mức báo cáo ở một số nước. [7-9]
Mặc dù truyền máu có thể cứu sống người bệnh, nó cũng có thể là một sự can thiệp đe dọa mạng sống. Các bác sĩ sử dụng truyền máu hàng ngày. Nâng cao nhận thức về rủi ro của thủ tục này là cần thiết bởi vì việc quản lý truyền máu phù hợp với bệnh nhân có thể làm giảm nguy cơ TRALI. Cách tiếp cận cá nhân như vậy hiện nay có thể thực hiện được khi sự hiểu biết về các yếu tố nguy cơ TRALI phát triển. Hơn nữa, báo cáo đúng về TRALI có thể ngăn ngừa sự tái phát. Trong tổng quan này, chúng tôi thảo luận về bệnh sinh, tần suất, các yếu tố nguy cơ và biểu hiện lâm sàng của TRALI. Chúng tôi cũng phác thảo các chiến lược hiện tại để giảm thiểu hội chứng, và những thách thức lâm sàng còn lại phía trước.
Định nghĩa và chẩn đoán
Trali có thể và trali chậm
TRALI là một chẩn đoán lâm sàng mà không có xét nghiệm chẩn đoán nào. Hội chứng ban đầu được coi là sự khởi đầu của suy hô hấp do phù phổi không do tim gây ra do kháng thể (antibody-induced non-cardiogenic lung oedema). Việc thiếu một định nghĩa quốc tế cho TRALI trước đây đã góp phần vào việc chẩn đoán sai. Như vậy, một ủy ban đồng thuận, và “The US National Heart, Lung and Blood Institute Working Group” năm 2004, đã đưa ra một định nghĩa về TRALI dựa trên các thông số lâm sàng và x quang. [2,10,11] Định nghĩa này xuất phát từ định nghĩa tổn thương phổi cấp tính (bảng 1). [12] Nghi ngờ TRALI được xác định là hoàn chỉnh về định nghĩa tổn thương phổi cấp tính trong vòng 6 giờ sau khi truyền không có yếu tố nguy cơ khác (bảng 1). [2,10,11]
Mặc dù định nghĩa này có vẻ đơn giản, đặc điểm của TRALI không thể phân biệt được với tổn thương phổi cấp do các nguyên nhân khác như nhiễm khuẩn huyết hay dập phổi. Do đó, định nghĩa này sẽ loại trừ khả năng chẩn đoán TRALI ở bệnh nhân có yếu tố nguy cơ tiềm ẩn đối với tổn thương phổi cấp tính cũng đã được truyền máu. Để xác định các trường hợp như vậy, thuật ngữ TRALI có thể được phát triển (bảng 1), [2] cho phép có một yếu tố nguy cơ khác cho tổn thương phổi cấp tính.
Mặc dù định nghĩa TRALI là một định nghĩa về sự đồng thuận quốc tế, các hệ thống giám sát ở một số nước, bao gồm Mỹ, Pháp và Hà Lan, sử dụng một giải pháp thay thế, trong đó có tính quy tội. [13,14] Tính quy tội nhằm xác định khả năng truyền máu là yếu tố căn nguyên (causal factor). Điểm bắt đầu là các nguyên nhân khác của tổn thương phổi cấp có thể được loại trừ, do đó chẩn đoán TRALI là chẩn đoán loại trừ. Tuy nhiên, các nghiên cứu quan sát và trên động vật [8,9,15-18] cho thấy các yếu tố nguy cơ của TRALI bao gồm các rối loạn khác nhau, chẳng hạn như nhiễm trùng huyết. Do đó, một định nghĩa về tính quy tội có thể dẫn đến sự chẩn đoán sai lệch của TRALI. Định nghĩa đồng thuận phù hợp với sự không chắc chắn của mối liên hệ giữa tổn thương phổi cấp tính với truyền máu trong TRALI có thể xảy ra. Định nghĩa thông thường của TRALI sử dụng khoảng thời gian 6 giờ mà trong đó tổn thương phổi cấp tính cần biểu hiện sau khi truyền máu. Ở những bệnh nhân nặng, truyền máu làm tăng nguy cơ (odds ratio 2.13, 95% CI, 1.75-2. 52) để phát triển tổn thương phổi cấp tính 6-72 giờ sau khi truyền máu. [19] Tuy nhiên, liệu cơ chế sinh bệnh của TRALI chậm có giống với cơ chế sinh bệnh TRALI thì điều này không rõ ràng. Trong bài đánh giá này, chúng tôi tập trung vào TRALI biểu hiện trong vòng 6 giờ của truyền máu.
Bệnh sinh
Mô hình hai quả đấm
Một giả thuyết hai quả đấm được đề xuất cho TRALI. [20] Quả đấm đầu tiên là các yếu tố cơ bản của bệnh nhân, kết quả là sự “kết dính” các bạch cầu đa nhân trung tính “được mồi” vào lớp tế bào nội mô phổi. Quả đấm thứ hai là do các hóa chất trung gian trong truyền máu kích hoạt các tế bào nội mô và bạch cầu trung tính trong phổi, dẫn đến sự rò rỉ mao mạch và phù phổi tiếp theo. Quả đấm thứ hai có thể là qua trung gian kháng thể hoặc không qua trung gian kháng thể.
Chuỗi những sự kiện
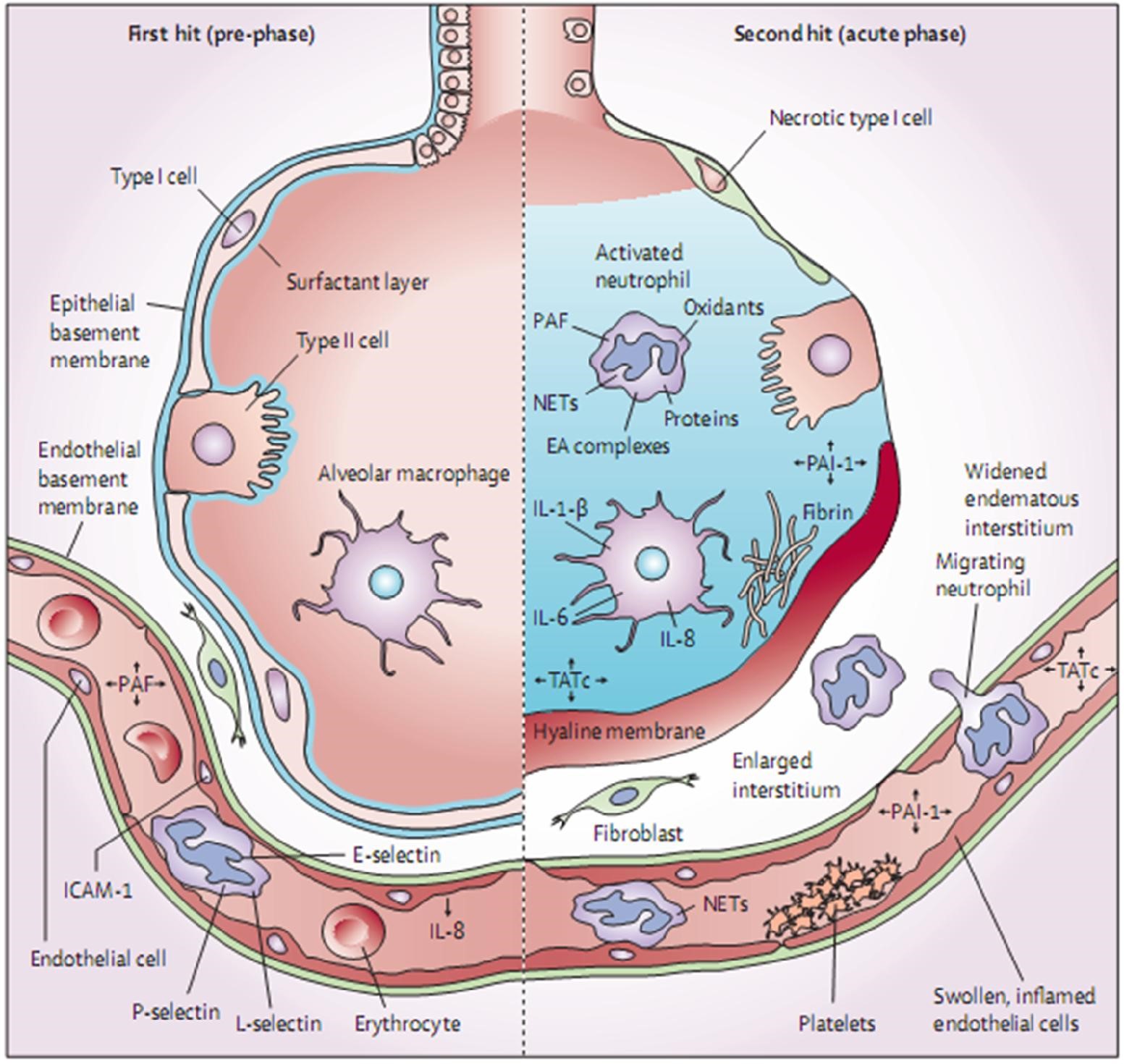
Không phụ thuộc vào yếu tố truyền máu, kích hoạt bạch cầu đa nhân trung tính ở phổi là một phần quan trọng của TRALI. [8,21,22] TRALI được thúc đẩy bởi nồng độ interleukin-8, interleukin-6 tăng lên, và phức hợp elastase-α1-antitrypsin (EA) (hình 1). Mặc dù cơ chế chính xác chưa được biết đến nhưng các nhà nghiên cứu đã cho rằng các tế bào nội mô sản sinh interleukin-8 để đáp ứng với cái gọi là quả đấm đầu tiên gây ra sự hấp dẫn của bạch cầu đa nhân trung tính đến phổi bằng cách tăng biểu hiện bề mặt của các phân tử kết dính tế bào. Sự thay đổi cấu trúc trong các integrins β2 cho phép tiếp xúc gần gũi các bạch cầu đa nhân trung tính với các tế bào nội mô [25], sau đó là sự kết dính các bạch cầu đa nhân trung tính trong các mao mạch nhỏ ở phổi. Việc dính các bạch cầu đa nhân trung tính này đối với các tế bào nội mô phổi là quả đấm đầu tiên gây ra bệnh sinh TRALI.
Hình 1: Sinh lý bệnh của tổn thương phổi cấp do truyền máu (TRALI) qua trung gian hai quả đấm. Giai đoạn trước của hội chứng bao gồm một cú đánh đầu tiên, chủ yếu là hệ thống. Tác động đầu tiên này là rối loạn cơ bản của bệnh nhân (ví dụ, nhiễm khuẩn huyết hoặc viêm phổi) làm cho thu hút bạch cầu đa nhân trung tính đến mao mạch phổi. Neutrophil bị thu hút bởi phổi thông qua việc giải phóng các cytokine và chemokine từ tế bào nội mạc phổi. Sự ràng buộc lỏng lẻo của L-selectin diễn ra. Độ bám chắc được trung gian bởi các chất chọn lọc E-selectin và P-selin và các phân tử kết dính nội bào (ICAM-1). Trong giai đoạn cấp tính của hội chứng, một cú đánh thứ hai gây ra bởi các hóa chất trung gian trong việc truyền máu. Kết quả này cho thấy kích hoạt trong phản ứng viêm và đông máu trong khoang phổi. Các neutrophils gắn liền với nội mạc mao mạch bị tổn thương và di vhuye63n từ khoảng kẽ vào khoảng khí, nó chứa đầy dịch phù giàu protein. Trong khoảng khí, các cytokine interleukin-1, -6, và -8, (IL-1, IL-6, và IL-8 tương ứng) được tiết ra, hoạt động cục bộ để kích thích hóa học và kích hoạt bạch cầu đa nhân trung tính dẫn đến sự hình thành elastase-α1-antitrypsin (EA) phức tạp. Neutrophil có thể giải phóng các chất oxy hóa, proteases, và các phân tử tiền viêm khác, chẳng hạn như yếu tố kích hoạt tiểu cầu (PAF, platelet-activating factor), và hình thành bẫy bạch cầu ngoài tế bào (NETs, neutrophil extracellular traps). Hơn nữa, sự kích hoạt của hệ thống đông máu xảy ra, thể hiện bởi sự gia tăng các phức hợp thrombin-antithrombin (TATc), cũng như sự giảm hoạt động của hệ thống phân hủy fibrinogen, được biểu hiện bằng sự giảm hoạt động của chất kích hoạt plasminogen. Sự xuất hiện của dịch phù giàu protein trong phế nang dẫn đến việc bất hoạt chất surfactant, góp phần tạo nên bức tranh lâm sàng về suy hô hấp cấp tính khi bắt đầu TRALI. PAI-1 = thuốc ức chế hoạt chất plasminogen-1.
Quả đấm thứ hai là truyền máu. Các phát hiện từ các nghiên cứu trên động vật cho thấy sự tương tác của tiểu cầu với bạch cầu đa nhân trung tính là rất quan trọng (hình 1) vì giảm tiểu cầu và tiền xử lý với aspirin thì ngăn ngừa được TRALI. Sự kích hoạt tiểu cầu cũng góp phần tham gia hình thành các bẫy tế bào bạch cầu đa nhân trung tính ngoại bào. [27,28] Mặc dù bảo vệ chống lại nhiễm trùng, những bẫy này có hại cho mô và đã được xác định trong máu và phổi của bệnh nhân với TRALI. Các thí nghiệm trên động vật cho thấy việc điều trị bằng DNase làm giảm sự hình thành bẫy bạch cầu đa nhân trung tính ngoại bào và mức độ nghiêm trọng của TRALI. [27,28] Ngoài các quan sát lâm sàng về giảm tiểu cầu thoáng qua ở TRALI, [29,30] cho thấy tiểu cầu có thể di chuyển đến phổi, các nghiên cứu lâm sàng về sự liên quan của tiểu cầu hầu như không có. Hơn nữa, ghi nhận tăng interleukin-8, -6 và -B, và phức hợp elastase-α1-antitrypsin ở các phế quản; phức hợp này cho biết kích hoạt bạch cầu đa nhân trung tính ở phổi. [9,31] Quả đấm đầu tiên chỉ mồi một số NADPH oxidase của bạch cầu trung tính, nhưng quả đấm thứ hai kích hoạt các oxidase NADPH và dẫn đến sự giải phóng elastase. Hơn nữa, có một luồng bạch cầu đa nhân trung tính đi vào trong khoảng phế nang. Ở những bệnh nhân có phẫu thuật tim, TRALI cũng được đặc trưng bởi sự kích hoạt đông máu, thể hiện bởi sự gia tăng các phức hợp thrombin-antithrombin và chất ức chế hoạt hóa plasminogen, và do giảm sự phân hủy fibrinogen, thể hiện bởi sự giảm nồng độ hoạt tính của chất hoạt hoá plasminogen. Mặc dù khoang phổi là cơ quan bị tổn thương nhất khi bắt đầu TRALI, các nghiên cứu trên động vật cho thấy TRALI qua trung gian kháng thể cũng dẫn đến tổn thương thận và gan do phản ứng kháng thể tại chỗ. [32]
Trali qua trung gian kháng thể (antibody-mediated trali)
TRALI qua trung gian kháng thể là do truyền máu thụ động của HLA hoặc kháng nguyên neutrophil của người (HNA) và các kháng thể tương ứng từ người hiến máu nhằm chống lại các kháng nguyên của người nhận. [33,34] Kích hoạt neutrophil xảy ra trực tiếp bằng cách kết hợp kháng thể với bề mặt neutrophil (các kháng thể HNA) hoặc gián tiếp, chủ yếu bằng cách liên kết với các tế bào nội mô với kích hoạt neutrophil (kháng thể HLA lớp I) hoặc các monocytes với sự kích hoạt bạch cầu trung tính (kháng thể HLA cấp II). [33,35] Hiệu giá kháng thể và thể tích huyết tương kháng thể làm tăng nguy cơ khởi phát TRALI. [8,36] Mặc dù vai trò của kháng thể HLA và HNA của người hiến máu từ máu được truyền đã được chấp nhận rộng rãi, [33] không phải tất cả các trường hợp TRALI đều có kháng thể. Ở nhiều bệnh nhân, không thể phát hiện kháng thể. [7,37] Hơn nữa, nhiều sản phẩm máu chứa kháng thể không dẫn đến TRALI. [38-40] Kết luận này đã dẫn đến sự phát triển của một giả thuyết khác cho sự khởi phát của TRALI, gọi là TRALI không qua trung gian kháng thể.
Trali không qua trung gian kháng thể (non-antibody-mediated trali)
TRALI không qua trung gian kháng thể là do sự tích tụ các chất trung gian tiền viêm trong quá trình lưu trữ các sản phẩm máu, và có thể do lão hóa hồng cầu và tiểu cầu. [16,41,42] Mặc dù hầu hết các nghiên cứu tiền lâm sàng đã ghi nhận mối tương quan giữa thời gian lưu trữ các sản phẩm có chứa máu và TRALI, cơ chế này đang gây tranh cãi. Hai cơ chế đã được đề xuất, bao gồm cả plasma hoặc các tế bào già. Trong một nghiên cứu nhỏ và các thí nghiệm trên động vật, việc tích tụ lipid sinh học và phối tử CD40 hòa tan (sCD40L) trong lớp huyết tương của các sản phẩm có chứa tế bào máu đã được liên kết với TRALI. [16,17,43,44]
Các lipid sinh học được cho là gây ra sự kích hoạt bạch cầu đa nhân trung tính thông qua thụ thể liên kết protein G trên neutrophil. Truyền tín hiệu sCD40L kích hoạt thụ thể CD40 trên bạch cầu trung tính và nội mô kết quả là phóng thích cytokine tiền viêm. Tuy nhiên, sự tham gia của các trung gian này trong TRALI đã không được khẳng định trong các nghiên cứu khác. [8,46,47]
Khác với huyết tương, các tế bào già có thể có vai trò. Trong quá trình bảo quản, hồng cầu bị thay đổi hình thái. Việc mất biểu hiện kháng nguyên của Duffy trên hồng cầu già trở lên làm giảm các triệu chứng hóa ứng động hồng cầu và góp phần vào TRALI trong một môi trường thực nghiệm. Ngoài ra, mất khả năng giải phóng adenosine-5′-triphosphate diễn ra trong suốt
quá trình bảo quản [42], làm tăng sự kết dính của hồng cầu vào các tế bào nội mô và dẫn đến tình trạng thiếu oxy và hồng cầu thoát mạch vào trong khoảng phế nang trong một mô hình thực nghiệm trên động vật. [42] Dữ liệu lâm sàng cho thấy kết quả cho vai trò của máu lão hóa trong TRALI. [8,15,18] Các nghiên cứu tiền lâm sàng cho thấy việc rửa các tế bào hồng cầu lưu trữ và tiểu cầu trước khi truyền máu đã ngăn ngừa TRALI trong mô hình động vật. [48,49] Rất ít dữ liệu có sẵn để hỗ trợ chính sách này trong thực hành lâm sàng.
Mô hình ngưỡng (Threshold model)
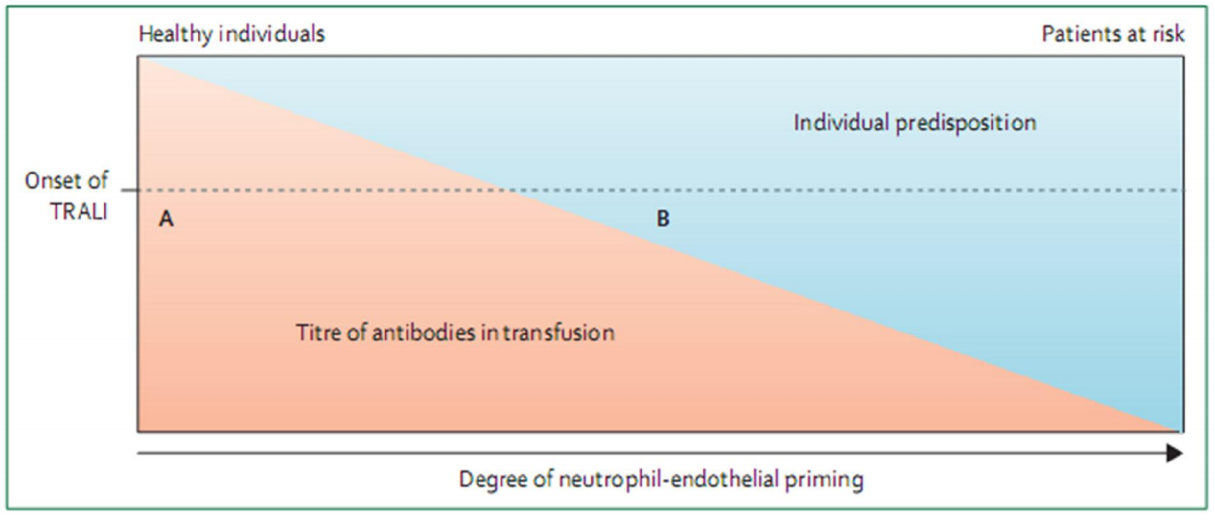
Mô hình hai quả đấm cho thấy rằng bệnh nhân ở tình trạng lâm sàng xấu có nguy cơ phát triển TRALI. Tuy nhiên, các trường hợp đã được mô tả về TRALI qua trung gian kháng thể phát triển ở người nhận khá lành mạnh. [11,50] Để giải thích sự khác biệt này, một mô hình ngưỡng đã được đề xuất [51], trong đó phải vượt qua một ngưỡng để gây ra phản ứng TRALI (hình 2).
Hình 2: Mô hình ngưỡng của tổn thương phổi cấp do truyền máu (TRALI) qua trung gian kháng thể. Một ngưỡng cụ thể phải được vượt qua để gây ra phản ứng TRALI. Để vượt qua ngưỡng đó, một vài yếu tố cùng tác động: kích hoạt của bạch cầu đa nhân trung tính phổi ở thời điểm truyền máu, sức mạnh của hoạt động mồi neutrophil của các hóa chất trung gian truyền vào (A), và tình trạng lâm sàng của bệnh nhân (B). [51]
Ngưỡng này phụ thuộc cả vào khuynh hướng của bệnh nhân (quả đấm đầu tiên) và số lượng kháng thể trong truyền máu (quả đấm thứ hai). Một lượng lớn kháng thể phù hợp với kháng nguyên của người nhận có thể gây TRALI nghiêm trọng ở người nhận không có tiền căn gì. Ở một bệnh nhân khá khỏe mạnh mà không có sự “mồi” của bạch cầu đa nhân trung tính, kháng thể có thể không đủ mạnh hoặc đủ lớn để vượt ngưỡng. Mô hình này nhấn mạnh khái niệm rằng các quần thể bệnh nhân cụ thể nhạy cảm với phản ứng TRALI do sự có mặt của đáp ứng viêm, dẫn đến việc “mồi” các bạch cầu đa nhân trung tính ở phổi. [2,11]
Tần suất
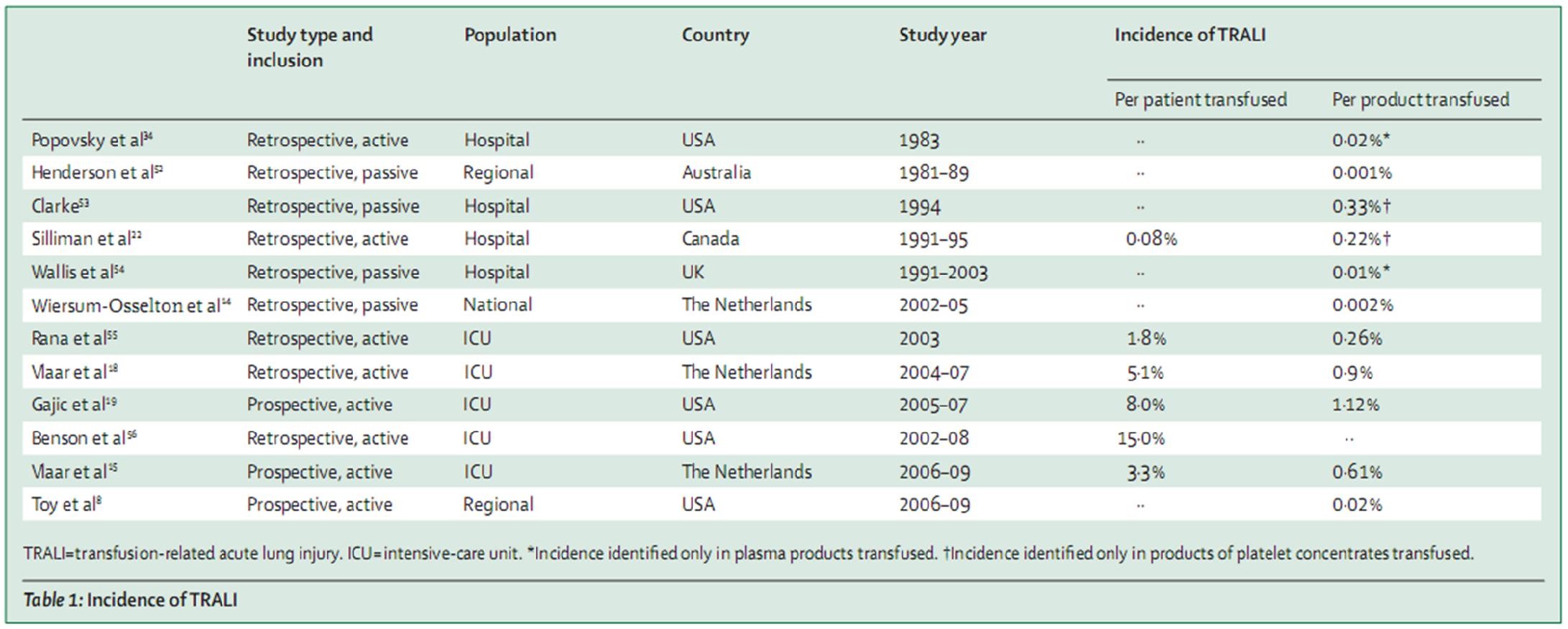
Tỷ lệ TRALI ước tính khoảng từ 0.08% đến 15% bệnh nhân được truyền máu (bảng 1). Sự đa dạng về các triệu chứng lâm sàng, không có dấu hiệu bệnh và các xét nghiệm chẩn đoán đặc hiệu, và sự thiếu vắng một định nghĩa rõ ràng có thể góp phần tạo ra một sự khác biệt lớn về ước tính tỷ lệ mắc bệnh TRALI. Sự khác biệt trong thiết kế nghiên cứu cũng cần lưu ý. Báo cáo thụ động thường mang lại tỷ lệ thấp hơn so với giám sát chủ động (bảng 1). Định nghĩa về sự đồng thuận năm 2004 cho phép ước lượng TRALI và TRALI có thể cho các quần thể mà ở đó có các yếu tố nguy cơ khác đối với tổn thương phổi cấp tính, thường là những bệnh nhân bị bệnh nặng. Lưu ý, tỷ lệ mắc bệnh TRALI cao gấp 50-100 lần ở nhóm bệnh nặng so với dân số bệnh viện tổng quát (bảng 1).
Một số lý do có thể giải thích được tỷ lệ mắc cao ở một số bệnh nhân. Những bệnh nhân bị bệnh nghiêm trọng đang phải đối phó với nguy cơ truyền máu, bởi vì đến 50-70% người nhận được một sản phẩm máu trong thời gian họ ở trong phòng ICU. [57,58] Hơn nữa, có những sự khác biệt liên quan đến quả đấm đầu tiên. Những người bị bệnh nặng thường có rối loạn lâm sàng, có thể bị “mồi” và hoạt hóa bạch cầu đa nhân trung tính, làm cho họ nhạy cảm với các chất trung gian trong máu truyền vào và sự phát triển TRALI. Cùng với yếu tố này, những người bệnh nặng với TRALI thường bị quả đấm đầu tiên trước khi truyền máu [18], điều này có thể giải thích sự gia tăng tỷ lệ TRALI trong dân số bị bệnh nặng.
Biểu hiện lâm sàng
Các rối loạn về đường hô hấp, bao gồm khó thở, thở nhanh và thiếu oxy máu là những triệu chứng lâm sàng trung tâm của TRALI. Những vấn đề này là kết quả của sự tăng tính thấm mạch máu và gây ra phù phổi. Tuy nhiên, có rất nhiều phản ứng khác có thể xảy ra do truyền các kháng thể vào, bao gồm chứng lạnh run, nhịp tim nhanh và sốt, giảm thân nhiệt và hạ huyết áp, và hiếm khi tăng huyết áp. [59,60]
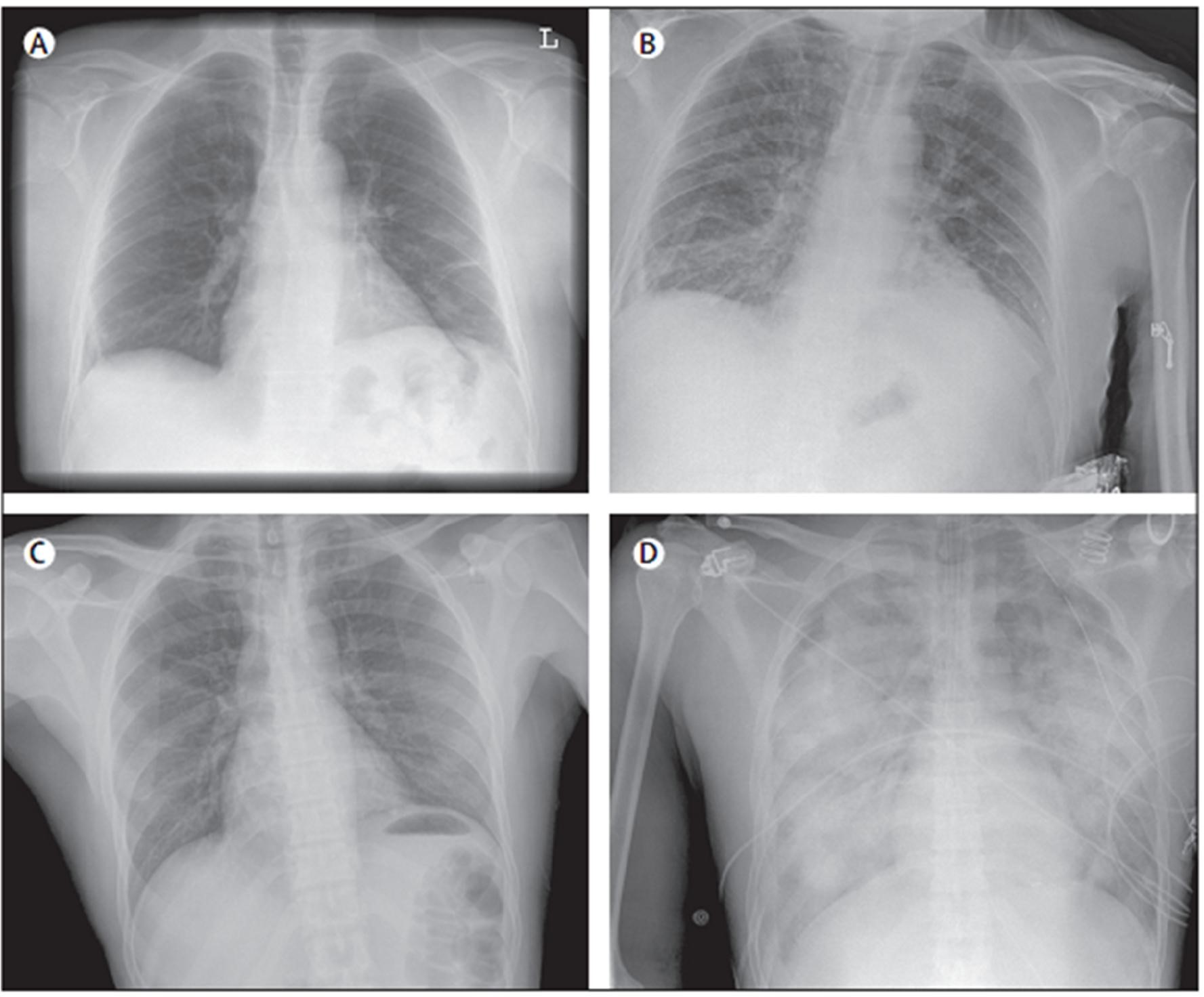
Dấu hiệu bất thường mô kẽ hai bên trên chụp X quang phổi để xác định định nghĩa TRALI. Mô tả trường hợp ban đầu của TRALI biểu hiện suy hô hấp cấp ở bệnh nhân 1 giờ sau khi truyền một sản phẩm chứa huyết tương cao, với xuất hiện phổi trắng trên X quang. Tuy nhiên, phổi trắng không phải lúc nào cũng có mặt; những bất thường về hình ảnh X quang có thể ít nổi bật hơn (hình 3). [60]
Hình 3: X quang phổi của bệnh nhân bị TRALI. Đây là x quang phổi của 2 bệnh nhân trước (A, C) và sau (B, D) khí khởi phát TRALI. Hình A và C cho thấy giường mạch máu phổi bình thường không có dấu hiệu phù phổi; B và D cho thấy các thay đổi thầm nhiễm gợi ý phù phổi. D cho thấy hình ảnh thâm nhiễm phổi 2 bên nặng, kinh điển cho TRALI; tuy nhiên , thường là các hình ảnh thay đổi ít nặng hơn, như ở hình B.
Xét nghiệm trong TRALI không cụ thể. Phổ biến nhất là giảm bạch cầu thoáng qua, xuất hiện ở 5-35% bệnh nhân sau khi truyền máu với một sản phẩm có chứa kháng thể và được cho là do các kháng thể đặc hiệu với bạch cầu đa nhân trung tính [59] Giảm tiểu cầu cũng có thể xảy ra. [29,30] Một câu hỏi hấp dẫn vẫn là tại sao các triệu chứng của phản ứng truyền máu lại nổi bật đến vậy trong khoang phổi. Mặc dù TRALI có thể dẫn đến rối loạn chức năng cơ quan khác với tổn thương phổi cấp tính, nhưng hầu hết các phản ứng lại xuất hiện khi suy cơ quan đơn lẻ. Chức năng phổi như là cơ chế phòng vệ chủ yếu vì vi sinh vật lây nhiễm có thể dễ dàng hít vào. Ngoài ra, neutrophils mồi trải dài và mất khả năng thay đổi hình dạng của chúng. Việc các bạch cầu đa nhân trung tính này đi qua các mao mạch phổi hẹp cho phép tiếp xúc gần gũi và tương tác với các tế bào nội mạc, có thể dẫn đến kích hoạt neutrophil. [51] Về mặt giải phẫu, phổi là cơ quan miễn dịch đầu tiên mà các chất trong truyền máu qua đó; như vậy, các hóa chất trung gian gây khởi phát của TRALI có thể không đến được với các cơ quan khác.
Phân biệt trali với phù phổi do các nguyên nhân khác
Phản ứng truyền máu nhiễm khuẩn có thể xuất hiện dưới dạng TRALI. Nếu có dấu hiệu nhiễm khuẩn huyết, nên bắt đầu điều trị nhiễm khuẩn huyết trong khi nhuộm Gram và cấy máu túi máu và cấy máu của bệnh nhân đang chờ kết quả. Phản ứng phản vệ, bao gồm thở nhanh và thở khò khè, cũng có thể suy hô hấp. Bởi vì các triệu chứng là kết quả của phù thanh quản và phế quản chứ không phải do phù phổi, chụp X quang phổi có thể giúp chẩn đoán. Các dấu hiệu khác cho thấy phản ứng dị ứng là nổi mày đay và ban đỏ trên mặt và thân.
Sự khác biệt lâm sàng giữa phù do tăng áp suất thủy tĩnh do suy tim mất bù, do quá tải tuần hoàn (TACO, transfusion-associated circulatory overload) và phù phổi do tăng tính thấm trong TRALI là một thách thức. Chụp X quang ngực không hữu ích trong việc phân biệt những rối loạn này (bảng 2).
Các kỹ thuật chẩn đoán đặc biệt – ví dụ siêu âm tim hoặc BNP (brain natriuretic peptide) – đã được sử dụng trong các thuật toán có thể hướng dẫn các bác sĩ lâm sàng, [62] nhưng không thử nghiệm nào có thể tự thành lập được chẩn đoán. [63] Áp lực động mạch phổi đã được thêm vào các định nghĩa của TRALI để loại trừ bệnh nhân với quá tải thể tích. Tuy nhiên, phù do thẩm thấu và phù do thủy tĩnh không loại trừ lẫn nhau và có thể xảy ra đồng thời. Tổn
thương phổi cấp có thể dẫn đến tình trạng xấu hơn của thất phải và thất trái. Ngược lại, sự cân bằng dịch hạn chế làm giảm số ngày thở máy của bệnh nhân bị tổn thương phổi cấp tính, cho thấy phù thủy tĩnh cũng tham gia vào gây tổn thương phổi. [65] Việc công nhận hội chứng TRALI là một thách thức. Do đó, nhiều trường hợp không được báo cáo, như được chứng minh bằng các nghiên cứu hồi cứu lại. Do đó, tỷ lệ thực sự của TRALI có lẽ là cao hơn sau khi nhận thức trong thực hành lâm sàng.
Đa dạng về mức độ nghiêm trọng của bệnh
Từ chuỗi sự kiện, mức độ nghiêm trọng của các triệu chứng TRALI thì khác nhau. Độ nặng có thể từ thở oxy đến thông khí cơ học và ngay cả các phản ứng gây tử vong xảy ra. [54] Cho dù TRALI qua trung gian kháng thể và TRALI không qua trung gian kháng thể khác nhau về mức độ trầm trọng triệu chứng không được biết. Các báo cáo [33] gợi ý rằng các kháng thể đối với HNA thường liên quan đến các phản ứng TRALI gây tử vong hơn là những kháng thể khác, nhưng sự kết hợp này vẫn chưa được khẳng định. Lưu ý, nhiều giai đoạn của TRALI có thể không bị phát hiện. Hướng dẫn đồng thuận loại trừ các dạng nhẹ của hội chứng này. Cần loại trừ này vì các trường hợp nhẹ được cho là khó theo dõi và khó so sánh giữa các hệ thống giám sát với nhau. [3] Từ các báo cáo trường hợp, TRALI có thể gây phản ứng nhẹ, một số trong đó không đáp ứng các tiêu chí của các khái niệm đồng thuận. [66]
Thời gian biểu hiện triệu chứng
Nói chung, có một đồng ý rằng suy hô hấp sẽ xảy ra trong vài giờ đầu tiên sau khi truyền máu; tuy nhiên, giả thiết này chủ yếu dựa vào kinh nghiệm cá nhân. [67] Cửa sổ thời gian 6 giờ được lựa chọn dựa trên mô tả của loạt trường hợp đầu tiên từ năm 1985, [34] và dựa trên ý kiến của một ban chuyên gia.
Điều trị
Không có điều trị nào cho hội chứng đe dọa tính mạng này. Điều trị của TRALI là hỗ trợ.
Bệnh nhân cần thêm oxy, và thông khí cơ học là không thể tránh được trong 70-90% trường hợp. [34,54] TRALI được coi là một phần của tổn thương phổi cấp tính (ALI) hoặc hội chứng suy hô hấp cấp tính (ARDS); do đó, việc áp dụng thông khí thể tích khí lưu thông hạn chế là hợp lý, bởi vì phương pháp này có lợi cho bệnh nhân có các rối loạn này. Mặc dù một số báo cáo trường hợp mô tả việc sử dụng corticosteroid ở bệnh nhân TRALI, không có bằng chứng nào cho thấy rằng những thuốc này nên được áp dụng. Thuốc lợi tiểu có thể có một vị trí điều trị TRALI, bởi vì sự cân bằng dịch dương tính là một yếu tố nguy cơ đối với TRALI và một chiến lược hạn chế dịch là có lợi trong ALI/ARDS do các nguyên nhân khác. Thí nghiệm trên động vật cho thấy kết quả hứa hẹn cho aspirin. [26] Lưu ý, việc sử dụng các chất ức chế kết tập tiểu cầu có liên quan đến tổn thương phổi giảm ở bệnh nhân ARDS, nhưng hiệu quả của những can thiệp này đã không được thử nghiệm ở bệnh nhân.
Tiên lượng
TRALI thường có tiên lượng tốt. Tử vong được coi là thấp ở khoảng 5-10%. [54,67,69]. Tuy nhiên, dữ liệu cho kết quả là rời rạc, và chủ yếu dựa trên các báo cáo loạt trường hợp nhỏ. Trong các nghiên cứu quan sát, tỷ lệ tử vong ở TRALI cao hơn ở những bệnh nhân bị bệnh nặng và phẫu thuật so với các ca kiểm soát truyền máu. [9,18,19,56] Một tổng kết cũng đã được báo cáo so sánh giữa truyền hồng cầu, huyết tương, và tiểu cầu, và tổn thương phổi cấp tính trong một số nghiên cứu quan sát khác. [70,71] Tuy nhiên, các kết luận từ các nghiên cứu quan sát này không làm rõ mức độ truyền máu hoặc các yếu tố nguy cơ khác đối với tổn thương phổi cấp tính góp phần vào tử vong.
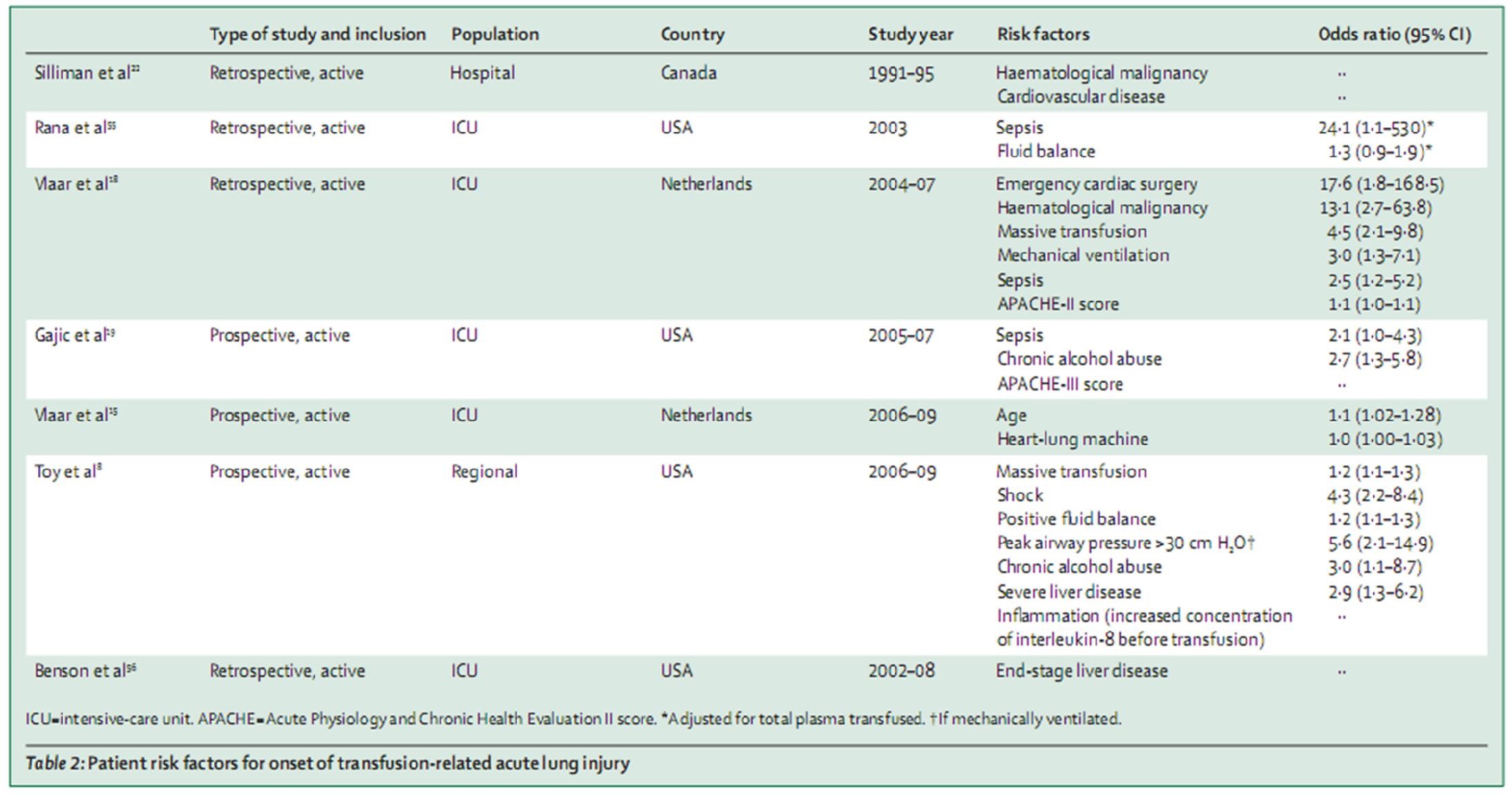
Các yếu tố nguy cơ khởi phát trali trên bệnh nhân
Trong 5 năm qua, các nhà nghiên cứu đã xác định được các yếu tố nguy cơ cụ thể cho TRALI ở người nhận truyền máu. 33% bệnh nhân thở máy đã phát triển thương tích phổi cấp tính trong vòng 48 giờ truyền máu trong một nghiên cứu quan sát [55]. Một nghiên cứu hồi cứu khẳng định rằng sự hiện diện của thông khí cơ học dẫn tới sự phát triển của TRALI (bảng 2 và hình 4). Bởi vì áp dụng áp lực đỉnh đường thở cao làm tăng nguy cơ TRALI ở bệnh nhân và ở các cơ sở thực nghiệm [36,72], chúng tôi giả sử rằng sự kéo giãn cơ học của phổi do thông khí áp lực dương dẫn đến việc “mồi” (priming) các bạch cầu đa nhân trung tính trong phổi hoặc nội mô.
Các tác động ngoài phổi cũng có khuynh hướng gây TRALI. Các phẫu thuật đặc biệt là một yếu tố nguy cơ (bảng 2). Nguy cơ gia tăng với một số thủ thuật có thể là do hội chứng đáp ứng viêm toàn thân, như được đề xuất bởi các mô hình thử nghiệm nội độc tố máu (endotoxaemia) [26,43] và được ghi nhận ở những bệnh nhân phẫu thuật tim đã được theo dõi sát cho sự xuất hiện của TRALI. [9] Nhiễm khuẩn huyết được xác định như là một yếu tố nguy cơ đối với TRALI trong một số nghiên cứu của bệnh nhân đang ở ICU (bảng 2). Trong phẫu thuật tim, thời gian trên tim phổi nhân tạo có liên quan với TRALI, [15] cho thấy thiết bị này có thể góp phần làm “mồi” bạch cầu đa nhân trung tính, như được trình bày trong các nghiên cứu trước đó. [73] Các điều kiện mà bệnh nhân thường nhận được truyền máu, bao gồm bệnh ác tính huyết học, xuất huyết nhiều trên bệnh nhân suy gan, và truyền máu số lượng lớn, dường như là những yếu tố nguy cơ rõ ràng cho TRALI. Cho dù nguy cơ chủ yếu được xác định bởi các điều kiện cơ bản hoặc truyền máu nhiều vẫn còn phải được xác định. Một sự cân bằng dịch dương có liên quan đến sự phát triển của TRALI, cho thấy rằng quá tải dịch có thể có một vai trò trong bệnh sinh TRALI. [8,55] Việc xác định các yếu tố nguy cơ liên quan đến người được truyền máu cụ thể cho phép các bác sĩ có cách tiếp cận chủ động đối với bệnh nhân cần truyền máu.
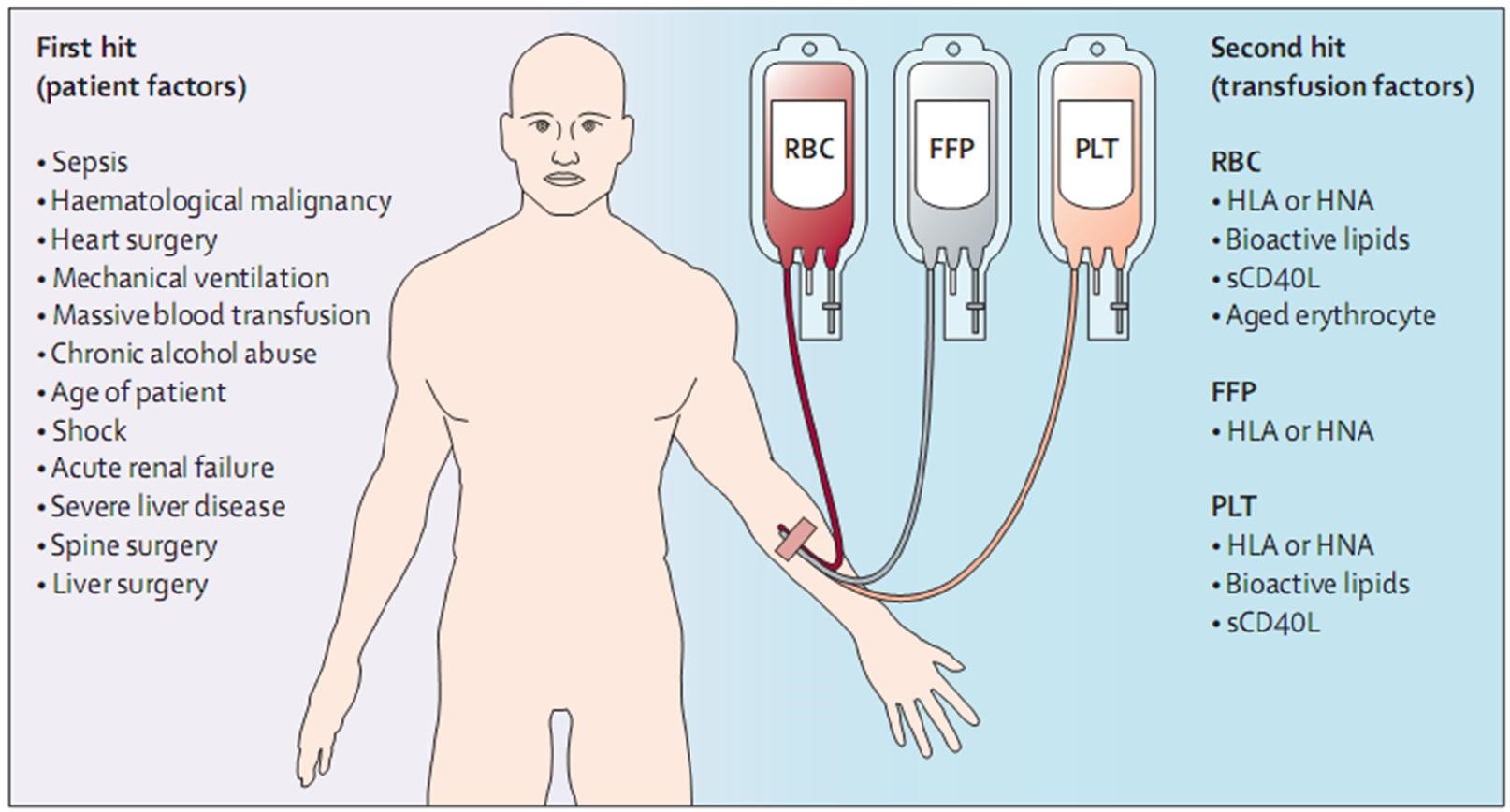
Hình 4: Các mô hình hai cú đấm của TRALI. Đợt tấn công đầu tiên bao gồm các yếu tố bệnh nhân dẫn đến sự mồi của bạch cầu đa nhân trung tính phổi. Các yếu tố nguy cơ đã được đề xuất có thể hoạt động như là một cú đấm đầu tiên. Đợt thứ hai là truyền máu dẫn đến sự kích hoạt của các tế bào nội mô, và các bạch cầu đa nhân trung tính phổi được làm mồi kết quả là rò rỉ mao mạch, lên đến đỉnh điểm là phù phổi. Một số yếu tố truyền là không phụ thuộc vào loại sản phẩm máu, trong khi một số khác chỉ định cho một loại sản phẩm. RBC=red blood cells. HLA=human leucocyte antibodies. HNA=human neutrophil antibodies. sCD40L=soluble CD40 ligand. FFP=fresh frozen plasma. PLT=platelet concentrate.
Bác sĩ có thể làm gì ?
Chính sách hạn chế truyền máu
Việc ngăn ngừa hiệu quả nhất là một chiến lược truyền máu hạn chế. Trong một thử nghiệm lâm sàng ngẫu nhiên ở những bệnh nhân nặng, chính sách truyền máu hạn chế đối với các hồng cầu có liên quan đến sự giảm tỷ lệ thương tổn phổi cấp so với chiến lược tự do (7.7% so với 11.4%), [74] gợi ý rằng một số trong những bệnh nhân này có thể đã có TRALI.
Ngưỡng hạn chế được dung nạp tốt và đã giúp rất nhiều trong việc hướng dẫn truyền hồng cầu trong ICU. Tuy nhiên, kết quả của thử nghiệm nền tảng này chỉ được triển khai một phần trong các ICU từ đó, [58,75] và một sự khác biệt lớn trong thực tiễn truyền máu vẫn còn. [76] Đối với huyết tương tươi đông lạnh, các cuộc kiểm tra liên tục báo cáo mức sử dụng huyết tương cao mà không có chỉ định lâm sàng rõ ràng. [77-80] Sử dụng hỗ trợ quyết định điện tử đã làm giảm các ca truyền máu không hợp lý, điều này liên quan đến việc giảm tổn thương phổi. [81] Đối với truyền máu không khẩn cấp, sự trì hoãn truyền máu đã được gợi ý cho đến khi tình trạng viêm cấp tính đã giảm xuống.
Chính sách truyền máu phù hợp với bệnh nhân
Không thể tránh được truyền máu. Phân tích đa biến ở bệnh nhân ICU cho thấy các yếu tố nguy cơ liên quan đến bệnh nhân đóng góp nhiều hơn cho sự khởi đầu của TRALI so với các yếu tố nguy cơ truyền máu, cho thấy rằng sự phát triển của phản ứng TRALI phụ thuộc nhiều hơn vào các yếu tố vật chủ, sau đó là các yếu tố trong sản phẩm máu. Vì vậy, một phương pháp tiếp cận phù hợp với bệnh nhân có thể làm giảm nguy cơ TRALI.
Xác định các yếu tố nguy cơ cụ thể cho phép các bác sĩ điều trị bệnh nhân cần truyền máu. Cân bằng dịch nên được giám sát. Cần tránh để bệnh nhân vào sốc trước khi truyền máu, cũng như quá tải dịch trước khi truyền máu. Đối với bệnh nhân thở máy, áp lực đường thở nên được hạn chế trước khi truyền máu. Vì thông khí có thể tích khí lưu thông thấp làm giảm tử vong ở bệnh nhân bị tổn thương phổi cấp tính, nên việc áp dụng thông khí như vậy ở những bệnh nhân cần truyền máu có vẻ thích hợp.
Đặt hàng các sản phẩm đặc biệt cho bệnh nhân có nguy cơ cao
Các yếu tố nguy cơ truyền máu đối với sự phát triển TRALI không qua trung gian kháng thể dường như liên quan sự dự trữ sản phẩm máu; do đó, bệnh nhân có nguy cơ đối với TRALI có thể được hưởng lợi từ các sản phẩm máu tươi. Trong khi thời gian bảo quản dường như là một phần trong sự khởi đầu của TRALI trong hầu hết các mô hình thí nghiệm, [16,17,41,43,48,49] các nghiên cứu lâm sàng cho thấy kết quả (bảng 3). Một nghiên cứu ngẫu nhiên được thực hiện ở trẻ sơ sinh không cho thấy sự khác biệt giữa kết quả giữa hồng cầu tươi và các tế bào hồng cầu dự trữ. [83] Một thử nghiệm ở những bệnh nhân người lớn đang được chăm sóc đặc biệt đang được tiến hành. [84] Tuy nhiên, các nghiên cứu này không trực tiếp điều tra TRALI, vì vậy không có khuyến cáo nào có thể được đưa ra. Thay vì cung cấp các tế bào hồng cầu tươi, các nghiên cứu tiền lâm sàng cho thấy việc rửa các sản phẩm chứa máu chứa trong tế bào có thể ngăn ngừa sự xuất hiện của TRALI. [48,49] Các nghiên cứu lâm sàng cho thấy rửa các sản phẩm như vậy ở tại giường là an toàn và khả thi. Cho dù các sản phẩm chứa máu đã rửa sạch sẽ có ngăn ngừa sự khởi phát của TRALI trong môi trường lâm sàng hay không, vẫn cần được xác định.
Báo cáo trali
Các phản ứng TRALI nghi ngờ phải được báo cáo cho ngân hàng máu để xác định và loại trừ các người hiến máu liên quan với các kháng thể để ngăn ngừa các phản ứng trong tương lai. Để chăm sóc các trường hợp nghi ngờ, một nhóm được thành lập bao gồm các nhân viên giám sát huyết học, các nhà huyết học, các bác sĩ truyền máu và các bác sĩ ICU. Vì TRALI là một chẩn đoán lâm sàng, nên việc thực hiện báo cáo có thể khác nhau; quả thực, việc kiểm tra giữa các báo cáo này cho thấy những khác biệt đáng kể tồn tại. Hơn nữa, việc thực hiện báo cáo không phù hợp với lý thuyết hai cú đấm, bởi vì nhiễm khuẩn huyết trước khi truyền máu được xem là một lý do quan trọng để không báo cáo trường hợp nghi ngờ.
Nơi cung cấp máu có thể làm gì?
Tất cả các sản phẩm máu có thể gây TRALI qua trung gian kháng thể nếu kháng thể đủ mạnh và bệnh nhân có các yếu tố nguy cơ dễ bị tổn thương, ngay cả các tế bào hồng cầu có chứa 10-20 mL huyết tương (hình 4). [86] Thay vì tập trung vào loại sản phẩm máu, thông tin về những người hiến máu có tỷ lệ cao về kháng thể HLA hoặc HNA là quan trọng hơn. Có thể xác định được hai nhóm các người hiến máu nguy cơ cao: các người hiến máu mang thai nhiều lần và người hiến máu tiếp xúc với truyền máu. Khả năng tiêm chủng tự-HLA ở những người hiến máu sẽ tăng theo số lần mang thai. [87-89] Giới tính của người hiến máu được thể hiện trong hai nghiên cứu của những bệnh nhân bị bệnh nặng biểu hiện oxy hóa trở nên trầm trọng hơn sau khi truyền huyết tương tươi đông lạnh từ các người hiến máu nữ và các người hiến máu nữ mang thai nhiều lần. Nghiên cứu cho thấy mối liên hệ giữa truyền máu và sự có mặt của các kháng thể leucocyte ở 3% số người hiến máu đã được truyền máu trước đây, làm cho người hiến máu này có nguy cơ cao. [88]
Loại trừ người hiến máu
Để giảm nguy cơ TRALI, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ khuyến khích các ngân hàng máu chấp nhận chiến lược chủ yếu là các người hiến máu nam giới. Một chính sách loại trừ các người hiến máu trong trường hợp TRALI với kháng thể HLA hoặc HNA đã được chứng minh phù hợp với kháng nguyên người nhận. Ở Hà Lan, các người hiến máu liên quan đến hai lần trong phản ứng TRALI được loại trừ khỏi sự đóng góp trong tương lai, ngay cả khi không có các kháng thể HLA hoặc HNA. Cách tiếp cận này dựa vào việc báo cáo đúng các trường hợp nghi ngờ TRALI; tuy nhiên, nó có thể dẫn đến mất mát không cần thiết của các người hiến máu.
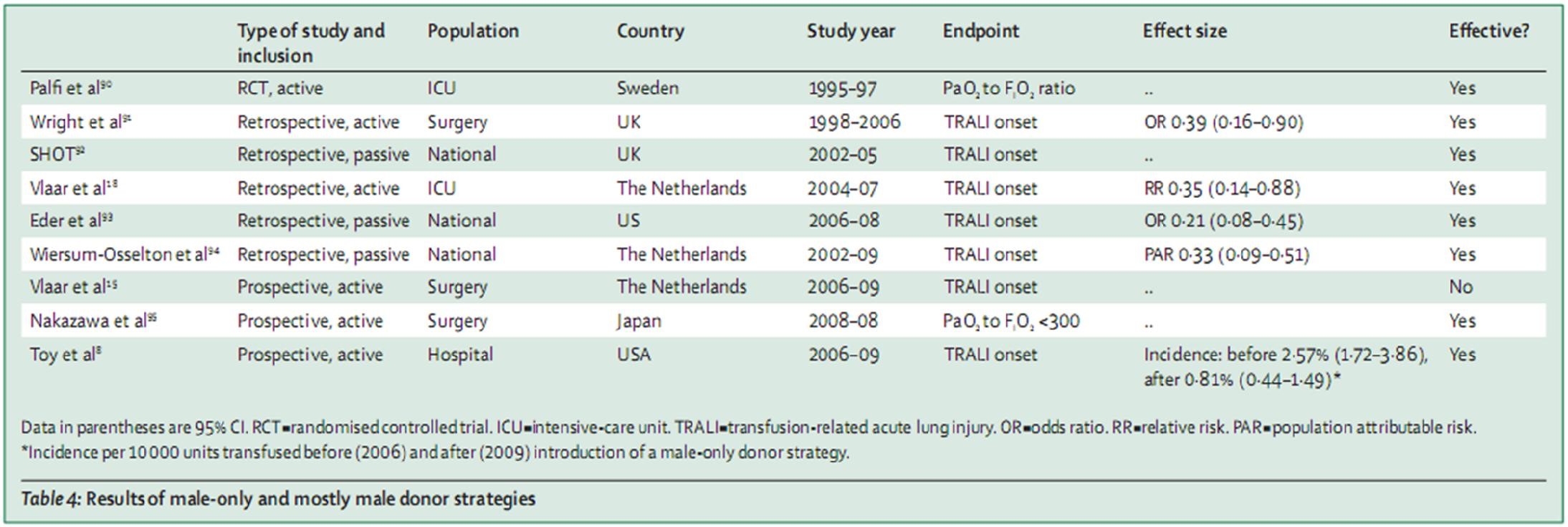
Cách tiếp cận khác là một chính sách loại trừ chủ động với việc loại trừ các người hiến máu có nguy cơ kháng thể HLA hoặc HNA. Như đã đề cập ở trên, các sản phẩm máu có nguồn gốc từ các người hiến máu mang thai nhiều lần liên quan đến sự khởi phát của TRALI. Từ năm 2003, chính sách chỉ sử dụng huyết tương từ các người hiến máu nam giới để sản xuất các thành phần máu huyết tương cao đã được thực hiện. Chính sách này đã dẫn đến giảm hai phần ba các trường hợp TRALI (bảng 4). [13,91,94,96,97]
Cho dù một chính sách của các người hiến máu chỉ dành cho nam giới ngăn ngừa TRALI liên quan đến sản phẩm có khối lượng huyết tương thấp, chẳng hạn như hồng cầu lắng, cần được xác định. Một chính sách khắt khe hơn là kiểm tra tất cả các người hiến máu hoặc các người hiến máu có nguy cơ đối với các kháng thể HLA hoặc HNA. Bên cạnh lao động và chi phí cao, các khả năng kiểm tra kháng thể HLA và HNA quy mô lớn không có sẵn trong năm 2003. Một số khó khăn đã được khắc phục bằng việc áp dụng kỹ thuật cytometry dựa trên hạt dựa vào hạt để kiểm tra kháng thể HLA. Tuy nhiên, những cutoff tiêu chuẩn được áp dụng là không rõ ràng. Ở một bệnh nhân nặng, ngay cả một liều lượng kháng thể hoặc thể tích kháng thể thấp cũng đủ để xảy ra TRALI.
Tập hợp huyết tương
Một giải pháp khác để giảm sự phơi nhiễm của người nhận kháng thể có trong huyết tương là tổng hợp tới 300 đơn vị, làm loãng bất kỳ kháng thể bạch cầu nào có trong máu. Không có khả năng phát hiện được HNA và HLA trong huyết tương. [98] Các nước sử dụng chất dung môi tẩy rửa không báo cáo bất kỳ trường hợp TRALI nào có nguồn gốc từ việc truyền các sản phẩm plasma này. [99] Các mối quan tâm của việc chia sẻ được tiếp xúc với nhiều người hiến máu là truyền virut và bệnh prion. Một bộ lọc prion đã được đưa ra để ngăn ngừa truyền bệnh Creutzfeldt-Jacob; [100] Tuy nhiên, việc tiếp xúc của bệnh nhân với hàng trăm người hiến máu vẫn có thể không mong muốn. Một sự không chắc chắn khác là tính hiệu quả của dung môi tẩy rửa huyết tương trong quá trình điều trị TRALI ở những bệnh nhân nặng, bởi vì những bệnh nhân này vẫn có thể phát triển TRALI sau khi pha loãng kháng thể.
Kết luận
Mặc dù các xét nghiệm chẩn đoán hạn chế, tỷ lệ TRALI có vẻ cao ở nhóm bệnh nhân có nguy cơ cao. Do đó, TRALI là một vấn đề về chăm sóc sức khoẻ bị đánh giá thấp. Các biện pháp phòng ngừa, như các chiến lược chủ yếu là các người hiến máu nam, đã thành công trong việc giảm nguy cơ TRALI. Xác định các yếu tố nguy cơ tiếp tục cải thiện việc đánh giá nguy cơ của việc truyền máu. Để tiếp tục làm giảm nguy cơ TRALI cần tăng nhận thức về hội chứng này trong các bác sĩ.
Thực hiện: BS. Đặng Thanh Tuấn (01/02/2018)