Tóm tắt
Thường được phát hiện trên lâm sàng khi bilirubin huyết thanh >85,5 micromol/L (5 mg/dL). Xảy ra ở 50% đến 70% trẻ sơ sinh đủ tháng. Hầu hết các trường hợp là vàng da sinh lý.
Vàng da trong 24 giờ đầu đời được xem là bệnh lý
Điều trị tăng bilirubin máu nặng bao gồm chiếu đèn và/hoặc thay máu.
Biến chứng chính của tăng bilirubin tự do là vàng da nhân.
Thông tin cơ bản
Định nghĩa
Vàng da sơ sinh là tình trạng da và củng mạc mắt trẻ sơ sinh đổi màu vàng, do tăng nồng độ bilirubin trong máu. Trẻ sơ sinh là trẻ nhỏ trong 28 ngày đầu đời.
Chủ đề này tập trung vào việc nhận biết và điều trị vàng da sơ sinh sớm, phổ biến nhất là do tăng bilirubin gián tiếp. Mặc dù vàng da kéo dài với tăng bilirubin máu trực tiếp có thể gặp trong giai đoạn này, việc điều trị thích hợp tùy theo nguyên nhân gây bệnh và bình luận chi tiết nằm ngoài phạm vi tài liệu này.
Dịch tễ
Vàng da là tình trạng thường gặp nhất ở trẻ sơ sinh cần chăm sóc y tế. Khoảng 50% đến 70% trẻ sơ sinh đủ tháng và 80% trẻ sinh non xuất hiện vàng da trong tuần đầu sau sinh.[2] Vàng da thường xuất hiện 2 đến 4 ngày sau khi sinh và tự hết sau 1 đến 2 tuần mà không cần điều trị.
Tỷ lệ tăng bilirubin máu thay đổi. Một nghiên cứu ở Anh và Ireland cho thấy tỷ lệ tăng bilirubin máu nặng (bilirubin gián tiếp tối đa trong huyết thanh ≥510 micromol/L [29,8 mg/dL]) trên 7,1 trong 100.000.[3] Một nghiên cứu ở Đan Mạch cho thấy tỷ lệ tăng bilirubin máu quá mức (492 micromol/L [28,8 mg/dL]) trên 25 trong 100.000.[4] Ở Hoa Kỳ, tăng bilirubin máu nặng (bilirubin huyết thanh toàn phần > bách phân vị thứ 95) xảy ra ở 8% đến 9% trẻ sơ sinh trong tuần đầu tiên; khoảng 4% sau 72 giờ đầu đời.[5] Dữ liệu về tỷ lệ mắc ở các quốc gia có thu nhập thấp và trung bình thay đổi[6]. Tỷ lệ mắc của người Đông Á trong một nghiên cứu dựa trên dân số ở bang Washington của Hoa Kỳ cao hơn so với trẻ sơ sinh da trắng.[7] Trong các nghiên cứu ở Hoa Kỳ, nhóm dân số chủ yếu là người da trắng và nuôi con bằng sữa mẹ tại Michigan cho thấy mức bilirubin huyết thanh toàn phần có bách phân vị thứ 95 sau 96 giờ đầu đời là 224,1 micromol/L (13,1 mg/dL).[8] Trong các nghiên cứu từ Pennsylvania và Bắc California, bách phân vị thứ 95 là 299,3 (17,5 mg/dL).[1] Trong nhóm trẻ sơ sinh hỗn hợp từ Hoa Kỳ, Hồng Kông, Nhật Bản, và Israel, bách phân vị thứ 95 là 265,1 micromol/L (15,5 mg/dL).[10] Nguy cơ tăng bilirubin máu trẻ sơ sinh cao hơn ở nam giới và tăng dần khi tuổi thai giảm.
Nguyên nhân
Vàng da sinh lý có thể là do :
Tăng lượng bilirubin thứ phát do tăng thể tích hồng cầu (RBC), giảm tuổi thọ RBC, hoặc tăng tuần hoàn gan-ruột
Giảm hấp thụ ở gan vì giảm ligandin hoặc ligandin gắn với các anion khác
Giảm liên hợp trong gan vì giảm hoạt tính uridine diphosphoglucuronyl transferase (UDPGT). Đa hình thái gen UGT1A1 của promoter Gly71Arg và TATA, giảm hoạt tính enzym UDPGT, được ghi nhận là yếu tố nguy cơ đáng kể liên quan đến tình trạng tăng bilirubin máu ở trẻ sơ sinh[11]
Giảm bài tiết vào mật.
Vàng da bệnh lý với tăng bilirubin tự do trong máu có thể là do:
Thiếu máu huyết tán: điều này dẫn đến tình trạng tăng phá hủy RBC, kết quả là tăng hem, nó được chuyển thành bilirubin tự do quá mức; gan chưa trưởng thành nên không thể xử lý được lượng bilirubin tự do dư thừa này. Có thể là do bất đồng nhóm máu (Rh, ABO), khiếm khuyết enzym RBC (thiếu glucose-6-phosphate dehydrogenase; thiếu pyruvate kinase), khiếm khuyết màng RBC (ví dụ như bệnh hồng cầu hình cầu di truyền, bệnh hồng cầu có nhân đặc ở trẻ sơ sinh), thalassemia, do thuốc (bởi vitamin K, sulphonamide, nitrofurantoin, thuốc kháng sốt rét, penicillin), hoặc nhiễm trùng máu Thoát mạch: máu bị cô lập vào các khoang dẫn đến tăng lượng bilirubin . Ví dụ bao gồm tụ máu dưới da đầu; xuất huyết nội sọ, phổi, hoặc đường tiêu hóa; u máu lớn; vết bầm máu; hoặc chấm xuất huyết diện rộng
Đa hồng cầu: tăng số lượng RBC dẫn đến tăng sản xuất bilirubin
Tăng tuần hoàn gan-ruột: chậm vận chuyển qua đường tiêu hóa làm tăng nồng độ bilirubin. Ví dụ bao gồm chít/hẹp ruột, hẹp môn vị, hội chứng Hirschsprung, hội chứng tắc/bít phân su
Quá trình liên hợp bị khiếm khuyết: thiếu enzyme UDPGT bẩm sinh bao gồm hội chứng Crigler-Najjar; ức chế enzyme UDPGT có thể là do thuốc (ví dụ như novobiocin), hoặc hội chứng Lucey-Driscoll
Các tình trạng chuyển hóa (rối loạn chuyển hóa galactose, suy giáp, rối loạn chuyển hóa tyrosin, tăng methionin máu, mẹ bị đái tháo đường)
Bú sữa mẹ (kể cả không tiết sữa)
Giảm gắn bilirubin với albumin: lượng bilirubin tự do (không liên hợp) tăng vượt qua hàng rào máu-não. Điều này có thể do nhiều loại thuốc (sulphonamide, penicillin, gentamicin), nhiễm toan, ngạt, hạ thân nhiệt, tăng áp lực thẩm thấu tăng, hoặc hạ đường huyết gây ra.
Vàng da bệnh lý với tăng bilirubin liên hợp trong máu (bilirubin trực tiếp là >34,2 micromol/L (2,0 mg/dL)) có thể là do:
Bệnh tế bào gan:
Khiếm khuyết chuyển hóa hoặc gen. Ví dụ bao gồm thiếu alpha1-antitrypsin, xơ nang, hội chứng Zellweger, hội chứng Dubin-Johnson (không có protein 2 liên quan đến kháng đa thuốc ở màng tiểu quản của tế bào gan), hội chứng Rotor (không có polypeptide vận chuyển anion hữu cơ [OATP]1B1 và OATP1B3 ở màng xoang của tế bào gan), và rối loạn chuyển hóa galactose
Nhiễm trùng. Ví dụ bao gồm rubella, cytomegalovirus, herpes, giang mai, viêm gan A và B, toxoplasma, và nhiễm trùng đường tiết niệu với Escherichia coli
Nuôi dưỡng tĩnh mạch hoàn toàn [12]
Bệnh thừa sắt sơ sinh
Viêm gan sơ sinh vô căn
Sốc
Bệnh đường mật trong gan do hội chứng Alagille (loạn sản động mạch gan), hoặc hội chứng mật đặc
Bệnh đường mật ngoài gan do teo đường mật, nang ống mật chủ, hẹp ống mật, sỏi mật.
Sinh lý bệnh
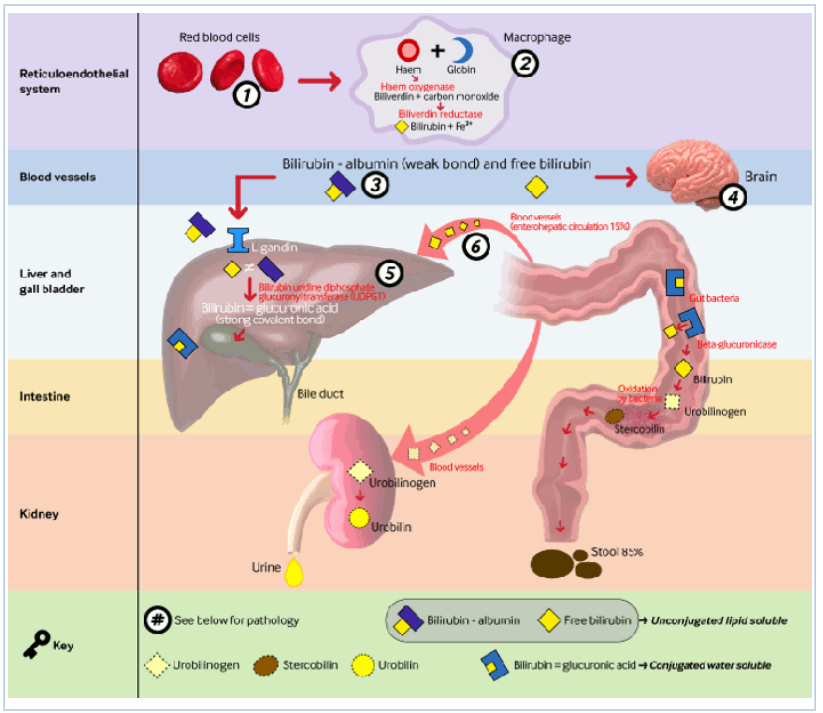
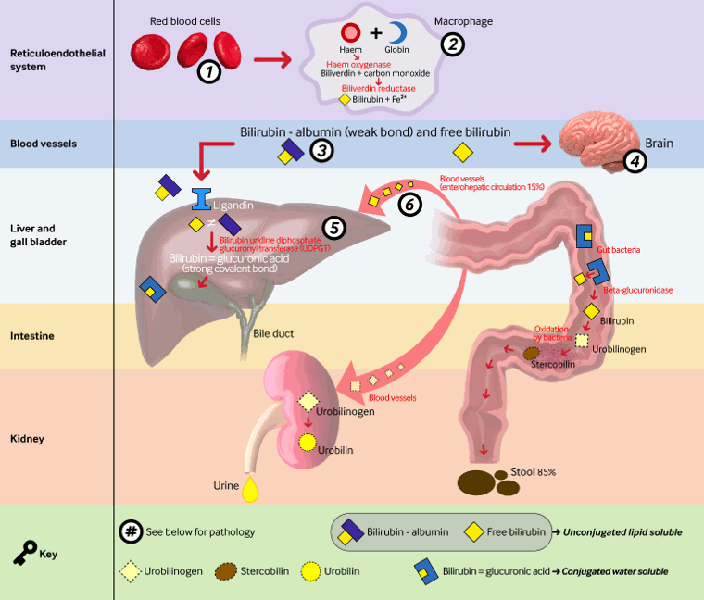
Bilirubin là sản phẩm cuối cùng của quá trình dị hóa hem, mà phần lớn có nguồn gốc từ hemoglobin. Phá vỡ hemoglobin hồng cầu dẫn đến sản xuất hem (75% nguồn bilirubin). Hem cũng có thể có nguồn gốc (25% nguồn bilirubin) từ việc phá vỡ các protein khác như myoglobin, cytochromes, và nitric oxide synthases. Trong hệ võng-nội mô, hem được dị hóa tiếp bởi hem oxygenase (bước hạn chế tốc độ sản xuất bilirubin) thành biliverdin. Quá trình này cần biliverdin reductase để tạo bilirubin. Sau đó bilirubin gắn với albumin huyết thanh trong huyết tương và được vận chuyển đến gan. Bilirubin phân ly khỏi albumin, và với sự trợ giúp của các protein mang như ligandin, được hấp thụ vào tế bào gan. Sau đó bilirubin được liên hợp nhờ uridine diphosphoglucuronyl transferase enzyme trong tế bào gan. Bilirubin glucuronide đến ruột thông qua túi mật và ống mật chủ. Trong ruột của trẻ sơ sinh, hầu hết bilirubin glucuronide không được liên hợp do beta glucuronidase. Một số bilirubin không liên hợp này được tái hấp thụ và tham gia tuần hoàn gan ruột. Lượng bilirubin liên hợp còn lại đến đại tràng, ở đó vi khuẩn phá hủy thành urobilinogen, sau đó được bài tiết theo phân. Khi quá trình hình thành và bài tiết bilirubin bình thường này bị gián đoạn, sẽ dẫn đến tình trạng tăng bilirubin máu.[13]
Con đường chuyển hóa bilirubin với các bệnh lý liên quan đến tăng bilirubin máu tự do. 1. Bất đồng nhóm máu ABO, bất đồng nhóm Rhesus, tuổi thọ RBC ngắn hơn ở trẻ sơ sinh, bầm tím trong khi sinh; 2. Do các chất trung gian gây viêm liên quan đến các bệnh đồng mắc do sinh non (ví dụ như hội chứng suy hô hấp, nhiễm trùng); 3. Phân ly tăng do nhiễm toan, nhiễm ceton, suy thận; 4. Hàng rào máu-não cho bilirubin gián tiếp thấm qua ở trẻ sơ sinh đủ tháng và trẻ sinh non; 5. Đột biến gen UGT1A1 dẫn đến hội chứng Gilbert hoặc hội chứng Crigler-Najjar I và II; 6. Lượng bilirubin gián tiếp tăng do giảm nhu động ruột
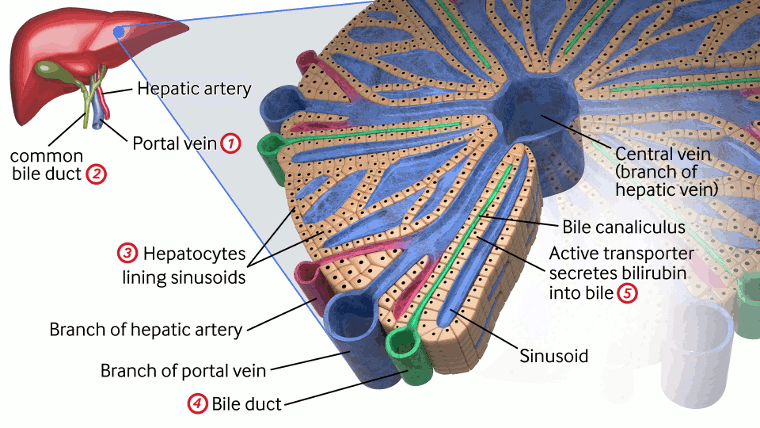
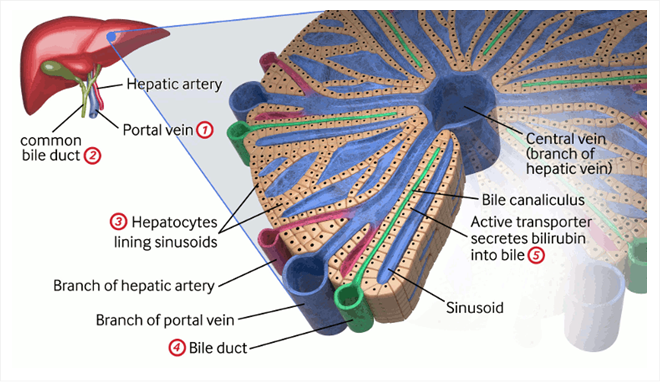
Chi tiết tiểu thùy gan và chức năng của nó, làm nổi bật các bệnh lý gây tăng bilirubin liên hợp trong máu. Các bệnh lý bao gồm: 1. Huyết khối tĩnh mạch cửa; 2. Nang ống mật chủ; 3. Nhiễm trùng (nhiễm trùng huyết, nhiễm trùng đường tiết niệu E coli, viêm gan A hoặc B, bệnh toxoplasma, cytomegalovirus, giang mai, herpes), chuyển hóa (hội chứng Rotor, rối loạn chuyển hóa galactose, rối loạn chuyển hóa tyrosin máu, thiếu alpha-1 antitrypsin, suy giáp, xơ nang, hội chứng Zellweger), thuốc, viêm gan sơ sinh vô căn, nuôi dưỡng tĩnh mạch hoàn toàn, bệnh thừa sắt sơ sinh, sốc/giảm oxy mô/thiếu máu cục bộ; 4. Thiểu sản đường mật, hẹp đường mật, hội chứng Alagille, ứ mật sơ sinh vô căn, ứ mật tiến triển trong gan có tính gia đình, hội chứng mật đặc; 5. Đột biến gen MRP2 (còn được biết đến là ABCC2) trên màng tiểu quản của tế bào gan dẫn đến hội chứng Dubin-Johnson, không có OATP1B1 và OATP1B3 ở màng xoang của tế bào gan dẫn đến hội chứng Rotor.
Phân loại
Vàng da sinh lý
Vàng da sinh lý thường được phát hiện vào ngày 2 sau sinh, cao điểm vào ngày 3 đến ngày 5, và sau đó giảm dần. Nồng độ bilirubin trong huyết thanh lên đến 205,2 micromol/L (12 mg/dL) được xem là sinh lý ở trẻ sơ sinh đủ tháng.
Vàng da bệnh lý
Bất kỳ trường hợp vàng da nào trong 24 giờ đầu đời đều được xem là bệnh lý. Nồng độ Bilirubin vượt quá bách phân vị thứ 95, được xác định bởi toán đồ, là bệnh lý.[1]
Dự phòng
Dự phòng sơ cấp
Cần khuyến nghị hỗ trợ thích hợp và tư vấn phụ nữ nuôi con bằng sữa mẹ, và tăng tần suất cho bú từ 8 đến 12 lần một ngày trong vài ngày đầu tiên.
Sàng lọc
Không có đủ bằng chứng ủng hộ việc tầm soát thường quy vàng da để phòng ngừa bệnh não do bilirubin mạn tính.[40]
[41] Tuy nhiên, tầm soát trẻ sơ sinh không có triệu chứng rất quan trọng để nhận biết sớm vàng da và/hoặc các dấu hiệu bệnh não do bilirubin để đánh giá nguyên nhân bệnh, theo dõi chặt chẽ nồng độ bilirubin huyết thanh, và can thiệp điều trị, nếu cần. Bởi vàng da chủ yếu xảy ra trong tuần đầu tiên của cuộc đời trẻ sơ sinh, đây là thời gian tốt nhất để tầm soát. Trước khi xuất viện, cần đánh giá tình trạng vàng da mỗi 8 đến 12 giờ một lần ở trẻ sơ sinh. Chỉ đánh giá vàng da bằng mắt thường được xem là không đáng tin cậy và sử dụng máy đo nồng độ bilirubin qua da cũng như bilirubin huyết thanh toàn phần là công cụ tầm soát thường được khuyết nghị.[42] [43] [44] [45]
Viện Nhi khoa Hoa Kỳ khuyến nghị tầm soát thường quy bilirubin trước khi xuất viện, sử dụng nồng độ bilirubin huyết thanh toàn phần (TSB) hoặc bilirubin qua da (TcB), khi phiên giải kết quả sử dụng vùng nguy cơ trong toán đồ đặc hiệu theo giờ, [Bhutani nomogram for designation of risk based on hour-specific serum bilirubin values] (http://pediatrics.aappublications.org/content/114/1/297#p-152) giúp đánh giá định lượng mức độ tăng bilirubin trong máu.[43] Kết hợp số đo TSB hoặc TcB trước khi xuất viện với các yếu tố nguy cơ lâm sàng được cho là cải thiện tính chính xác trong việc dự báo nguy cơ. Do đó gợi ý một cách tiếp cận điều trị và theo dõi có hệ thống bằng TSB/TcB trước khi xuất viện, tuổi thai, và các yếu tố nguy cơ khác đối với tình trạng tăng bilirubin máu. Khi có từ hai số đo TSB hoặc TcB liên tiếp, đánh dấu chúng trên toán đồ sẽ giúp ích trong việc đánh giá tốc độ tăng bilirubin. Nếu nồng độ TSB/TcB cắt ngang bách phân vị trên toán đồ, có khả năng là huyết tán và cần chỉ định thêm xét nghiệm và theo dõi.
Dự phòng thứ cấp
Tùy theo nguyên nhân bệnh, nếu mức bilirubin tự do cao (ví dụ như trong khiếm khuyết enzym liên hợp một phần), cần chiếu đèn từng đợt suốt đời để phòng ngừa thương tổn thần kinh. Cần tiếp tục điều trị đặc hiệu trong hầu hết ca bệnh do nguyên nhân chuyển hóa/gen/phẫu thuật để kiểm soát tình trạng tăng bilirubin máu liên hợp. Phòng ngừa suy dinh dưỡng và thiếu vitamin rất quan trọng để giúp thông đường mật và tránh chảy máu.
Chẩn đoán
Bệnh sử ca bệnh
Bệnh sử ca bệnh #1
Một bé trai được sinh ra khi tuổi thai khoảng 36 tuần bởi người mẹ mang thai lần đầu. Thai kỳ và quá trình sinh không có biến chứng với điểm Apgar là 9 ở 1 và 5 phút. Cả mẹ và em bé đều có nhóm máu O+. Người mẹ chọn nuôi con hoàn toàn bằng sữa mẹ. Lúc 24 giờ đầu đời, nhận thấy em bé bị vàng da và bilirubin toàn phần trong huyết thanh là 119,7 micromol/L (7 mg/dL). Bé được xuất viện về nhà vào cùng ngày với lịch hẹn khám theo dõi với bác sĩ nhi khoa lúc 1 tuần tuổi. Tuy nhiên, 48 giờ sau đó, em bé được đưa vào khoa cấp cứu. Khai thác bệnh sử từ người mẹ, thấy rằng em bé càng bị vàng da nhiều hơn, bú kém và ngủ gà. Khám cũng cho thấy bằng chứng thiếu dịch mức độ trung bình và vàng da đáng kể (cả lòng bàn chân). Khám thần kinh thì bình thường và bilirubin toàn phần trong huyết thanh là 342,1 micromol/L (20 mg/dL).
Bệnh sử ca bệnh #2
Một em bé đủ tháng được sinh ra bởi người mẹ đã có con trước đó có tiền sử vàng da trong giai đoạn sơ sinh, nhưng không cần nhập viện. Thai kỳ và quá trình sinh không có biến chứng với điểm Apgar là 8 và 9 lần lượt ở 1 và 5 phút. Mẹ và em bé lần lượt có nhóm máu O+ và B+. Lúc 12 giờ đầu đời, nhận thấy em bé bị vàng da và bilirubin toàn phần trong huyết thanh là 85,5 micromol/L (5 mg/dL). Xét nghiệm cho thấy test Coombs trực tiếp dương tính và có tế bào hồng cầu hình cầu nhỏ trên tiêu bản máu ngoại vi.
Các biểu hiện khác
Trẻ sơ sinh có thể có các dấu hiệu lâm sàng của bệnh não do bilirubin. Các dấu hiệu này bao gồm cáu kỉnh kèm theo khóc thét lên, có thể sốt và tăng trương lực cơ (thường ảnh hưởng đến nhóm cơ duỗi), và cổ và thân mình ưỡn cong ra sau thành từng đợt rất đặc trưng. Trương lực cơ giảm và phản xạ Moro bất thường là những biểu hiện có thể có.
Cách tiếp cận chẩn đoán từng bước
Vàng da thường được phát hiện bằng mắt thường bởi da và củng mạc mắt đổi màu vàng.[34] [35] [36] [37]Tuy nhiên, ược lượng mức độ vàng da bằng mắt thường có thể dẫn đến sai sót, nhất là ở trẻ sơ sinh có sắc tố da sẫm màu. Do đó, mỗi trẻ sơ sinh bị vàng da cần được đo nồng độ bilirubin qua da. Vàng da có tính chất sinh lý nếu xảy ra vào ngày thứ 2 sau sinh và hết trước một tuần đầu đời và số đo qua da bình thường. Tất cả trẻ sơ sinh bị vàng da trong 24 giờ đầu đời và những trẻ có số đo bilirubin qua da tăng sau 24 giờ đầu đời cần được đánh giá thêm.
Đánh giá vàng da bệnh lý
Nếu trẻ nhỏ hơn 24 giờ tuổi hoặc số đo bilirubin qua da là 205,2 micromol/L (12 mg/dL), cần định lượng bilirubin toàn phần huyết thanh. Nếu bilirubin toàn phần huyết thanh >205,2 micromol/L (12 mg/dL) hoặc > bách phân vị thứ 95 theo độ tuổi (tính bằng giờ) trên toán đồ, cần thực hiện test Coombs.[1] [Bhutani nomogram for designation of risk based on hour-specific serum bilirubin values] (http://pediatrics.aappublications.org/content/114/1/297#p-152). Nếu test Coombs dương tính, phải kiểm tra nhóm máu ABO và Rh của mẹ và trẻ sơ sinh. Nếu không có sự bất đồng (bất đồng xảy ra khi mẹ thuộc nhóm máu O và trẻ sơ sinh thuộc nhóm máu A hoặc B hoặc khi mẹ là Rhesus – và trẻ sơ sinh là Rhesus +), cần xem xét bất đồng kháng nguyên nhóm máu phụ. Nếu âm tính, phải kiểm tra bilirubin trực tiếp huyết thanh.
Bilirubin trực tiếp >34.2 micromol/L (2 mg/dL)
Nếu bilirubin trực tiếp >34,2 micromol/L (2 mg/dL), cần xem xét và xét nghiệm các nguyên nhân khác gây tăng bilirubin liên hợp trong máu như bệnh tế bào gan thứ phát do nhiễm trùng/nguyên nhân chuyển hóa hoặc gen và bệnh đường mật ngoài gan.[38] Các xét nghiệm bao gồm xét nghiệm chức năng gan, nuôi cấy máu, tìm các chất chuyển hóa carbohydrate trong nước tiểu, axit amin huyết tương, axit amin nước tiểu, nuôi cấy nước tiểu, siêu âm bụng, và sinh thiết gan qua da.
Bilirubin trực tiếp
Nếu bilirubin trực tiếp 65%, cần xác định bệnh tăng hồng cầu bằng mức hematocrit (với mẫu máu tĩnh mạch hoặc động mạch). Nếu hematocrit bình thường hoặc giảm, cần kiểm tra số lượng hồng cầu lưới và tiêu bản máu ngoại vi. Nếu số lượng hồng cầu lưới tăng, cần xem xét các nguyên nhân gây thiếu máu huyết tán (bất đồng nhóm máu, thiếu enzym hồng cầu). Các xét nghiệm bao gồm nhóm máu và tầm soát glucose-6-phosphate dehydrogenase. Nếu tiêu bản máu bất thường, cần xác định khiếm khuyết màng hồng cầu đặc hiệu bằng xét nghiệm sức bền hồng cầu.
Các yếu tố nguy cơ
Mạnh
Người châu Á
Nồng độ bilirubin cao hơn được ghi nhận ở trẻ sơ sinh gốc Á với nồng độ đỉnh xảy ra muộn nhất ở trẻ sơ sinh gốc Tây Ban Nha và vào các thời điểm trung gian ở các nhóm dân cư Châu Âu và Bắc Mỹ chủ yếu dân tộc/ chủng tộc da trắng. [14] [15] [16] Cơ chế có thể liên quan đến việc tăng sản xuất thứ phát do ảnh hưởng của gen.
Người Mỹ bản địa
Trẻ sơ sinh Mỹ bản địa có bilirubin toàn phần huyết thanh tối đa trung bình cao hơn, có thể là kết quả của việc tăng sản xuất thứ phát do ảnh hưởng của gen [17]
Mẹ bị đái tháo đường
Mẹ bị đái tháo đường làm tăng nguy cơ trẻ bị vàng da sơ sinh.[18] [19] [20] [21] Trẻ sơ sinh quá to có mẹ bị đái tháo đường phụ thuộc insulin có nồng độ erythropoietin cao và quá trình sinh hồng cầu tăng.[22] [23] Nồng độ beta-glucuronidase trong sữa của người mẹ bị đái tháo đường tăng gấp 3 lần.[22]
Cân nặng khi sinh thấp
Yếu tố nguy cơ vàng da sơ sinh.[27]
Tuổi thai giảm
Trẻ sơ sinh có tuổi thai nhỏ hơn có nhiều khả năng đạt mức bilirubin cần phải can thiệp hơn[28] [29]. Điều này có lẽ là thứ phát do sự chưa trưởng thành của các enzym tham gia vào chuyển hóa bilirubin
Giảm lượng calo nạp vào và sút cân
Trẻ sơ sinh sút cân nhiều và lượng calo nạp vào cơ thể ít có bilirubin toàn phần huyết thanh cao hơn đáng kể.[30] [31] [17] [9] Các cơ chế tiềm năng bao gồm khả năng thanh thải bilirubin của gan giảm, tăng hoạt tính của hem oxygenase, tăng nồng độ axit béo không este hóa ảnh hưởng đến việc gắn bilirubin trên màng tế bào gan, gắn cạnh tranh với ligandin và ức chế diphosphoglucuronyl transferase.
Nuôi con bằng sữa mẹ
Quan sát thấy tỷ lệ mắc vàng da gia tăng ở trẻ bú sữa mẹ.[27] [28] [14] Dạng khởi phát sớm có lẽ là thứ phát do chậm tiết sữa và bú kém, dẫn đến lượng calo nạp vào cơ thể giảm và mất nước, dẫn đến nồng độ bilirubin huyết thanh toàn phần cao hơn. Dạng khởi phát muộn được cho là do tăng tuần hoàn gan ruột của bilirubin. Các yếu tố khác trong sữa mẹ có liên quan, bao gồm 3-alpha 20-beta pregnanediol, axit béo tự do không ester hóa (ức chế glucuronyl transferase gan), lipoprotein lipase, và hoạt tính beta-glucuronidase.
Yếu
Oxytocin khi chuyển dạ
Tỷ lệ vàng da sơ sinh gia tăng ở trẻ sơ sinh có mẹ nhận oxytocin đã được báo cáo.[24] [25] Điều này là vì tan máu thứ phát do giảm sức bền hồng cầu.[26]
Chậm kẹp dây rốn (2-3 phút)
Có sự gia tăng đáng kể số trẻ cần chiếu đèn để điều trị vàng da ở nhóm kẹp dây rốn muộn so với kẹp dây rốn sớm.[32]
Các yếu tố về gen
Một nghiên cứu bệnh-chứng được thực hiện ở Đông Nam Trung Quốc (tỉnh Phúc Kiến) báo cáo rằng đột biến G211 ở gen UGT1A1, bất đồng nhóm máu ABO, thiếu G6PD , và sự lặp lại kiểu gen SS ở vùng promoter của gen HO-1 là các yếu tố nguy cơ của tình trạng tăng bilirubin máu ở trẻ sơ sinh.[33]
Các yếu tố bệnh sử & thăm khám
Các yếu tố chẩn đoán chính
Có các yếu tố nguy cơ (thường gặp)
Các yếu tố nguy cơ chính bao gồm gốc Châu Á, mẹ bị đái tháo đường, cân nặng khi sinh thấp, tuổi thai giảm, giảm lượng calo nạp vào và sút cân, và bú sữa mẹ.
Tiến triển từ đầu đến chân (thường gặp)
Đầu tiên xuất hiện ở mặt, tiến triển theo hướng từ đầu đến chân khi bilirubin toàn phần huyết thanh tăng.
Tuổi thai giảm (thường gặp)
Nguy cơ vàng da tăng khi tuổi thai giảm
Nam giới (thường gặp)
Vàng da sơ sinh thường gặp hơn ở nam giới.
Tiền sử gia đình bị vàng da (không thường gặp)
Tiền sử vàng da ở anh chị em ruột trước đó gợi ý bất đồng nhóm máu, vàng da do sữa mẹ, hoặc thiếu glucose-6- phosphate dehydrogenase.
Tiền sử gia đình bị thiếu máu (không thường gặp)
Ở bệnh nhân bị thiếu máu huyết tán di truyền (bệnh hồng cầu hình cầu di truyền, bệnh hồng cầu hình bầu dục di truyền, thiếu glucose-6-phosphate dehydrogenase, thiếu pyruvate kinase, thiếu máu tế bào hình liềm, thalassemia), các đặc điểm lâm sàng bao gồm vàng da sơ sinh, sỏi mật, và thiếu máu. Trong một số trường hợp, cắt lách là một lựa chọn điều trị (ví dụ như với bệnh thiếu máu hồng cầu hình liềm). Do đó, nếu có tiền sử gia đình bị thiếu máu và/hoặc cắt lách, cần nghi ngờ các tình trạng chuyển hóa/gen.
Tiền sử gia đình cắt lách (không thường gặp)
Ở bệnh nhân bị thiếu máu huyết tán di truyền (bệnh hồng cầu hình cầu di truyền, bệnh hồng cầu hình bầu dục di truyền, thiếu glucose-6-phosphate dehydrogenase, thiếu pyruvate kinase, thiếu máu tế bào hình liềm, thalassemia), các đặc điểm lâm sàng bao gồm vàng da sơ sinh, sỏi mật, và thiếu máu. Trong một số trường hợp, cắt lách là lựa chọn điều trị (ví dụ như với bệnh thiếu máu hồng cầu hình liềm). Do đó, nếu có tiền sử gia đình bị thiếu máu và/hoặc cắt lách, cần nghi ngờ các tình trạng chuyển hóa/gen.
Mẹ phơi nhiễm với sulphonamides hoặc thuốc chống sốt rét (không thường gặp)
Điều này dẫn đến tình trạng tăng phá hủy hồng cầu và tăng sản xuất hem, nó được chuyển thành bilirubin tự do quá mức; gan chưa trưởng thành nên không thể xử lý được lượng bilirubin tự do dư thừa này
Gan lách to (không thường gặp)
Gợi ý bệnh tế bào gan
Tật đầu nhỏ (không thường gặp)
Gợi ý nhiễm trùng bẩm sinh
Viêm màng mạch võng mạc (không thường gặp)
Gợi ý nhiễm trùng bẩm sinh
Nhỏ so với tuổi thai (không thường gặp)
Gợi ý nhiễm trùng bẩm sinh
Tụ máu dưới da đầu (không thường gặp)
Thoát mạch hồng cầu.
Tăng trương lực cơ (không thường gặp)
Dấu hiệu muộn của bệnh não do bilirubin.
Khóc thét (không thường gặp)
Dấu hiệu muộn của bệnh não do bilirubin.
Cổ ưỡn cong ra sau (không thường gặp)
Dấu hiệu muộn của bệnh não do bilirubin
Lưng ưỡn cong ra sau (không thường gặp)
Dấu hiệu muộn của bệnh não do bilirubin.
Các yếu tố chẩn đoán khác
Ngạt chu sinh (không thường gặp)
Có thể làm giảm gắn bilirubin với albumin và tăng lượng bilirubin tự do (không liên hợp) qua hàng rào máu-não.
Thai to (không thường gặp)
Gợi ý mẹ bị đái tháo đường, tăng nguy cơ.
Đa huyết (không thường gặp)
Gợi ý bệnh đa hồng cầu
Giảm trương lực cơ (không thường gặp)
Dấu hiệu sớm của bệnh não do bilirubin.
Ngủ gà (không thường gặp)
Dấu hiệu sớm của bệnh não do bilirubin.
Xét nghiệm chẩn đoán
Xét nghiệm hàng đầu cần chỉ định
|
Xét nghiệm |
Kết quả |
|
Chỉ số bilirubin qua da Xét nghiệm sàng lọc. Cần xác định bằng thông số bilirubin toàn phần huyết thanh nếu giá trị số đo qua da >205,2 micromol/L (12 mg/dL). |
sinh lý or tăng cao |
|
Bilirubin toàn phần huyết thanh Xét nghiệm tốt nhất để xác định chẩn đoán. Lấy máu và tránh nguồn sáng mạnh; gửi đến phòng xét nghiệm để xử lý càng sớm càng tốt. Giá trị cụ thể trên toán đồ đặc hiệu theo tuổi (giờ). Bilirubin toàn phần >205,2 micromol/L (12 mg/dL) cần xét nghiệm thêm. |
tăng |
|
Xét nghiệm Coombs trực tiếp Chẩn đoán đồng miễn dịch ABO hoặc Rh. |
dương tính hoặc âm tính |
|
Bilirubin trực tiếp huyết thanh Thành phần trực tiếp >34,2 micromol/L (2 mg/dL) cần xét nghiệm tập trung vào tình trạng vàng da do tăng bilirubin liên hợp. Bilirubin gián tiếp là phần không liên hợp, từ việc trừ đi giá trị bilirubin trực tiếp từ bilirubin toàn phần huyết thanh. |
tăng hoặc giảm |
|
Hematocrit Thường chỉ cần mẫu mao mạch là đủ. Cần mẫu máu (tĩnh mạch hoặc động mạch) trung tâm để xác định bệnh đa hồng cầu. |
thiếu máu tan máu nếu 65% |
|
Công thức máu toàn phần Số lượng bạch cầu cao hay thấp có thể gợi ý nhiễm trùng huyết. Giảm tiểu cầu có thể gợi ý nhiễm trùng huyết. |
số lượng bạch cầu hoặc tiểu cầu cao hoặc thấp |
|
Số lượng hồng cầu lưới Số lượng tăng gợi ý tan máu. |
bình thường hoặc tăng |
|
Tiêu bản máu ngoại vị Bằng chứng huyết tán. Có thể hỗ trợ chẩn đoán bệnh hồng cầu hình cầu di truyền. |
hình dạng/kích thước hồng cầu bình thường hoặc bất thường |
|
Nhóm máu Nếu mẹ có nhóm máu O và trẻ sơ sinh có nhóm máu A hoặc B, gợi ý bất đồng ABO. Mẹ có Rh âm tính với trẻ sơ sinh có Rh dương tính gợi ý bất đồng Rh |
tình trạng ABO và Rh |
Các xét nghiệm khác có thể cân nhắc
|
Xét nghiệm |
Kết quả |
|
Sàng lọc glucose-6-phosphate dehydrogenase Nên thực hiện sau vài tuần để tránh âm tính giả, vì mức enzym cao hơn ởRBC non trong tuần hoàn. |
Mức enzym bình thường hoặc giảm |
|
Xét nghiệm sức bền hồng cầu Dương tính trong bệnh hồng cầu hình cầu di truyền |
Dương tính hoặc âm tính |
|
Nuôi cấy máu Dương tính trong nhiễm trùng huyết |
Dương tính hoặc âm tính |
|
Xét nghiệm chức năng gan Mức albumin giảm có thể giúp đánh giá khả năng gắn bilirubin và nguy cơ nhiễm độc bilirubin. Men gan có thể tăng trong nhiễm trùng bẩm sinh. |
Bình thường, tăng hoặc giảm |
|
Tìm các chất chuyển hóa carbohydrat trong nước tiểu Xuất hiện trong rối loạn chuyển hóa galactose máu, nếu trẻ sơ sinh đang ăn đồ ăn có chứa galactose. |
Có hoặc không có |
|
Axít amin huyết tương Bất thường trong rối loạn chuyển hóa bẩm sinh đặc hiệu |
Bình thường hoặc tăng |
|
Axít hữu cơ nước tiểu Bất thường trong rối loạn chuyển hóa bẩm sinh đặc hiệu |
Bình thường hoặc tăng |
|
Nuôi cấy nước tiểu Dương tính trong nhiễm trùng đường tiết niệu. |
Dương tính hoặc âm tính |
|
Siêu âm bụng Bất thường trong các ca bệnh tế bào gan đặc hiệu hoặc các nguyên nhân tắc nghẽn gây vàng da liên hợp.[39] |
Bình thường hoặc bất thường |
|
Sinh thiết gan qua da Bất thường trong thiểu sản đường mật trong gan, rối loạn chuyển hóa và dự trữ, nhiễm trùng.[39] |
Bình thường hoặc bất thường |
Chẩn đoán phân biệt
|
Tình trạng |
Các dấu hiệu/triệu chứng giúp chẩn đoán phân biệt |
Các xét nghiệm giúp chẩn đoán phân biệt |
|
Caroten huyết |
Màu vàng chủ yếu thấy ở lòng bàn tay và lòng bàn chân nhưng không thấy ở củng mạc mắt và niêm mạc.[Fig-3] |
Nồng độ bilirubin toàn phần huyết thanh sẽ bình thường. Nồng độ carotene huyết thanh tăng |
Điều trị
Các khuyến cáo
Mục tiêu điều trị chính tình trạng tăng bilirubin huyết không liên hợp là phòng ngừa nhiễm độc bilirubin,đặc biệt là bệnh não do bilirubin và vàng da nhân.[34] [35] [36] [37] Toán đồ Bhutani giúp đánh giá nguy cơ dựa trên nồng độ bilirubin. [Bhutani nomogram for designation of risk based on hour-specific serum bilirubin values] (http://pediatrics.aappublications.org/content/114/1/297#p-152) [Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’ gestation] (http:// pediatrics.aappublications.org/content/114/1/297#xref- fig-3-1) [Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-4-1)
Tăng bilirubin không liên hợp
Chiếu đèn
Trẻ sơ sinh có nồng độ bilirubin toàn phần huyết thanh > bách phân vị thứ 95 trên toán đồ đặc hiệu theo giờ được điều trị chiếu đèn để làm giảm mức bilirubin. [Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’ gestation] (http:// pediatrics.aappublications.org/content/114/1/297#xref-fig-3-1) Có thể bắt đầu chiếu đèn ở những trẻ sơ sinh này nếu đánh giá lâm sàng gợi ý rằng bilirubin dự kiến tăng cao.
Chiếu đèn sử dụng năng lượng ánh sáng gây phản ứng quang hóa để biến đổi bilirubin thành các đồng phân ít ái tính với lipid và dễ dàng bài xuất hơn, phá vỡ các sản phẩm không cần thiết cho quá trình liên hợp trong gan. Bước sóng chiếu đèn hiệu quả nhất từ 425 nm đến 490 nm.[47]
Chiếu đèn với ánh sáng đôi thường được cho là có hiệu quả hơn chiếu đèn ánh sáng đơn hoặc sợi quang.[48][49] [50] Chiếu đèn sợi quang và diode phát sáng (LED) là biện pháp thay thế cho chiếu đèn thông thường ở trẻ sơ sinh đủ tháng.[51] [52] [53]Chiếu đèn LED có hiệu quả tương đương chiếu đèn thông thường,[54] và chiếu sáng từ trên xuống (so với chiếu sáng từ bên dưới trẻ ) rút ngắn thời gian chiếu đèn trung bình và tăng tốc độ giảm bilirubin toàn phần huyết thanh (TSB). [55] [56] [53]
Chiếu đèn huỳnh quang ánh sáng xanh đặc biệt không tốt hơn chiếu đèn tuýp dài tiêu chuẩn ánh sáng xanh đặc biệt về tính hiệu quả và tác dụng bất lợi trên trẻ sơ sinh cũng như ảnh hưởng đến nhân viên y tế.[57]
Dữ liệu nguy cơ/lợi ích tuyệt vời, với khởi phát tác dụng ngay khi bật đèn. Tác dụng bất lợi thường nhẹ và bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Có thể phòng ngừa những tác dụng phụ này bằng cách duy trì bổ sung nước đầy đủ và đảm bảo sử dụng kính che mắt cho em bé trong khi chiếu đèn
Hai nghiên cứu hồi cứu lớn cho thấy mối liên quan giữa đèn chiếu ở trẻ sơ sinh và động kinh ở trẻ em, nhưng không phải co giật do sốt. [58] [59]Trong cả hai nghiên cứu, tác động này chỉ xảy ra ở bé trai. Mặc dù sự khác biệt về giới tính có thể là do sự gia tăng tính nhạy cảm của trẻ sơ sinh nam với tổn thương chu sinh, nhưng chiếu đèn làm tăng nguy cơ co giật ở trẻ em như thế nào thì vẫn chưa rõ. Những dữ liệu này bị hạn chế vì một số lý do, bao gồm thiếu thông tin về liều lượng hoặc loại đèn chiếu được dùng và phụ thuộc vào Phân loại mã bệnh quốc tế (ICD) -9 cho một số dữ liệu hiệp biến. Tuy nhiên, có thể cần thận trọng hơn khi bắt đầu chiếu đèn ở các giá trị ngưỡng (nghĩa là tránh điều trị dự phòng) và ngừng chiếu đèn khi bilirubin huyết thanh giảm xuống dưới các mức này.
Một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng chiếu đèn tích cực không ảnh hưởng đến kết cục suy giảm phát triển thần kinh hay tử vong ở trẻ có cân nặng khi sinh cực thấp (ELBW) (cân nặng khi sinh .[60]
Tuy nhiên, một tổng quan hệ thống 9 nghiên cứu cho thấy rằng chiếu đèn dự phòng có thể làm giảm tình trạng suy giảm phát triển thần kinh lâu dài.[61] Trong khi đó chiếu đèn tích cực chỉ giúp làm giảm tỷ lệ suy giảm phát triển thần kinh, nhưng làm tăng tỷ lệ tử vong ở trẻ có cân nặng khi sinh từ 500 g đến 750 g.[60] Vì vậy, không khuyến nghị phương pháp chiếu đèn tích cực cho trẻ có cân nặng khi cực thấp.
Bù dịch
Có thể tiếp tục cho trẻ bú sữa mẹ/bú bình trong hầu hết các trường hợp trong khi chiếuđèn
Thay máu
Quyết định thay máu được đưa ra có tham khảo toán đồ Bhutani về thay máu. [Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/content/114/1/297#xref-fig-4-1)
Chỉ định thay máu ngay lập tức nếu:
Có các dấu hiệu lâm sàng như tăng trương lực cơ, người cong ra sau, cổ ưỡn cong ra sau, lưng cong ra sau, sốt, hoặc khóc thét, cho dù TSB đang giảm.
TSB ≥ 5 mg/dL trên các đường biểu diễn trong toán đồ Bhutani về thay máu.
Nguy cơ bệnh não bilirubin cấp tính được cho là cao nếu:
Giá trị Bilirubin đạt đến mức 428 micromol/L (25 mg/dL)
Mức bilirubin thấp hơn kèm theo các yếu tố nguy cơ khác, bao gồm bệnh huyết tán đồng miễn dịch, thiếu glucose-6-phosphate dehydrogenase, thân nhiệt không ổn định, li bì, ngạt chu sinh, nhiễm trùng huyết, và nhiễm toan
Vàng da kháng trị với chiếu đèn (ví dụ : bilirubin không giảm sau 4 đến 6 giờ kể từ khi chiếu đèn).
Điều trị hỗ trợ bao gồm bù dịch khi giá trị bilirubin ở bách phân vị thứ 95 trong toán đồ đặc hiệu theo giờ.[62] Có thể xem xét truyền Albumin trước khi thay máu[63] mặc dù hiệu quả của các can thiệp này không cho thấy có tác dụng nhất quán.[64] [65]
Cần tiếp tục chiếu đèn trong khi chuẩn bị thay máu và tiếp tục sau thủ thuật nếu cần trong khi đánh dấuthông số TSB trên toán đồ tương ứng để đánh giá nhu cầu tiếp tục chiếu đèn hoặc thay máu lặp lại.
Globulin miễn dịch đường tĩnh mạch (IVIG)
Sử dụng IVIG trong trường hợp tăng bilirubin huyết sơ sinh không liên hợp thứ phát do bệnh huyết tán còn nhiều tranh cãi. IVIG cho thấy giảm đáng kể nhu cầu thay máu,[66] nhưng không có dữ liệu rõ ràng chứng minh tính hiệu quả của nó.[67]Lý do dẫn đến khác biệt này vẫn chưa giải thích được. Hướng dẫn của Viện Nhi khoa Hoa Kỳ năm 2004 khuyến nghị dùng IVIG trong bệnh huyết tán đồng miễn dịch nếu TSB đang tăng mặc dù đã chiếu đèn tích cực hoặc mức TSB trong khoảng 34-51 micromol/L (2-3 mg/dL) của mức thay máu. Tổng quan Cochrane năm 2018 , 9 nghiên cứu với 658 trẻ sơ sinh đủ tháng và sinh non bất đồng Rh hoặc ABO (hoặc cả hai) kết luận rằng cần nghiên cứu thêm trước khi có thể khuyến nghị sử dụng IVIG để điều trị bệnh huyết tán đồng miễn dịch ở trẻ sơ sinh.[68]
Tăng bilirubin huyết liên hợp
Điều trị tăng bilirubin huyết liên hợp phụ thuộc vào nguyên nhân bệnh. Chống chỉ định chiếu đèn ở những bệnh nhân này vì có thể dẫn đến hội chứng ‘trẻ có da màu nâu đồng’. Không chỉ định truyền máu đơn thuần hoặc thay máu. Có thể cần hội chẩn với bác sĩ chuyên khoa thích hợp để điều trị thêm, tùy theo nguyên nhân bệnh.
Vàng da sinh lý
Không cần điều trị
Do sữa mẹ
Nếu trẻ sơ sinh bị vàng da do sữa mẹ, có thể xem xét ngừng bú sữa mẹ trong 24-48 giờ và cho ăn bổ sung nếu mức bilirubin huyết thanh cần chiếu đèn, có thể làm giảm mức bilirubin.
Tổng quan về các chi tiết điều trị
Lưu ý rằng công thức/đường dùng và liều lượng có thể khác nhau giữa các tên và nhãn hiệu thuốc, chế phẩm thuốc hoặc vị trí địa lý. Các khuyến cáo điều trị dành riêng cho các nhóm bệnh nhân see disclaimer
|
Cấp tính |
|
( tóm tắt ) |
|
Tăng bilirubin máu sinh lý |
||
|
|
1 |
Trấn an và theo dõi |
|
Tăng bilirubin máu bệnh lý: không liên hợp |
||
|
Bệnh não bilirubin cấp tính |
1 |
Thay máu ngay lập tức |
|
thêm |
Chiếu đèn |
|
|
thêm |
Bù dịch |
|
|
bổ sung |
Globulin miễn dịch đường tĩnh mạch (IVIG) |
|
|
Mức bilirubin toàn phần > bách phân vị thứ 95 trên toán đồ đặc hiệu theo giờ để chiếu đèn |
1 |
Chiếu đèn |
|
thêm |
Bù dịch |
|
|
Mức bilirubin toàn phần > bách phân vị thứ 95 trên toán đồ đặc hiệu theo giờ để thay máu |
1 |
Thay máu |
|
thêm |
Chiếu đèn |
|
|
thêm |
Bù dịch |
|
|
bổ sung |
Globulin miễn dịch đường tĩnh mạch (IVIG) |
|
|
Tăng bilirubin máu bệnh lý: liên hợp |
||
|
|
1 |
Điều trị nguyên nhân nền |
|
Vàng da do sữa mẹ |
||
|
|
1 |
Tạm thời ngừng bú mẹ + cho ăn bổ sung |
|
2 |
Chiếu đèn |
|
|
thêm |
Bù dịch |
|
|
3 |
Thay máu |
|
Các lựa chọn điều trị
Lưu ý rằng công thức/đường dùng và liều lượng có thể khác nhau giữa các tên và nhãn hiệu thuốc, chế phẩm thuốc hoặc vị trí địa lý. Các khuyến cáo điều trị dành riêng cho các nhóm bệnh nhân see disclaimer
|
Cấp tính |
|
|
|
Tăng bilirubin máu sinh lý |
|
|
|
|
1 |
Trấn an và theo dõi Vàng da là sinh lý nếu xảy ra vào ngày thứ hai sau sinh và hết trong vòng 7-10 ngày và số đo qua da bình thường. Không cần điều trị |
|
Tăng bilirubin máu bệnh lý: không liên hợp |
|
|
|
Bệnh não bilirubin cấp tính |
1 |
Thay máu ngay lập tức Các dấu hiệu bệnh não cấp tính do bilirubin bao gồm tăng trương lực cơ, người cong ra sau, cổ ưỡn cong ra sau, lưng ưỡn cong ra sau, sốt, hoặc khóc thét, cho dù TSB đang giảm Đây là một cấp cứu nội khoa Bắt đầu ngay khi có thể chuẩn bị được máu để thay máu. Cơ sở của phương pháp là loại bỏ bilirubin không liên hợp bằng cách thay máu gấp đôi thể tích, cho phép loại bỏ bilirubin ra khỏi mô não và do đó giảm nguy cơ nhiễm độc thần kinh. Thay máu cũng sẽ loại bỏ các kháng thể gây thiếu máu huyết tán. Trong các trường hợp tăng nguyên hồng cầu nặng và/hoặc phù thai, thủ thuật này cũng sẽ điều chỉnh tình trạng thiếu máu. Không có đủ bằng chứng ủng hộ hay bác bỏ việc thay máu cùng thể tích trái ngược với thay máu gấp đôi thể tích ở trẻ sơ sinh bị vàng da.[70] Các biến chứng chính có thể xảy ra từ thủ thuật này bao gồm rối loạn điện giải, chảy máu, nhiễm trùng, rối loạn nhịp tim, huyết khối với thuyên tắc mạch, viêm ruột hoại tử, và bệnh lý mảnh ghép chống lại vật chủ. |
|
|
thêm
|
Chiếu đèn Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn. Bắt đầu chiếu đèn trong khi chuẩn bị thay máu và tiếp tục chiếu đèn sau khi thay máu. Tiếp tục đánh dấu mức bilirubin toàn phần huyết thanh theo tuổi thai và số giờ sau khi sinh trên toán đồ để đánh giá nhu cầu tiếp tục chiếu đèn hoặc thay máu lặp lại. [Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-3-1) [Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-4-1) Các yếu tố nguy cơ bao gồm bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt chu sinh, li bì, thân nhiệt không ổn định, nhiễm trùng huyết, nhiễm toan, và albumin Chiếu đèn sử dụng năng lượng ánh sáng gây phản ứng quang hóa để biến đổi bilirubin thành các đồng phân ít ái tính với lipid và dễ dàng bài xuất hơn, phá vỡ các sản phẩm không cần thiết cho quá trình liên hợp trong gan. Bước sóng chiếu đèn hiệu quả nhất từ 425 nm đến 490 nm.[47] Như là một liệu pháp đầu tay, chiếu đèn ánh sáng đôi thường được cho là có hiệu quả hơn chiếu đèn ánh sáng đơn hoặc sợi quang.[53] Chiếu đèn sợi quang và diode phát sáng (LED) là biện pháp thay thế hàng thứ 2 cho chiếu đèn thông thường ở trẻ sơ sinh đủ tháng.[51] [52] [53]Chiếu đèn LED như là biện pháp thay thế hàng thứ 2 khác vì có hiệu quả tương đương chiếu đèn thông thường,[54] và chiếu sáng từ trên xuống (so với chiếu sáng từ bên dưới trẻ) rút ngắn thời gian chiếu đèn trung bình và tăng tốc độ giảm bilirubin toàn phần huyết thanh (TSB). [55] [53] Chiếu đèn huỳnh quang ánh sáng xanh đặc biệt không tốt hơn chiếu đèn tuýp dài tiêu chuẩn ánh sáng xanh đặc biệt về tính hiệu quả và tác dụng bất lợi trên trẻ sơ sinh cũng như ảnh hưởng đến nhân viên y tế. [57] Dữ liệu nguy cơ/lợi ích tuyệt vời, với khởi phát tác dụng ngay khi bật đèn. Tác dụng bất lợi thường nhẹ và bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Có thể phòng ngừa những tác dụng phụ này bằng cách duy trì bổ sung nước đầy đủ và đảm bảo sử dụng kính che mắt cho em bé trong khi chiếu đèn Có thể tiếp tục cho trẻ bú sữa mẹ/bú bình ở hầu hết các trường hợp trong khi chiếu đèn Một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng chiếu đèn tích cực không ản hưởng đến kết cục suy giảm phát triển thần kinh hay tử vong ở trẻ có cân nặng khi sinh cực thấp (ELBW) (cân nặng khi sinh [60] Tuy nhiên, một tổng quan hệ thống 9 nghiên cứu cho thấy rằng chiếu đèn dự phòng có thể làm giảm tình trạng suy giảm phát triển thần kinh lâu dài. [61] Trong khi đó chiếu đèn tích cực chỉ giúp làm giảm tỷ lệ suy giảm phát triển thần kinh, nhưng làm tăng tỷ lệ tử vong ở trẻ có cân nặng khi sinh từ 500 g đến 750 g. [60]Vì vậy, không khuyến nghị phương pháp chiếu đèn tích cực cho trẻ có cân nặng khi cực thấp Có thể cần thận trọng hơn khi bắt đầu chiếu đèn ở các giá trị ngưỡng (nghĩa là tránh điều trị dự phòng) và ngừng chiếu đèn khi bilirubin huyết thanh giảm xuống dưới các mức này vì mối liên quan giữa đèn chiếu ở trẻ sơ sinh và tăng nguy cơ mắc bệnh động kinh ở trẻ em (không phải co giật do sốt), đặc biệt ở bé trai.[58] [59]
|
|
|
thêm |
Bù dịch Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn Bù dịch đường tĩnh mạch thường được dành cho trẻ sơ sinh đang chiếu đèn có mức bilirubin gần với giá trị cần thay máu. Bổ sung dịch đường tĩnh mạch như vậy có thể làm giảm nồng độ bilirubin nhanh hơn.[71] Mặt khác, tiếp tục bù dịch với sữa mẹ hoặc sữa công thức đường miệng. |
|
|
bổ sung |
Globulin miễn dịch đường tĩnh mạch (IVIG) Điều trị được khuyến cáo cho MỘT SỐ bệnh nhân trong nhóm bệnh nhân được chọn Primary options globulin miễn dịch người bình thường: 0,5 đến 1 g/kg truyền tĩnh mạch trong 2 giờ; lặp lại trong 12 giờ nếu cần Ở trẻ nhũ nhi mắc bệnh huyết tán đồng miễn dịch, có thể bắt đầu điều trị IVIG nếu bilirubin toàn phần huyết thanh đang tăng mặc dù đang chiếu đèn tích cực hoặc mức bilirubin toàn phần huyết thanh trong phạm vi từ 34 đến 51 micromol/L (2-3 mg/dL) của mức thay máu.[68] |
|
Bilirubin toàn phần > bách phân vị thứ 95 trên toán đồ đặc hiệu theo giờ để chiếu đèn |
1 |
Chiếu đèn Mức ngưỡng phụ thuộc vào tuổi thai, tình trạng sức khỏe, và sự hiện diện của các yếu tố nguy cơ khác. [Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-3-1) Các yếu tố nguy cơ bao gồm bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt chu sinh, li bì, thân nhiệt không ổn định, nhiễm trùng huyết, nhiễm toan, và albumin Chiếu đèn sử dụng năng lượng ánh sáng gây phản ứng quang hóa để biến đổi bilirubin thành các đồng phân ít ái tính với lipid và dễ dàng bài xuất hơn, phá vỡ các sản phẩm không cần thiết cho quá trình liên hợp trong gan. Bước sóng chiếu đèn hiệu quả nhất từ 425 nm đến 490 nm.[47] Như là một liệu pháp đầu tay, chiếu đèn ánh sáng đôi thường được cho là có hiệu quả hơn chiếu đèn ánh sáng đơn hoặc sợi quang.[53] Chiếu đèn sợi quang và diode phát sáng (LED) là biện pháp thay thế hàng thứ 2 cho chiếu đèn thông thường ở trẻ sơ sinh đủ tháng.[51] [52] [53]Chiếu đèn LED như là biện pháp thay thế hàng thứ 2 khác vì có hiệu quả tương đương chiếu đèn thông thường,[54] và chiếu sáng từ trên xuống (so với chiếu sáng từ bên dưới trẻ) rút ngắn thời gian chiếu đèn trung bình và tăng tốc độ giảm bilirubin toàn phần huyết thanh (TSB). [55] [53] Chiếu đèn huỳnh quang ánh sáng xanh đặc biệt không tốt hơn chiếu đèn tuýp dài tiêu chuẩn ánh sáng xanh đặc biệt về tính hiệu quả và tác dụng bất lợi trên trẻ sơ sinh cũng như ảnh hưởng đến nhân viên y tế. [57] Dữ liệu nguy cơ/lợi ích tuyệt vời, với khởi phát tác dụng ngay khi bật đèn. Tác dụng bất lợi thường nhẹ và bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Có thể phòng ngừa những tác dụng phụ này bằng cách duy trì bổ sung nước đầy đủ và đảm bảo sử dụng kính che mắt cho em bé trong khi chiếu đèn. Có thể tiếp tục cho trẻ bú sữa mẹ/bú bình ở hầu hết các trường hợp trong khi chiếu đèn. Một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng chiếu đèn tích cực không ảnh hưởng đến kết cục suy giảm phát triển thần kinh hay tử vong ở trẻ có cân nặng khi sinh cực thấp (ELBW) (cân nặng khi sinh Trong khi đó chiếu đèn tích cực chỉ giúp làm giảm tỷ lệ suy giảm phát triển thần kinh, nhưng làm tăng tỷ lệ tử vong ở trẻ có cân nặng khi sinh từ 500 g đến 750 g. [60]Vì vậy, không khuyến nghị phương pháp chiếu đèn tích cực cho trẻ có cân nặng khi cực thấp. Có thể cần thận trọng hơn khi bắt đầu chiếu đèn ở các giá trị ngưỡng (nghĩa là tránh điều trị dự phòng) và ngừng chiếu đèn khi bilirubin huyết thanh giảm xuống dưới các mức này vì mối liên quan giữa đèn chiếu ở trẻ sơ sinh và tăng nguy cơ mắc bệnh động kinh ở trẻ em (không phải co giật do sốt), đặc biệt ở bé trai.[58] [59] |
|
|
thêm |
Bù dịch Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn Điều trị tình trạng mất nước và tiếp tục bù dịch với sữa mẹ hoặc sữa công thức đường miệng.. Bù dịch đường tĩnh mạch thường được dành cho trẻ sơ sinh đang chiếu đèn có mức bilirubin gần với giá trị cần thay máu. Bổ sung dịch đường tĩnh mạch như vậy có thể làm giảm nồng độ bilirubin nhanh hơn.[71] |
|
Mức bilirubin toàn phần > bách phân vị thứ 95 trên toán đồ đặc hiệu theo giờ để chiếu đèn |
1 |
Thay máu Mức ngưỡng phụ thuộc vào tuổi thai, tình trạng sức khỏe, và sự hiện diện của các yếu tố nguy cơ khác. [Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-4-1) Các yếu tố nguy cơ bao gồm bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt, li bì, thân nhiệt không ổn định, nhiễm trùng huyết và nhiễm toan. Nguy cơ bệnh não bilirubin cấp tính được cho là cao khi giá trị bilirubin tiệp cận mức > 428 micromol/L (>25 mg/dL) hoặc mức bilirubin thấp hơn kèm theo các yếu tố nguy cơ khác. Bắt đầu ngay khi đã chuẩn bị được máu để thay máu. Tiếp tục chiếu đèn trong khi chờ thay máu, dừng chiếu trong khi thực hiện thay máu và bắt đầu chiếu đèn lại ngay sau khi quá trình truyền máu hoàn tất. Cơ sở của phương pháp là loại bỏ bilirubin không liên hợp bằng cách thay máu gấp đôi thể tích, cho phép loại bỏ bilirubin ra khỏi mô não và do đó giảm nguy cơ nhiễm độc thần kinh. Thay máu cũng sẽ loại bỏ các kháng thể gây thiếu máu huyết tán. Trong các trường hợp tăng nguyên hồng cầu nặng và/hoặc phù thai, thủ thuật này cũng sẽ điều chỉnh tình trạng thiếu máu Không có đủ bằng chứng ủng hộ hay bác bỏ việc thay máu cùng thể tích trái ngược với thay máu gấp đôi thể tích ở trẻ sơ sinh bị vàng da.[70] Các biến chứng chính có thể xảy ra từ thủ thuật này bao gồm rối loạn điện giải, chảy máu, nhiễm trùng, rối loạn nhịp tim, huyết khối với thuyên tắc mạch, viêm ruột hoại tử, và bệnh lý mảnh ghép chống lại vật chủ. |
|
|
thêm |
Chiếu đèn Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn. Thực hiện chiếu đèn tích cực cho trẻ trong khi chờ thay máu và tiếp tục chiếu đèn sau khi thay máu. Tiếp tục sử dụng toán đồ để đánh dấu mức bilirubin toàn phần huyết thanh theo tuổi thai và số giờ sau khi sinh, và đánh giá nhu cầu có cần chiếu đèn thêm hoặc thay máu lặp lại hay không. Các yếu tố nguy cơ bao gồm bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt chu sinh, li bì, thân nhiệt không ổn định, nhiễm trùng huyết, nhiễm toan, và albumin Chiếu đèn sử dụng năng lượng ánh sáng gây phản ứng quang hóa để biến đổi bilirubin thành các đồng phân ít ái tính với lipid và dễ dàng bài xuất hơn, phá vỡ các sản phẩm không cần thiết cho quá trình liên hợp trong gan. Bước sóng chiếu đèn hiệu quả nhất từ 425 nm đến 490 nm.[47] Như là một liệu pháp đầu tay, chiếu đèn ánh sáng đôi thường được cho là có hiệu quả hơn chiếu đèn ánh sáng đơn hoặc sợi quang.[53] Chiếu đèn sợi quang và diode phát sáng (LED) là biện pháp thay thế hàng thứ 2 cho chiếu đèn thông thường ở trẻ sơ sinh đủ tháng.[51] [52] [53]Chiếu đèn LED như là biện pháp thay thế hàng thứ 2 khác vì có hiệu quả tương đương chiếu đèn thông thường,[54] và chiếu sáng từ trên xuống (so với chiếu sáng từ bên dưới trẻ) rút ngắn thời gian chiếu đèn trung bình và tăng tốc độ giảm bilirubin toàn phần huyết thanh (TSB). [55] [53] Chiếu đèn huỳnh quang ánh sáng xanh đặc biệt không tốt hơn chiếu đèn tuýp dài tiêu chuẩn ánh sáng xanh đặc biệt về tính hiệu quả và tác dụng bất lợi trên trẻ sơ sinh cũng như ảnh hưởng đến nhân viên y tế. [57] Dữ liệu nguy cơ/lợi ích tuyệt vời, với khởi phát tác dụng ngay khi bật đèn. Tác dụng bất lợi thường nhẹ và bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Có thể phòng ngừa những tác dụng phụ này bằng cách duy trì bổ sung nước đầy đủ và đảm bảo sử dụng kính che mắt cho em bé trong khi chiếu đèn Có thể tiếp tục cho trẻ bú sữa mẹ/bú bình ở hầu hết các trường hợp trong khi chiếu đèn Một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng chiếu đèn tích cực không ảnh hưởng đến kết cục suy giảm phát triển thần kinh hay tử vong ở trẻ có cân nặng khi sinh cực thấp (ELBW) (cân nặng khi sinh Có thể cần thận trọng hơn khi bắt đầu chiếu đèn ở các giá trị ngưỡng (nghĩa là tránh điều trị dự phòng) và ngừng chiếu đèn khi bilirubin huyết thanh giảm xuống dưới các mức này vì mối liên quan giữa đèn chiếu ở trẻ sơ sinh và tăng nguy cơ mắc bệnh động kinh ở trẻ em (không phải co giật do sốt), đặc biệt ở bé trai.[58] [59] |
|
|
thêm |
Bù dịch Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn Bù dịch đường tĩnh mạch thường được dành cho trẻ sơ sinh đang chiếu đèn có mức bilirubin gần với giá trị cần thay máu. Bổ sung dịch đường tĩnh mạch như vậy có thể làm giảm nồng độ bilirubin nhanh hơn.[71] Mặt khác, tiếp tục bù dịch với sữa mẹ hoặc sữa công thức đường miệng. |
|
|
bổ sung |
Globulin miễn dịch đường tĩnh mạch (IVIG) Điều trị được khuyến cáo cho MỘT SỐ bệnh nhân trong nhóm bệnh nhân được chọn Các lựa chọn hàng đầu globulin miễn dịch người bình thường: 0,5 đến 1 g/kg truyền tĩnh mạch trong 2 giờ; lặp lại trong 12 giờ nếu cần Ở trẻ nhũ nhi mắc bệnh huyết tán đồng miễn dịch, có thể bắt đầu điều trị IVIG nếu mức bilirubin toàn phần huyết thanh đang tăng mặc dù đang chiếu đèn tích cực hoặc trong khoảng 34-51 micromol/L (2-3 mg/dL) của mức thay máu, mặc dù chất lượng bằng chứng ủng hộ chiến lực này thì thấp.[68] |
|
Tăng bilirubin máu bệnh lý: liên hợp |
|
|
|
|
1 |
Điều trị nguyên nhân nền Điều trị tăng bilirubin huyết liên hợp phụ thuộc vào nguyên nhân bệnh. Có thể cần hội chẩn với bác sĩ chuyên khoa thích hợp để điều trị thêm, tùy theo nguyên nhân bệnh. |
|
Vàng da do sữa mẹ |
|
|
|
|
1 |
Tạm thời ngừng bú mẹ + cho ăn bổ sung Trẻ sơ sinh bị vàng da do sữa mẹ, có thể xem xét ngừng bú sữa mẹ trong 24 đến 48 giờ và cho ăn bổ sung nếu mức bilirubin huyết thanh cần chiếu đèn, có thể làm giảm mức bilirubin.[69] |
|
|
2 |
Chiếu đèn Mức ngưỡng phụ thuộc vào tuổi thai, tình trạng sức khỏe, và sự hiện diện của các yếu tố nguy cơ khác. [Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-3-1) Các yếu tố nguy cơ bao gồm bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt, li bì, thân nhiệt không ổn định, nhiễm trùng huyết, nhiễm toan, và albumin Chiếu đèn sử dụng năng lượng ánh sáng gây phản ứng quang hóa để biến đổi bilirubin thành các đồng phân ít ái tính với lipid và dễ dàng bài xuất hơn, phá vỡ các sản phẩm không cần thiết cho quá trình liên hợp trong gan. Bước sóng chiếu đèn hiệu quả nhất từ 425 nm đến 490 nm.[47] Như là một liệu pháp đầu tay, chiếu đèn ánh sáng đôi thường được cho là có hiệu quả hơn chiếu đèn ánh sáng đơn hoặc sợi quang.[53] Chiếu đèn sợi quang và diode phát sáng (LED) là biện pháp thay thế hàng thứ 2 cho chiếu đèn thông thường ở trẻ sơ sinh đủ tháng.[51] [52] [53]Chiếu đèn LED như là biện pháp thay thế hàng thứ 2 khác vì có hiệu quả tương đương chiếu đèn thông thường,[54] và chiếu sáng từ trên xuống (so với chiếu sáng từ bên dưới trẻ) rút ngắn thời gian chiếu đèn trung bình và tăng tốc độ giảm bilirubin toàn phần huyết thanh (TSB). [55] [53] Chiếu đèn huỳnh quang ánh sáng xanh đặc biệt không tốt hơn chiếu đèn tuýp dài tiêu chuẩn ánh sáng xanh đặc biệt về tính hiệu quả và tác dụng bất lợi trên trẻ sơ sinh cũng như ảnh hưởng đến nhân viên y tế. [57] Dữ liệu nguy cơ/lợi ích tuyệt vời, với khởi phát tác dụng ngay khi bật đèn. Tác dụng bất lợi thường nhẹ và bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Có thể phòng ngừa những tác dụng phụ này bằng cách duy trì bổ sung nước đầy đủ và đảm bảo sử dụng kính che mắt cho em bé trong khi chiếu đèn. Có thể tiếp tục cho trẻ bú sữa mẹ/bú bình ở hầu hết các trường hợp trong khi chiếu đèn. Một thử nghiệm ngẫu nhiên có đối chứng cho thấy rằng chiếu đèn tích cực không ảnh hưởng đến kết cục suy giảm phát triển thần kinh hay tử vong ở trẻ có cân nặng khi sinh cực thấp (ELBW) (cân nặng khi sinh [60] Tuy nhiên, một tổng quan hệ thống 9 nghiên cứu cho thấy rằng chiếu đèn dự phòng có thể làm giảm tình trạng suy giảm phát triển thần kinh lâu dài. [61]. Trong khi đó chiếu đèn tích cực chỉ giúp làm giảm tỷ lệ suy giảm phát triển thần kinh, nhưng làm tăng tỷ lệ tử vong ở trẻ có cân nặng khi sinh từ 500 g đến 750 g. [60]Vì vậy, không khuyến nghị phương pháp chiếu đèn tích cực cho trẻ có cân nặng khi cực thấp. Có thể cần thận trọng hơn khi bắt đầu chiếu đèn ở các giá trị ngưỡng (nghĩa là tránh điều trị dự phòng) và ngừng chiếu đèn khi bilirubin huyết thanh giảm xuống dưới các mức này vì mối liên quan giữa đèn chiếu ở trẻ sơ sinh và tăng nguy cơ mắc bệnh động kinh ở trẻ em (không phải co giật do sốt), đặc biệt ở bé trai.[58] [59] |
|
|
thêm |
Bù dịch Điều trị được khuyến cáo cho TẤT CẢ bệnh nhân trong nhóm bệnh nhân được chọn Khuyến nghị bù nước đường miệng với sữa mẹ hoặc sữa công thức trừ khi bilirubin toàn phần huyết thanh rất cao.[69] Bù dịch đường tĩnh mạch thường được dành cho trẻ sơ sinh đang chiếu đèn có mức bilirubin gần với giá trị cần thay máu. Bổ sung dịch đường tĩnh mạch như vậy có thể làm giảm nồng độ bilirubin nhanh hơn.[71] |
|
|
3 |
Thay máu Nguy cơ bệnh não bilirubin cấp tính được cho là cao khi giá trị bilirubin tiệp cận mức > 428 micromol/L (>25 mg/dL) hoặc mức bilirubin thấp hơn kèm theo các yếu tố nguy cơ khác theo biểu đồ Bhutani. [Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’ gestation] (http://pediatrics.aappublications.org/ content/114/1/297#xref-fig-4-1) (như bệnh huyết tán đồng miễn dịch , thiếu glucose-6-phosphate dehydrogenase, ngạt chu sinh, li bì, thân nhiệt không ổn định, nhiễm trùng huyết và nhiễm toan, các dấu hiệu bệnh não bilirubin cấp tính. Bắt đầu ngay khi đã chuẩn bị được máu để thay máu. Tiếp tục chiếu đèn trong khi chờ thay máu, dừng chiếu trong khi thực hiện thay máu và bắt đầu chiếu đèn lại ngay sau khi quá trình truyền máu hoàn tất. Cơ sở của phương pháp là loại bỏ bilirubin không liên hợp bằng cách thay máu gấp đôi thể tích, cho phép loại bỏ bilirubin ra khỏi mô não và do đó giảm nguy cơ nhiễm độc thần kinh. Thay máu cũng sẽ loại bỏ các kháng thể gây thiếu máu huyết tán. Trong các trường hợp tăng nguyên hồng cầu nặng và/hoặc phù thai, thủ thuật này cũng sẽ điều chỉnh tình trạng thiếu máu Không có đủ bằng chứng ủng hộ hay bác bỏ việc thay máu cùng thể tích trái ngược với thay máu gấp đôi thể tích ở trẻ sơ sinh bị vàng da.[70] Các biến chứng chính có thể xảy ra từ thủ thuật này bao gồm rối loạn điện giải, chảy máu, nhiễm trùng, rối loạn nhịp tim, huyết khối với thuyên tắc mạch, viêm ruột hoại tử, và bệnh lý mảnh ghép chống lại vật chủ. |
Các phương pháp mới
Stannsoporfin
Stannsoporfin ( còn được biết đến như là tin-mesoporphyrin) có tác dụng ức chế hem oxygenase, một bước ban đầu quan trọng trong quá trình sản xuất bilirubin. Vẫn chưa được chấp thuận ở nhiều quốc gia, nhưng đã được sử dụng dưới dạng nhân đạo.[72] Nếu điều trị này thất bại, một lựa chọn thay thế đó là thay máu. Có thể sử dụng Tin-mesoporphyrin ở tất cả trẻ sơ sinh không đáp ứng với liệu pháp chiếu đèn tích cực, để cố gắng tránh thay máu và có thể sử dụng vào bất kỳ lúc nào trong khi chiếu đèn.[73] Một mũi tiêm bắp duy nhất được tiêm trước khi xuất viện làm giảm thời gian chiếu đèn, đảo ngược quỹ đạo của nồng độ bilirubin toàn phần và giảm mức độ tăng bilirubin máu sau đó. Thuốc đã nhận được trạng thái theo dõi nhanh từ FDA. Vào tháng 8 năm 2018, FDA đã từ chối phê duyệt thuốc, yêu cầu đánh giá thêm để được xem xét trước khi gửi lại đơn xin phê duyệt.
Ánh sáng mặt trời được lọc
Trong một thử nghiệm ngẫu nhiên có đối chứng không thua kém được tiến hành ở Nigeria, ánh sáng mặt trời được lọc đã được chứng minh là an toàn và hiệu quả như chiếu đèn thông thường. [75]Điều quan trọng cần lưu ý là nghiên cứu này được thực hiện ở trẻ có tuổi thai ít nhất 35 tuần hoặc cân nặng > 2,2 kg, tuổi sau sinh lên đến 14 ngày và có mức bilirubin không vượt quá 257 micromol / L (15 mg/dL). [75]
Ursodiol
Acit mật kỵ nước làm giảm sự bài tiết cholesterol từ gan và hấp thụ đường ruột ở trẻ sơ sinh được nuôi dưỡng tĩnh mạch, chít hẹp đường mật, và xơ nang. Dữ liệu nguy cơ/lợi ích thì chưa rõ.
Clofibrate
Clofibrate tăng cường hoạt tính enzyme glucuronyl transferase, do đó tăng khả năng liên hợp của bilirubin tự do trong gan. Phân tích gộp các thử nghiệm lâm sàng gợi ý rằng liệu pháp clofibrate giảm nhu cầu và thời gian chiếu đèn cũng như nồng độ đỉnh bilirubin toàn phần huyết thanh. Các tác dụng này rõ ràng hơn ở trẻ sinh đủ tháng và ở trẻ không mắc bệnh huyết tán. Tuy nhiên, không có nghiên cứu nào báo cáo bệnh não do bilirubin hoặc tỷ lệ tử vong sơ sinh.[76] [77] Một nghiên cứu từ năm 2017 báo cáo rằng một liều clofibrate duy nhất trước khi bắt đầu chiếu đèn làm giảm đáng kể thời gian chiếu đèn. [78] Do đó, mặc dù dường như có một số lợi ích ngắn hạn của liệu pháp này, nhưng vẫn cần thêm các thử nghiệm để xác nhận kết cục phát triển thần kinh lâu dài trước khi đưa ra các khuyến nghị rõ ràng.
Theo dõi
Các khuyến cáo
Theo dõi
Cần theo dõi mức bilirubin toàn phần huyết thanh và hematocrit ở trẻ sơ sinh điều trị tăng bilirubin huyết tự do.
Ở trẻ sơ sinh bị thiếu máu huyết tán (thứ phát do bất đồng nhóm máu), đa hồng cầu, và thoát mạch, theo dõi hematocrit là rất quan trọng để loại trừ thiếu máu khởi phát muộn và bất kỳ vấn đề đang diễn ra nào khác khi quá trình liên hợp và bài xuất bilirubin bình thường.
Cũng cần đánh giá thính giác và phát triển thần kinh để nhận biết bất kỳ hậu quả nào của bệnh não do bilirubin[42]
Cần theo dõi các nguyên nhân ngoại khoa gây tăng tuần hoàn ruột gan bởi bác sĩ ngoại nhi để đảm bảo bài xuất mật thích hợp.
Trẻ sơ sinh bị khiếm khuyến một phần enzym liên hợp đặc hiệu cần theo dõi định kỳ mức bilirubin toàn phần huyết thanh để tránh giá trị cao kéo dài.
Trẻ sơ sinh bị tăng bilirubin máu liên hợp cần theo dõi dựa trên nguyên nhân gây bệnh: những trẻ bị khiếm khuyến chuyển hóa/gen và hội chứng lâm sàng (như thiếu alpha1-antitrypsin, xơ nang, hội chứng Zellweger, Dubin-Johnson, và Rotor) cần tái khám và theo dõi bởi nhóm bác sĩ chuyên khoa có thể điều trị các vấn đề lâm sàng khác nhau ngoài tình trạng tăng bilirubin máu liên hợp. Trẻ sơ sinh bị tăng bilirubin máu liên hợp do viêm gan thứ phát do nhiễm trùng thường không cần tái khám, theo dõi khi nhiễm trùng đã được điều trị và viêm gan đã khỏi.
Hướng dẫn bệnh nhân
Tái khám theo dõi với bác sĩ nhi khoa 48 giờ sau khi xuất viện để kiểm tra giá trị bilirubin toàn phần huyết thanh và hematocrit. Tiếp tục cho trẻ bú sữa mẹ hoặc bú bình như thường lệ.
Các biến chứng
|
Các biến chứng |
Khung thời gian |
Khả năng xảy ra |
|
Tổn thương thần kinh |
Ngắn hạn |
Trung bình |
|
Có thể phát hiện sớm nhiễm độc thần kinh do bilirubin bằng cách đánh giá đáp ứng kích thích thính giác thân não. Điều này có lẽ là do bilirubin đi vào tế bào thần kinh qua con đường thính giác. Ở trẻ sơ sinh bị vàng da, thời gian tiềm tàng đỉnh sóng và liên đỉnh sóng không có hoặc kéo dài. Những trẻ được điều trị cho thấy xu hướng hồi phục đáp ứng kích thích thính giác [80] Điều trị bao gồm chiếu đèn và/hoặc thay máu để làm giảm mức bilirubin tự do huyết thanh, có lẽ sẽ làm giảm mức bilirubin trong não và bình thường hóa đáp ứng kích thích thính giác. |
||
|
Bệnh não bilirubin cấp tính |
Ngắn hạn |
Trung bình |
|
Bilirubin là chất độc tế bào trong não và được ưu tiên hấp thụ bởi hạch nền, nhân bèo nhạt, nhân bèo sẫm, và nhân đuôi. Quá trình chuyển hóa năng lượng của tế bào bị gián đoạn bởi chức năng ti thể bị ảnh hưởng. Giai đoạn đầu được đặc trưng bởi ngủ gà, giảm trương lực cơ và bú kém với khóc thét . Giai đoạn trung gian, trẻ dễ cáu kỉnh, trương lực cơ thay đổi và khóc thét. Giai đoạn tiến triển, trẻ đi vào trạng thái sững sờ hoặc hôn mê, với tăng trương lực cơ (cổ ưỡn cong ra sau và/hoặc lưng ươn cong ra sau). Điều trị bao gồm chiếu đèn và/hoặc thay máu để làm giảm mức bilirubin tự do huyết thanh, có lẽ sẽ làm giảm mức bilirubin trong não và bình thường hóa đáp ứng kích thích thính giác. |
||
|
Các biến chứng do thay máu |
Ngắn hạn |
Trung bình |
|
Các biến chứng này bao gồm rối loạn điện giải, chảy máu, nhiễm trùng, rối loạn nhịp tim, huyết khối với thuyên tắc mạch, viêm ruột hoại tử, và bệnh lý mảnh ghép chống lại vật chủ. Khuyến nghị chiếu xạ máu trước khi dùng để thay máu làm giảm nguy cơ bệnh lý mảnh ghép chống lại vật chủ. Cần theo dõi thích hợp trong khi thay máu. Cần điều trị nếu trẻ có triệu chứng và/hoặc có kết quả xét nghiệm bất thường về các biến chứng đặc hiệu: ví dự như truyền canxi đối với hạ canxi máu, truyền tiểu cầu đối với giảm tiểu cầu.[42] [43] [47] |
||
|
Các biến chứng do chiếu đèn |
Ngắn hạn |
Thấp |
|
Bao gồm mất nước không thể nhận thấy được, phân lỏng, phát ban da, và khả năng tổn thương võng mạc. Các biến chứng này thường có thể được điều trị bằng cách đảm bảo bù dịch đầy đủ và sử dụng kính che mắt trong khi chiếu đèn Phát ban da lành tính và sẽ khỏi sau khi ngừng chiếu đèn.[42] [43] [47] |
||
|
Các biến chứng |
Khung thời gian |
Khả năng xảy ra |
|
Vàng da nhân ( Bệnh não bilirubin mạn tính ) |
Thay đổi |
Thấp |
|
Về mặt bệnh học, chẩn đoán vàng da nhân bởi nhuộm vàng đại thể và hoại tử các tế bào thần kinh ở hạch nền, vùng hồi hải mã, và tiểu não. Bệnh này xảy ra thứ phát do bilirubin đi vào trong não, gây gián đoạn quá trình chuyển hóa năng lượng tế bào ở hạch nền, vùng hồi hải mã, và tiểu não. Bệnh này hiếm gặp: hồ sơ đăng ký thử nghiệm vàng da nhân ở Hoa Kỳ báo cáo có 125 trẻ bị ảnh hưởng từ năm 1984 đến năm 2002. Vỏ não thường ít bị ảnh hưởng. Nếu trẻ sơ sinh sống sót, các đặc điểm lâm sàng bao gồm bại não gây múa giật- múa vờn, liệt ngước nhìn lên phía trên, mất thính giác thần kinh cảm giác, loạn sản răng, và khiếm khuyết trí tuệ (thường ít gặp ở khoảng thiểu năng trí tuệ).[47] Có thể phòng ngừa vàng da nhân bằng cách chiếu đèn và/hoặc thay máu sớm và tích cực. |
||
Tiên lượng
Hầu hết trẻ sơ sinh bị tăng bilirubin huyết không liên hợp sẽ cải thiện sau khi chiếu đèn và/hoặc thay máu. Vàng da nhân có thể phòng ngừa được nếu các khuyến nghị điều trị tăng bilirubin huyết được thực hiện đúng lúc.[43]
Đối với trẻ sơ sinh bị thiếu máu huyết tán thứ phát do bất đồng nhóm máu, tình trạng tan máu không còn là vấn đề khi không còn kháng thể của mẹ.
Trẻ bị đa hồng cầu và thoát mạch sẽ không có bất kỳ vấn đề nào khi tình trạng phá hủy hemoglobin thêm được quan tâm.
Nguyên nhân ngoại khoa gây tăng tuần hoàn ruột gan sẽ khỏi khi bệnh lý đặc hiệu được điều trị. Mức bilirubin ở trẻ nhỏ có khiếm khuyết một phần enzym liên hợp đặc hiệu thường có thể được kiểm soát với chiếu đèn vào ban đêm.
Đối với trẻ nhỏ bị tăng bilirubin huyết liên hợp, tiên lượng phụ thuộc vào nguyên nhân gây bệnh. Diễn biến lâm sàng khác nhau ở các trẻ nhỏ bị thiếu alpha 1-antitrypsin và xơ nang. Ở trẻ nhỏ bị hội chứng Zellweger, tiên lượng kém, với hầu hết trẻ sơ sinh tử vong trong năm đầu tiên hoặc sống sót với chứng chậm phát triển trí tuệ và co giật nặng. Bệnh nhân bị hội chứng Dubin-Johnson và Rotor (di truyền lặn trên nhiễm sắc thể thường) có tiên lượng tuyệt vời. Tiên lượng ở những trẻ bị các khiếm khuyết chuyển hóa/gen khác tùy thuộc vào việc nhận biết và điều trị sớm các thiếu hụt enzyme đặc hiệu và tích tụ các chất chuyển hóa. Ứ mật do nuôi dưỡng đường tĩnh mạch sẽ cải thiện nếu có thể cho ăn đường miệng. Một số nguyên nhân nhiễm trùng (như giang mai bẩm sinh, vi khuẩn) gây viêm gan cải thiện với các điều trị đặc hiệu; những nguyên nhân khác khỏi dần theo thời gian. Cần điều trị hỗ trợ đối với những người sống sót sau vàng da nhân. Khuyến nghị điều trị phục hồi đối với các khiếm khuyết thần kinh đặc hiệu.
Hướng dẫn
Hướng dẫn chẩn đoán
|
Châu Âu |
|
|
Jaundice in newborn babies under 28 days (http://guidance.nice.org.uk/ CG98) |
|
|
Published by: National Institute for Health and Care Excellence |
Last published: 2016 |
|
Bắc Mỹ |
|
|
Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation (http://pediatrics.aappublications.org/content/114/1/297.long) |
|
|
Published by: American Academy of Pediatrics |
Last published: 2004 |
|
Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation: an update with clarifications (http:// pediatrics.aappublications.org/content/124/4/1193) |
|
|
Published by: American Academy of Pediatrics Subcommittee on Hyperbilirubinemia |
Last published: 2009 |
|
Guidelines for detection, management and prevention of hyperbilirubinemia in term and late preterm newborn infants (http://www.cps.ca/en/documents/ authors-auteurs/fetus- and-newborn-committee) |
|
|
Published by: Canadian Paediatric Society |
Last published: 2007 (re- affirmed 2018) |
|
Châu Á |
|
|
Guidelines on evaluation and management of neonatal jaundice (https:// www.ams.edu.sg/policy-advocacy/guidelines-consensus-statements-for- healthcare- professionals) |
|
|
Published by: Academy of Medicine Singapore/College of Paediatrics and Child Health Singapore |
Last published: 2018 |
|
Integrated plan for detection and management of neonatal jaundice (https:// mpaeds.my/guideline-protocols/) |
|
|
Published by: Ministry of Health Malaysia |
Last published: 2017 |
|
Châu Đại dương |
|
|
Maternity and neonatal clinical guideline: neonatal jaundice (http:// www.health.qld.gov.au/qcg/html/publications.asp) |
|
|
Published by: Queensland Clinical Guidelines |
Last published: 2019 |
|
Neonatal – jaundice identification and management in neonates ≥32 weeks gestation (http://www.health.nsw.gov.au/policies/Pages/default.aspx) |
|
|
Published by: New South Wales Government |
Last published: 2016 |
Hướng dẫn điều trị
Châu âu |
|
|
Jaundice in newborn babies under 28 days (http://guidance.nice.org.uk/ CG98) |
|
|
Published by: National Institute for Health and Care Excellence |
Last published: 2016 |
|
Postnatal care up to 8 weeks after birth (http://guidance.nice.org.uk/CG37) |
|
|
Published by: National Institute for Health and Care Excellence |
Last published: 2015 |
Quốc tế |
|
|
Postnatal care of the mother and newborn (http://www.who.int/publications/ guidelines/child_health/en/) |
|
|
Published by: World Health Organization |
Last published: 2013 |
|
Pocket book of hospital care for children: guidelines for the management of common childhood illnesses (http://www.who.int/publications/guidelines/ child_health/en/) |
|
|
Published by: World Health Organization |
Last published: 2013 |
|
Bắc Mỹ |
|
|
Technical report: phototherapy to prevent severe neonatal hyperbilirubinemia in the newborn infant 35 or more weeks of gestation (http:// pediatrics.aappublications.org/content/128/4/e1046) |
|
|
Published by: American Academy of Pediatrics |
Last published: 2011 |
|
Prevention of acute bilirubin encephalopathy and kernicterus in newborns (http://nann.org/about/position-statements) |
|
|
Published by: National Association of Neonatal Nurses |
Last published: 2010 |
|
Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation: an update with clarifications (http:// pediatrics.aappublications.org/content/124/4/1193)
|
|
|
Published by: American Academy of Pediatrics Subcommittee on Hyperbilirubinemia |
Last published: 2009 |
|
Guidelines for detection, management and prevention of hyperbilirubinemia in term and late preterm newborn infants (http://www.cps.ca/en/documents/ authors-auteurs/fetus- and-newborn-committee) |
|
|
Published by: Canadian Paediatric Society |
Last published: 2007 (re- affirmed 2018) |
|
Management of hyperbilirubinemia in the newborn infant 35 or more weeksof gestation (http://pediatrics.aappublications.org/content/114/1/297) |
|
|
Published by: American Academy of Pediatrics Subcommittee on Hyperbilirubinemia |
Last published: 2004 |
|
Châu Á |
|
|
Guidelines on evaluation and management of neonatal jaundice (https:// www.ams.edu.sg/policy-advocacy/guidelines-consensus-statements-for- healthcare- professionals) |
|
|
Published by: Academy of Medicine Singapore/College of Paediatrics and Child Health Singapore |
Last published: 2018 |
|
Integrated plan for detection and management of neonatal jaundice (https:// mpaeds.my/guideline-protocols/) |
|
|
Published by: Ministry of Health Malaysia |
Last published: 2017 |
|
Châu Đại Dương |
|
|
Neonatal jaundice (http://www.health.qld.gov.au/qcg/html/publications.asp) |
|
|
Published by: Queensland Health Statewide Maternity and Neonatal Clinical Guidelines Program |
Last published: 2019 |
|
Neonatal – jaundice identification and management in neonates ≥32 weeks gestation (http://www.health.nsw.gov.au/policies/Pages/default.aspx) |
|
|
Published by: New South Wales Government |
Last published: 2016 |
Nguồn hỗ trợ trực tuyến
Bhutani nomogram for designation of risk based on hour-specific serum bilirubin values (http:// pediatrics.aappublications.org/content/114/1/297#p-152) (external link)
Bhutani nomogram guidelines for phototherapy in hospitalised infants of 35 or more weeks’ gestation (http://pediatrics.aappublications.org/content/114/1/297#xref-fig-3-1) (external link)
Bhutani nomogram guidelines for exchange transfusion in infants 35 or more weeks’ gestation (http:// pediatrics.aappublications.org/content/114/1/297#xref-fig-4-1) (external link)
Tài liệu tham khảo
Key articles
Bhutani VK, Johnson L, Sivieri EM. Predictive ability of a predischarge hour-specific serum bilirubin for subsequent significant hyperbilirubinemia in healthy term and near-term newborns. Pediatrics. 1999 Jan;103(1):6-14.
Abstract(http://www.ncbi.nlm.nih.gov/pubmed/9917432?tool=bestpractice.bmj.com)
Queensland Clinical Guidelines. Maternity and neonatal clinical guideline: neonatal jaundice. Jun 2019 [internet publication]. Full text (https://www.health.qld.gov.au/ data/assets/pdf_file/0018/142038/g- jaundice.pdf)
Maisels MJ, Bhutani VK, Bogen D, et al. Hyperbilirubinemia in the newborn infant ≥35 weeks’ gestation: an update with clarifications. Pediatrics. 2009 Oct;124(4):1193-8. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/19786452?tool=bestpractice.bmj.com)
Mehta S, Kumar P, Narang A. A randomized controlled trial of fluid supplementation in term neonates with severe hyperbilirubinemia. J Pediatr. 2005 Dec;147(6):781-5. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/16356431?tool=bestpractice.bmj.com)
Bhandari V, Narang A, Mann SB, et al. Brain stem electric response audiometry in neonates with hyperbilirubinemia. Indian J Pediatr. 1993 May-Jun;60(3):409-13. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/8253490?tool=bestpractice.bmj.com)
References
Bhutani VK, Johnson L, Sivieri EM. Predictive ability of a predischarge hour-specific serum bilirubin for subsequent significant hyperbilirubinemia in healthy term and near-term newborns. Pediatrics. 1999 Jan;103(1):6-14. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/9917432?tool=bestpractice.bmj.com)
Kumar RK. Neonatal jaundice: an update for family physicians. Aust Fam Physician. 1999 Jul;28(7):679-82. Abstract(http://www.ncbi.nlm.nih.gov/pubmed/10431423?tool=bestpractice.bmj.com)
Manning D, Todd P, Maxwell M, et al. Prospective surveillance study of severe hyperbilirubinaemia in the newborn in the UK and Ireland. Arch Dis Child Fetal Neonatal Ed. 2007 Sep;92(5):F342-6. Full text (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2675352/) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/17074786?tool=bestpractice.bmj.com)
Ebbesen F, Andersson C, Verder H, et al. Extreme hyperbilirubinaemia in term and near-term infants in Denmark. Acta Paediatr. 2005 Jan;94(1):59-64. Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/15858962?tool=bestpractice.bmj.com)
Smitherman H, Stark AR, Bhutani VK. Early recognition of neonatal hyperbilirubinemia and its emergent management. Semin Fetal Neonatal Med. 2006 Jun;11(3):214-24. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/16603425?tool=bestpractice.bmj.com)
Greco C, Arnolda G, Boo NY, et al. Neonatal Jaundice in Low- and Middle-Income Countries: Lessons and Future Directions from the 2015 Don Ostrow Trieste Yellow Retreat. Neonatology. 2016;110(3):172-80. Full text (https://www.doi.org/10.1159/000445708) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/27172942?tool=bestpractice.bmj.com)
Setia S, Villaveces A, Dhillon P, et al. Neonatal jaundice in Asian, white, and mixed-race infants. Arch Pediatr Adolesc Med. 2002 Mar;156(3):276-9. Full text (https://www.doi.org/10.1001/ archpedi.156.3.276) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/11876673? tool=bestpractice.bmj.com)
Maisels MJ, Kring E. Transcutaneous bilirubin levels in the first 96 hours in a normal newborn population of > or = 35 weeks’ gestation. Pediatrics. 2006 Apr;117(4):1169-73. Abstract(http:// www.ncbi.nlm.nih.gov/pubmed/16585312?tool=bestpractice.bmj.com)
American Academy of Pediatrics Subcommittee on Hyperbilirubinemia. Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation. Pediatrics. 2004 Jul;114(1):297-316. Full text (https://www.doi.org/10.1542/peds.114.1.297) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/15231951?tool=bestpractice.bmj.com)
Maisels MJ. What’s in a name? Physiologic and pathologic jaundice: the conundrum of defining normal bilirubin levels in the newborn. Pediatrics. 2006 Aug;118(2):805-7. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/16882840?tool=bestpractice.bmj.com)
Yu Z, Zhu K, Wang L, et al. Association of neonatal hyperbilirubinemia with UGT1A1 gene polymorphisms: a meta-analysis. Med Sci Monit. 2015 Oct 15;21:3104-14. Full text (https:// www.ncbi.nlm.nih.gov/pmc/articles/PMC4612146/) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/26467199?tool=bestpractice.bmj.com)
Klein CJ, Revenis M, Kusenda C, et al. Parenteral nutrition-associated conjugated hyperbilirubinemia in hospitalized infants. J Am Diet Assoc. 2010 Nov;110(11):1684-95. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/21034882?tool=bestpractice.bmj.com)
Gottesman LE, Del Vecchio MT, Aronoff SC. Etiologies of conjugated hyperbilirubinemia in infancy: a systematic review of 1692 subjects. BMC Pediatr. 2015 Nov 20;15:192. Full text () Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/26589959?tool=bestpractice.bmj.com)
Lain SJ, Roberts CL, Bowen JR, et al. Early discharge of infants and risk of readmission for jaundice. Pediatrics. 2015 Feb;135(2):314-21. Full text (http://pediatrics.aappublications.org/ content/135/2/314.long) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/25583922? tool=bestpractice.bmj.com)
De Luca D, Jackson GL, Tridente A, et al. Transcutaneous bilirubin nomograms: a systematic review of population differences and analysis of bilirubin kinetics. Arch Pediatr Adolesc Med. 2009 Nov;163(11):1054-9. Full text (http://archpedi.ama-assn.org/cgi/content/full/163/11/1054) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/19884597?tool=bestpractice.bmj.com)
Centers for Disease Control and Prevention. What are Jaundice and Kernicterus? Nov 2019 [internet publication]. Full text (https://www.cdc.gov/ncbddd/jaundice/facts.html)
Porter ML, Dennis BL. Hyperbilirubinemia in the term newborn. Am Fam Physician. 2002 Feb 15;65(4):599-606. Full text (https://www.aafp.org/afp/2002/0215/p599.html) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/11871676?tool=bestpractice.bmj.com)
Abu-Heija AT, Al-Bash M, Mathew M. Gestational and Pregestational Diabetes Mellitus in Omani Women: Comparison of obstetric and perinatal outcomes. Sultan Qaboos Univ Med J. 2015 Nov;15(4):e496-500. Full text (https://www.doi.org/10.18295/squmj.2015.15.04.009) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/26629376?tool=bestpractice.bmj.com)
Ghosh S, Ghosh K. Maternal and neonatal outcomes in gestational diabetes mellitus. J Indian Med Assoc. 2013 May;111(5):330-1, 336. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/24765693? tool=bestpractice.bmj.com)
Cosson E, Benchimol M, Carbillon L, et al. Universal rather than selective screening for gestational diabetes mellitus may improve fetal outcomes. Diabetes Metab. 2006 Apr;32(2):140-6. Full text (https://www.doi.org/10.1016/s1262-3636(07)70260-4) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/16735962?tool=bestpractice.bmj.com)
Khatun N, Latif SA, Uddin MM. Infant outcomes of gestational diabetes mellitus. Mymensingh Med J. 2005 Jan;14(1):29-31. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/15695950? tool=bestpractice.bmj.com)
Berk MA, Mimouni F, Miodovnik M, et al. Macrosomia in infants of insulin-dependent diabetic mothers. Pediatrics. 1989 Jun;83(6):1029-34. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/2726329? tool=bestpractice.bmj.com)
Widness JA, Susa JB, Garcia JF, et al. Increased erythropoiesis and elevated erythropoietin in infants born to diabetic mothers and in hyperinsulinemic rhesus fetuses. J Clin Invest. 1981 Mar;67(3):637-42. Full text (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC370612/) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/7009647?tool=bestpractice.bmj.com)
Singla DA, Sharma S, Sharma M, et al. Evaluation of risk factors for exchange range hyperbilirubinemia and neurotoxicity in neonates from hilly terrain of India. Int J Appl Basic Med Res. 2017 Oct-Dec;7(4):228-32. Full text (https://www.doi.org/10.4103/ijabmr.IJABMR_298_16) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/29308359?tool=bestpractice.bmj.com)
Gundur NM, Kumar P, Sundaram V, et al. Natural history and predictive risk factors of prolonged unconjugated jaundice in the newborn. Pediatr Int. 2010 Oct;52(5):769-72. Full text (https:// www.doi.org/10.1111/j.1442-200X.2010.03170.x) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/20497361?tool=bestpractice.bmj.com)
Oral E, Gezer A, Cagdas A, et al. Oxytocin infusion in labor: the effect different indications and the use of different diluents on neonatal bilirubin levels. Arch Gynecol Obstet. 2003 Jan;267(3):117-20. Full text (https://www.doi.org/10.1007/s00404-002-0298-3) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/12552319?tool=bestpractice.bmj.com)
Olusanya BO, Slusher TM. Infants at risk of significant hyperbilirubinemia in poorly-resourced countries: evidence from a scoping review. World J Pediatr. 2015 Nov;11(4):293-9. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/26454433?tool=bestpractice.bmj.com)
Muchowski KE. Evaluation and treatment of neonatal hyperbilirubinemia. Am Fam Physician. 2014 Jun 1;89(11):873-8. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/25077393?tool=bestpractice.bmj.com)
Kuzniewicz MW, Escobar GJ, Wi S, et al. Risk factors for severe hyperbilirubinemia among infants with borderline bilirubin levels: a nested case-control study. J Pediatr. 2008 Aug;153(2):234-40. Full text (https://www.doi.org/10.1016/j.jpeds.2008.01.028) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/18534217?tool=bestpractice.bmj.com)
Fonseca MJ, Severo M, Barros H, et al. Determinants of weight changes during the first 96 hours of life in full-term newborns. Birth. 2014 Jun;41(2):160-8. Full text (https://www.doi.org/10.1111/ birt.12087) Abstract(http://www.ncbi.nlm.nih.gov/pubmed/24635542?tool=bestpractice.bmj.com)
Yang WC, Zhao LL, Li YC, et al. Bodyweight loss in predicting neonatal hyperbilirubinemia 72 hours after birth in term newborn infants. BMC Pediatr. 2013 Sep 21;13:145. Full text (https:// www.doi.org/10.1186/1471-2431-13-145) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/24053490? tool=bestpractice.bmj.com)
McDonald SJ, Middleton P. Effect of timing of umbilical cord clamping of term infants on maternal and neonatal outcomes. Cochrane Database Syst Rev. 2013 Jul 11;(7):CD004074. Full text (http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD004074.pub3/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/23843134?tool=bestpractice.bmj.com)
Zhou J, Yang C, Zhu W, et al. Identification of Genetic Risk Factors for Neonatal Hyperbilirubinemia in Fujian Province, Southeastern China: A Case-Control Study. Biomed Res Int. 2018;2018:7803175. Full text (https://www.doi.org/10.1155/2018/7803175) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/30298137?tool=bestpractice.bmj.com)
Queensland Clinical Guidelines. Maternity and neonatal clinical guideline: neonatal jaundice. Jun 2019 [internet publication]. Full text (https://www.health.qld.gov.au/ data/assets/pdf_file/0018/142038/g- jaundice.pdf)
National Institute for Health and Care Excellence. Jaundice in newborn babies under 28 days. October 2016 [internet publication]. Full text (https://www.nice.org.uk/guidance/cg98)
National Association of Neonatal Nurses. Prevention of acute bilirubin encephalopathy and kernicterus in newborns. Position Statement #3049. NANN Board of Directors, March 2010. Adv Neonatal Care. 2010 Jun;10(3):112-8. Abstract(http://www.ncbi.nlm.nih.gov/pubmed/20505419? tool=bestpractice.bmj.com)
New South Wales Government. Neonatal – jaundice identification and management in neonates ≥32 weeks gestation. November 2016 [internet publication]. Full text (http://www1.health.nsw.gov.au/pds/ ActivePDSDocuments/GL2016_027.pdf)
Benchimol EI, Walsh CM, Ling SC, et al. Early diagnosis of neonatal cholestatic jaundice: test at 2 weeks. Can Fam Physician. 2009 Dec;55(12):1184-92. Full text(https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2793221/) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/20008595? tool=bestpractice.bmj.com)
Fawaz R, Baumann U, Ekong U, et al. Guideline for the evaluation of cholestatic jaundice in infants: joint recommendations of the North American Society for Pediatric Gastroenterology, Hepatology, and Nutrition and the European Society for Pediatric Gastroenterology, Hepatology, and Nutrition. J Pediatr Gastroenterol Nutr. 2017 Jan;64(1):154-68. Full text (https://journals.lww.com/jpgn/ fulltext/2017/01000/Guideline_for_the_Evaluation_of_Cholestatic.23.aspx) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/27429428?tool=bestpractice.bmj.com)
Trikalinos TA, Chung M, Lau J, et al. Systematic review of screening for bilirubin encephalopathy in neonates. Pediatrics. 2009 Oct;124(4):1162-71. Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/19786450?tool=bestpractice.bmj.com)
Ip S, Chung M, Trikalinos T, et al. Screening for bilirubin encephalopathy. Agency for Healthcare Research and Quality. 2009;1. Full text (http://www.ncbi.nlm.nih.gov/bookshelf/br.fcgi?book=es72) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/20722171?tool=bestpractice.bmj.com)
Bhutani VK, Johnson LH, Keren R. Diagnosis and management of hyperbilirubinemia in the term neonate: for a safer first week. Pediatr Clin North Am. 2004 Aug;51(4):843-61. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/15275978?tool=bestpractice.bmj.com)
Maisels MJ, Bhutani VK, Bogen D, et al. Hyperbilirubinemia in the newborn infant ≥35 weeks’ gestation: an update with clarifications. Pediatrics. 2009 Oct;124(4):1193-8. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/19786452?tool=bestpractice.bmj.com)
Mishra S, Chawla D, Agarwal R, et al. Transcutaneous bilirubinometry reduces the need for blood sampling in neonates with visible jaundice. Acta Paediatr. 2009 Dec;98(12):1916-9. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/19811459?tool=bestpractice.bmj.com)
De Luca D, Jackson GL, Tridente A, et al. Transcutaneous bilirubin nomograms: a systematic review of population differences and analysis of bilirubin kinetics. Arch Pediatr Adolesc Med. 2009 Nov;163(11):1054-9. Full text (http://archpedi.ama-assn.org/cgi/content/full/163/11/1054) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/19884597?tool=bestpractice.bmj.com)
Dijk PH, Hulzebos CV. An evidence-based view on hyperbilirubinaemia. Acta Paediatr. 2012 Apr;101(464):3-10. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/22404885? tool=bestpractice.bmj.com)
Maisels MJ. Neonatal jaundice. Pediatr Rev. 2006 Dec;27(12):443-54. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/17142466?tool=bestpractice.bmj.com)
Donneborg ML, Vandborg PK, Hansen BM, et al. Double versus single intensive phototherapy with LEDs in treatment of neonatal hyperbilirubinemia. J Perinatol. 2018 Feb;38(2):154-8. Full text (https:// www.doi.org/10.1038/jp.2017.167) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/29095431? tool=bestpractice.bmj.com)
Nuntnarumit P, Naka C. Comparison of the effectiveness between the adapted-double phototherapy versus conventional-single phototherapy. J Med Assoc Thai. 2002 Nov;85 Suppl 4:S1159-66. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/12549790?tool=bestpractice.bmj.com)
Sarici SU, Alpay F, Unay B, et al. Double versus single phototherapy in term newborns withsignificant hyperbilirubinemia. J Trop Pediatr. 2000 Feb;46(1):36-9. Full text (https://www.doi.org/10.1093/ tropej/46.1.36) Abstract(http://www.ncbi.nlm.nih.gov/pubmed/10730039?tool=bestpractice.bmj.com)
Mills JF, Tudehope D. Fibreoptic phototherapy for neonatal jaundice. Cochrane Database Syst Rev. 2001;(1):CD002060. Full text (https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD002060/full) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/11279748? tool=bestpractice.bmj.com)
Kumar P, Murki S, Malik GK, et al. Light emitting diodes versus compact fluorescent tubes for phototherapy in neonatal jaundice: a multi center randomized controlled trial. Indian Pediatr. 2010 Feb;47(2):131-7. Full text (http://www.indianpediatrics.net/feb2010/131.pdf) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/19578227?tool=bestpractice.bmj.com)
Woodgate P, Jardine LA. Neonatal jaundice: phototherapy. BMJ Clin Evid. 2015 May 22;2015:. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/25998618?tool=bestpractice.bmj.com)
Kumar P, Chawla D, Deorari A. Light-emitting diode phototherapy for unconjugated hyperbilirubinaemia in neonates. Cochrane Database Syst Rev. 2011 Dec 7;(12):CD007969. Full text (https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD007969.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/22161417?tool=bestpractice.bmj.com)
Tayman C, Tatli MM, Aydemir S, et al. Overhead is superior to underneath light-emitting diode phototherapy in the treatment of neonatal jaundice: a comparative study. J Paediatr Child Health. 2010 May;46(5):234-7. Abstract(http://www.ncbi.nlm.nih.gov/pubmed/20337873?tool=bestpractice.bmj.com)
Tridente A, De Luca D. Efficacy of light-emitting diode versus other light sources for treatment of neonatal hyperbilirubinemia: a systematic review and meta-analysis. Acta Paediatr. 2012 May;101(5):458-65. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/22168543? tool=bestpractice.bmj.com)
Sarin M, Dutta S, Narang A. Randomized controlled trial of compact fluorescent lamp versus standard phototherapy for the treatment of neonatal hyperbilirubinemia. Indian Pediatr. 2006 Jul;43(7):583-90. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/16891677?tool=bestpractice.bmj.com)
Maimburg RD, Olsen J, Sun Y. Neonatal hyperbilirubinemia and the risk of febrile seizures and childhood epilepsy. Epilepsy Res. 2016 Aug;124:67-72. Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/27259071?tool=bestpractice.bmj.com)
Newman TB, Wu YW, Kuzniewicz MW, et al. Childhood seizures after phototherapy. Pediatrics. 2018 Oct;142(4):e20180648. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/30249623? tool=bestpractice.bmj.com)
Morris BH, Oh W, Tyson JE, et al; NICHD Neonatal Research Network. Aggressive vs. conservative phototherapy for infants with extremely low birth weight. N Engl J Med. 2008 Oct30;359(18):1885-96. Full text (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2821221/) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/18971491?tool=bestpractice.bmj.com)
Okwundu CI, Okoromah CA, Shah PS. Prophylactic phototherapy for preventing jaundice in preterm or low birth weight infants. Cochrane Database Syst Rev. 2012 Jan 18;(1):CD007966. Full text (https://www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD007966.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/22258977?tool=bestpractice.bmj.com)
Mehta S, Kumar P, Narang A. A randomized controlled trial of fluid supplementation in term neonates with severe hyperbilirubinemia. J Pediatr. 2005 Dec;147(6):781-5. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/16356431?tool=bestpractice.bmj.com)
Mitra S, Samanta M, Sarkar M, et al. Pre-exchange 5% albumin infusion in low birth weight neonates with intensive phototherapy failure: a randomized controlled trial. J Trop Pediatr. 2011 Jun;57(3):217-21. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/20823089? tool=bestpractice.bmj.com)
Lai NM, Ahmad Kamar A, Choo YM, et al. Fluid supplementation for neonatal unconjugated hyperbilirubinaemia. Cochrane Database Syst Rev. 2017 Aug 1;(8):CD011891. Full text (https:// www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD011891.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/28762235?tool=bestpractice.bmj.com)
Dash N, Kumar P, Sundaram V, et al. Pre-exchange albumin administration in neonates with hyperbilirubinemia: a randomized controlled trial. Indian Pediatr. 2015 Sep;52(9):763-7. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/26519710?tool=bestpractice.bmj.com)
Huizing K, Røislien J, Hansen T. Intravenous immune globulin reduces the need for exchange transfusions in Rhesus and AB0 incompatibility. Acta Paediatr. 2008 Oct;97(10):1362-5. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/18616629?tool=bestpractice.bmj.com)
Beken S, Hirfanoglu I, Turkyilmaz C, et al. Intravenous immunoglobulin G treatment in ABO hemolytic disease of the newborn, is it myth or real? Indian J Hematol Blood Transfus. 2014 Mar;30(1):12-5. Full text (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3921323/) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/24554813?tool=bestpractice.bmj.com)
Zwiers C, Scheffer-Rath ME, Lopriore E, et al. Immunoglobulin for alloimmune hemolytic disease in neonates. Cochrane Database Syst Rev. 2018 Mar 18;(3):CD003313. Full text (https:// www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD003313.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/29551014?tool=bestpractice.bmj.com)
Flaherman VJ, Maisels MJ, Academy of Breastfeeding Medicine. ABM Clinical Protocol #22: Guidelines for management of jaundice in the breastfeeding infant 35 weeks or more of gestation- revised 2017. Breastfeed Med. 2017 Jun;12(5):250-7. Full text(https:// www.doi.org/10.1089/bfm.2017.29042.vjf) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/29624434? tool=bestpractice.bmj.com)
Thayyil S, Milligan DW. Single versus double volume exchange transfusion in jaundiced newborn infants. Cochrane Database Syst Rev. 2006 Oct 18;(4):CD004592. Full text (https:// www.cochranelibrary.com/cdsr/doi/10.1002/14651858.CD004592.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/17054210?tool=bestpractice.bmj.com)
Goyal P, Mehta A, Kaur J, et al. Fluid supplementation in management of neonatal hyperbilirubinemia: a randomized controlled trial. J Matern Fetal Neonatal Med. 2018 Oct;31(20):2678-84. Full text (https://www.doi.org/10.1080/14767058.2017.1351535) Abstract (http://www.ncbi.nlm.nih.gov/ pubmed/28675983?tool=bestpractice.bmj.com)
Reddy P, Najundaswamy S, Mehta R, et al. Tin-mesoporphyrin in the treatment of severe hyperbilirubinemia in a very-low-birth-weight infant. J Perinatol. 2003 Sep;23(6):507-8. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/13679941?tool=bestpractice.bmj.com)
Drummond GS, Kappas A. Chemoprevention of severe neonatal hyperbilirubinemia. Semin Perinatol. 2004 Oct;28(5):365-8. Abstract (http://www.ncbi.nlm.nih.gov/pubmed/15686268? tool=bestpractice.bmj.com)
Bhutani VK, Poland R, Meloy LD, et al. Clinical trial of tin mesoporphyrin to prevent neonatal hyperbilirubinemia. J Perinatol. 2016 Jul;36(7):533-9. Full text (https://www.doi.org/10.1038/ jp.2016.22) Abstract(http://www.ncbi.nlm.nih.gov/pubmed/26938918?tool=bestpractice.bmj.com)
Slusher TM, Olusanya BO, Vreman HJ, et al. A randomized trial of phototherapy with filtered sunlight in African neonates. N Engl J Med. 2015 Sep 17;373(12):1115-24. Full text (http://www.nejm.org/ doi/full/10.1056/NEJMoa1501074) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/26376136? tool=bestpractice.bmj.com)
Gholitabar M, McGuire H, Rennie J, et al. Clofibrate in combination with phototherapy for unconjugated neonatal hyperbilirubinaemia. Cochrane Database Syst Rev. 2012 Dec 12;(12):CD009017. Full text (http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD009017.pub2/full) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/23235669?tool=bestpractice.bmj.com)
Xiong T, Chen D, Duan Z, et al. Clofibrate for unconjugated hyperbilirubinemia in neonates: a systematic review. Indian Pediatr. 2012 Jan;49(1):35-41. Full text (http://www.indianpediatrics.net/ jan2012/35.pdf) Abstract(http://www.ncbi.nlm.nih.gov/pubmed/22318100?tool=bestpractice.bmj.com)
Kumar P, Adhisivam B, Vishnu Bhat B. Clofibrate as an adjunct to phototherapy for unconjugated hyperbilirubinemia in term neonates. Indian J Pediatr. 2017 Oct;84(10):763-7. Full text (https:// www.doi.org/10.1007/s12098-017-2360-y) Abstract (http://www.ncbi.nlm.nih.gov/pubmed/28512725? tool=bestpractice.bmj.com)
Bhandari V, Narang A, Mann SB, et al. Brain stem electric response audiometry in neonates with hyperbilirubinemia. Indian J Pediatr. 1993 May-Jun;60(3):409-13. Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/8253490?tool=bestpractice.bmj.com)
Funato M, Teraoka S, Tamai H, et al. Follow-up study of auditory brainstem responses in hyperbilirubinemic newborns treated with exchange transfusion. Acta Paediatr Jpn. 1996 Feb;38(1):17-21. Full text (https://www.doi.org/10.1111/j.1442-200x.1996.tb03428.x) Abstract (http:// www.ncbi.nlm.nih.gov/pubmed/8992853?tool=bestpractice.bmj.com)
Hình ảnh
Hình 1: Con đường chuyển hóa bilirubin với các bệnh lý liên quan đến tăng bilirubin máu tự do. 1. Bất đồng nhóm máu ABO, bất đồng nhóm Rhesus, tuổi thọ RBC ngắn hơn ở trẻ sơ sinh, bầm tím trong khi sinh; 2. Do các chất trung gian gây viêm liên quan đến các bệnh đồng mắc do sinh non (ví dụ như hội chứng suy hô hấp, nhiễm trùng); 3. Phân ly tăng do nhiễm toan, nhiễm ceton, suy thận; 4. Hàng rào máu-não cho bilirubin gián tiếp thấm qua ở trẻ sơ sinh đủ tháng và trẻ sinh non; 5. Đột biến gen UGT1A1 dẫn đến hội chứng Gilbert hoặc hội chứng Crigler-Najjar I và II; 6. Lượng bilirubin gián tiếp tăng do giảm nhu động ruột
Hình 2: Chi tiết tiểu thùy gan và chức năng của nó, làm nổi bật các bệnh lý gây tăng bilirubin liên hợp trong máu. Các bệnh lý bao gồm: 1. Huyết khối tĩnh mạch cửa; 2. Nang ống mật chủ; 3. Nhiễm trùng (nhiễm trùng huyết, nhiễm trùng đường tiết niệu E coli, viêm gan A hoặc B, bệnh toxoplasma, cytomegalovirus, giang mai, herpes), chuyển hóa (hội chứng Rotor, rối loạn chuyển hóa galactose, rối loạn chuyển hóa tyrosin máu, thiếu alpha-1 antitrypsin, suy giáp, xơ nang, hội chứng Zellweger), thuốc, viêm gan sơ sinh vô căn, nuôi dưỡng tĩnh mạch hoàn toàn, bệnh thừa sắt sơ sinh, sốc/giảm oxy mô/thiếu máu cục bộ; 4. Thiểu sản đường mật, hẹp đường mật, hội chứng Alagille, ứ mật sơ sinh vô căn, ứ mật tiến triển trong gan có tính gia đình, hội chứng mật đặc; 5. Đột biến gen MRP2 (còn được biết đến là ABCC2) trên màng tiểu quản của tế bào gan dẫn đến hội chứng Dubin-Johnson, không có OATP1B1 và OATP1B3 ở màng xoang của tế bào gan dẫn đến hội chứng Rotor.
Hình 3: Sự đổi màu vàng cam ở lòng bàn tay và lòng bàn chân tương phản với màu da bình thường của mẹ
Miễn trừ trách nhiệm
Disclaimer
BMJ Best Practice is intended for licensed medical professionals. BMJ Publishing Group Ltd (BMJ) does not advocate or endorse the use of any drug or therapy contained within this publication nor does it diagnose patients. As a medical professional you retain full responsibility for the care and treatment of your patients and you should use your own clinical judgement and expertise when using this product.
This content is not intended to cover all possible diagnosis methods, treatments, follow up, drugs and any contraindications or side effects. In addition, since such standards and practices in medicine change as new data become available, you should consult a variety of sources. We strongly recommend that you independently verify specified diagnosis, treatments and follow-up and ensure it is appropriate for your patient within your region. In addition, with respect to prescription medication, you are advised to check the product information sheet accompanying each drug to verify conditions of use and identify any changes in dosage schedule or contraindications, particularly if the drug to be administered is new, infrequently used, or has a narrow therapeutic range. You must always check that drugs referenced are licensed for the specified use and at the specified doses in your region.
Information included in BMJ Best Practice is provided on an “as is” basis without any representations, conditions or warranties that it is accurate and up to date. BMJ and its licensors and licensees assume no responsibility for any aspect of treatment administered to any patients with the aid of this information. To the fullest extent permitted by law, BMJ and its licensors and licensees shall not incur any liability, including without limitation, liability for damages, arising from the content. All conditions, warranties and other terms which might otherwise be implied by the law including, without limitation, the warranties of satisfactory quality, fitness for a particular purpose, use of reasonable care and skill and non-infringement of proprietary rights are excluded.
Where BMJ Best Practice has been translated into a language other than English, BMJ does not warrant the accuracy and reliability of the translations or the content provided by third parties (including but not limited to local regulations, clinical guidelines, terminology, drug names and drug dosages). BMJ is not responsible for any errors and omissions arising from translation and adaptation or otherwise.Where BMJ Best Practice lists drug names, it does so by recommended International Nonproprietary Names (rINNs) only. It is possible that certain drug formularies might refer to the same drugs using different names.
Please note that recommended formulations and doses may differ between drug databases drug names and brands, drug formularies, or locations. A local drug formulary should always be consulted for full prescribing information.
Treatment recommendations in BMJ Best Practice are specific to patient groups. Care is advised when selecting the integrated drug formulary as some treatment recommendations are for adults only, and external links to a paediatric formulary do not necessarily advocate use in children (and vice-versa). Always check that you have selected the correct drug formulary for your patient.
Where your version of BMJ Best Practice does not integrate with a local drug formulary, you should consult a local pharmaceutical database for comprehensive drug information including contraindications, drug interactions, and alternative dosing before prescribing.
Interpretation of numbers
Regardless of the language in which the content is displayed, numerals are displayed according to the original
English-language numerical separator standard. For example 4 digit numbers shall not include a comma nor a decimal point; numbers of 5 or more digits shall include commas; and numbers stated to be less than 1 shall be depicted using decimal points. See Figure 1 below for an explanatory table.
BMJ accepts no responsibility for misinterpretation of numbers which comply with this stated numerical separator standard.
This approach is in line with the guidance of the International Bureau of Weights and Measures Service.
Figure 1 – BMJ Best Practice Numeral Style
5-digit numerals: 10,000
4-digit numerals: 1000
numerals
Our full website and application terms and conditions can be found here: Website Terms and Conditions.
Contact us
+ 44 (0) 207 111 1105
support@bmj.com
BMJ
BMA House Tavistock Square London
WC1H 9JR UK
Contributors:
Authors:
Vineet Bhandari, MBBS, MD, DM
Professor of Pediatrics Obstetrics and Gynecology
Drexel University College of Medicine, Chief, Section of Neonatal Medicine, St. Christopher’s Hospital for Children/Hahnemann University Hospital/Temple University Hospital, Philadelphia, PA
DISCLOSURES: VB declares that he has no competing interests.
Peer Reviewers:
Gautham K. Suresh, MD, DM, MS
Professor of Pediatrics
Baylor College of Medicine, Section Head and Service Chief of Neonatology, Texas Children’s Hospital, Houston, TX
DISCLOSURES: GKS declares that he has no competing interests.
Helen McElroy, MBChB, MRCPI, MSc
Consultant Neonatologist
Neonatology, Medway Maritime Hospital, Gillingham, UK DISCLOSURES: HM declares that she has no competing interests.