Cơ học và sinh lý học hô hấp ảnh hưởng đến nhiều mặt của sinh lý tim gặp trong đơn vị chăm sóc đặc biệt tim mạch (CVICU), theo nhiều cách liên kết và phức tạp. Nói cách khác, bệnh nhân bị ảnh hưởng bởi bệnh tim thường dễ bị thay đổi chức năng phổi và điều ngược lại cũng đúng: sự thay đổi chức năng và giải phẫu tim ảnh hưởng đến sinh lý hô hấp theo những cách rất ấn tượng. Do đó, điều bắt buộc là bác sĩ lâm sàng phải nhận thức được làm thế nào cơ học hô hấp bình thường và bất thường có thể tạo ra nhu cầu quá mức đối với cung lượng tim và làm thế nào chúng có thể ảnh hưởng xấu đến cả sự tăng trưởng ngắn và dài hạn. Các cơ chế gây bất lợi cho cung lượng tim và tăng trưởng xảy ra là đa yếu tố và thực sự xứng đáng là một cuốn sách giáo khoa đa chủng loại dành riêng cho chủ đề này. Chúng tôi trình bày cho người đọc trong chương này một cuộc thảo luận giới thiệu về một số khái niệm và cơ chế này.
Phân bố thông khí
Các yếu tố quyết định phụ thuộc vào trọng lực của thông khí
Phổi là một cấu trúc nhớt đàn (viscoelastic structure) nằm bên trong và được hỗ trợ bởi thành ngực. Trọng lực làm cho phổi giả hình dạng hình cầu với áp lực âm tương đối nhiều hơn ở đỉnh và áp lực dương hơn ở đáy phổi. Độ lớn của gradient áp lực màng phổi (Ppl) phụ thuộc vào mật độ của phổi. Ppl thường tăng 7,5 cm H2O từ đỉnh đến đáy phổi người trưởng thành.47
Trong phổi bình thường, áp lực của không khí trong phế nang (áp lực phế nang [PA]) bằng nhau trong phổi và độ dốc Ppl dẫn đến sự khác biệt trong khu vực về áp lực xuyên phổi (PA – Ppl). Khi Ppl dương tính nhất (nghĩa là âm tính nhỏ nhất), sự chênh lệch áp lực xuyên thành dẫn đến phế nang bị nén và nhỏ hơn phế nang đỉnh. Do đó, phế nang nhỏ nằm ở vùng đáy phổi, nằm trên phần giữa của đường cong áp lực – thể tích bình thường của phổi, và phế nang lớn hơn của các đỉnh phổi thì nằm ở phần trên của đường cong
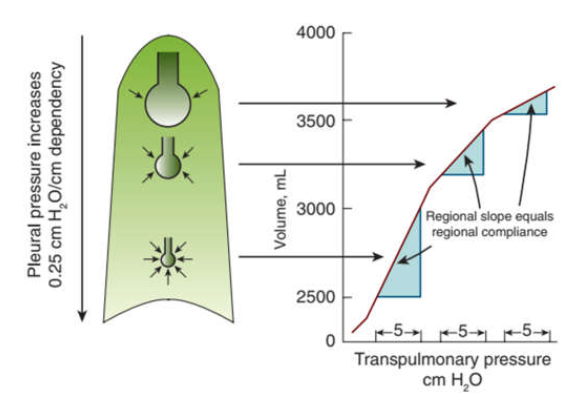
(Hình 14.1). Phế nang phụ thuộc (dependent alveoli) tương đối giãn nở hơn (có sự thay đổi thể tích lớn hơn đối với một sự thay đổi áp lực nhất định [nghĩa là, nằm trên phần dốc dốc hơn của đường cong thể tích áp lực]), trong khi phế nang không phụ thuộc (non-dependent alveoli) tương đối ít giãn nở hơn (nằm trên độ dốc phẳng hơn). Do đó, phần lớn thể tích khí lưu thông trong quá trình thông khí bình thường được phân phối trước cho phế nang phụ thuộc vì các phế nang này mở rộng nhiều hơn trên mỗi đơn vị thay đổi áp lực so với phế nang không phụ thuộc.
Hình 14.1 Áp lực phổi tăng 0,25 cm H2O trên mỗi cm đi xuống phổi. Sự gia tăng áp lực màng phổi làm giảm gấp bốn lần thể tích phế nang. Đường kính của đường dẫn khí cũng giảm khi thể tích phổi giảm. Khi thể tích phế nang khu vực được đặt lên trên đường cong thể tích phế nang -áp lực xuyên phổi vùng, thì phế nang nhỏ nằm trên phần dốc (độ dốc lớn) của đường cong và phế nang lớn nằm trên phần phẳng (độ dốc nhỏ) của đường cong. Do độ dốc khu vực bằng với độ giãn nở của khu vực, các phế nang nhỏ phụ thuộc thường nhận được phần lớn nhất của thể tích khí lưu thông. Trong phạm vi thể tích khí lưu thông bình thường (thể tích phổi tăng 500 mL từ 2500 mL [dung tích cặn chức năng bình thường] lên 3000 mL), mối quan hệ áp lực – thể tích là tuyến tính. Giá trị thể tích phổi trong sơ đồ này liên quan đến vị trí thẳng đứng. (Từ Benumof JL. Respiratory physiology and respiratory function during anesthesia. In: Miller RD, ed. Anesthesia. New York: Churchill Livingstone; 1990.)
Các yếu tố quyết định độc lập với trọng lực của thông khí
Cơ hô hấp.
Để trao đổi khí xảy ra ở cấp độ của phế nang, không khí được hít vào phải đi vào phổi qua đường thở. Các cơ hô hấp, bao gồm cơ hoành và các cơ liên sườn ngoài, chủ động co lại trong khi hít vào để cho không khí vào, trong khi thở ra yên tĩnh xảy ra một cách thụ động thông qua sự co giãn đàn hồi của hệ thống. Các cơ phụ của hít vào, chẳng hạn như cơ vân và cơ ức đòn chũm, hỗ trợ hô hấp trong khi tập thể dục. Thở ra cũng trở nên tích cực trong khi tập thể dục với sự co cơ của thành bụng (tức là cơ thẳng bụng, cơ chéo trong và chéo ngoài và cơ ngang bụng), và cơ liên sườn trong.93
Thể tích phổi và Đóng đường thở.
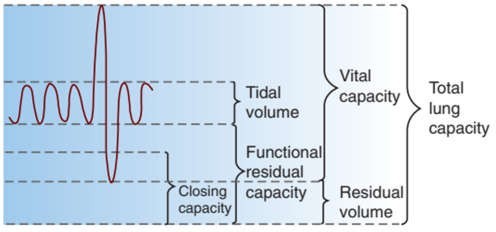
Dung tích cặn chức năng (FRC, functional residual capacity) được định nghĩa là thể tích khí còn lại trong phổi bình thường khi thở ra, khi PA bằng với áp lực xung quanh (Pambient). FRC phụ thuộc vào sự cân bằng của các đặc tính đàn hồi nội tại của phổi có xu hướng cho việc giảm thể tích và xu hướng tự nhiên của thành ngực hướng ra bên ngoài, chống lại việc giảm thể tích. Sự thay đổi tính chất đàn hồi của một trong hai thành phần này của hệ hô hấp làm thay đổi FRC. Tổng dung tích phổi (TLC, total lung capacity) là toàn bộ thể tích khí của nhu mô phổi khi hít vào tự phát tối đa và đường thở trong lồng ngực. Nó cung cấp điểm tham chiếu cho tất cả các thể tích và dung tích phổi khác (Hình 14.2). Dung tích sống (VC, vital capacity) xác định thể tích thu được khi thở ra tối đa từ TLC và là thể tích tối đa có thể trong quá trình thông khí tự phát. Như vậy, nó cung cấp một biện pháp dự trữ thông khí.
Một mối quan hệ quan trọng xảy ra giữa thể tích khí tồn tại trong phổi bình thường ở cuối thì thở ra (FRC) và thể tích khí trong phổi tại điểm mà ở đó đường thở bị xẹp xuống, được gọi là dung tích đóng (CC, closing capacity). Sử dụng kỹ thuật rửa khí trơ trong quá trình hít vào và thở ra tối đa, CC có thể được xác định là điểm mà đường dẫn khí ở các vùng phổi phụ thuộc bắt đầu sụp đổ.11 Nếu thể tích phổi cuối thì thở ra (EELV, end- expiratory lung volume) giảm xuống dưới CC, hoặc ngược lại CC được nâng lên trên EELV, những khu vực này bị xẹp phổi và không tham gia trao đổi khí.
Độ giãn nở. Mối quan hệ giữa sự thay đổi của thể tích (ΔV) và thay đổi áp lực căng (ΔP) xác định độ giãn nở.
C= ΔV/ ΔP
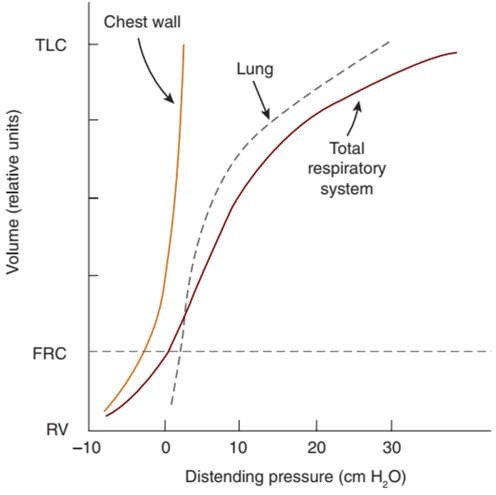
Các tính chất đàn hồi của hệ hô hấp và các thành phần của nó, phổi và thành ngực, được xác định bằng đồ họa bởi các mối quan hệ áp lực thể tích tương ứng của chúng (Hình 14.3). Phổi có lực giật đàn hồi do các sợi elastin và collagen kéo phổi về trạng thái xẹp xuống. Độ giãn nở của phổi được xác định bởi ΔV và độ dốc áp lực xuyên phổi (PA – Ppl, ΔP cho phổi). Ngược lại, thành ngực có một lực kéo ra bên ngoài. Thành ngực thể hiện độ giãn nở của chính nó, phụ thuộc vào PV và độ dốc áp lực xuyên thành (Ppl – Pambient, PP cho thành ngực). FRC xảy ra tại điểm cân bằng trong đó các lực này được cân bằng hoàn hảo. 21 Độ giãn nở tổng của hệ hô hấp được xác định bởi độ giãn nở của phổi và thành ngực.68 Để xác định tổng độ giãn nở hệ hô hấp, PV và độ dốc áp lực xuyên ngực (PA – Pambient, ΔP cho phổi và thành ngực) phải được biết.
Hình 14.2 Thành phần chức năng của thể tích phổi. (Từ From Scarpelli EM. Pulmonary Physiology of the Fetus, Newborn, and Child. Philadelphia: Lea & Febiger; 1975:27.)
Hình 14.3 Mối quan hệ thể tích – áp lực (tức là đường cong độ giãn nở) của thành ngực, phổi và toàn bộ hệ hô hấp ở trẻ em bình thường. Tại FRC, áp lực căng của phổi và thành ngực bằng nhau và đối trọng nhau, dẫn đến việc gây áp lực căng bằng không lên toàn bộ hệ hô hấp. Ở thể tích phổi vượt quá FRC, thành ngực của trẻ sơ sinh thể hiện các đặc điểm độ giãn nở rất cao so với người trưởng thành. Ngoài ra, các mối quan hệ áp lực – thể tích toàn bộ hệ thống hô hấp cho thấy các đặc điểm như đường sigma, với độ giãn nở giảm ở mức cực đoan của thể tích phổi. FRC, dung tích cặn chức năng; RV, thể tích cặn; TLC, tổng dung tích phổi. (Được sửa đổi từ Kendig EL, Chernick V. Disorders of the Respiratory Tract in Children. Philadelphia: WB Saunders; 1977:17)
Trong một số chế độ nhất định của bơm phồng phổi áp lực dương hoặc âm, độ dốc áp lực xuyên lồng ngực trước tiên tăng lên giá trị cực đại và sau đó giảm xuống giá trị cao nguyên thấp hơn. Áp lực xuyên lồng ngực đỉnh là áp lực cần thiết để vượt qua cả sức cản đàn hồi và đường thở (xem phần sau). Áp lực xuyên lồng ngực giảm xuống giá trị cao nguyên vì khí phân phối lại theo thời gian cho các phế nang với hằng số thời gian dài hơn. Khi khí phân phối lại với số lượng các phế nang tăng lên, áp lực được tạo ra ít hơn bởi cùng một thể tích khí và áp lực giảm. Do đó, hai cách đo độ giãn nở có thể được thực hiện, động và tĩnh. Trong quá trình thông khí áp lực dương, độ giãn nở động (dynamic compliance) có thể được ước tính bằng cách tính toán sự thay đổi thể tích (thể tích khí lưu thông) chia cho áp lực hít vào tối đa (peak inspiratory pressure) trừ đi áp lực cuối thì thở ra (áp lực dương cuối thì thở ra [PEEP]). Như vậy, việc độ giãn nở động tạo ra một tài khoản cho sự chuyển động của khí thông qua hệ thống. Ngược lại, độ giãn nở tĩnh (static compliance) có thể được tính gần đúng bằng cách đo sự thay đổi về thể tích chia cho áp lực hít vào cao nguyên (plateau inspiratory pressure) trừ đi áp lực cuối thì thở ra. Áp lực cao nguyên giảm xuống dưới áp lực hít vào tối đa vì phân phối lại khí; do đó độ giãn nở tĩnh lớn hơn độ giãn nở động. Độ giãn nở tĩnh là một đánh giá tốt hơn của toàn bộ hệ thống hô hấp, bởi vì phép đo phản ánh nhiều hơn các phế nang trao đổi khí.
Mối quan hệ độ giãn nở của thành ngực và các đơn vị phổi là dạng sigma. Ở các cực trị của thể tích phổi, độ giãn nở giảm và tăng áp lực hít vào tối đa lớn hơn để có được những thay đổi tương tự về thể tích. Do đó, bơm phồng dưới mức (xẹp phổi, giảm lưu lượng, EELV FRC) cần phải tránh, vì cần áp lực cao hơn để thay đổi thể tích phổi.
Một lực bổ sung góp phần vào độ giật đàn hồi của phổi là sức căng bề mặt (surface tension). Sức căng bề mặt là một lực được tạo ra bởi lực hút mạnh hơn giữa các phân tử chất lỏng liền kề so với giữa các phân tử chất lỏng và khí. Do lực này, chất lỏng giả định hình dạng của một khối cầu, cung cấp diện tích bề mặt nhỏ nhất có thể cho một thể tích nhất định.93 Chất lỏng tạo ra sức căng của bề mặt và được mô tả theo định luật Laplace, trong đó áp lực (P) tăng lên một phế nang tỷ lệ thuận với sức căng bề mặt (T) của chất lỏng lót phế nang và tỷ lệ nghịch với bán kính (R) của phế nang:
P=2T/R
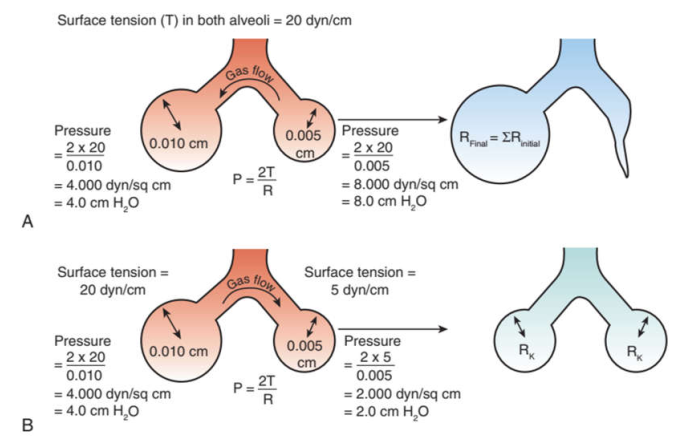
Sử dụng mối quan hệ này, áp lực bên trong phế nang nhỏ sẽ cao hơn bên trong phế nang lớn. Bởi vì phế nang nhỏ sẽ có áp lực lớn hơn so với những cái lớn, khí trong phế nang nhỏ sẽ di chuyển qua các phế nang lớn hơn, cho đến khi về mặt lý thuyết, một phế nang khổng lồ sẽ hình thành và các phế nang nhỏ bị xẹp (Hình 14.4A). Hiện tượng này không xảy ra trong phổi vì những thay đổi trong sức căng bề mặt phế nang.
Trong phổi khỏe mạnh bình thường, áp lực căng bị giảm đi do sự xuất hiện của chất hoạt động bề mặt (surfactant), là hỗn hợp của phospholipid, lipid trung tính và protein được tạo ra bởi các tế bào phổi loại II. Nó làm giảm đáng kể sức căng bề mặt trong phế nang do tính chất hỗn hợp của phân tử phospholipid của nó là ưa nước ở một đầu và kỵ nước ở đầu kia. Bằng cách giảm sức căng bề mặt và do đó áp lực cần thiết để làm phồng phế nang, chất hoạt động bề mặt làm tăng độ giãn nở của phổi. Surfactant cũng cho phép ổn định các phế nang nhỏ hơn, ức chế chúng thải chất chứa của chúng vào các phế nang lớn (xem hình 14.4B). Phù phổi có thể bị trầm trọng hơn do lực căng bề mặt hút chất lỏng từ các mao mạch vào trong phế nang. Bằng cách giảm sức căng bề mặt, chất hoạt động bề mặt ngăn chặn sự tiết dịch bằng cách giảm lực đẩy thủy tĩnh cho phù phổi.14
Đối với trẻ sinh non không có khả năng sản xuất đủ lượng chất hoạt động bề mặt nội sinh, việc thay thế chất hoạt động bề mặt ngoại sinh đã được sử dụng trong nhiều năm nay với việc giảm đáng kể tỷ lệ mắc bệnh và tử vong. Ngoài chất hoạt động bề mặt có nguồn gốc từ bò và nhím, chất hoạt động bề mặt tổng hợp cũng đã trở nên có sẵn.
Hình 14.4 Mối quan hệ giữa sức căng bề mặt (T), bán kính phế nang (R) và áp lực xuyên phế nang (P). A, Mối quan hệ áp lực trong hai phế nang có kích thước khác nhau nhưng có cùng sức căng bề mặt trong chất lỏng lót của chúng. Hướng của dòng khí sẽ là từ phế nang nhỏ áp lực cao hơn đến phế nang lớn áp lực thấp hơn. Kết quả cuối cùng là một phế nang lớn (RFinal = SRInitial). B, Mối quan hệ áp lực của hai phế nang có kích thước khác nhau khi phụ cấp được thực hiện cho những thay đổi dự kiến về sức căng bề mặt (ít căng hơn trong phế nang nhỏ hơn). Hướng của dòng khí là từ phế nang lớn hơn đến phế nang nhỏ hơn cho đến khi hai phế nang có kích thước bằng nhau và ổn định thể tích (RK). K, Hằng số; SR, tổng của tất cả các bán kính riêng lẻ. (Từ Benumof JL. Respiratory physiology and respiratory function during anesthesia. In: Miller RD,ed. Anesthesia. New York: Churchill Livingstone; 1990.)
Các nghiên cứu mới hơn đang nghiên cứu tính hiệu quả của các kỹ thuật quản lý chất hoạt động bề mặt xâm lấn tối thiểu, chẳng hạn như nebulization, cho phép sử dụng ở trẻ sơ sinh không đặt nội khí quản.71
Thay đổi độ giãn nở thành ngực và phổi là tình trạng quan trọng đòi hỏi phải đánh giá liên tục ở trẻ em bị bệnh nghiêm trọng. Mặc dù cả việc tăng và giảm độ giãn nở đều có thể dẫn đến thay đổi thể tích phổi, việc giảm độ giãn nở đòi hỏi phải xác định và can thiệp kịp thời. Việc giảm độ giãn nở nội tại của phổi và/hoặc thành ngực sẽ dẫn đến giảm tổng độ giãn nở và giảm thể tích phổi cho một PA nhất định và giảm FRC. Trong nhiều trường hợp lâm sàng, điều này có thể cần phải áp dụng thêm áp lực căng (PA) dưới dạng thông khí áp lực dương và/hoặc áp lực đường thở dương liên tục (áp lực đường thở dương liên tục [CPAP]/PEEP) để thiết lập lại thể tích phổi bình thường.
Sức cản.
Để có hiện tượng di chuyển khí xảy ra, độ dốc áp lực phải là được tạo ra để vượt qua sức cản đường thở không đàn hồi của phổi. Về mặt toán học, trở kháng (R) được xác định bởi độ dốc áp lực (ΔP) cần thiết để tạo ra một luồng khı́ (V˙ ) nhất định. Về mặt vật lý, sức cản là do ma sát trong quá trình di chuyển của các phân tử khí trong đường thở (sức cản đường thở) và ma sát từ chuyển động của phổi và thành ngực (sức cản nhớt mô). Những thành phần này tạo nên tổng sức cản không đàn hồi của hệ hô hấp. Thông thường sức cản đường thở chiếm khoảng 75% tổng sức cản không đàn hồi.17 Tuy nhiên, trong điều kiện sinh lý bệnh lý đường hô hấp làm thay đổi tình trạng sức cản nhớt mô, sức cản đường thở có thể bị thay đổi.
Độ dốc áp lực (ΔP) dọc theo đường thở phụ thuộc vào đường kính của đường thở và tốc độ và mô hình của luồng khí. Trong dòng chảy tầng, sự giảm áp lực đường thở tỷ lệ thuận với tốc độ dòng chảy. Khi dòng chảy vượt quá vận tốc tới hạn, nó trở nên hỗn loạn và sự giảm áp lực đường thở tương ứng với bình phương của tốc độ dòng chảy.84 Khi dòng chảy trở nên hỗn loạn hơn, áp lực tăng hơn lưu lượng và sức cản tăng. Tăng sức cản đường thở đòi hỏi một độ dốc áp lực lớn hơn giữa cửa thông khí và phế nang để duy trì lưu lượng. Trong quá trình thông khí áp lực dương, điều này đòi hỏi phải tạo ra áp lực hít vào cao hơn để đạt được thông khí tương tự, trong khi trong quá trình thở tự nhiên, phải đạt được áp lực trong lồng ngực và phế nang âm tính hơn để duy trì thông khí tương tự. Trong cả hai trường hợp, công việc cần thiết để tạo ra lưu lượng khí đầy đủ được tăng lên.
Sức cản của đường thở được tính gần đúng bằng đường kính của đường thở, vận tốc của luồng khí và tính chất của khí hít vào. Sức cản được xác định theo định luật Poiseuille, chi phối dòng chảy tầng trong các ống không phân nhánh:
Trong đó P là áp lực, V˙ là dòng chảy, L là chiều dài, r là bán kính của ống và ή là độ nhớt của khí.10,29 Khi lưu lượng vượt quá vận tốc tới hạn, mô hình của nó thay đổi từ tầng sang hỗn loạn. Sức cản của đường thở tỷ lệ nghịch với bán kính của đường dẫn khí được nâng lên mức lũy thừa 4 trong dòng chảy tầng và với lũy thừa 5 trong dòng chảy hỗn loạn.
Sức cản đường thở cũng phụ thuộc vào sự thay đổi thể tích phổi. Khi thể tích phổi tăng lên trên FRC, sức cản đường thở chỉ tăng một lượng nhỏ.2,17 Ngược lại, khi thể tích phổi giảm xuống dưới FRC, sức cản đường thở tăng lên đáng kể. Sức cản đường thở cũng phụ thuộc vào độ thông thoáng của đường thở. Trong quá trình thông khí áp lực âm bình thường, đường dẫn khí xâm nhập có xu hướng thu hẹp khi thở ra và mở theo hít vào. Kết quả là sự gia tăng sức cản đường thở trong quá trình thở ra. Trong điều kiện làm giảm tổng diện tích mặt cắt ngang và sức cản đường thở tăng lên, sự sụp đổ đường thở nhỏ và hạn chế dòng chảy xảy ra trong khi thở ra.
Hằng số thời gian.
Sự tương tác giữa độ giãn nở và sức cản phần lớn quyết định sự phân phối thông khí trong phổi. Mối quan hệ này được định nghĩa là tích số của sức cản (R) và độ giãn nở (C), gọi là hằng số thời gian (τ), và được đo bằng giây:
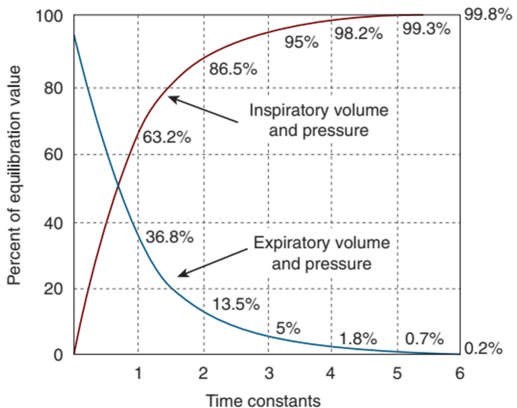
Hằng số thời gian xác định thời gian cần thiết cho mỗi khoang để đạt sự thay đổi về thể tích sau khi ứng dụng hoặc ngưng mức áp lực căng không đổi. Nó cũng mô tả thời gian cần thiết để áp lực trong phế nang cân bằng. Ví dụ, một áp lực căng liên tục áp dụng cho đường thở vượt qua sức cản của đường thở và mở rộng phổi (lực đàn hồi). Thành phần của áp lực vượt qua khả năng chống lại luồng không khí ban đầu là tối đa và giảm theo cấp số nhân khi luồng không khí giảm. Thành phần khắc phục lực đàn hồi tăng tỷ lệ thuận với sự thay đổi thể tích phổi. Do đó, áp lực cần thiết để vượt qua độ giãn nở ban đầu là tối thiểu, sau đó tăng theo cấp số nhân với tăng thể tích phổi. Thể tích phổi đạt đến trạng thái cân bằng theo hàm số mũ với tiến trình thay đổi theo thời gian của các đường cong hàm mũ này được mô tả bởi hằng số thời gian của chúng. Về mặt toán học, 63% bơm phồng phổi (hoặc xẹp xuống) xảy ra trong một thời gian không đổi (Hình 14.5).
Hầu hết các nguyên nhân gây suy hô hấp đều có những bất thường về sức cản và độ giãn nở của phổi, dẫn đến sự không đồng nhất nổi bật trong các hằng số thời gian trong khu vực. Do đó, với nhịp thở khí lưu thông bình thường, một số khoang nhất định lấp đầy và trống rỗng nhanh chóng (hằng số thời gian ngắn) trong khi những khoang khác lấp đầy và trống rỗng chậm (hằng số thời gian dài). Sự không đồng nhất này của hằng số thời gian dẫn đến sự bất thường rõ rệt trong phân phối thông khí với trao đổi khí bất thường.72,80 Trong những điều kiện này, thông khí áp lực dương thành công có thể yêu cầu điều chỉnh thời gian hít vào và thở ra để cho phép phân phối đồng đều hơn (thông khí đồng nhất) giữa các khoang phổi. Chiến lược này, được mô tả ở nơi khác, thường xuyên cải thiện kết hợp thông khí/tưới máu (V/Q).
Hình 14.5 Sự tăng giảm theo cấp số nhân của áp lực phổi và thể tích phổi trong khi hít vào và thở ra được biểu thị theo các hằng số thời gian. (Từ Chatburn RL. Principles and practice of neonatal and pediatric mechanical ventilation. Respir Care. 1991;36:569.)
Công thở.
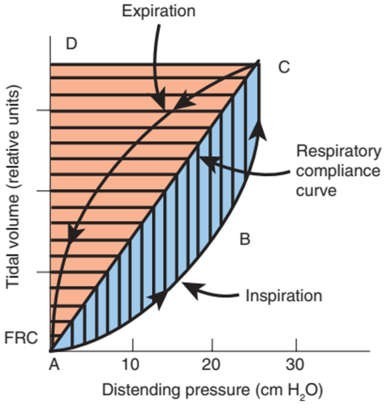
Công thở (work of breathing) được định nghĩa là năng lượng cần thiết để thực hiện thông khí khí lưu thông trong một đơn vị thời gian. Công thở được xác định bởi các đặc tính thể tích-áp lực (độ giãn nở và sức cản) của hệ hô hấp (Hình 14.6). Trong quá trình thở, công phải được thực hiện để khắc phục xu hướng phổi bị xẹp xuống và thành ngực bị bung ra (xem Hình 14.6, khu vực ADC) và khả năng chống ma sát đối với dòng khí xảy ra trong đường thở (xem Hình 14.6, khu vực ABC). Công hô hấp (xem hình 14.6, khu vực ABCD) được tăng lên nhờ các điều kiện làm tăng sức cản hoặc giảm độ giãn nở hoặc khi tần số hô hấp tăng.
Hình 14.6 Vòng lặp thể tích-áp lực hít vào/thở ra được ghi lại trong chu kỳ hô hấp. Chu kỳ hô hấp bình thường đòi hỏi phải tiêu tốn công sức trong khi hít vào để vượt qua trở kháng và đàn hồi để cho phép bơm phồng phổi. Tổng công thở (áp lực × thể tích) được xác định bằng tổng công trở kháng (diện tích được xác định bởi ABC) cộng với công đàn hồi (diện tích được xác định bởi ACD). Tổng công hô hấp (diện tích được xác định bởi ABCD) tăng lên khi tăng tính chất trở kháng của hệ hô hấp hoặc giảm độ giãn nở hô hấp (độ dốc của đường giữa A và C). (Từ Goldsmith JP, Karotkin EH. Assisted Ventilation of the Neonate. Philadelphia: WB Saunders; 1981:29)
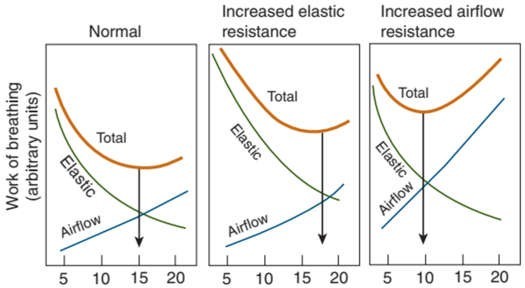
Nếu thể tích phút không đổi, thành phần công của “độ giãn nở” tăng lên khi thông khí thể tích khí lưu thông lớn và nhịp thở chậm. Thành phần công của “sức cản đường thở” tăng lên khi nhịp hô hấp nhanh và thông khí thể tích khí lưu thông giảm. Khi hai thành phần được tổng hợp và tổng công được vẽ theo tần số hô hấp, có thể thu được tần số hô hấp tối ưu để giảm thiểu tổng công việc hô hấp (Hình 14.7). Ở trẻ em bị bệnh phổi hạn chế (EELV FRC, sức cản cao) với hằng số thời gian dài có tần số hô hấp tối ưu thấp hơn.
Hình 14.7 Công được thực hiện chống lại sự đàn hồi và sức cản của luồng không khí và tổng hợp để chỉ ra tổng công thở ở các tần số hô hấp khác nhau ở người lớn. Tổng công thở có giá trị tối thiểu vào khoảng 15 nhịp thở/phút trong các chu kỳ bình thường. Đối với cùng một thể tích phút, công tối thiểu được thực hiện ở tần số cao hơn với phổi cứng (ít độ giãn nở) và ở tần số thấp hơn khi sức cản của luồng không khí được tăng lên. (Từ Nunn JF. Applied Respiratory Physiology. Boston: Butterworth; 1987:109.)