Case 51
Bệnh nhân nữ 20 tuổi đang mang thai tuần 32/40. Cô ấy tới khoa tiền sản để khám định kỳ. Xét nghiệm công thức máu được thực hiện và có kết quả như sau:
| Chỉ số |
Bệnh nhân |
Khoảng tham chiếu |
|
Hb |
101 g/L |
115 – 135 g/L |
|
WBC |
6.2 x 109/L |
6 – 10 x 109/L |
|
PLT |
80 x 109/L |
150 -400 x 109/L |
|
MPV |
13.1 fL |
7.5 – 9.2 fL |
|
MCV |
89 fL |
80 – 98 fL |
|
Phân loại bạch cầu |
Bình thường |
|
Câu hỏi 1: Những kết quả này nói lên điều gì và nguyên nhân giải thích cho các kết quả này là gì?
Câu hỏi 2: Bạn sẽ chỉ định thêm xét nghiệm gì?
Bạn yêu cầu:
a/Đếm tiểu cầu trên ống chống đông citrat, cho kết quả tiểu cầu 78 x 109/L.
b/Tiêu bản máu đàn được báo cáo là bình thường, không có các đám tiểu cầu.
c/Sàng lọc kháng đông Lupus có kết quả âm tính
d/ANA dương tính và ENA thể hiện sự có mawth của Anti-Ro (nồng độ 60 U/mL – khoảng tham chiếu là
Câu hỏi 3: Bạn sẽ làm gì tiếp?
Khi thai được 36 tuần, tiểu cầu của bệnh nhân là 62 x 109/L.
Câu hỏi 4: Bạn đưa ra lời khuyên gì cho bác sĩ sản khoa và các sĩ khoa và bác sĩ gây mê sản khoa?
Đáp án
Câu hỏi 1: Những kết quả này nói lên điều gì và nguyên nhân giải thích cho các kết quả này là gì?
Kết quả công thức máu thể hiện tình trạng thiếu máu nhẹ, macrothrombocytopaenia. Các nguyên nhân có thể là:
a/Giảm tiểu cầu thai nghén – tiểu cầu giảm hơn bình thường trong thời kỳ mang thai.
b/Giảm tiểu cầu miễn dịch
c/Macrothrombocytopaenia di truyền.
d/Tiền sản giật
e/Rối loạn chức năng gan
Giảm tiểu cầu nhân tạo phải được loại trừ bằng cách chỉ định xét nghiệm đếm tiểu cầu bằng ống citrated. Tuy nhiên, nó thường không liên quan với tình tràng tăng MPV. Tiêu bản máu ngoại vi nên được phân tích để tìm kiếm bằng chứng của các đám tiểu cầu, loại trừ các nguyên nhân khác gây giảm tiểu cầu (ví dụ Hegglin anomaly) và tìm kiếm mảnh vỡ hồng cầu, có thể gợi ý các chẩn đoán như TTP, HELLP hoặc các tan máu vi mạch khác (MAHA). Cũng quan trọng nếu có thể xem lại các công thức máu trước đây của bệnh nhân, để xác định tình trạng Macrothrombocytopaenia có được chú ý trước đây chưa đặc biệt khi bệnh nhân chưa mang thai.
Có rất nhiều nguyên nhân gây giảm tiểu cầu thai kỳ cao gồm:
a/Rối loạn tự miễn, ví dụ SLE.
b/DIC
c/Các rối loạn liên quan tới thuốc.
d/VWD
e/Lách to
f/Thiếu vitamin B12 và acid folic.
Rất nhiều các nguyên nhân trên sẽ được loại trừ bằng nghiên cứu tiền sử bệnh nhân, bao gồm cả tiền sử chảy máu.
Câu hỏi 2: Bạn sẽ chỉ định thêm xét nghiệm gì?
Lặp lại xét nghiệm công thức máu và phân tích lam máu ngoại vi.
Đếm tiểu cầu bằng ống chống đông Citrat (hoặc tương tự). Khoảng 1/200 dân số có giảm tiểu cầu do EDTA và khoảng 20% các trường hợp hiện tượng này vẫn tồn tại khi mẫu máu đã được lấy bằng ống chống đông citrate.
Lấy mẫu sang ống chống đông Heparin có thể tránh được vấn đề này.
Nếu khẳng định tình trạng Macrothrombocytopaenia, thì sau đó nên:
a/Sàng lọc kháng thể kháng Phospholipid (Kháng đông Lupus, anti- cardiolipin, và anti – β2 GPI).
b/ANA + ENA
c/Huyết thanh học virus – việc này có vẻ như được thực hiện ở các giai đoạn đầu mang thai như một xét nghiệm tiền sản routine, thực hiện ở tất cả các phụ nữ mang thai tại UK.
Xem xét khả năng đây là một Macrohrombocytopaenia di truyền đặc biệt nếu số lượng tiểu cầu ngoài giai đoạn mang thai cũng thấp và/hoặc có tiền sử gia đình của Macrohrombocytopaenia hoặc có các triệu chứng lâm sàng liên quan ví dụ nghi ngờ đột biến gen MyH9.
Công thức máu cho thấy thiếu máu nhẹ và vì vậy, nên sàng lọc các nguyên nhân thiếu máu trong thai kỳ.
Câu hỏi 3: Bạn sẽ làm gì tiếp?
Kết quả ENA Anti-Ro/Anti-La dương tính ủng hộ khả năng bệnh nhân có thể có một bệnh lý nền là các rối loạn miễn dịch như Lupus ban đỏ hệ thống (SLE) hoặc hội chứng Sjogren’s để giải thích cho nguyên nhân tiểu cầu giảm và kích thước lớn. Kháng thể AntiRo/AntiLa liên quan tới nguy cơ block nhĩ thất ở em bé, do vậy bạn nên cảnh báo bác sĩ sản khoa/bác sĩ sơ sinh về vấn đề này. Có nhiều nguyên nhân khác liên quan tới sự có mặt của kháng thể ở thai nhi bao gồm hội chứng lupus sơ sinh.
Bạn nên lặp lại xét nghiệm ANA và ENA và sắp xếp cho bệnh nhân khám lại để kiểm tra lại số lượng tiểu cầu.
Bạn cũng nên để ý rằng MPV tăng. Điều này gợi ý rằng nguyên nhân tiểu cầu giảm có khả năng do tăng phá huỷ tiểu cầu ở máu ngoại vi hơn là do giảm sinh tại tuỷ. Ở những người có giảm tiểu cầu do nguyên nhân tuỷ xương thì MPV thường thấp. Trong thời kỳ mang thai, MPV thường cao.
Câu hỏi 4: Bạn đưa ra lời khuyên gì cho bác sĩ sản khoa và các sĩ khoa và bác sĩ gây mê sản khoa?
Số lượng tiểu cầu đo trên máy xét nghiệm tự động hầu hết dựa vào kích thước tiểu cầu và ở những bệnh nhân có MPV tăng, số lượng tiểu cầu có thể không được xác định chính xác. Vì những nguyên nhân này, nên kiểm tra tiểu cầu bằng phương pháp miễn dịch. Đó là gắn việc gắn kháng thể miễn dịch với các thụ thể GpIIb/IIIa, sau đó đếm trên máy tế bào dòng chảy, và do vậy số lượng tiểu cầu được đếm mà không phụ thuộc số lượng.
Ở bệnh nhân này, tiểu cầu đo bằng phương pháp miễn dịch là 93 x 109/L. Nhìn chung, nếu giả định chức năng tiểu cầu bình thường thì số lượng tiểu cầu >80×109/L là đủ cho quá trình sinh đẻ bình thường và cho gây mê tuỷ sống. Tiểu cầu từ 50 – 80 x 109/L có thể an toàn cho cuộc đẻ tuy nhiên nên tránh gây mê tuỷ sống. Nếu tiểu cầu 9/L thì nên truyền tiểu cầu để nâng số lượng tiểu cầu trong cuộc đẻ.
Nếu bạn không thể loại trừ ITP ở sản phụ này, có khả năng đứa trẻ sinh ra sẽ có tiểu cầu giảm do sự truyền Immunoglobulins qua rau thai thông qua thụ thể Fc sơ sinh. Bạn nên đề nghị đếm tiểu cầu ở máu cuống rốn, và nếu tiểu cầu ở máu cuống rốn thấp, nó có thể tiếp tục giảm nữa tới mức nguy hiểm ở ngày thứ 3 sau sinh. Bác sĩ sản khoa nên cảnh giác trong cuộc đẻ và không nên dùng thủ thuật kẹp kéo thai như forceps, giác hút…
Sản phụ này có kháng thể Anti-Ro và Anti-La dương tính, do vậy bạn nên cân nhắc viễn cảnh đứa trẻ sinh ra có block nhĩ thất và cần điều trị ổn định nhịp tim ngay lập tức và đứa trẻ có thể có giảm tiểu cầu do truyền IgG miễn dịch qua rau thai. Điện tim nên được làm nhiều lần trong quá trình mang thai.
Có vẻ như sản phụ này có rối loạn miễn dịch gây giảm tiểu cầu do việc tìm thấy kháng thể Anti-Ro và AntiLa nhưng có thể bất thường chức năng tiểu cầu không thể được loại trừ hoàn toàn và nó có thể ảnh hưởng tới quyết định điều trị hoặc lời khuyên của bạn cho bác sĩ sản khoa/bác sĩ gây mê.
Điều quan trọng là theo dõi số lượng tiểu cầu sau sinh đặc biệt là quan sát các đáp ứng điều trị. Các xét nghiệm khác như chức năng tiểu cầu và phân tích di truyền nên được chỉ định để xác định nguyên nhân
Macrohrombocytopaenia nếu điều trị không đáp ứng như mong đợi. Bệnh nhân này sau đó được chẩn đoán bởi các bác sĩ khớp là Lupus ban đỏ hệ thống (SLE).
|
Tóm tắt: Đây là trường hợp Macrohrombocytopaenia ở phụ nữ mang thai thứ phát do bệnh lý rối loạn miễn dịch. |
Case 52
Bệnh nhân nam 23 tuổi được xét nghiệm để chẩn đoán các rối loạn chảy máu khi bệnh nhân không ở UK. Bệnh nhân có xét nghiệm máu chảy kéo dài 26 phút (bình thường
Câu hỏi 1: Tóm tắt nguyên lý của xét nghiệm máu chảy.
Câu hỏi 2: Bất thường nào có thể giải thích tình trạng máu chảy kéo dài?
Câu hỏi 3: Bạn cần thêm xét nghiệm gì?
Một số xét nghiệm được thực hiện và cho kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
11.2 s |
11 – 14 s |
|
APTT |
51 s |
23 – 35 s |
|
FVIII:C |
0.12 IU/mL |
0.5 – 1.5 IU/mL |
|
vWF:Ag |
0.11 IU/mL |
0.5 – 1.5 IU/mL |
|
vWF:Act |
0.12 IU/mL |
0.5 – 1.5 IU/mL |
Xét nghiệm công thức máu bình thường.
Câu hỏi 4: Các xét nghiệm trên gợi ý điều gì?
Câu hỏi 5: Các xét nghiệm này có thể giải thích tại sao thời gian máu chảy kéo dài không?
Câu hỏi 6: Bạn cần thêm xét nghiệm gì?
Câu hỏi 7: Xét nghiệm máu chảy có thường xuyên được thực hiện hay không?
Đáp án
Câu hỏi 1: Tóm tắt nguyên lý của xét nghiệm máu chảy.
Phương pháp Ivy là phương pháp kinh điển để xét nghiệm thời gian máu chảy. Trong phương pháp Ivy, băng huyêt áp được đặt trên cánh tay và duy trì áp lực khoảng 40mmHg. Dùng một lancet để tạo 2 điểm cắt ở cẳng tay, thường cách nhau 5-10cm. Khởi động đồng hồ bấm giây ngay lập tức và mỗi 30s, dùng giấy thấm để thấm máu. Thời gian từ khi tạo điểm chảy máu ở cẳng tay đến khi máu ngừng chảy gọi là thời gian máu chảy.
Để chuẩn hoá xét nghiệm máu chảy, phương pháp Template được phát triển. Trong đó sử dụng một lưỡi dao tự động tạo tại vết cắt có kích thước chuẩn (khoảng 6mm chiều dài và 1mm chiều sâu) ở cạnh trong cẳng tay.
Xét nghiệm phụ thuộc vào số lượng và chức năng tiểu cầu dính vào tế bào nội mạc để ngưng tập. Thời gian máu chảy kéo dài nếu:
|
Bất thường Collagen |
Ví dụ hội chứng Ehlers Danlos |
|
Tiểu cầu giảm |
Quan trọng là đếm số lượng tiểu cầu trước khi thực hiện xét nghiệm máu chảy (BT). Nếu tiểu cầu 9/L thì thường sẽ cho BT kéo dài. |
|
Bất thường tiểu cầu bẩm sinh hoặc mắc phải bao gồm sử dụng thuốc chống ngưng tập tiểu cầu như Aspirin và Clopiidogrel sẽ làm BT kéo daiif. BT không thể dự đoán nguy cơ chảy máu trong phẫu thuật nêu bệnh nhân sử dụng các thuốc này. |
|
|
Bất thường chất lượng tiểu cầu |
Paraprotein máu có thể dẫn đến bất thường chức năng tiểu cầu, và do đó gây BT kéo dài. |
|
Các bất thường chức năng tiểu cầu mắc phải khác như trong thiếu máu và rối loạn sinh tuỷ, tăng sinh tuỷ cũng có thể có BT kéo dài. |
|
|
Von Willebrand Disease (VWD) |
Thiếu vWF có thể làm BT kéo dài nhưng không phải tất cả các trường hợp. BT không được khuyến nghị sử dụng trong chẩn đoán VWD. |
|
Thiếu máu nặng |
Bệnh nhân có thiếu máu sẽ có thay đổi trong phân bố tiểu cầu và giảm tương tác của tiểu cầu với tế bào nội mô thành mạch, kết quả là BT kéo dài. Điều trị thiếu máu sẽ làm BT trở về bình thường. |
|
Thiếu Fibrinogen |
Fibrinogen cần cho tương tác giữa tiểu cầu và tiểu cầu, và do vậy BT sẽ kéo dài khi Fibrinogen giảm. |
Câu hỏi 2: Bất thường nào có thể giải thích tình trạng máu chảy kéo dài?
Xét nghiệm BT bị ảnh hưởng bởi rất nhiều yếu tố (tất nhiên đã loại trừ nguyên nhân kỹ thuật) như số lượng và chất lượng tiểu cầu, nồng độ và chất lượng yếu tố vWF và khi có bất thường lớp collagen/nội mô thành mạch. Bệnh nhân sử dụng thuốc kháng tiểu cầu sẽ có BT kéo dài. Bởi vì có rất nhiều yếu tố khách quan và chủ quan ảnh hưởng tới kỹ thuật này, do đó hiện nay tại UK, xét nghiệm máu chảy không còn được khuyến nghị sử dụng.
Câu hỏi 3: Bạn cần thêm xét nghiệm gì?
Trong bối cảnh BT kéo dài, sẽ hợp lý nếu bạn kiểm tra công thức máu, số lượng tiểu cầu và xét nghiệm FVIII, vWF. Hơn nữa, các câu hỏi tiền sử và phả hệ gia đình nên được xây dựng để tìm hiểu chẩn đoán.
Câu hỏi 4: Các xét nghiệm trên gợi ý điều gì?
Dữ liệu cho thấy APTT kéo dài và giảm FVIII, vWF kháng nguyên và hoạt tính. Trong trường hợp này, chẩn đoán là VWD type I, loại này chiếm khoảng 80% các trường hợp VWD.
Câu hỏi 5: Các xét nghiệm này có thể giải thích tại sao thời gian máu chảy kéo dài không?
Có. Thiếu VWF có nghĩa là tiểu cầu không thể gắn vào vị trí tổn thương thành mạch, do đó làm thời gian máu chảy kéo dài.
Câu hỏi 6: Bạn cần thêm xét nghiệm gì?
a/Nhóm máu b/ Phân tích phả hệ gia đình để tìm các thành viên cùng bị bệnh. c/ Phân tích di truyền để xác định đột biến gen VWF.
d/Thử nghiệm điều trị DDAVP để quan sát đáp ứng với DDAVP. Trong trường hợp đáp ứng kém với DDAVP, có thể là biến thể của VWF như biến thể Vicenza. Trong trường hợp này, định lượng VWF bằng phương pháp VWF:pp sẽ có giá trị chẩn đoán, mặc dù hiện nay phương pháp này không được sử dụng rộng rãi. Xét nghiệm gen sẽ giúp giải quyết vấn đề.
Câu hỏi 7: Xét nghiệm máu chảy có thường xuyên được thực hiện hay không?
Không. Xét nghiệm BT bị ảnh hưởng bởi rất nhiều yếu tố (tất nhiên đã loại trừ nguyên nhân kỹ thuật) như số lượng và chất lượng tiểu cầu, nồng độ và chất lượng yếu tố vWF và khi có bất thường lớp collagen/nội mô thành mạch. Bệnh nhân sử dụng thuốc kháng tiểu cầu sẽ có BT kéo dài. Bởi vì có rất nhiều yếu tố khách quan và chủ quan ảnh hưởng tới kỹ thuật này, do đó hiện nay tại UK, xét nghiệm máu chảy không còn được khuyến nghị sử dụng.
Sẹo tại vị tri máu chảy có thể xảy ra và bệnh nhân cần được giải thích về hiện tượng này. Vì lý do này nên BT rất hiếm được thực hiện ở trẻ em.
|
Tóm tắt: Đây là trường hợp thời gian máu chảy kéo dài do Type I VWD |
Case 53
Bệnh nhân nam 56 tuổi có tiền sử COPD (Chronic Obstructive Pulmonary Disease) kéo dài được nhập viện để phẫu thuật.
Xét nghiệm trước mổ của ông ta cho kết quả Hb 190 g/L và Hct là 0.58.
Kết quả PT và APTT như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
20 s |
11 – 14 s |
|
APTT |
47 s |
23 – 35 s |
Câu hỏi 1: Giải thích các kết quả trên như thế nào?
Câu hỏi 2: Bạn đưa ra lời khuyên nào?
Đáp án
Câu hỏi 1: Giải thích các kết quả trên như thế nào?
Bệnh nhân này có tăng Hb và Hct, và đây là giải thích hợp lý nhất cho tình trạng kéo dài PT và APTT. Khi bệnh nhân có Hct cao được lấy máu xét nghệm vào ống chống đông Citrat để làm xét nghiệm PT và APTT, lượng plasma thu được ít hơn so với bình thường, do vậy nồng độ citrat trong mẫu huyết tương bệnh nhân cao hơn so với trường hợp bệnh nhân có Hct bình thường. Khi huyết tương được phục hồi canxi trong xét nghiệm PT và APTT, chỉ một phần calci được phục hồi do vì nồng độ citrat cao và do đó thời gian đông máu kéo dài.
Câu hỏi 2: Bạn đưa ra lời khuyên nào?
Vấn đề sẽ được giải quyết bằng cách điều chỉnh lượng chống đông citrat trong ống xét nghiệm trước khi lấy mẫu cho bệnh nhân này.
|
Tóm tắt: Đây là trường hợp PT và APTT kéo dài giả tạo do tăng Hct |
Case 54
Bệnh nhân nữ 45 tuổi biểu hiện DVT cẳng chân trái tư phát. Bà ta được điều trị thuốc chống đông Heparin trọng lượng phân tử thấp (LMWH) và sau đó là Warfarin để duy trì INR khoảng 2.5.
Thời gian ngắn sau sử dụng Warfarin, bệnh nhân bị bầm tím và 5 tuần sau điều trị Warfarin, bệnh nhân có tụ máu lớn ở bắp chân phải. Xét nghiệm của bệnh nhân như sau (trước khi dùng chống đông, PT-APTT và Fib bình thường).
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
INR |
2.3 |
1.0 |
|
APTT |
117 s |
28 – 34.5 s |
|
Fib (Clauss) |
3.9 g/L |
2 – 4 g/L |
|
Hemoglobin |
122 g/L |
135 – 162 g/L |
|
Tiểu cầu |
298 x 109/L |
150 -400 x 109/L |
Câu hỏi 1: Bạn sẽ chỉ định thêm xét nghiệm gì và tại sao?
Chức năng gan của bệnh nhân bình thường. Không có tiền sử gia đình hoặc tiền sử của bệnh nhân về các bệnh lý rối loạn chảy máu.
Bạn yêu cầu xét nghiệm yếu tố đông máu và có kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân (U/dL) |
Dải tham chiếu |
|
FVIII |
120 |
50 – 150 |
|
FIX |
50 – 150 |
|
|
FXI |
83 |
50 – 150 |
|
FXII |
112 |
50 – 150 |
|
FX |
23 |
50 – 150 |
Câu hỏi 2: Bạn giải thích các kết quả trên như thế nào?
Câu hỏi 3: Bạn sẽ chỉ định thêm xét nghiệm gì?
Kết quả sàng lọc kháng thể kháng FIX âm tính.
Phân tích gen F9 ở bệnh nhân xác định đột biến (Ala-10Thr) tại vị trí Ala-10 trong propeptide của FIX.
Câu hỏi 4: Nhận xét các kết quả trên?
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Câu hỏi 6: Bạn sẽ chỉ định thêm xét nghiệm gì và tại sao?
Đáp án
Câu hỏi 1: Bạn sẽ chỉ định thêm xét nghiệm gì và tại sao?
APTT kéo dài không cân xứng với INR gợi ý các bất thường liên quan tới yếu tố VIII, IX, XI, XII. Bởi vì PT và APTT bình thường trước khi bệnh nhân sử dụng thuốc chống đông cho nên đây là một bất thường mắc phải (tất cả bệnh nhân muốn bắt đầu sử dụng thuốc chống đông đều cần được làm xét nghiệm PT, APTT và Fib).
Bạn nên chỉ định:
Xét nghiệm Mixtest 50:50 với huyết tương bình thường để loại trừ chất ức chế và kháng đông Lupus.
Xét nghiệm yếu tố VIII, IX, XI, XII. Thiếu hụt yếu tố XII thường không có biểu hiện chảy máu trên lâm sàng nhưng trong thực hành vẫn nên xét nghiệm yếu tố này.
Bạn nên xét nghiệm chức năng gan để chắc chắn rằng chức năng gan bình thường.
Sẽ có giá trị nếu bạn xét nghiệm một trong các yếu tố phụ thuộc vitamin K như yếu tố X.
Xác định xem liệu có bất kỳ tiền sử bệnh nhân hoặc tiền sử gia đình gợi ý các bệnh lý chảy máu hay không?
Câu hỏi 2: Bạn giải thích các kết quả trên như thế nào?
Bệnh nhân có giảm yếu tố IX và đặc biệt yếu tố X (là một yếu tố phụ thuộc vitamn K) cũng giảm.
Đây có thể là bệnh nhân có chất ức chế yếu tố IX mặc dù tình huống này rất hiếm gặp. Có vẻ phù hợp hơn trong tình huống giảm yếu tố IX ở bệnh nhân bắt đầu sử dụng thuốc kháng vitamin K như Warfarin là có đột biến trên gen F9.
Câu hỏi 3: Bạn sẽ chỉ định thêm xét nghiệm gì?
Phân tích đột biến gen F9.
Câu hỏi 4: Nhận xét các kết quả trên?
Đột biến Ala-10Thr trên gen F9 gây trở ngại cho vị trí nhận dạng gammaglutamylcarboxylase – enzyme tham gia vào quá trình carboxylation của acid glutamic của các yếu tố phụ thuộc vitamin K. Trong trường hợp có đột biến Ala-10Thr, dẫn tới giảm gắn với enzyme carboxylase, làm cho yếu tố IX nhạy cảm hơn với Warfarin. Do vậy, nồng độ FIX đo được sẽ giảm hơn so với nồng độ các yếu tố phụ thuộc vitamin K khác.
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Có nhiều cách:
Bạn nên quay lại sử dụng LMWH ở bệnh nhân này.
Bạn có thể chuyển sang sử dụng DOAC.
|
Tóm tắt: Đây là trường hợp thiếu hụt FIX mắc phải do đột biến gen F9 (Ala-10Thr) dân đến giảm yếu tố IX không tương ứng khi sử dụng Warfarin. |
Case 55
Bệnh nhân nam 57 tuổi không có tiền sử đặc biệt, cần được thay van động mạch chủ. Ông ta được sàng lọc đông máu trước mổ cho kết quả như sau:
| Xét ngiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
13 s |
11 -14 s |
|
APTT |
>120 s |
28 – 34.5 s |
|
Fib (Clauss) |
3.9 g/L |
2 – 4 g/L |
|
Thrombin time |
14 s |
11.5 – 13.5 s |
|
Tiểu cầu |
358 x 109/L |
150 -400 x 109/L |
Câu hỏi 1: Bạn sẽ làm gì tiếp theo?
Bạn sử dụng các câu hỏi về tiền sử chảy máu nhưng không phát hiện gì bất thường. Bệnh nhân đã được làm các thủ thuật nha khoa nhiều lần nhưng không có vấn đề gì xảy ra.
APTT về bình thường trong xét nghiệm Mixtest.
Yếu tố VIII, IX, XI bình thường.
Câu hỏi 2: Chẩn đoán có thể là gì?
Bệnh nhân có yếu tố XII
Câu hỏi 3: Bác sĩ phẫu thuật yêu cầu các điều trị cần thiết cho bệnh nhân thiếu hụt yếu tố XII trong trường hợp bệnh nhân phải phẫu thuật tim. Bạn sẽ điều trị như thế nào?
Câu hỏi 4: Bác sĩ gây mê yêu cầu bạn tư vấn về sử dụng Heparin khi bệnh nhân sử dụng tuần hoàn ngoài cơ thể và liệu họ có thể sử dụng xét nghiệm ACT để theo dõi đông máu và điều chỉnh liều Heparin hay không?
Đáp án
Câu hỏi 1: Bạn sẽ làm gì tiếp theo?
Bệnh nhân có APTT không đông nhưng không có tiền sử y tế nào liên quan.
Có 2 khả năng có thể xảy ra:
Nguyên nhân APTT kéo dài mới xuất hiện trong thời gian gần đây.
APTT kéo dài không liên quan tới các biểu hiện chảy máu trên lâm sàng. Điều quan trọng là xác định xem có các bất thường chảy máu đáng chú ý trong tiền sử không, do vậy bộ câu hỏi về chảy máu Quantitative Bleeding Questionaire nên được sử dụng.
Bạn nên xác định xem APTT có trở về bình thường trong xét nghiệm Mixtest hay không. Nếu có thì xét nghiệm yếu tố VIII, IX, XI, XII nên được thực hiện. Nếu APTT không về bình thường ở xét nghiệm Mixtest thì các xét nghiệm sàng lọc chất ức chế và kháng đông Lupus nên được thực hiện.
Câu hỏi 2: Chẩn đoán có thể là gì?
Chẩn đoán có thể có lý nhất là thiếu hụt FXII do vậy xét nghiệm định lượng yếu tố XII nên được thực hiện.
Câu hỏi 3: Bác sĩ phẫu thuật yêu cầu các điều trị cần thiết cho bệnh nhân thiếu hụt yếu tố XII trong trường hợp bệnh nhân phải phẫu thuật tim. Bạn sẽ điều trị như thế nào?
Bạn cần khẳng định với bác sĩ phẫu thuật rằng bệnh nhân sẽ không chảy máu do thiếu hụt yếu tố XII và do vậy bệnh nhân không cần truyền thay thế FXII.
Câu hỏi 4: Bác sĩ gây mê yêu cầu bạn tư vấn về sử dụng Heparin khi bệnh nhân sử dụng tuần hoàn ngoài cơ thể và liệu họ có thể sử dụng xét nghiệm ACT để theo dõi đông máu và điều chỉnh liều Heparin hay không?
Kiểm soát đông máu khi sử dụng tuần hoàn ngoài cơ thể sẽ khó khăn bởi vì ACT đã kéo dài trước khi sử dụng Heparin. Trong trường hợp này bạn cần kiểm soát đông máu bằng xét nghiệm antiXa. Việc này cần sự phối hợp chặt chẽ giữa bác sĩ phẫu thuật/gây mê và khoa xét nghiệm. Mức AntiXa >4.0 U/mL là cần thiết chứng tỏ lượng chống đông sử dụng là phù hợp.
|
Tóm tắt: Đây là trường hợp APTT kéo dài do thiếu hụt nặng FXII với gợi ý theo dõi đông máu khi sử dụng tuần hoàn ngoài cơ thể. |
Case 56
Bệnh nhân nam 67 tuổi nhập khoa điều trị mạch vành do đau thắt ngực. Bệnh nhân được nong mạch vành cấp cứu và được sử dụng 5000 đơn vị Unfractionated Heparin và Abciximab để dự phòng tái tắc mạch vành. 3 ngày sau thủ thuật, bệnh nhân có bầm tím và tiểu cầu đếm được là 5 x 109/L (khi nhập viện, tiểu cầu là 189 x 109/L). Các chỉ số khác của công thức máu bình thường.
Câu hỏi 1: Nguyên nhân giảm tiểu cầu là gì?
Câu hỏi 2: Bạn sẽ điều trị bệnh nhân này như thế nào?
Câu hỏi 3: Cơ chế giảm tiểu cầu trong trường hợp này?
Câu hỏi 4: Abciximab là gì?
Đáp án
Câu hỏi 1: Nguyên nhân giảm tiểu cầu là gì?
Trường hợp này, cần chẩn đoán phân biệt giảm tiểu cầu cho Abciximab hay do Heparin (HIT). HIT có vẻ không phù hợp vì bệnh nhân mới dùng liều Heparin duy nhất ngay cả nếu bệnh nhân đã có tiền sử của HIT. Trong thực hành, hầu hết các bác sĩ lâm sàng sẽ sàng lọc HIT và tránh sử dụng tiếp UFH. Do đó chẩn đoán là giảm tiểu cầu do Abciximab.
Điều quan trọng là cần loại trừ giảm tiểu cầu giả bằng phân tích lam máu ngoại vi.
Câu hỏi 2: Bạn sẽ điều trị bệnh nhân này như thế nào?
Truyền tiểu cầu, cần truyền 4 – 5 ngày tới khi vấn đề giảm tiểu cầu được giải quyết.
Câu hỏi 3: Cơ chế giảm tiểu cầu trong trường hợp này?
Bệnh nhân này bị giảm tiểu cầu do Abciximab. Điều này là do sự xuất hiện kháng thể anti-chimeric người. Ở một số bệnh nhân, kháng thể xuất hiện tự nhiên và gắn với các tiểu cầu gắn Abciximab, kết quả làm tăng phá huỷ tiểu cầu tại lách, gây giảm tiều cầu. Trong một số trường hợp khác, kháng thể xuất hiện sau điều trị Abciximab và thường xuất hiện trong vòng 30 ngày kể từ liều đầu tiên.
Tỉ lệ gặp giảm tiểu cầu nặng (9/L) sau sử dụng Abciximab khoảng 0.3 – 0.69% sau liều đầu tiên, 1-2% nếu bệnh nhân dùng lần thứ 2 và cao hơn nếu bệnh nhân dùng trong 2 tuần.
Điển hình, tiểu cầu sẽ giảm sau 2 – 4 h sau khi bắt đầu điều trị và cần 5 – 10 ngày để giải quyết vấn đề này.
Chất ức chế GpIIb/IIIa gắn với thụ thể trền bề mặt tiểu cầu và tạo nên các vị trí gắn phối tử. So với bình thường, thì việc thêm chất ức chế GpIIb/IIIa có thể dẫn đến mở rộng vị trí gắn phối tử, làm tăng phá huỷ tiểu cầu.
Câu hỏi 4: Abciximab là gì?
Abciximab là một kháng thể đơn dòng lai giữa chuột và người, ức chế GpIIb/IIIa và là một trong các chất ức chế thụ thể GpIIb/IIIa. Tuy nhiên Eptifibatide và Tirofiban là phân tử chống thụ thể tổng hợp. Nó ngăn cản Fib, vWF và các phân tử khác gắn vào tiểu cầu.
|
Tóm tắt: Đây là trường hợp giảm tiểu cầu do Abciximab |
Case 57
Bệnh nhân nam 64 tuổi đến khám bác sĩ gia đình vì dễ bị bầm tím và chảy máu cam nhiều lần. Bệnh nhân không sử dụng loại thuốc gì mới và không có tiền sử nào gợi ý các bất thường chảy máu. Khám lâm sàng không có gì đặc biệt ngoài tiếng thổi tâm thu phù hợp với hẹp động mạch chủ.
Bệnh nhân được làm công thức máu và đông máu cơ bản cho kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
12 s |
11 -14 s |
|
APTT |
33 s |
28 – 34.5 s |
|
Fib (Clauss) |
3.6 g/L |
2 – 4 g/L |
|
Thrombin time |
14 s |
11.5 – 13.5 s |
|
Tiểu cầu |
314 x 109/L |
150 -400 x 109/L |
|
Hb |
112 g/L |
115 – 155 g/L |
|
WBC |
7.6 x 109/L |
5 -16 x 109/L |
Câu hỏi 1: Nhận xét các kết quả xét nghiệm trên?
Câu hỏi 2: Các xét nghiệm nào sẽ có giá trị để chẩn đoán tình trạng của bệnh nhân này?
Bạn yêu cầu thêm một số xét nghiệm và có kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
FVIII |
89 IU/dL |
57 – 141 IU/dL |
|
VWF: Ag |
75 IU/dL |
50 – 150 IU/dL |
|
VWF: RCo |
38 IU/dL |
50 – 150 IU/dL |
|
PFA100 (Collagen:ADP) |
155 s |
Câu hỏi 3: Nhận xét các kết quả xét nghiệm trên?
Câu hỏi 4: Bạn cần thêm những xét nghiệm gì?
Bạn chỉ định xét nghiệm VWF multimers – xét nghiệm này xác định mất multimers trọng lượng phân tử cao.
Câu hỏi 5: Chẩn đoán là gì và bạn điều trị bệnh nhân này như thế nào?
Đáp án
Câu hỏi 1: Nhận xét các kết quả xét nghiệm trên?
Các xét nghiệm ban đầu không phát hiện bất thường. Tuy nhiên trong bệnh cảnh bệnh nhân có bầm tím dễ dàng và chảy máu cam tái đi tái lại trong thời gian gần đây gợi ý các bất thường chảy máu mắc phải. Tiền sử của bệnh nhân gợi ý bất thường chắc năng tiểu cầu hoặc bệnh lý VWD.
Câu hỏi 2: Các xét nghiệm nào sẽ có giá trị để chẩn đoán tình trạng của bệnh nhân này?
Các xét nghiệm sau sẽ có giá trị để chẩn đoán bệnh:
a/Chức năng tiểu cầu, phương pháp LTA hoặc trở kháng.
b/Xét nghiệm yếu tố VIII và yếu tố VWF. Xét nghiệm APTT ở hầu hết các labo sẽ bình thường nếu nông độ FVIII, IX, XI hoặc XII > 40 IU/dL.
Câu hỏi 3: Nhận xét các kết quả xét nghiệm trên?
FVIII trong giới hạn bình thường nhưng VWF: Rco giảm, hơn nữa PFA-100 kéo dài. Các kết quả này gọi ý VWD và trong hoàn cảnh các triệu chứng mới xuất hiện gần đây, nên đây là hội chứng von Willebrand mắc phải (AVWS).
Câu hỏi 4: Bạn cần thêm những xét nghiệm gì?
Bạn cần:
a/Lặp lại xét nghiệm FVIII và VWF.
b/Lặp lại xét nghiệm PFA-100 để khẳng định khiếm khuyết chức năng tiểu cầu.
Khi nghi ngờ hội chứng von Willebrand mắc phải, bạn nên chỉ định các xét nghiệm:
a/ Điện di protein huyết thanh và Ig.
b/Chức năng gan thận
c/Công thức máu, để loại trừ các bệnh lý rối loạn tăng sinh tuỷ
d/Điện tim để đánh giá triệu chứng thổi tâm thu trên lâm sàng
e/Xem xét khả năng bệnh tự miễn và chất ức chế vWF.
Câu hỏi 5: Chẩn đoán là gì và bạn điều trị bệnh nhân này như thế nào?
Kết quả xét nghiệm VWF multimers phù hợp với VWD type 2 (nhưng không phải type 2M).
Chẩn đoán là bệnh von Willebrand type 2 mắc phải. Phần quan trọng trong tiền sử và khám lâm sàng là các triệu chứng mới xuất hiện và phát hiện hẹp động mạch chủ.
Bệnh VWD type 2 mắc phải đã được báo cáo trên nhiều bệnh nhân hẹp động mạch chủ (NEJM 2003;349:343-349). Chúng xuất hiện do áp lực máu tăng qua van động mạch chủ dẫn đến thay đổi hình dạng yếu tố vWF, làm cho vWF dễ bị cắt bởi ADAMTS13, kết quả là mất các multimers trọng lượng phân tử cao. Vấn đề chảy máu sẽ được giải quyết khi bệnh nhân được thay van động mạch chủ.
Hội chứng Heyde’s là hội chứng chảy máu đường tiêu hoá do chảy máu ở các thương tổn mạch máu nhỏ tại ruột (Angiodysplastic) trong bệnh cảnh hẹp động mạch chủ.
|
Tóm tắt: Đây là trường hợp hội chứng von Willebrand mắc phải do hẹp động mạch chủ. |
Case 58
Bệnh nhân nam 47 tuổi nhập viện khoa cấp cứu với triệu chứng dễ bầm tím trong vòng 2 tuần và gần gây chảy máu cam lâu cầm. Tiền sử y khoa của bệnh nhân không có gì đặc biệt. Anh ta không sử dụng thuốc gì mới và tiền sử gia đình không có gì đáng chú ý.
Bệnh nhân được làm xét nghiệm cộng thức máu và đông máu cho kết quả như sau:
| Xét ngiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
15.9 s |
11 -14 s |
|
APTT |
41.3 s |
28 – 34.5 s |
|
Fib (Clauss) |
0.6 g/L |
2 – 4 g/L |
|
D dimer |
>60.000 ng/mL |
0 -230 ng/mL |
|
Tiểu cầu |
14 x 109/L |
150 -400 x 109/L |
|
Hb |
72 g/L |
115 – 155 g/L |
|
WBC |
276 x 109/L |
5 -16 x 109/L |
Câu hỏi 1: Nhận xét các kết quả trên?
Câu hỏi 2: Bạn cần chỉ định thêm các xét nghiệm gì?
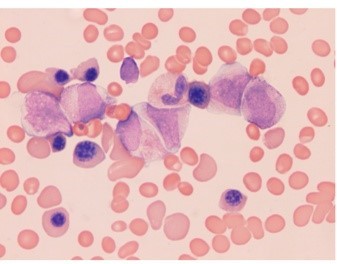
Bạn chỉ định xét nghiệm huyết đồ cấp và có hình ảnh lam máu như sau:
Câu hỏi 3: Nhận xét hình ảnh lam máu trên?
Câu hỏi 4: Tại sao bệnh nhân bị chảy máu?
Đáp án
Câu hỏi 1: Nhận xét các kết quả trên?
Kết quả cho thấy WBC tăng cao và PT/APTT kéo dài, Fib giảm, D dimer tăng gợi ý có thể bệnh nhân bị DIC.
Câu hỏi 2: Bạn cần chỉ định thêm các xét nghiệm gì?
Cần phân tích lam máu ngoại vi để đánh giá tình trạng tăng bạch cầu.
Câu hỏi 3: Nhận xét hình ảnh lam máu trên?
Lam máu ngoại vi phù hợp với chẩn đoán Bạch cầu cấp thể tiền tuỷ bào (M3). Phân tích di truyền sau khẳng định PML-RARa do chuyển đoạn t(15;17).
Câu hỏi 4: Tại sao bệnh nhân bị chảy máu?
Khác với bệnh lý đông máu liên quan tới DIC, rối loạn đông máu trong Bạch cấu cấp tiền tuỷ bào (APML) do tăng tiêu sợi huyết.
Cơ chế do:
Yếu tố mô (Tissue Factor) bộc lộ trên tế bào bạch cầu non
Yếu tố tiền đông ung thư – một cysteine tiền đông được phát hiện trên tế bào bạch cầu non, có thể hoạt hoá yếu tố X một cách độc lập với yếu tố VIIa.
Tăng biểu hienj của Annexin (A2I) trên bề mặt tế bào non APL, có thể tác động như một thụ thể bề mặt cho plasminogen và t-PA và do đó điều hoà tiêu sợi huyết.
Elatase, Cathepsin-G và proteinase-3 có mặt trong hạt của tế bào non APL và có thể giáng hoá trưc tiếp nhiều yếu tố đông máu bao gồm Fib, vWF và alpha-2 anti plasmin.
Tăng biểu hiện của uPA, tPA, thụ thể uPAR trên tế bào non APML.
|
Tóm lại: Đây là trường hợp tăng tiêu sự huyết thứ phát do APML. |
Case 59
Bệnh nhân nam 57 tuổi được chuyển tới ITU (Intensive Therapy Unit) sau phẫu thuật bắc cầu động mạch vành. Bệnh nhân có xét nghiệm thường qui sau mổ cho kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
11 s |
11 -14 s |
|
APTT |
34 s |
28 – 34.5 s |
|
Fib (Clauss) |
2.2 g/L |
2 – 4 g/L |
|
Thrombin time |
>120 s |
11.5 – 13.5 s |
|
Tiểu cầu |
187 x 109/L |
150 -400 x 109/L |
Câu hỏi 1: Nguyên nhân giải thích cho các kết quả trên?
Câu hỏi 2: Bạn cần thêm xét nghiệm gì?
Bạn lặp lại xét nghiệm Thrombin time và có kết quả TT = 110s. Bạn chỉ định xét nghiệm Reptilase time, có kết quả bình thường (13s).
24 h sau bạn lặp lại xét nghiệm TT, có kết quả TT >60s. Bệnh nhân này không sử dụng Heparin và mẫu bệnh phẩm không được lấy từ đường ven có Heparin.
Câu hỏi 3: Bạn có thể giải thích cho các kết quả trên như thế nào?
Câu hỏi 4: Bạn cần thêm xét nghiệm gì?
Bạn lặp lại xét nghiệm TT nhưng sử dụng Thrombin người (mà không phải Thrombin bò) và có kết quả TT bình thường.
Câu hỏi 5: Bạn giải thích hiện tượng trên như thế nào?
Đáp án
Câu hỏi 1: Nguyên nhân giải thích cho các kết quả trên?
Bệnh nhân này có trải qua gia đoạn sử dụng tuần hoàn ngoài cơ thể (CPB), cho nên có sử dụng UFH. Heparin này tồn dư sau giai đoạn phẫu thuật, và có thể được trung hoà bằng Protamin Sulphate. Thrombin time rất nhạy cảm với UFH, và việc TT kéo dài có khả năng do UFH vẫn tồn tại và lượng Protamin Sulphate sử dụng để trung hoà UFH sau mổ không đủ. Tuy nhiên APTT bình thường và mặc dù không nhạy cảm với UFH như TT nhưng điều này gợi ý rằng UFH không phải là giải thích hợp lý cho hiện tượng TT kéo dài. Fibrinogen bình thường, loại trừ nguyên nhân TT kéo dài do giảm Fib.
Câu hỏi 2: Bạn cần thêm xét nghiệm gì?
Lặp lại xét nghiệm TT. Liệu mẫu bệnh phẩm có phải đã được lấy từ đường truyền có Heparin hay không? Rất phù hợp nếu bạn chỉ định làm thời gian Reptilase. Reptilase time sẽ bình thường nếu UFH là nguyên nhân làm TT kéo dài.
Câu hỏi 3: Bạn có thể giải thích cho các kết quả trên như thế nào?
TT vẫn kéo dài 24h sau khi ngừng CPB. Khả năng còn tồn dư UFH có vẻ không đúng. Quan trọng là chắc chắn mẫu bệnh phẩm không được lấy từ đường truyền có Heparin. Hơn nữa, APTT bình thường khi bệnh nhân ngừng CPB, do vậy nguyên nhân do UFH có vẻ không phù hợp. Hơn nữa, Fib bình thường nên TT dài do giảm Fib bị loại trừ.
Câu hỏi 4: Bạn cần thêm xét nghiệm gì?
Các dữ liệu cho thấy vấn đề có thể nằm ở xét nghiệm TT, do vậy cần lặp lại xét nghiệm này. TT nên được lặp lại trên thuốc thử khác.
Câu hỏi 5: Bạn giải thích hiện tượng trên như thế nào?
TT sử dụng Thrombin bò kéo dài là do bệnh nhân có kháng thể anti-bovine. Kháng thể này có thể xuất hiện tự nhiên hoặc sau phơi nhiễm với thrombin bò. Bệnh nhân cần được theo dõi sự có mặt UFH bằng xét nghiệm TT sử dụng Thrombin người.
|
Tóm tắt: Đây là trường hợp xét nghiệm Thrombin time dài đơn độc do sự có mặt của kháng thể anti-bovine. |
Case 60
Bệnh nhân nữ 56 tuổi nhập viện khoa cấp cứu và tai nạn do chồng cô phát hiện cô bị lơ mơ, lú lẫn tại nhà.
Xét nghiệm ban đầu có kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
14 s |
11 -14 s |
|
APTT |
35 s |
28 – 34.5 s |
|
Fib (Clauss) |
2.1 g/L |
2 – 4 g/L |
|
Thrombin time |
14 s |
11.5 – 13.5 s |
|
Hb |
86 g/L |
115 – 135 g/L |
|
Tiểu cầu |
23 x 109/L |
150 -400 x 109/L |
|
WBC |
11.2 x 109/L |
6 – 10 x 109/L |
|
LDH |
2342 U/L |
|
|
Creatinin |
356µmol/L |
52 – 90 µmol/L |
Câu hỏi 1: Bạn cần thêm những xét nghiệm gì?
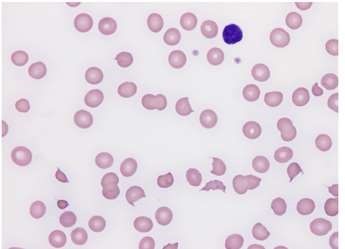
Bạn yêu cầu phân tích huyết đồ và có hình ảnh như sau:
Câu hỏi 2: Hình ảnh trên gợi ý điều gì?
Câu hỏi 3: Chẩn đoán có thể là gì?
Câu hỏi 4: Những thông tin gì bạn cần hỏi thêm và thảo luận với chồng của bệnh nhân?
Câu hỏi 5: Bạn nghĩ tới chẩn đoán Thrombotic Thrombocytopenic Purpura (TTP). Xét nghiệm gì có thể giúp chẩn đoán bệnh này?
Bạn chỉ định xét nghiệm ADAMTS13 và kết quả như sau:
| Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
ADAMTS13 Act |
66 – 126 % |
|
|
IgG Anti- ADAMTS13 |
85% |
Câu hỏi 6: Nhận xét kết quả trên?
Đáp án
Câu hỏi 1: Bạn cần thêm những xét nghiệm gì?
Dựa vào tiền sử, kết quả xét nghiệm có tăng LDH, Creatinin và giảm tiểu cầu, xét nghiệm huyết đồ cần được chỉ định.
Câu hỏi 2: Hình ảnh trên gợi ý điều gì?
Lam máu ngoại vi có hình ảnh mảnh vỡ hồng cầu.
Câu hỏi 3: Chẩn đoán có thể là gì?
Triệu chứng lâm sàng, kết quả xét nghiệm có tăng LDH, Creatinin và giảm tiểu cầu, mảnh vỡ hồng cầu trên lam máu ngoại vi gợi ý chẩn đoán là TTP (Thrombotic Thrombocytopenic Purpura).
Câu hỏi 4: Những thông tin gì bạn cần hỏi thêm và thảo luận với chồng của bệnh nhân?
Bạn nên thảo luận với gia đình liệu bệnh nhân có sử dụng thuốc gì mới gần đây, xem xét khả năng bệnh nhân có thai, bị HIV hoặc nguyên nhân khác gây TTP.
TTP bẩm sinh do đột điến trên gen ADAMTS13 có thể biểu hiện lần đầu tiên ở tuổi trưởng thành.
Câu hỏi 5: Bạn nghĩ tới chẩn đoán Thrombotic Thrombocytopenic Purpura (TTP). Xét nghiệm gì có thể giúp chẩn đoán bệnh này?
Bạn nên chỉ định xét nghiệm ADAMTS13 cấp cứu cùng với sàng lọc chất ức chế. Nếu ADAMTS13 thấp và xét nghiệm chất ức chế âm tính thì cần giải trình tự gen ADAMTS13 để loại trừ đột biến.
Câu hỏi 6: Nhận xét kết quả trên?
Kết quả sàng lọc ADAMTS13 phù hợp với chẩn đoán TTP do chất ức chế của ADAMTS13.
|
Tóm tắt: Đây là trường hợp bệnh nhân Thrombotic Thrombocytopenic Purpurav(TTP) do có mặt tự kháng thể chống ADAMTS13. |
Case 61
Câu hỏi 1: Giải thích ngắn gọn nguyên lý của xét nghiệm ACT (Activated Clotting Time) và Thrombin Time (TT).
Câu hỏi 2: Các yếu tố ảnh hưởng tới xét nghiệm ACT?
Câu hỏi 3: Các yếu tố ảnh hưởng tới xét nghiệm TT?
Câu hỏi 4: Tại sao chúng ta sử dụng xét nghiệm ACT mà không phải là TT để kiểm soát bệnh nhân dùng tuần hoàn ngoài cơ thể?
Đáp án
Câu hỏi 1: Giải thích ngắn gọn nguyên lý của xét nghiệm ACT (Activated Clotting Time) và Thrombin Time (TT).
ACT (Activated Clotting Time) là xét nghiệm đông máu tại chỗ cần thiết trong kiểm soát điều trị UFH ở bệnh nhân phẫu thuật có dùng tuần hoàn cơ thể, ECMO (extracorporeal membrane oxygenation), nong mạch vành qua da, lọc máu hoặc chạy thận nhân tạo.
Trong những ngày đầu sử dụng tuần hoàn ngoài cơ thể (CPB), liều heparin được sử dụng để ngăn chặn cục đông trong vòng tuần hoàn ngoài cơ thể theo kinh nghiệm – thường là liều thấp nhất để cục máu đông không xuất hiện. Thời gian ACT tối thiểu an toàn là
Trong hầu hết các trường hợp CPB- liều Heparin dao động từ 300 – 400 IU/kg trước thực hiện CPB cộng với liều bolus khi cần duy trì ACT >400s. Xét nghiệm ACT rất hữu ích cho theo dõi UFH khi heparin là biến thể duy nhất, nhưng khi có cả các biến thể khác thì nó trở nên không đặc hiệu với Heparin.
Xét nghiệm ACT lần đầu tiên được sử dụng trong lâm sàng giữa những năm 1970 để hướng dẫn sử dụng cũng như trung hoà Heparin trong phẫu thuật có tuần hoàn ngoài cơ thể. Mặc dù ban đầu ACT được sử dụng như một xét nghiệm sàng lọc thường qui trước mổ, ngày nay nó được sử dụng chủ yếu để theo dõi bệnh nhân dùng CPB.
Máu tươi toàn phần được thêm vào ống nghiệm có chứa chất hoạt hoá bề mặt (ban đầu là celite, nhưng những chất khác như kaolin, bóng thuỷ tinh cũng thường được sử dụng) – kết quả là hoạt hoá đông máu theo con đường nội sinh . Nguyên thuỷ, ống xét nghiệm sẽ được ủ ở 37ºC trong 60s, lấy ra và nghiêng 5s một lần đến khi hình thành cục đông. Thời gian để cục đông hình thành được gọi là thời gian ACT. Xét nghiệm ngày nay thường được thực hiện sử dụng phương pháp tự động hoàn toàn trong đó điểm đông được tự động ghi lại – tuy nhiên nguyên lý vẫn giữ nguyên. Xét nghiệm được thực hiện ngay lập tức trên máu toàn phần và bệnh phẩm không thể lưu lại sau xét nghiệm.
Thrombin time (TT) cần thêm Thrombin người hoặc bò vào huyết tương nghèo tiểu cầu. Thrombin sẽ chuyển Fibrinogen thành Fibrin nhưng cũng nhạy cảm với sự có mặt của các chất ức chế đông máu, ví dụ Heparin.
Thrombin sẽ chẻ Fibrinogen, tạo nên các fibrinpeptide A (FpA) và fibrinpeptideB (FpB). Sản phẩm ban đầu, fibrinpeptide A(FpA) được tách từ fibrin sau amino acid 16 và đôi khi là sau acid amin 19, trong khi sản phẩm thứ 2 fibrinpeptide B (FpB) được chẻ ra tại acid min 14.
Câu hỏi 2: Các yếu tố ảnh hưởng tới xét nghiệm ACT?
|
Số lượng và chức năng tiểu cầu |
ACT sẽ kéo dài trong trường hợp tiểu cầu giảm khi TC 9/L. Aspirin và Clopidogrel có nhiều ảnh hưởng rất khác nhau lên xét nghiệm ACT với một số nghiên cứu báo cáo làm kéo dài ACT, một số nghiên cứu khác cho rằng ảnh hưởng ít. Chất ức chế GpIIb/IIIa gây kéo dài ACT một cách có ý nghĩa. |
|
Kháng đông Lupus |
Ở một số bệnh nhân có kháng đông Lupus có dấu hiệu ACT nhưng một số bệnh nhân khác thì không thấy bị ảnh hưởng. |
|
Thiếu yếu tố đông máu |
ACT rất nhạy với thiếu yếu tố VIII ( Trước đây, ACT được sử dụng để đánh giá điều trị truyền thay thế yếu tố đông máu ở bệnh nhân Hemophilia và theo dõi điều trị Heparin. |
|
Kháng đông đường uống |
ACT nhạy cảm với kháng đông đường uống vì giảm các yếu tố phụ thuộc vitamin K |
|
Hạ nhiệt độ |
Hạ nhiệt độ gây kéo dài APTT ngay cả không có mặt Heparin. Khi bệnh nhân được làm ấm trở lại, có tăng thanh thải UFH và thông thường, dùng ACT để theo dõi tình trạng chống đông có thể cần thiết. Thanh thải Heparin tăng ở bệnh nhân nhi. |
|
Pha loãng máu |
Pha loãng máu ảnh hưởng rõ rệt tới ACT do giảm nồng độ nhiều yếu tố đông máu. |
|
Aprotinin |
Aprotinin kéo dài ACT dùng yếu tố tiếp xúc là cilite nhưng ảnh hưởng ít hơn nếu ACT sử dụng yếu tố tiếp xúc là kaolin. Do vậy ACT dựa trên cilite có thể không đánh giá được nồng độ Heparin khi có mặt Aptotinin. |
|
UFH liều cao |
Với liều cao UFH, APTT không thể được sử dụng để theo dõi điều trị Heparin bởi vì APTT không đo được. Xét nghiệm ACT hoặc antiXa được sử dụng thay thế APTT trong trường hợp này. |
|
ACT và APTT |
Có nhiều nghiên cứu so sánh độ nhạy của ACT và APTT và thiết lập đường cong tuyến tính đáp ứng heparin/liều lượng cho ACT và đáp ứng logarite cho APTT. Tuy nhiên, dữ liệu ít ỏi so sánh APTT và ACT gợi ý rằng 2 xét nghiệm này không đủ và có thể thiếu sót trong đánh giá các nghiên cứu lâm sàng. |
|
Heparinase |
Heparinase được sử dụng để trung hoà UFH trong ACT, cho phép theo dõi tình trạng đông máu đã được che dấu bởi Heparin. Bằng việc thực hiện ACT có/hoặc không có Heparinase khi bệnh nhân ngừng CPB –bất kỳ lượng Heparin nào còn dư do không được trung hoà bằng Protamin Sulphate sẽ được xác định. |
Câu hỏi 3: Các yếu tố ảnh hưởng tới xét nghiệm TT?
|
Giảm Fibrinogen |
Thiếu Fibrinogen bẩm sinh Giảm hoặc thiếu Fibrinogen máu Mất chức năng Fibrinogen: có thể có nồng độ Fin bình thường hoặc giảm. Thiếu Fibrinogen mắc phải DIC Sau điều trị tiêu cục máu đông Bệnh gan Bệnh ác tính |
|
Một số thuốc chống đông có thể gây TT kéo dài |
LMWHs thường không gây kéo dài TT trừ khi ở nồng độ rất cao, ví dụ quá liều. Hirudin Argatroban Warfarin không ảnh hưởng tới TT . |
|
|
TT không được khuyến cáo sử dụng để theo dõi điều trị thuốc ức chế trực tiếp Thrombin. |
|
Tăng Fibringen, Fibrin, sản phẩm giáng hoá cảu Fib (FDPs) |
Những sản phẩm này ảnh tưởng tới quá trình polymer hoá Fibrin và ở nồng độ cao dẫn dẫn đến kéo dài TT. |
|
Paraprotein |
Có thể ảnh tưởng tới quá trình polymer hoá Fibrin và gây kéo dài TT. |
|
Giảm Albumin máu |
Việc này có thể dẫn đến kéo dài cả TT và Reptilase time. Hiện tượng kéo dài xảy ra ngoài cơ thể có thể được khắc phục bằng việc thêm Albumin vào huyết tương bệnh nhân, TT và RT sẽ trở lại bình thường. Những bệnh nhân này thường ít có nguy cơ chảy chảy máu và có một số bằng chứng cho rằng họ có thể có tình trạng tăng ngưng tập tiểu cầu làm tăng nguy cơ huyết khối. |
|
Amyloidosis |
Kéo dài TT và RT được quan sát thấy ở bệnh nhân bệnh Amyloidosis do ức chế sự chuyển fibrinogen thành fibrin. |
|
Sau sử dụng Thrombin bò |
Bệnh nhân phơi nhiễm với Thrombin bò có thể phát triển chất ức chế gây kéo dài TT dựa trên Thrombin bò. Nếu kháng thể phản ứng chéo với thrombin người, TT dựa trên thuốc thử thrombin người cũng bị kéo dài. RT sẽ bình thường khi có các chất ức chế này. |
|
Ức chế đông máu |
Chất chống đông giống Heparin đã được báo cáo |
|
do bệnh lý |
(hiếm) ở một số bệnh nhân có bệnh ác tính hoặc các rối loạn khác, dẫn đến kéo dài TT nhưng RT bình thường. |
|
Tăng Fibrinogen máu |
Tăng Fibrinogen máu thỉnh thoảng có liên quan với việc TT kéo dài (và cả RT). Cơ chế không rõ nhưng có thể phản ánh sự can thiệp vào việc tổ hợp fibrin do quá nhiều fibrin. |
|
Fibrinogen bào thai |
TT ở trẻ sơ sinh thường kéo dài do sự có mặt của Fibrinogen bào thai. Fibrinogen được chứng minh tồn tại ở dạng “bào thai” khi tồn tại trogn máu cuống rốn của trẻ sơ sinh, với tăng acid sialic so với Fibrinogen người trưởng thành. Cần phải nhớ rằng, khi đánh giá đông cầm máu ở trẻ sơ sinh và trẻ nhỏ, cần sử dụng khoảng tham chiếu phù hợp. |
Câu hỏi 4: Tại sao chúng ta sử dụng xét nghiệm ACT mà không phải là TT để kiểm soát bệnh nhân dùng tuần hoàn ngoài cơ thể?
Nồng độ cao UFH sử dụng để chống đông ở bệnh nhân sử dụng CPB làm xét nghiệm TT không đông được và do vậy không thể dùng TT để theo dõi những bệnh nhân này.
|
Tóm tắt: Xét nghiệm ACT và TT – nguyên lý và các yếu tố ảnh hưởng đến kết quả xét nghiệm |
Case 62
Bệnh nhân nam 64 tuổi sau mổ thay van động mạch chủ. Trước khi ngừng tuần hoàn ngoài cơ thể (CPB), bệnh nhân được sử dụng Protamin Sulphate để trung hoà UFH. Huyết áp giảm dần và bện nhân bị hạ huyết áp trầm trọng.
Câu hỏi 1: Tại sao sử dụng Protamin Sulphate và cơ chế hoạt động như thế nào?
Câu hỏi 2: Tại sao bệnh nhân bị hạ huyết áp?
Đáp án
Câu hỏi 1: Tại sao sử dụng Protamin Sulphate và cơ chế hoạt động như thế nào?
Protamin Sulphate khởi đầu được phân lập từ tinh trùng cá hồi và một vài loại cá khác nhưng hiện nay thường được sản xuất bằng công nghệ tái tổ hợp. Đây là một protein cationic cao, gắn mạnh mẽ với Heparin (chủ yếu là UFH) trung hoà tác dụng của chúng. Protamin Sulphate liều cao có tác dụng kháng đông kéo dài cả tuần. Khả năng trung hoà tác dụng chống đông của UFH rất hiệu quả , nhưng giảm hơn ở LMWHs và không có tác dụng đối với bệnh nhân dùng DOAC.
Một số bệnh nhân bị dị ứng cá có thể có phản vệ khi sử dụng Protamin. Sốc phản vệ đã được báo cáo ở một số bệnh nhân thắt ống dẫn tinh và một số bệnh nhân đã sử dụng Protamin chứa insulin trong quá khứ (loại này hiếm khi được sử dụng ngày nay). 1mg Protamine Sulphate trung hoà được 100IU UFH.
Câu hỏi 2: Tại sao bệnh nhân bị hạ huyết áp?
Bệnh nhân này có dị ứng cá và phát triển sốc phản vệ sau trung hoà UFH sử dụng trong khi dùng CPB.
|
Tóm tắt: Đây là trường hợp dị ứng với Protamine Sulphate. |
Case 63
Bệnh nhân nữ 84 tuổi sống một mình, được nhập viện do bầm tím diện rộng ở chân, bụng và cánh tay. Bệnh nhân cũng có chảy máu lợi hơn 8-10 tuân trước.
Kết quả xét nghiệm ban đầu có kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
12 s |
11 -14 s |
|
APTT |
33 s |
28 – 34.5 s |
|
Fib (Clauss) |
3.6 g/L |
2 – 4 g/L |
|
Hb |
90 g/L |
115 – 155 g/L |
|
Tiểu cầu |
284 x 109/L |
150 -400 x 109/L |
|
MCV |
76 fL |
78 – 98 fL |
|
WBC |
7.6 x 109/L |
5 – 16 x 109/L |
|
Chức năng thận |
Bình thường |
|
|
Chức năng gan |
Bình thường |
|
Câu hỏi 1: Bạn sẽ chỉ định thêm xét nghiệm gì?
FVIII và vWF bình thường. Điện di Protein huyết thanh: không phát hiện band kháng thể đơn dòng.
Ngưng tập tiểu cầu: Ngưng tập bình thường với ADP, Collagen,
Epinephrine, acid Arachidonic và dính bình thường với Ristocetin.
Vitamin B12, Folate và Ferritin đều giảm.
Câu hỏi 2: Chẩn đoán có thể là gì và tại sao có hiện tượng bầm tím/chảy máu?
ĐÁP ÁN
Câu hỏi 1: Bạn sẽ chỉ định thêm xét nghiệm gì?
Hình thái chảy máu và tiền sử gợi ý các bất thường đông cầm máu thời kỳ đầu hơn là thiếu hụt các yếu tố đông máu. Hơn nữa, tiền sử của bệnh nhân gợi ý bệnh lý mắc phải chứ không phải bệnh di truyền bẩm sinh.
Xét nghiệm ban đầu thể hiện thiếu máu hồng cầu bình thường nhưng không có các bất thường khác.
Các xét nghiệm nên được chỉ định thêm bao gồm:
Yếu tố VIII và vWF.
Điện di Protein huyết thanh
Ngưng tập tiểu cầu
Vitamin B12, Folate và Ferritin
Lam máu ngoại vi
Hơn nữa, nhật ký chế độ ăn cũng quan trọng.
Thời gian máu chảy hiện không còn được sử dụng rộng rãi nhưng nó là một trong số ít các xét nghiệm phản ánh tương tác của thành mạch với vWF và tiểu cầu.
Câu hỏi 2: Chẩn đoán có thể là gì và tại sao có hiện tượng bầm tím/chảy máu?
Sau khi có các xét nghiệm trên, có thể nghĩ đến là bệnh lý thành mạch kết hợp với thiếu vitamin C. Vì thế khai thác chế độ ăn uống rất quan trọng. Chẩn đoán thiếu vitamin C được khẳng định bằng việc do Acid Ascorbic bạch cầu hoặc lượng Acid Ascorbic trong máu toàn phần và ở bệnh nhân này Acid Ascorbic bạch cầu 8 tế bào và Acid Ascorbic máu
Dấu hiệu của thiếu vitamin C bao gồm chảy máu tự phát từ lợi, vết thương lâu lành, khối máu tụ và đau khớp.
Vitamin C cần thiết cho tổng hợp collagen bởi vì nó là đồng yếu tố cho quá trình hydroxyl hoá của proline tạo thành hydroxylproline trong quá trình hình thành collagen. Không có bước này, collagen không thể lắp ráp chính xác và việc thay thế lớp collagen (lớp cơ bản trong cấu trúc mạch máu) bằng collagen bị lỗi dẫn đến mất tính toàn vẹn của mạch máu gây hiện tượng chảy máu và bầm tím ở bệnh nhân.
Vitamin C cũng tăng hấp thụ sắt và có thể giải thích tại sao thiếu sắt cũng được thấy ở bệnh nhân thiếu vitamin C.
|
Tóm tắt: Đây là trường hợp thiếu hụt vitamin C dẫn đến bầm tím và chảy máu. |
Case 64
Bệnh nhân nữ 45 tuổi nhập viện để thay van hai lá. Phẫu thuật được thực hiện thành công không có xảy ra vấn đề ngoài ý muốn nhưng 5 ngày sau khi phẫu thuật, bệnh nhân bị DVT chi dưới và được chỉ định sử dụng UFH. Vào ngày +7, tiểu cầu của bệnh nhân (số lượng tiểu cầu bình thường trước khi mổ) giảm xuống còn 25 x 109/L và đã được khẳng định bằng việc lặp lại xét nghiệm.
Câu hỏi 1: Giải thích nguyên nhân giảm tiểu cầu?
Câu hỏi 2: Bạn sẽ yêu cầu thêm xét nghiệm gì?
Câu hỏi 3: Điểm 4T bằng bao nhiêu?
Sàng lọc HIT dương tính.
Câu hỏi 4: Cơ chế giảm tiểu cầu trong HIT?
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Đáp án
Câu hỏi 1: Giải thích nguyên nhân giảm tiểu cầu?
Các khả năng có thể giải thích cho tình trạng giảm tiểu cầu trên là:
HIT (Heparin Induced Thrombocytopaenia)
DIC
Nhiễm trùng
Giảm tiểu cầu do thuốc (không phải HIT)
Bệnh gan
Câu hỏi 2: Bạn sẽ yêu cầu thêm xét nghiệm gì?
Bạn cần cân nhắc các xét nghiệm sau:
Công thức máu
Chức năng gan thận
Đông máu cơ bản: PT/APTT/Fib
D dimers
Sàng lọc nhiễm trùng bao gồm cả cấy máu
Sàng lọc HIT
Câu hỏi 3: Điểm 4T bằng bao nhiêu?
|
Chỉ số |
Kết quả |
Điểm |
|
Số lượng tiểu cầu |
25 x 109/L |
+2 |
|
Bắt đầu giảm tiểu cầu rõ ràng trong 5-10 ngày |
Có |
+2 |
|
Tắc mạch hoặc biến chứng khác |
Không |
0 |
|
Các nguyên nhân khác gây giảm tiểu cầu |
Không |
+2 |
|
Tổng |
|
+6 |
Điểm 4T của bệnh nhân là 6. Dấu hiệu DVT có thể bỏ qua khi tính điểm vì mặc dù bệnh nhân nhận UFH trong quá trình sử dụng tuần hoàn ngoài cơ thể, số lượng tiểu cầu của bệnh nhân sau phẫu thuật là bình thường và số lượng tiểu cầu cũng bình thường khi bệnh nhân bị DVT.
Câu hỏi 4: Cơ chế giảm tiểu cầu trong HIT?
PF4 được dự trữ trong hạt α của tiểu cầu và được giải phóng khi tiểu cầu hoạt hóa. PF4 gắn với glycosaminglycans (GAGs) trên tế bào nội mô thay thế Antithrombin.
PF4 có ái tính cao với UFH và khi có mặt UFH, sẽ kéo PF4 vào tuần hoàn nơi nó sẽ tương tác với Heparin để tạo thành phức hợp PF4-Heparin. PF4 cũng có thể gắn với vi khuẩn Gam âm và Gram dương, cùng với sự hoạt hóa tiểu cầu và giải phóng PF4, có thể kích thích đáp ứng miễn dịch sau phơi nhiễm với Heparin. Sự hình thành kháng thể chống lại phức hợp HeparinFP4 dẫn đến hình thành phức hợp miễn dịch gắn với thụ thể FcRIIa, dẫn đến hoạt hóa tiểu cầu và giải phóng các vi hạt tiền đông và giảm tiểu cầu. Tiểu cầu hoạt hóa trong HIT còn do Thrombin, có thể thông qua hoạt hóa thụ thể FcRIIa của tế bào mono, do đó làm tăng biểu hiện của Tissue Factor và do đó tiểu cầu được hoạt hóa thông qua thrombin.
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Dừng truyền UFH và chuyển sang dùng các thuốc chống đông đường tiêm thay thế như Danaparoid.
|
Tóm tắt: Đây là trường hợp HIT sau sử dụng Unfractionated Heparin. |
Case 65
Bệnh nhân 22 ngày tuổi, tiền sử bình thường, bú mẹ, được bố mẹ phát hiện hôn mê tại nhà, có chảy máu từ miệng và lợi. Tiền sử đáng chú ý duy nhất là mẹ bệnh nhân bị băng huyết sau sinh và cần nhập viện cấp cứu.
Xét nghiệm đông máu như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
102 s |
11 -14 s |
|
APTT |
>120 s |
23 – 35 s |
|
Fib (Clauss) |
1.9 g/L |
1.5 – 4 g/L |
|
Thrombin time |
13 s |
10 – 13 s |
Xét nghiệm công thức máu không có gì đặc biệt.
Câu hỏi 1: Chẩn đoán có thể là gì?
Câu hỏi 2: Bạn làm gì để khẳng định chẩn đoán?
Kết quả các xét nghiệm sau đó phù hợp với chẩn đoán thiếu hụt Vitamin K.
Câu hỏi 3: Tại sao trẻ sơ sinh có nguy cơ xuất huyết do thiếu vitamin K?
Đáp án
Câu hỏi 1: Chẩn đoán có thể là gì?
PT và APTT kéo dài rõ rệt với Fibrinogen và TT bình thường. Trong bệnh cảnh là bệnh nhân sơ sinh, thiếu hụt vitamin K là chẩn đoán nên nghĩ đến nhiều nhất. Tuy nhiên, khả năng thiếu hụt các yếu tố con đường chung cũng chưa thể loại trừ, do đó các yếu tố này nên được xét nghiệm. Mặc dù thiếu hụt kết hợp yếu tố V và VIII có thể gây bất thường PT và APTT nhưng thường nó không làm PT và APTT kéo dài ở mức độ như của bệnh nhân này.
Câu hỏi 2: Bạn làm gì để khẳng định chẩn đoán?
Xét nghiệm các yếu tố đông máu phụ thuộc vitamin K, sử dụng khoảng tham chiếu dành cho trẻ sơ sinh. Nồng độ các yếu tố đông máu phụ thuộc vitamin K không thể đạt tới mức bình thường như người lớn cho tới khi trẻ được 6 tháng tuổi, và đối với Protein C có thể lâu hơn nữa. Hơn nữa, yếu tố không phụ thuộc vitamin K như yếu tố V cũng cần được xét nghiệm.
Câu hỏi 3: Tại sao trẻ sơ sinh có nguy cơ xuất huyết do thiếu vitamin K?
Bệnh xuất huyết ở trẻ sơ sinh thường do thiếu hụt vitamin K.
Trẻ sơ sinh bị thiếu hụt vitamin K do các nguyên nhân sau:
Vitamin K không được truyền qua rau thai
Ruột vô khuẩn và do vậy không thể tổng hợp được vitamin K. Trong thực tế, vitamin K được hấp thu ở đại tràng và
Sữa mẹ không có vitamin K trong khi sữa bò thì giàu vitamin K.
Gan chưa trưởng thành.
Vitamin K được bổ sung thường qui cho trẻ mới sinh ở UK để dự phòng bệnh xuất huyết ở trẻ sơ sinh. Trong trường hợp này, đã bỏ qua việc bổ sung vitamin K cho trẻ vì mẹ của em bé phải nhập viện cấp cứu do chẩy máu nặng sau đẻ.
|
Tóm tắt: Đây là trường hợp Bệnh xuất huyết ở trẻ sơ sinh do thiếu vitamin K. |
Case 66
Bệnh nhân nam 73 tuổi khám tại khoa cấp cứu do tiểu máu, bầm tím và khó chịu nói chung. Tiền sử y khoa của bệnh nhân không có gì đặc biệt và bệnh nhân không sử dụng thuốc gì. Không có tiền sử gia đình nào đáng chú ý.
Một loạt các xét nghiệm được thực hiện và cho kết quả như sau:
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
32 s |
11 -14 s |
|
APTT |
88 s |
23 – 35 s |
|
Fib (Clauss) |
1.5 – 4 g/L |
|
|
Thrombin time |
110 s |
10 – 13 s |
|
Hb |
90 g/L |
123 – 175 g/L |
|
Tiểu cầu |
49 x 109/L |
150 -400 x 109/L |
|
WBC |
9.9 x 109/L |
4.5 – 10.0 x 109/L |
|
Lam máu |
Leucoerythroblastic |
|
|
Chức năng thận |
Bình thường |
|
Câu hỏi 1: Bạn giải thích các kết quả trên như thế nào và bạn sẽ làm gì tiếp theo?
Kết quả D-dimer tăng = 2500ng/mL (khoảng tham chiếu là
PSA >500 ng/mL (khoảng tham chiếu là 1-25 ng/mL) Câu hỏi 2: Các xét nghiệm này gợi ý điều gì?
Câu hỏi 3: Điểm DIC của bệnh nhân?
Đáp án
Câu hỏi 1: Bạn giải thích các kết quả trên như thế nào và bạn sẽ làm gì tiếp theo?
Kết quả xét nghiệm của bệnh nhân phù hợp với chẩn đoán DIC hoặc tăng tiêu sợi huyết – đặc biệt là chẩn đoán tăng tiêu sợi huyết do có Fibronogen rất thấp.
Trong bệnh cảnh lam máu ngoại vi có Leucoerythroblastic (có hồng cầu có nhân và bạch cầu các tuổi trung gian ở máu ngoại vi), gợi ý khả năng bệnh nhân có bệnh ác tính hoặc nhiễm trùng nặng.
Các nguyên nhân này cần được tìm hiểu chi tiết hơn.
Câu hỏi 2: Các xét nghiệm này gợi ý điều gì?
Kết hợp kết quả D dimer và PSA của bệnh nhân, có thể nghĩ nhiều tới DIC hoặc Tăng tiêu sợi huyết do bệnh lý ác tính của tuyến tiền liệt.
Câu hỏi 3: Điểm DIC của bệnh nhân?
Điểm DIC theo ISTH của bệnh nhân là 8 và do vậy các dữ liệu xét nghiệm phù hợp với DIC (overt DIC).
Các xét nghiệm sau đó phát hiện các tổn thương xơ cứng diện rộng phù hợp với chẩn đoán ung thư tiền liệt tuyến di căn, và được khẳng định bằng chẩn đoán sinh thiết. DIC là một rối loạn đông máu thường gặp trong ung thư tiền liệt tuyến.
|
Tóm tắt: Đây là trường hợp DIC hoặc Tăng tiêu sợ huyết do ung thư tiền liệt tuyến di căn |
Case 67
Nhận xét các trường hợp sau và trong mỗi trường hợp, bàn luận các câu hỏi được đặt ra.
Case 67a:
Bệnh nhân nam 74 tuổi có tiền sử Rung nhĩ được điều trị với Apixaban. Bệnh nhân cần sinh thiết khối u đại tràng và bác sĩ tiêu hóa đã chỉ định xét nghiệm đông máu có kết quả như sau, bạn được yêu cầu giải thích các kết quả xét nghiệm và đưa ra lời khuyên liệu bệnh nhân có an toàn nếu được tiến hành sinh thiết hay không?
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
12 s |
11 -14 s |
|
APTT |
29 s |
23 – 35 s |
|
Fib (Clauss) |
2.9 g/L |
2 – 4 g/L |
|
Thrombin time |
12 s |
11 – 17 s |
|
Tiểu cầu |
325 x 109/L |
150 -400 x 109/L |
Case 67b:
Bệnh nhân nữ 34 tuổi nhập viện do Huyết khối tĩnh mạch sâu. Bệnh nhân được điều trị chống đông bằng Rivaroxaban và được làm xét nghiệm đông máu. Nhận xét các kết quả dưới đây và liệu các kết quả này có giải thích được tình trạng huyết khỗi tĩnh mạch sâu của bệnh nhân hay không ?
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
13 s |
11 -14 s |
|
APTT |
34 s |
23 – 35 s |
|
dRVVT |
1.39 |
|
|
dRVVT+ phospholipid |
1.28 |
– |
Case 67c:
Bệnh nhân nam 52 tuổi có tiền sử rung nhĩ được điều trị Warfarin. Bệnh nhân nhập viện do chảy máu đường tiêu hóa và được làm các xét nghiệm đông máu. Nhận xét kết quả xét nghiệm của bệnh nhân.
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
14 s |
11 -14 s |
|
INR |
1.2 |
– |
|
APTT |
35 s |
23 – 35 s |
|
Fib (Clauss) |
2.9 g/L |
2 – 4 g/L |
|
Tiểu cầu |
225 x 109/L |
150 -400 x 109/L |
Case 67d:
Bện nhân nam 65 tuổi đang điều trị Dabigatran do Rung nhĩ được nhập viện để thay khớp gối. Nhận xét các kết quả xét nghiệm trước phẫu thuật của bệnh nhân.
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
12 s |
11 -14 s |
|
APTT |
33 s |
23 – 35 s |
|
Fib (Clauss) |
2.9 g/L |
2 – 4 g/L |
|
Thrombin time |
15 s |
11 – 17 s |
|
Tiểu cầu |
195 x 109/L |
150 -400 x 109/L |
Case 67e:
Bệnh nhân nữ 54 tuổi nhập viện khoa cấp cứu do tiểu máu 2 ngày. Bệnh nhân có tiền sử bệnh tâm lý nên được sử dụng thuốc Fluoxetine.
Xét nghiệm của bệnh nhân như sau :
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
>120 s |
11 -14 s |
|
INR |
>10 |
– |
|
APTT |
115 s |
23 – 35 s |
|
APTT 50:50 Mix |
27 s |
23 – 35 s |
|
Fib (Clauss) |
2.9 g/L |
2 – 4 g/L |
|
Tiểu cầu |
195 x 109/L |
150 -400 x 109/L |
|
Chức năng gan thận |
Bình thường |
– |
Nhận xét các kết quả trên. Bạn cần thêm xét nghiệm gì và giải thích hợp lý nhất cho các kết quả trên là gì ?
Đáp án
Case 67a:
Apixaban không ảnh hưởng tới xét nghiệm PT, TT hoặc số lượng tiểu cầu, chỉ ảnh hưởng chút ít tới APTT mặc dù APTT cũng phụ thuộc rất nhiều vào loại thuốc thử sử dụng.
Trong trường hợp này, đánh giá nồng độ Apixaban bwangf xét nghiệm antiXa có thể có giá trị. Về cơ bản, lời khuyên cho trường hợp này là dừng Apixaban trước sinh thiết u và dùng lại sau khi sinh thiết.
Case 67b:
Kết quả xét nghiệm phù hợp với sự có mặt của Rivaroxaban. dRVVT hoạt hóa yếu tố X và do vậy, khi có mặt của thuốc ức chế yếu tố Xa như Rivaroxaban sẽ dẫn đến kéo dài dRVVT và dRVVT+PL.
Nên dừng Rivaroxoban 1 ngày và ngày làm xét nghiệm để đánh giá xem bệnh nhân có kháng đông Lupus hay không .
Case 67c:
PT bị kéo dài chút ít (thực tế là kết quả nằm ở giới hạn trên của khoảng tham chiếu), điều này gợi ý khả năng bệnh nhân không sử dụng Warfarin. Nhưng có vẻ không phù hợp, vì nếu không phải do thuốc chống đông thì tại sao bệnh nhân có tình trạng chảy máu đường tiêu hóa, tuy nhiên cũng có thể bệnh nhân mới dừng thuốc chống đông khi có biểu hiện chảy máu đường tiêu hóa. Cần hỏi tiền sử một cách cẩn thận để xác định xem bệnh nhân dừng Warfarin khi nào?
Case 67d:
Thrombin time rất nhạy cảm với sự có mặt của Dabigatran (chất ức chế trực tiếp Thrombin), do vậy từ kết quả xét nghiệm có thể dự đoán: bệnh nhân đang không sử dụng Dabigatran.
Case 67e:
Dữ liệu xét nghiệm cho thấy PT và APTT kéo dài rõ rệt và APTT trở về bình thường trên hỗn hợp Mix với huyết tương bình thường. Trường hợp này phù hợp với tình huống thiếu hụt yếu tố đông máu.
Cần định lượng nồng độ các yếu tố phụ thuộc vitamin K và các yếu tố không phụ thuộc vitamin K như yếu tố V. Trong thực hành, có thể cả các yếu tố con đường chung như yếu tố II và X cũng được định lượng.
Thời gian đông của PT và APTT gợi ý rằng dù là nguyên nhân gì thì đây cũng là trường hợp thiếu yếu tố nặng.
Kết quả sau đó cho thấy giảm nồng độ yếu tố II, VII, IX, X nhưng FV bình thường, phù hợp với tình huống dùng thuốc kháng vitamin K. Bệnh nhân sau khi nhập viện được chẩn đoán đã tiêu thụ một siêu Warfarin, khẳng định thông qua việc tìm thấy Difenacoum trong huyết thanh bệnh nhân. Difenacoum là một siêu Warfarin tác dụng kéo dài có trong thuốc diệt chuột, với thời gian bán thải trong huyết ≈ 20 ngày và trong mô là ≈ 62 ngày trên mô hình động vật.
|
Tóm tắt: Đây là một loạt các báo cáo chứng minh ảnh hưởng khác nhau của thuốc chống đông. |
Case 68
Bệnh nhân nữ 45 tuổi được thấy ở khoa cấp cứu với triệu chứng sưng đau cánh tay trái. Triệu chứng này đã xuất hiện 8 ngày. Tiền sử y khoa của và tiền sử gia đình của bệnh nhân không có gì đặc biệt mặc dù các thông tin bệnh nhân cung cấp sau đó có tiền sử bị bầm tím trong khoảng 6 tuần. Bệnh nhân không dùng thuốc gì trong 12 tuần gần đây.
Siêu âm vùng cánh tay cho thấy khối máu tụ lớn.
Câu hỏi 1 : Bạn sẽ chỉ định xét nghiệm gì để làm rõ nguyên nhân khối máu tụ ?
Kết quả các xét nghiệm ban đầu có kết quả như sau :
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
13 s |
11 -14 s |
|
APTT |
33 s |
28 – 34.5 s |
|
Fib (Clauss) |
4.2 g/L |
2 – 4 g/L |
|
Thrombin time |
13 s |
11.5 – 13.5 s |
|
PFA -100 (Collagen:ADP) |
Bình thường |
– |
|
FVIII |
185 IU/dL |
50 – 150 IU/dL |
|
VWF:RCo |
177 IU/dL |
47 – 142 IU/dL |
|
Hemoglobin |
124 g/L |
130 – 170 g/L |
|
WBC |
8.2 x 109/L Thành phần bạch cầu bình thường |
4 – 11 x 109/L |
|
Tiểu cầu |
192 x 109/L |
150 – 400 x 109/L |
|
Chức năng gan thận |
Bình thường |
– |
Câu hỏi 2 : Bạn cần chỉ định thêm xét nghiệm gì ?
Bạn chỉ định xét nghiệm FXIII và có kết quả như sau :
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
FXIII |
60 – 130 IU/dL |
|
|
Chất ức chế FXIII |
Dương tính (45 BU) |
– |
Câu hỏi 3 : Chẩn đoán là gì và bạn điều trị bệnh nhân này như thế nào ?
Đáp án
Câu hỏi 1 : Bạn sẽ chỉ định xét nghiệm gì để làm rõ nguyên nhân khối máu tụ ?
Tiền sử và triệu chứng lâm sàng gợi ý bệnh lý rối loạn chảy máu mắc phải và phù hợp là chỉ định các xét nghiệm vòng đầu và kiểm tra chức năng tiểu cầu. Thường gặp nhất là chất ức chế yếu tố VIII, do vậy kiểm tra nồng độ yếu tố VIII và VWF là hợp lý.
Câu hỏi 2 : Bạn cần chỉ định thêm xét nghiệm gì ?
Các xét nghiệm ban đầu chưa giải thích được tình trạng chảy máu ở bệnh nhân. Do vậy bạn nên chỉ định thêm các xét nghiệm :
FXIII
TEG hoặc ROTEM
Câu hỏi 3 : Chẩn đoán là gì và bạn điều trị bệnh nhân này như thế nào ?
Kết quả sau đó phù hợp với chẩn đoán thiếu hụt yếu tố FVIII mắc phải thứ phát do chất ức chế yếu tố XIII. Đây là tình huống hiếm gặp và chỉ có một vài trường hợp được báo cáo. Trong một số trường hợp, bệnh cảnh này liên quan tới việc sử dụng Isoniazid nhưng không phải trường hợp bệnh nhân này.
Điều trị nên bao gồm :
Tăng FXIII để kiểm soát chảy máu bằng sử dụng Cryoprecipitate, FFP hoặc FXIII cô đặc (nếu có).
Loại bỏ chất ức chế bằng steroids và thuốc ức chế miễn dịch như cyclophosphamide. Rituximab đã được sử dụng trong thiếu FXIII mắc phải với hiệu quả tốt.
|
Tóm tắt : Đây là trường hợp có chất ức chế FXIII mắc phải. |
Case 70
Bệnh nhân nam 2 tuổi được chuyển tới từ bác sĩ phẫu thuật tai mũi họng do giảm tiểu cầu. Bệnh nhân có tiền sử chảy máu cam nhiều lần, dễ bầm tím và eczema nhẹ. Trẻ phát triển bình thường và không có tiền sử gia đình nào đặc biệt.
Xét nghiệm của bệnh nhân như sau :
|
Xét nghiệm |
Kết quả bệnh nhân |
Dải tham chiếu |
|
PT |
12 s |
11 -14 s |
|
APTT |
32 s |
28 – 34.5 s |
|
Fib (Clauss) |
3.1 g/L |
2 – 4 g/L |
|
Hb |
140 g/L |
135 – 175 g/L |
|
WBC |
11.5 x 109/L Thành phần bạch cầu bình thường |
5 -10 x 109/L |
|
MCV |
82 fL |
80 – 98 fL |
|
Tiểu cầu |
96 x 109/L |
150 – 400 x 109/L |
|
MPV |
5 fL |
8 -11 fL |
Câu hỏi 1 : Nhận xét các kết quả trên ? Chúng có gợi ý chẩn đoán nào không ?
Phân tích PFA-100 sử dụng cả ADP cartridge và Adrenaline cartridge có kết quả bất thường và kéo dài rõ rệt.
Câu hỏi 2 : Nhận xét kết quả trên và bạn sẽ làm gì tiếp theo ?
Đáp án
Câu hỏi 1 : Nhận xét các kết quả trên ? Chúng có gợi ý chẩn đoán nào không ?
Bệnh nhân có tiền sử chảy máu rõ rệt và chỉ có một bất thường phát hiện được trong xét nghiệm ban đầu là giảm tiểu cầu và tiểu cầu nhỏ (Microthrombocytopaenia). Điều này gợi ý rằng bệnh nhân có thể bị hội chứng Wiskott Aldrich.
Định lượng FVIII và VWF là hợp lý bởi vì rối loạn các protein này thường gặp hơn nhưng nó không giải thích được tình trạng tiểu cầu giảm, kích thước nhỏ.
Xét nghiệm chức năng tiểu cầu bằng phương pháp LTA khá khó khăn để thực hiện ở lứa tuổi này của bệnh nhân do lượng máu xét nghiệm lớn, do vậy phương pháp PFA-100 nên được sử dụng.
Cũng nên gửi mẫu máu của bệnh nhân đi phân tích di truyền.
Câu hỏi 2 : Nhận xét kết quả trên và bạn sẽ làm gì tiếp theo ?
Kết quả PFA-100 thấy bất thường chức năng tiểu cầu. Đợi kết quả phân tích đột biến gen để khẳng định chẩn đoán hội chứng Wiskott Aldrich.
Hội chứng Wiskott Aldrich (WAS) là một rối loạn di truyền lặn liên kết nhiễm sắc thể giới tính X, đặc trưng là giảm tiểu cầu và tiểu cầu nhỏ, eczema và nhiễm trùng lặp lại. WAS liên quan tới đột biến gen WAS trên cánh ngắn nhiễm sắc thể X (Xp11.23). Gen WAS mã hoá cho protein gồm 502 amino acid tham gia vào quá trình polymer hoá Actin và đột biến trong gen WAS dẫn đến những bất thường quan sát được trọng hội chứng Wiskott Aldrich. Đột biến xoá gen dẫn đến không có protein WAS hoặc protein WAS bị cắt ngắn liên quan với các kiểu hình Wiskott Aldrich nặng hơn những đột biến khác.
|
Tóm tắt : Đây là trường hợp Microthrombocytopaenia do hội chứng Wiskott Aldrich. |