Thu thập mẫu máu là bước tối quan trọng trong việc đo Homocysteine huyết tương. Một bữa ăn nhẹ có lẽ ít tác động lên mức homocystein, nhưng một bữa ăn giàu protein sẽ dẫn đến tăng homocystein đến 15-20% và đạt cực đại 6-8h sau ăn.
Homocysteine được tạo ra từ hồng cầu, bạch cầu và tiếp tục được tạo ra sau khi lấy máu. Mức Hcy tăng với tốc độ 10-15%/giờ. Nếu việc xử lý mẫu không làm ngay được, thì đặt mẫu trong nước đá sẽ làm giảm ảnh hưởng của hiện tượng này.
Sau khi ly tâm tách huyết tương, Hcy có thể ổn định trong nhiều năm khi đông ở -20 độ C.
Trong máu toàn phần và trong huyết tương, luôn có sự tái phân phối các dạng Hcy và trong vòng 1 giờ sau thu thập tại nhiệt độ phòng sau khi rã đông, phần lớn Hcy ở dạng kết hợp với protein.
Để ước tính chính xác lượng Hcy tự do, cần khử hiện tượng protein hóa ngay lập tức trước khi xử lý mẫu.
Một chế độ ăn hạn chế và quá trình xử lý mẫu cẩn thận sẽ không ảnh hưởng đến chẩn đoán Hcy niệu cổ điển, nhưng nó sẽ trở nên quan trọng khi đánh giá nguy cơ mạch máu.
Một sự tăng Hcy 4-5µmol/l sẽ làm tăng 40-50% bệnh mạch máu.
Có sự giảm đáng kể Hcy trong đột biến C677T MTHFR như là một yếu tố nguy cơ của VTE. BCSH Guidline không khuyến cáo sàng lọc điều này ở bệnh nhân VTE.
Giới thiệu
Hcy là một amino acid chứa nhóm sulfur xuất phát từ Methionine, một amino acid thiết yếu tìm thấy phổ biến trong các protein có nguồn gốc động vật, Hcy có nguồn duy nhất ở người. Hcy được chuyển hóa hoặc bởi remethylation hoặc transsulphuration.
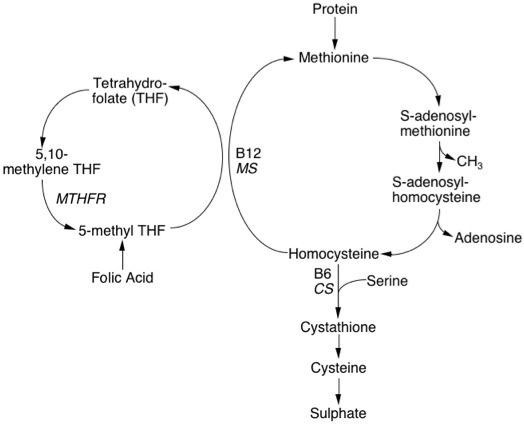
Con đường Remethylation: trong con đường này, Hcy cần một nhóm methyl được lấy từ hoặc do sự chuyển đổi 5-methyltetrahydrofolate thành tetrahydrofolate hoặc từ betaine thành N,N-dimethylglycine. Phản ứng trước phụ thuộc B12, xảy ra ở tất cả các mô và đòi hỏi enzyme methionine synthase (MS). Phản ứng sau chiếm phần phụ, độc lập B12 xảy ra chủ yếu ở gan và cần enzyme khác betaine homocysteine methyltransferase. Hcy nếu không được methylated thì sẽ được chuyển hóa theo con đường thứ 2 còn gọi là transsulphuration.
Con đường transsulphuration: trong con đường này, Hcy sẽ ngưng tụ với serine tạo thành cystathione, một phản ứng không thể đảo ngược được xúc tác bởi enzyme cystathionine-β-synthase (CβS) và nó đòi hỏi pyridoxal-5′-phosphate (vitamin B6) như một cofactor. Cystathionine được chuyển hóa tiếp thành cysteine và αketobutyrate bởi gamma-cystathionase. Methionine được chuyển thành homocysteine thông qua S-adenosylmethionine (SAM), SAM hoạt động như một người cho methyl trong một số lớn các phản ứng sinh học như quá trinh tổng hợp purine và pyrimidine. S-adenosylhomocysteine (SAH) là kết quả của sự khử methyl từ SAM, sau đó được thủ phân thành Hcy và adenosine, bắt đầu một chu trình mới.
Hcy tồn tại trong huyết tương ở nhiều dạng
|
Dạng |
|
|
Tự do |
Phân tử thiol (sulphydryl) tự do. Hcy tự do nhanh chóng bị oxy hóa tại pH sinh lý và chỉ hiện diện lượng nhỏ trong huyết tương. |
|
Hcy |
Hcy có thể liên hợp với các phân tử Hcy khác bằng cầu nối disulphide để tạo thành dạng homocystein. |
|
Kết hợp với protein khác |
Phần lớn Hcy ở dạng kết hợp với các protein khác qua cầu nối disulphide với các phân tử cysteine. Tổng lượng dự do và kết hợp tạo ra lượng hcy toàn phần (tHcy). |
Nguyên lý và phương pháp
Test Cyanide-nitroprussic acid: ít khi được thực hiện ngày nay. Trước đây người ta dùng phản ứng homocysteine disulphide hiện diện trong nước tiểu với dung dịch cyanide-nitroprussic acid tạo thành ferric thiocyanate – một phức hợp cơ-kim có màu hồng tím.
Một số phương pháp đo Hcy xin phép không viết chi tiết. Bạn đọc quan tâm có thể đọc thêm.
Phân tích kết quả
Homocysteine niệu thường là kết quả của bệnh lý di truyền lặn do khiếm khuyết enzyme CβS hoặc MS liên quan đến con đường transsulphuration và remethylation. tHcy huyết tương ở những bệnh nhân này thường >50µmol/L, vào khoảng 200-400µmol/L liên kết với tăng methionine huyết tương. Những người bị ảnh hưởng thường có bất thường chậm phát triển tâm thần, dị dạng xương và nguy cơ cao bệnh lý mạch máu. Một số bệnh nhân với homocysteine niệu điển hình do khiếm khuyết CβS sẽ đáp ứng điều trị với bổ sung pyridoxine, làm giảm mức Hcy cũng như giảm nguy cơ bệnh lý mạch máu. Đột biến dị hợp CβS xảy ra ở 0.5-1.5% dân số chung và có thể liên kết với tăng nhẹ Hcy.
Có một số yếu tố ảnh hưởng lên kết quả của Hcy, tham khảo thêm ở bảng:
|
Di truyền |
CβS deficiency MS deficiency MTHFR deficiency TL-MTHFR (C677T) |
|
Sinh lý |
Age: Homocysteine levels increase with age Sex: Pre- and postmenopausal women have lower tHcy levels than men Pregnancy: Levels fall Diet: tHcy levels directly related to methionine intake and inversely related to folate, B12, B6 and rarely choline, intake. Alcohol |
|
Bệnh lý |
Vitamin deficiencies Renal disease: tHcy correlates with increasing creatinine and decreasing GFR Renal/cardiac transplantation: tHcy levels increased Severe psoriasis: Levels increased Leukaemia: Levels increased |
|
Thuốc |
Oral contraceptives/Hormone Replacement Therapy: levels reduced Steroids: Levels increased Ciclosporin: Levels increased Anti-folate drugs: Levels increased Smoking: Levels increased |
Khoảng tham chiếu
Giá trị bình thường
Đề nghị xét nghiệm nào tiếp?
Ở một người tăng Hcy, điều quan trọng nhất phải loại trừ suy giảm folate hoặc B12. Những nguyên nhân khác nên được xem xét đã tổng kết ở bảng trên. Nhớ rằng, việc đo Hcy huyết tương là khó và chịu nhiều ảnh hưởng của các yếu tố tiền phân tích. Một kết quả bất thường nên được làm lại để khẳng định.
Tài liệu tham khảo
McCully, K.S. (1969) Vascular pathology of homocysteinemia: implications for the pathogenesis of arteriosclerosis. Am J Pathol, 56, 111-128.
McCully, K.S. & Wilson, R.B. (1975) Homocysteine theory of arteriosclerosis. Atherosclerosis, 22, 215-227.
Refsum, H., Ueland, P.M., Nygard, O. & Vollset, S.E. (1998) Homocysteine and cardiovascular disease. Annu Rev Med, 49, 31-62.
Jacques, P.F., Selhub, J., Bostom, A.G., Wilson, P.W. & Rosenberg, I.H. (1999) The effect of folic acid fortification on plasma folate and total homocysteine concentrations. N Engl J Med, 340, 1449-1454.
Baric, I. (2009) Inherited disorders in the conversion of methionine to homocysteine. J Inherit Metab Dis, 32, 459-471.
Khandanpour, N., Loke, Y.K., Meyer, F.J., Jennings, B. & Armon, M.P. (2009) Homocysteine and peripheral arterial disease: systematic review and meta-analysis. Eur J Vasc Endovasc Surg, 38, 316-322.
Marti-Carvajal, A.J., Sola, I., Lathyris, D. & Salanti, G. (2009) Homocysteine lowering interventions for preventing cardiovascular events. Cochrane Database Syst Rev, CD006612