Trong một số trường hợp người ta có thể nói ung thư là một bệnh di truyền, trong đó các tế bào ác tính đã trải qua quá trình đột biến và có những thay đổi có tính chất biểu sinh (epigenic) duy trì một kiểu hình biến nạp (transformed phenotype) ngay cả khi nuôi cấy hoặc khi tiêm vào các động vật thí nghiệm đã dung nạp miễn dịch. Tuy nhiên, hầu hết các biến cố di truyền trong các khối u lại là soma (tức là không di truyền), nó được mang đến từ môi trường hoặc do ngẫu nhiên nào đó và các nguyên nhân di truyền đã được xác định (thường gọi là nguyên nhân di truyền) chỉ chiếm một tỷ lệ rất nhỏ trong tất cả các ung thư.
Đặc biệt, các gen đột biến liên quan tới quá trình ung thư lại nằm trong 2 lớp: lớp gen kiềm chế các khối u và lớp gen gây ung thư. Việc phân biệt giữa các nguyên nhân do di truyền hay do môi trường có thể dễ dàng thấy được nếu như các hội chứng ung thư do các tác động đã được phơi bày, chẳng hạn như việc hút thuốc lá hay virus papilloma (virus gây các bệnh u nhú) là các tác nhân gây rủi ro cao. Trong hầu hết các ung thư thường gặp thì không phải như vậy và chúng được xem xét như là các bệnh phức tạp gây nên bởi sự tương tác giữa các yếu tố di truyền và môi trường. Các hiệu ứng di truyền sẽ dẫn đến ung thư có tính chất gia đình. Tuy nhiên, lớp ung thư này cũng có thể là do môi trường hoặc lối sống và việc tăng các rủi ro có tính chất gia đình thì không thể nói đó là do di truyền hay do môi trường.
Chúng tôi sẽ đề cặp dưới đây những nguyên nhân gây ung thư và các cơ chế phân tử đặc trưng nhất theo cách tiếp cận của gen trị liêu. Dĩ nhiên, việc nâng cao hiểu biết về nguyên nhân gây ung thư sẽ rất hữu ích đối với các nhà khoa học, với các nhà lâm sàng cũng như với việc xác định các chỉ số có tính chất dự phòng ung thư.
Cơ sở di truyền của sinh ung thư
Một cách ngắn gọn, ung thư có thể được coi như một bệnh do các gen ung thư và các đột biến cũng như những biến đổi biểu sinh (khiếm khuyết methyl hóa) trong các gen kìm chế khối u. Thông thường nhất có 2 dạng đột biến, một dạng có thể làm mất nghĩa -[missense] (làm biến đổi amino acid), thay đổi khung đọc và một dạng vô nghĩa -[nonsense] (do sự thay thế nucleotid tạo nên codon kết thúc, làm ngừng quá trình dịch mã và tổng hợp protein, quá trình này còn được gọi là đột biến kết thúc chuỗi).
Tuy vậy, đôi khi các đột biến không tác động tới trình tự amino acid nhưng lại ảnh hưởng khá nhiều tới promoter hoặc các vị trí ghép nối. Những đột biến trình tự DNA tuy không có liên hệ trực tiếp tới kiểu hình nhưng lại giữ vai trò quan trọng về sự đa hình.
Có nhiều cơ chế gây nên đột biến, bao gồm loại bỏ các đoạn lớn hoặc nhỏ DNA, đảo đoạn, chuyển vị, tạo vòng dẫn tới cắt bỏ trình tự v.v.. Nguyên nhân khởi đầu cho các cơ chế này là do bức xạ cực tím đối với các chất hóa học và các gen ung thư của virus. Nhưng với hầu hết các trường hợp ung thư thì việc xác định nguyên nhân vẫn rất sơ sài. Cũng có khả năng là, thực phẩm và các nguyên nhân thuộc môi trường giữ vai trò chủ chốt. Tuy nhiên, mối liên hệ giữa nguyên nhân và hiệu ứng thì rất khó chứng minh một cách rành mạch, bởi vì từ lúc khởi đầu của một khối u tới lúc có biểu hiện lâm sàng là một khoảng thời gian rất dài.
Bây giờ chúng ta hãy bàn luận về các đột biến di truyền đã được xác định là nguyên nhân gây ra ung thư.
Người ta đã xác định được rằng, những biến đổi di truyền rất quan trọng đối với sinh ung thư (có thể nhận diện như những biến đổi dòng trong các khối u ác tính), nó làm bất hoạt các gen kìm chế khối u. Tuy đã có hàng chục thành viên gây ung thư được xác định một cách rõ ràng nhưng vẫn còn hàng trăm thành viên khác chưa được tường tận. Một ví dụ kinh điển về gen ung thư là RAS, gen này khởi đầu được xác định là một gen hoạt hóa mạnh quá trình cảm ứng tạo khối u. Nhưng sau này những đột biến của RAS lại thường thấy ở rất nhiều dạng ung thư. Hầu hết các sản phẩm protein của gen ung thư đều liên quan tới sự truyền tín hiệu và điều hòa tăng trưởng. Cần phải lưu ý rằng chỉ cần một đột biến hoạt hóa một alen là đã đủ gây ra những hậu quả nghiêm trọng.
Chức năng bình thường của các protein được mã bởi các gen kiềm chế khối u thường liên quan mật thiết tới chức năng điều hòa hay quản gia (housekeeping) quan trọng đối với sự toàn vẹn các chức năng tế bào bao gồm phân chia và chết theo chương trình của tế bào. Vì vậy, khi các chức này bị mất sẽ tạo điều kiện thuận lợi cho sự tiến triển ác tính. Trong hầu hết các trường hợp, cả 2 alen ức chế khối u đều bị mất đi do vậy mà làm mất chức năng của các sản phẩm protein. Thường thì một alen bị mất do đột biến “cục bộ”; còn alen kia thì bị mất do loại bỏ lớn -[large deletion] (mất tính dị hợp tử). Các gen kiềm chế khối u kinh điển là p53 và APC (adenomatous polyposis coli). Các gen này có thay đổi rất lớn về chức năng liên quan tới kiểm soát chu kỳ sống cũng như chết theo chương trình của tế bào. Các đột biến của p53 được xác định trong hơn phân nửa các trường hợp ung thư.
APC khởi đầu được xác định như là một gen chứa đựng các đột biến mầm ở những bệnh nhân đa u tuyến (adenomatous polyposis) – một bệnh di truyền dẫn tới việc hình thành hàng trăm polyp ở ruột nếu không được điều trị, sau đó sẽ trở thành ác tính và là nguyên nhân gây chết ở lứa tuổi rất trẻ. APC có nhiều chức năng liên quan tới sự truyền tín hiệu và kết dính tế bào. APC là một ví dụ rất hay vì 2 lý do: thứ nhất, đây là một ví dụ hữu ích cho việc khám phá cơ sở phân tử một bệnh thông thường nhưng lại trên một bệnh di truyền hiếm gặp. Mặc dầu APC là hiếm gặp, nhưng những đột biến của APC (hoặc các thành viên con đường truyền tín hiệu của nó) lại liên tiếp phát hiện thấy trong tất cả các ung thư kết – trực tràng. Thứ hai là, theo các công trình nghiên cứu của Bert Vogelstein và cộng sự ở John Hopkins, Baltimore về APC và cơ sở di truyền của ung thư kết – trực tràng lại khám phá được một khía cạnh khác có thể là phổ biến ở nhiều dòng ác tính. Rõ ràng là sự bất hoạt của APC có thể là bước khởi đầu hay là giai đoạn sớm trong nhiều trường hợp ung thư kết – trực tràng, nhưng đó không phải là những biến đổi duy nhất thấy ở các khối u đã phát triển đến giai đoạn cao.
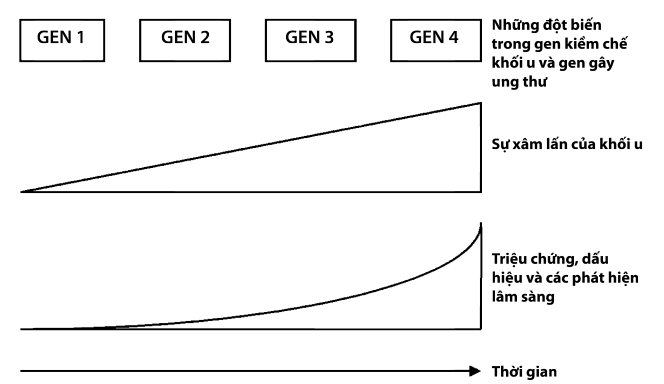
Thay vào đó, sự sinh ung thư thường là một quá trình xảy ra với nhiều bước, trong đó những đột biến tiếp theo lại tạo thuận lợi cho tăng sinh và làm giảm nhạy cảm đối với điều hòa tăng trưởng (Hình 1.1).
Đáng tiếc là tất cả đột biến xảy ra lại đều có lợi đối với dòng ác tính. Nhiều trường hợp đã tạo ra các dưới dòng (subclone) với khả năng sống kém hoặc dễ bị phát hiện bởi hệ miễn dịch. Tuy nhiên cũng có những biến đổi lại có lợi cho tăng trưởng, do vậy mà người ta phát hiện được các sản phẩm cuối của quá trình nhiều bước trong sự sinh ung thư, khi mà trong hầu hết các trường hợp khối u đã xâm lấn rộng và có thể đã di căn.
Những gen duy trì các đột biến khởi đầu cho phép quá trình ung thư tiếp tục được gọi là gen gác cổng (gatekeeper gene) (gen 1 – Hình 1.1). Theo lý thuyết thì mỗi dạng tế bào đều có vòng điều hòa tăng trưởng chủ chốt: việc làm bất hoạt chúng là điều cần thiết đối với sinh ung thư. APC đã từng được coi là người gác cổng đối với biểu mô kết – trực tràng.
Một lớp khác của gen kiềm chế khối u là gen lâm thời (caretaker gene): gen này có thể tạo thuận lợi cho các quá trình sinh ung thư đa bước do nó cho phép tích tụ nhanh các đột biến xa hơn. Những gen này thường liên quan tới sửa chữa DNA và duy trì tính toàn vẹn của hệ gen.
Đối với các nhà trị liệu gen, vấn đề quan trọng là cần phải tính xem cần bao nhiêu bước trong quá trình ngăn chặn để can thiệp một cách hiệu quả. Hiện giờ, câu trả lời chính xác vẫn còn bỏ ngỏ. Có lẽ khả dĩ nhất là hiệu đính một khiếm khuyết đơn, chẳng hạn như thay thế một gen kiềm chế ung thư bị khiếm khuyết hoặc làm bất hoạt một gen ung thư đang hoạt hóa quá mức. Làm được như vậy đã là đủ đối với kiểm soát quá trình ác tính hóa. Chẳng hạn như, khi p53 biểu lộ ở các tế bào ung thư có p53 đột biến thì các tế bào này sẽ trải qua apoptosis và trên thực tế nó có thể làm cho các tế bào ung thư kế cận cũng có hành động tương tự.
Hinh 1.1. Tính chất đa bước của ung thư. Những đột biến tích tụ dần trong các gen kiềm chế khối u và gen ung thư sẽ làm tăng khả năng xâm lấn của khối u cũng như sự di căn của chúng. Cùng với tăng về kích thước, cũng dần dần xuất hiện các triệu chứng và biểu hiện lâm sàng. Hầu hết các tổ chức và các bộ phận của cơ thể đều có khả năng dự phòng cao, vì thế nên các triệu chứng thường xuất hiện chậm hơn so với tiến triển của khối u.
(Theo Akseli Hemminki & Kari Hemminki. (2005) Cancer Gene Therapy. Human Press. Totowwa, New Jersey)
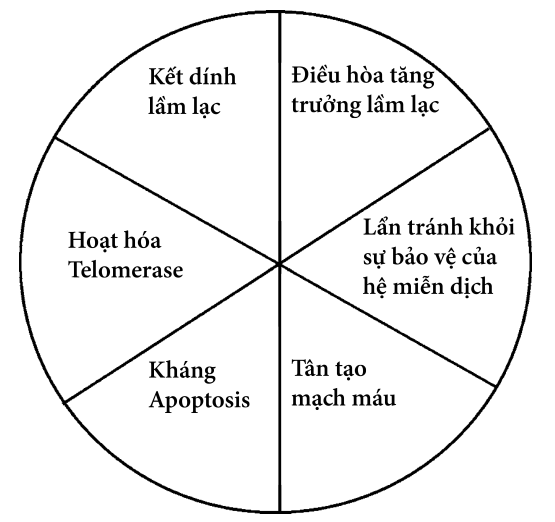
Hình 1.2. Những tác nhân thông thường làm ung thư tiến triển.
(Theo Akseli Hemminki & Kari Hemminki (2005), Cancer Gene Therapy. Human Press. Totowwa, New Jersey)
Bởi vậy, kiểu hình ác tính có thể được so sánh như một ngôi nhà có nhiều thành viên, nếu loại bỏ đi bất kỳ thành viên nào cũng gây nên sự sụp đổ toàn bộ cấu trúc của nó. Không có gì ngạc nhiên khi chúng ta xem xét các phương thức bảo vệ khác nhau của cơ thể con người kháng lại các tế bào ác tính. Cũng cần phải lưu ý rằng, các tế bào ác tính có thể đang lưu hành trong các cá thể khỏe mạnh chưa hề phát triển ung thư. Tuy nhiên, bệnh ung thư dễ phát triển ở những người tuổi cao, khi mà các cơ chế bảo vệ của cơ thể đã trở nên chậm chạp. Nhưng có lẽ phải trải qua nhiều thập kỷ thì ung thư mới có thể có được một tổ hợp cân bằng tinh tế các đặc trưng cho phép nó duy trì tăng trưởng mà không bị phát hiện bởi hệ miễn dịch.
Số lượng các gen được xác định là gen kiềm chế khối u hay gen ung thư ngày càng nhiều. Các sản phẩm protein tương ứng dường như có sự biến đổi lớn về chức năng. Tuy nhiên, các biến đổi di truyền liên quan tới ung thư thường rơi vào 6 loại sau đây (Hình 1.2): (1) kết dính lầm lạc (mất ức chế tiếp xúc), (2) đáp ứng tăng quá mức hoặc phi sinh lý đối với các tín hiệu thúc đẩy tăng trưởng và giảm đáp ứng với các tín hiệu điều hòa tăng trưởng, (3) thất bại trong quá trình chết theo chương trình của tế bào do có sự hủy hoại về mặt di truyền (mất chức năng trạm kiểm soát checkpoint chu kỳ tế bào), (4) bất tử hóa (nhờ hoạt tính của telomerase), (5) tránh né được sự bảo vệ của hệ miễn dịch và (6) các yếu tố thúc đẩy tân tạo mạch máu (neovasculogenesis) (các khối u phát triển nhanh nên cần phải được cung cấp nhiều oxy và các chất dinh dưỡng). Điều quan trọng là tất cả các hình ảnh này khác với các đặc trưng thấy trong hầu hết các tế bào không bị ác tính, vì thế chúng ta mới có thể can thiệp được.
Phân loại ung thư
Mặc dầu hầu hết các trường hợp ung thư đều có tính chất soma, tức là không có các thành phần đặc trưng gia đình, nhưng các nghiên cứu về hội chứng di truyền ngày nay đã cho phép chúng ta hiểu ung thư như là một bệnh di truyền. Tuy nhiên, cũng chưa có lý do nào đảm bảo chắc chắn rằng điều này sẽ đúng trong tương lai, bởi vậy chúng ta chỉ bàn luận ở đây một cách vắn tắt về tính di truyền của ung thư.
Có hai công trình nghiên cứu cung cấp cho chúng ta những hiểu biết về những thành phần có tính chất gia đình của các ung thư thường gặp. Công trình thứ nhất sử dụng thiết kế cặp đôi (twin) kinh điển, tức là so sánh sự tương quan của cặp đôi ung thư đơn hợp tử (monozygotic) và nhị hợp hợp tử (dizygotic) từ 3 nước Bắc Âu. Trong mô hình này, chắc chắn là cả 2 dạng cặp đôi đều chịu các hiệu ứng như nhau từ môi trường; cặp đôi đơn hợp tử được xác định là tương đồng di truyền, còn cặp đôi nhị hợp tử thì giống như trường hợp các anh chị em ruột, chỉ chia xẻ trung bình 50% số gen. Công trình thứ 2 dựa trên các dữ liệu về ung thư có tính chất gia đình trên toàn lãnh thổ Thụy Điển với 3 triệu gia đình. Người ta so sánh mối tương quan ung thư giữa tất cả các thành viên trong gia đình với cùng một mẫu thống kê như đã được sử dụng trong mô hình nghiên cứu cặp đôi. Các số liệu thu được có ý nghĩa thống kê cao hơn nhiều so với mô hình nghiên cứu cặp đôi bởi vì toàn bộ dân số Thụy Điển với 1 triệu khối u đã được xem xét một cách kỹ lưỡng. Mặt khác phần lớn các ung thư liên quan tới giới tính đặc biệt lại không thể đánh giá được theo mô hình này. Những kết quả của cả 2 mô hình nghiên cứu được trình bày ở Bảng 1.1.
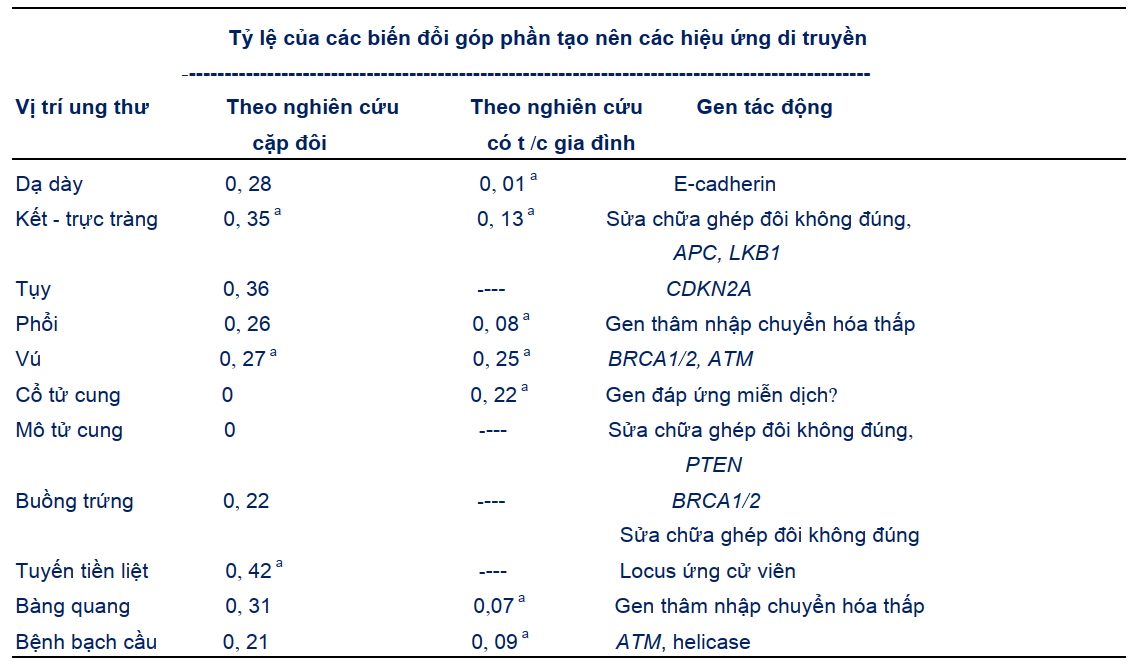
Bảng 1.1. Hiệu ứng di truyền và một số gen liên quan
Ghi chú: Khoảng tin cậy 95%, tức là có ý nghĩa thống kê (theo các số liệu từ các nghiên cứu cặp đôi ở Băc Âu và các nghiên cứu có tính chất gia đình ở Thụy Điển)
Đối với ung thư dạ dày, có 28% là di truyền theo nghiên cứu cặp đôi và 1% theo nghiên cứu gia đình. Với các ung thư khác thì các số liệu thu được lần lượt là 72% và 99%. Nguyên nhân của các ung thư cũng có thể là hoàn toàn do các hiệu ứng của môi trường.
Trong nghiên cứu cặp đôi, các chỉ số di truyền có ý nghĩa thống kê (độ tin cậy 95%) với ung thư kết – trực tràng là 35%, ung thư vú 27% và ung thư tuyến tiền liệt 42%. Các nghiên cứu về chỉ số gia đình cho các con số tương đương với ung thư vú, nhưng với ung thư kết – trực tràng thì thấp hơn. Chỉ số di truyền ung thư cổ tử cung là 22%, nhưng với ung thư phổi, ung thư bàng quang và các bệnh bạch cầu thì thấp hơn 10%. Tuy nhiên, một số ung thư thường gặp lại có thang di truyền rất cao so với các quan sát so sánh các rủi ro có tính chất gia đình giữa những người họ hàng ở cấp độ thứ nhất. Nếu ước tính về ung thư kết – trực tràng, ung thư vú và ung thư tuyến tiền liệt với các con số 27-42% thì rõ ràng vẫn còn một lỗ hổng rất lớn trong sự hiểu biết của chúng ta về cơ sở di truyền các u tân sinh.
Một số gen truyền các rủi ro có tính chất gia đình được liệt kê ở Bảng 1.1. Tần số đột biến trong các gen mẫn cảm cao đã được biết rất rõ như BRCA1 và BRCA2 trong ung thư vú và các gen sửa chữa DNA trong ung thư kết – trực tràng không polyp được di truyền là rất thấp. Đối với ung thư tuyến tiền liệt, tuy các gen ứng cử đã được xác định bản đồ nhưng lại chưa xác định được các chỉ số cụ thể. Những phát hiện này chứng minh rằng còn nhiều gen khác nữa vẫn chưa được xác định và cần phải có thêm các nghiên cứu tiếp theo.
CÁC MẪU UNG THƯ
Những hội chứng ung thư đã được nghiên cứu kỹ càng như u nguyên bào võng mạc, ung thư vú liên quan tới BRCA và HNPCC (hereditary nonpolyposis colorectal cancer) tuân theo mẫu di truyền Mendel trội với tần số cao (các vật mang có kiểu gen hợp với kiểu hình). Vì thế gần 50% hậu duệ của các bố mẹ bị tác động có biểu hiện bệnh. Tuy nhiên, những hội chứng này là hiếm và tần số gen đột biến là 1/1000 (tần số mắc bệnh là 1/500) hoặc nhỏ hơn. Hội chứng ung thư BRCA1, BRCA2 và HNPCC thường gặp nhất đối với tất cả ung thư vú và ung thư kết – trực tràng có lẽ là 1-3%. Hội chứng Bloom, hay mất điều hòa mao mạch (ataxia telangiectasia) và khô da nhiễm sắc tố (xeroderma pigmentosum) là các ví dụ về hội chứng ung thư Mendel trội. Khoảng 25% con cháu của các bậc cha mẹ có biểu hiện triệu chứng, bao hàm cả các khối u. Chúng ta có thể ước tính tương đối dễ dàng tỷ lệ của tất cả các dạng ung thư. Hội chứng đơn gen thường gây rủi ro cao, và 1% là một tỷ số tốt.
Hầu hết các ung thư thường gặp đều do các biến đổi ở nhiều gen. Theo lý thuyết đa giai đoạn về ung thư thì một khối xuất hiện là kết quả của rất nhiều đột biến ở một tế bào đơn. Những đột biến đầu tiên xảy ra ở các tế bào bình thường sẽ tạo nên một quần thể tiền u, tăng trưởng chậm. Những biến đổi phụ kèm theo trong một tế bào của quần thể tiền u là điều kiện cần thiết để tạo nên tế bào khối u có khả năng tăng sinh như một khối u ác tính. Nhiều đột biến có thể bị biến đổi và nó phụ thuộc vào các gen và các dạng tế bào bị tác động. Điều này có thể là đúng với các trường hợp sinh u do các đột biến di truyền. Đột biến gen gác cổng khởi đầu có thể tạo lợi thế cho sự tăng trưởng vì thế mà làm tăng kích cỡ đích (có rất nhiều tế bào khiếm khuyết sự khởi đầu) cho những đột biến kế tiếp.
Theo cách tính toán về tỷ số các đột biến, số các tế bào gốc và vòng đời của các tế bào người bình thường thì điều kiện thích hợp cho một quá trình sinh ung thư cần phải có ít nhất 3 đột biến, chẳng hạn như 2 đột biến ở giai đoạn khởi đầu và ít nhất một đột biến ở giai đoạn tiếp theo.
Khi hai hoặc nhiều gen có liên quan với nhau thì khó mà quan sát được chỉ số di truyền Mendel một cách thuần chủng, bởi vì rất có thể có một hậu duệ nào đó chỉ được truyền lại một cách ít ỏi bộ gen bệnh của cha mẹ. Vì thế thật khó mà phân biệt được rõ ràng các chỉ số di truyền đa yếu tố từ các gen đơn tần suất thấp hoặc các hiệu ứng môi trường; đó là một thách thức lớn đối với các phân tích phân ly hiện nay. Trong mô hình cặp đôi, chỉ số di truyền đa gen ở cặp đôi đơn hợp tử cho độ rủi ro cao hơn rất nhiều so với cặp đôi nhị hợp tử. Một mẫu khác về sự di truyền đa gen được phân biệt rõ ràng là đa ung thư sơ cấp ở một cá thể tương tự.
Các gen gây ung thư
Chỉ có một số nhỏ ung thư là do gen đơn. Tuy nhiên, từ những gia đình bị tác động ung thư đã giúp cho chúng ta định loại gen và phần lớn các khối u liên quan tới gen có tần số xuất hiện cao đã được mô tả từ những gia đình này. Những kết quả thu được ngay cả với các hội chứng hiếm gặp như Peutz – Jegher (bệnh nốt ruồi son ở mặt, nhất là quanh miệng, đôi khi ở niêm mạc miệng và bàn tay, kết hợp với bệnh polyp đường tiêu hóa rải rác ở dạ dày, trực tràng thường thoái hóa thành ác tính, bệnh di truyền theo kiểu trội), hay bệnh u lành tính cơ trơn tử cung và da, nếu các gia đình này là đồng nhất thì thường có rủi ro cao. Một khía cạnh lý thú của công trình nghiên cứu bệnh u lành tính cơ trơn là gen này lại mã cho một enzym trong vòng tricarboxylic là fumarat hydrase. Một enzym khác trong con đường chuyển hóa này là succinat dehydrogenase cũng liên quan với u cận hạch (paraganglioma) và u tế bào ưa chrom (pheochromecytoma) có thể được di truyền. Những số liệu này đã mở rộng tầm quan sát với các gen ung thư liên quan tới chuyển hóa, gen quản gia (housekeeping) trong quá trình điều hòa chu kỳ tế bào ở ngay các giai đoạn sớm, gen sửa chữa DNA và biến hóa chuyển nạp tín hiệu.
Các gen hiếm gặp nhưng rủi ro cao
Người ta đã xác định được nhiều dạng ung thư gen đơn gây rủi ro cao. Có khoảng 4700 di truyền trội và 2800 di truyền thoái hóa đã được biết đến từ đầu những năm 1990, trong số 440 gen đơn đã xuất hiện ung thư biến thái, nhiều dạng ung thư cực kỳ hiếm gặp với chỉ vài gia đình trên toàn thế giới. Hầu hết các hội chứng ung thư đã biết đều là trội ở mức rất đại chúng (mặc dầu thoái hóa ở mức độ phân tử), vật mang gen là typ Aa, trong đó a = gen đột biến. Trong nhiều khối u, alen bình thường đã bị biến mất (mất tính dị hợp tử) vì thế khối u này sẽ là bán hợp tử (hemizygote) hoặc đồng hợp tử (homozygote) aa nếu có một đột biến khác xảy ra để thay thế cho alen đã mất. Ở hội chứng ung thư trội, tần số xuất hiện đặc biệt cao, thường lên tới 100%. Điều này rất có lợi cho việc xác định các mẫu trội bởi vì những trường hợp này đều phát hiện thấy ở tất cả các thế hệ.
Một vài hội chứng ung thư hiếm gặp như bệnh khô da nhiễm sắc tố (xeroderma pigmentosum), mất điều hòa giãn mao mạch (ataxia telangiectasia) và hội chứng Bloom (ban đỏ giãn mao mạch ở mặt và bàn tay, những vùng teo da, những tổn thương bọng nước và cảm quang) là biểu hiện di truyền thoái hóa ở cả mức độ quần thể cũng như phân tử. Việc phát hiện các biểu hiện thoái hóa rất khó khăn bởi vì những trường hợp này đòi hỏi phải là xuất hiện một cách ngẫu nhiên trong điều kiện thuần chủng.
Những nhà di truyền học quần thể đặt nhiều câu hỏi tại sao lại chỉ có một số lượng tương đối nhỏ hội chứng thoái hóa ở người. Trong các mẫu ở động vật thí nghiệm, biểu hiện thoái hóa lại chiếm ưu thế, trái ngược lại – ở người, biểu hiện trội lại phổ biến hơn. Không ngoại trừ rằng đây là một quan sát lệch bởi vì có rất nhiều khó khăn khi xác định một mẫu thoái hóa. Một vấn đề phức tạp nữa là, trong nhiều hội chứng ung thư, các đột biến lại là đột biến mầm de novo không có trong mẫu gia đình. Đây là trường hợp của hầu hết các rối loạn khi ung thư xảy ra ở giai đoạn sớm, vì thế việc di truyền lại các khuyết tật cho các thế hệ sau sẽ bị giảm đi. Chẳng hạn như trường hợp khối u Wilms (u ác tính thận ở tuổi thơ: u có thể to, đau vùng bụng và thường bị tăng huyết áp, được hình thành từ tế bào dạng phôi thai), u nguyên bào võng mạc và u xơ thần kinh (neurofibromatose).
Nguy cơ tương đối (relative risk RR) của ung thư có thể rất cao trong các ung thư hiếm gặp. Trên thực tế, nếu tần số gần tới 100% thì RR chỉ phụ thuộc vào tần số quần thể của bệnh. Hầu hết các hội chứng đã biết đều tác động lên các cá thể trẻ tuổi. Những nguy cơ ngoại lệ của ung thư hiếm gặp ở những cá thể trẻ đã tạo thuận lợi cho việc xác định các hội chứng như Li – Fraumeri (các gia đình có thành viên bị ung thư các loại sớm: sarcom cơ vân ở vú, não), hội chứng tạo mới đa nội tiết 2 (multiple endocrine neoplasia 2- MEN2) và HNPCC. RR của ung thư thời thơ ấu trong hội chứng Li -Fraumeri (đột biến p53 di truyền) đã được xác định là > 100 và chỉ số này ở ung thư kết – trực tràng của HNPCCl là 70. Theo ước tính từ các số liệu ung thư gia đình ở Thụy Điển thì chỉ số RR là 30 với ung thư nội mạc tử cung ở HNPCC và 5000 cho ung thư tủy giáp ở MEN2.
Tỷ lệ các vật mang phụ thuộc vào quần thể và các đánh giá của Châu Âu và Âu Mỹ được coi là chính xác nhất. Trong số các hội chứng ung thư trội đã biết thì tần số vật mang gen cao nhất cho HNPCC vào khoảng 1/500 và với BRCA1 và BRCA2 đều là 1/1000. Đối với các hội chứng khác như Li -fraumeri, MEN1 và MEN2, u xơ thần kinh 1 và ung thư tế bào thận di truyền (đột biến ở VHL), u nguyên bào võng mạc, hội chứng Wilms, ung thư Gorlin (hội chứng di truyền xảy ra chủ yếu ở phụ nữ, có khả năng di truyền theo phương thức trội, biểu hiện tổn thương da teo và nhiễm sắc tố rải rác, bệnh u nhú niêm mạc thường kèm theo chậm phát triển tâm thần và rất nhiều các dị tật khác ở mặt hoặc ngón tay) thì tần số vật mang từ 1/3000 tới 1/50.000. Trong các ung thư thoái hóa như da khô nhiễm sắc tố và mất điều hòa giãn mao mạch (ataxia telangiectasia) thì tần số bệnh (a2) là thấp (1/1000.000 và 1/4000 theo thứ tự), nhưng tần số vật mang (2Aa) của mất điều hòa giãn mao mạch được xác định là 1-5% ở các quần thể thuộc Hoa Kỳ. Nếu ở dị hợp tử thì nguy cơ ung thư là rất có ý nghĩa. Các dị hợp tử của hội chứng mất điều hòa giãn mao mạch gây nguy cơ cao cho nhiều dạng ung thư trong đó có ung thư vú vì có rất nhiều vật mang. Theo các tính toán còn đang gây tranh cãi thì tỷ lệ góp phần làm mất điều hòa giãn mao mạch trong ung thư vú là cao hơn BRAC1 và BRCA2.
Một khía cạnh xa hơn nữa của các hội chứng ung thư có tính chất gia đình là chúng thường tác động vào nhiều vị trí, ngay cả khi phát hiện ra rằng các ung thư này ở vị trí có chỉ số (index) đặc biệt. Hội chứng Li -Fraumeri là một ví dụ với hơn 100 RR ở vị trí index (ung thư thời niên thiếu), tuy nhiên lại có mẫu RR cho các bệnh thông thường hơn như bệnh ung thư vú chẳng hạn. Các ví dụ khác nữa là HNPCC, BRCA 1 và BRCA2. Trong các hội chứng ung thư thoái hóa bao gồm mất điều hòa giãn mao mạch và hội chứng Bloom, các cá thể bị tác động có thể biểu lộ bất kỳ dạng u ác tính nào.
Một khía cạnh liên quan tới việc xác định sự tồn tại lâm sàng là sự hiện diện của các bệnh khác trong nhiều hội chứng đã biết. Những bệnh nhân có hội chứng thoái hóa là những người mất năng lực một cách trầm trọng như đã mô tả ở một số trường hợp. Tuy nhiên, có những bệnh không phải là ung thư nhưng rất nghiêm trọng vẫn thường vây quanh con người, thậm chí trội hơn các bệnh NF1 và NF2, MEN1 và MEN2 cũng như ung thư tế bào thận di truyền.
Các gen thường gặp rủi ro thấp
Những hiệu ứng có tính chất gia đình trong ung thư không những do các gen khiếm khuyết như đã trình bày ở trên mà còn có sự đóng góp của các khiếm khuyết thông thường với tần số đủ để tạo nên tính đa dạng (đôi khi được định nghĩa như là một biến thể có mặt ở > 1% quần thể). Nhiều tính đa dạng đã được mô tả trong các lĩnh vực thuốc và chuyển hóa của các chất gây ung thư, với một số dẫn liệu hiện đại về các receptor hormon và các gen sửa chữa DNA. Mặc dầu có vẻ như nhiều gen nguy cơ thấp lại làm thúc đẩy quá trình sinh ung thư ở người nhưng lại có rất nhiều trái ngược trong các tài liệu đương thời về vai trò của các gen chuyển hóa trong ung thư.
Sự trông nom miễn dịch giữ vai trò quan trọng trong ung thư, khi các bệnh nhân bị kiềm chế miễn dịch thì rõ ràng phải gánh chịu các nguy cơ như u lympho và nhiều dạng ung thư tế bào vảy (squamous cell carcinoma). Các thể nhẹ hơn của thiếu hụt miễn dịch có thể được lý giải trong các hội chứng có tính chất gia đình như u lympho không Hodgkin, bệnh Hodgkin, ung thư cổ tử cung và ung thư da tế bào vảy (squamous cell skin cancer). Khi chức năng miễn dịch bị kiềm chế thì có vẻ như là lại thúc đẩy đáp ứng của vật chủ đối với virus như virus gây u nhú ở người và virus Epstein- Barr.
Kết luận
Chưa có số liệu nào về nguyên nhân của ung thư để có thể bác bỏ vai trò nổi bật của môi trường với tư cách là một yếu tố gây hậu quả. Tuy nhiên, do báo cáo có tính chất kỷ nguyên của Doll và Peto năm 1981 mà đã có những tiến bộ nho nhỏ trong các nghiên cứu nhằm tìm ra những nguyên nhân mới của việc sinh ung thư do môi trường. Người ta suy luận rằng sinh ung thư bởi môi trường là do mối tương tác giữa các yếu tố bên ngoài và các yếu tố của vật chủ, điều đó chưa thể làm sáng tỏ chỉ bằng các phương pháp dịch tễ học hoặc sinh học phân tử. Cũng không có hy vọng rằng tập hợp các cách tiếp cận này trong dịch tễ học phân tử thậm chí sâu hơn nữa là dịch tễ học di truyền phân tử sẽ vạch ra được pha trung gian (interpha) giữa ngoại sinh (exogeneous) và nội sinh (endogeneous) của sinh ung thư trên người. Tuy nhiên, cũng không còn phải nghi ngờ gì nữa là nguyên nhân gây ra ác tính ở mức độ phân tử là do đột biến và biến đổi biểu sinh trong các gen kiềm chế khối u và gen gây ung thư. Hơn thế nữa, việc tích lũy dần các đột biến trong những gen này sẽ làm nới rộng các dòng vì thế mà cấu thành quá trình nhiều bước trong sự sinh ung thư.
Tất cả các dạng chính của ung thư đều có một thành phần mang tính chất gia đình với tần số thay đổi thường từ 1 đến 5%. Những nguy cơ có tính chất gia đình quan sát được trong số các cặp đôi và đa ung thư nguyên phát (multiple primary cancer) càng củng cố thêm cho quan điểm “sinh ung thư đa giai đoạn” trên người ở mức quần thể.
Về phương diện gen trị liệu, một vấn đề đặt ra là nếu nhiều gen tham dự vào một ung thư thì việc ngăn chặn hoặc sửa chữa một khiếm khuyết đã đủ làm đảo ngược được kiểu hình ác tính chưa? Với những bằng chứng hiện đại thì khi loại bỏ một thành viên (đột biến) khỏi ngôi nhà nhiều thành viên (khối u đã tiến triển) thì đã đủ hiệu lực chưa?
Tuy nhiên, khi xem xét những khả năng phi thường của ung thư đối với sức đề kháng thu được thì hiệu ứng kìm hãm tế bào là không đáng kể và thay vào đó là cần phải tiêu diệt ngay các tế bào ung thư càng nhanh càng tốt. Hơn nữa, ngoài sự đề kháng ở mức tế bào các khối u còn thu được sự đề kháng ở mức độ mô. Điều này ngụ ý rằng, có sự tồn tại các dưới dòng không nhạy cảm với việc xử lý. Vì thế, loại bỏ các thành viên tạp một cách đồng thời hoặc liên tục sẽ rất có lợi cho điều trị.
Nếu xem ung thư như là một bệnh gây bởi các đột biến và những biến đổi biểu sinh ở các gen thì ngay lập tức thấy rằng gen trị liệu là một phương tiện sinh học can thiệp cần thiết. Vì thế, nếu các khiếm khuyết về nguyên nhân gây bệnh được hiệu chỉnh hoặc được ngăn chặn thì kiểu hình của bệnh có thể sẽ bị đảo ngược. Sau chót là, những biến đổi di truyền hiện diện trên các tế bào ung thư đã cho chúng ta những đặc trưng để tách biệt chúng với các tế bào không bị ung thư. Những đặc trưng này là mất điều hòa promoter và các yếu tố tăng cường, biểu lộ nhầm lẫn các receptor và epitope vì tế bào đã mất cơ chế kháng virus. Những vấn đề đã được đề cập trên có thể được ứng dụng trong khi lập kế hoạch các chiến lược gen trị liệu nhằm tiêu diệt trực tiếp các tế bào ung thư.