Giới thiệu
Trong khi tưới máu mô là một trong những mục tiêu chính của chúng tôi để hồi sức huyết động, theo dõi huyết động cổ điển chỉ cung cấp bằng chứng gián tiếp về tưới máu mô. Nhiều bệnh nhân bị suy tuần hoàn có sự thay đổi trong tưới máu mô mặc dù đã tối ưu hóa huyết động học toàn thân. Trong khi suy yếu phân phối lưu lượng máu phải được xem xét, thay đổi vi tuần hoàn cũng đã được quan tâm. Sự thay đổi vi tuần hoàn đã được chứng minh trong các mô hình thực nghiệm khác nhau. Tuy nhiên, việc xác định các thay đổi vi tuần hoàn ở bệnh nhân bị bệnh nghiêm trọng từ lâu đã rất khó khăn do thiếu công nghệ thích hợp. Những tiến bộ gần đây trong công nghệ, tuy nhiên, đã cho phép đánh giá vi tuần hoàn ở bệnh nhân. Rối loạn chức năng vi mạch đã được báo cáo đầu tiên ở những bệnh nhân bị nhiễm trùng huyết và sốc nhiễm trùng [1] nhưng sau đó đã được báo cáo trong nhiều tình trạng khác gặp phải ở những bệnh nhân nguy kịch. Trong chương này, chúng ta sẽ thảo luận về tính đặc hiệu của vi tuần hoàn, bằng chứng cho sự thay đổi vi mạch và các công cụ có thể được sử dụng để đánh giá vi tuần hoàn.
Cấu trúc giải phẫu của vi tuần hoàn.
Các vi tuần hoàn bao gồm các mạch nhỏ hơn 100 micron và bao gồm các tiểu động mạch, mao mạch và tĩnh mạch. Cấu trúc thông thường nhất là khía cạnh cây phân nhánh, với các tiểu động mạch phân chia tại một số điểm nhánh thành những điểm nhỏ hơn, đến các mao mạch, tập trung lại trong các tĩnh mạch, sau đó chúng hợp lại trong các tĩnh mạch lớn hơn. Vai trò của tiểu động mạch về cơ bản là phân phối lưu lượng máu đến các bộ phận khác nhau của cơ quan, điều chỉnh dòng chảy để chuyển hóa cục bộ. Các tiểu động mạch lớn hơn được gọi là tiểu động mạch trở kháng, vì chúng bị giảm áp lực lớn giữa lối vào và lối ra của các mạch máu này. Các tiểu động mạch đoạn xa và mao mạch là nơi diễn ra trao đổi oxy với các mô. Khi oxy khuếch tán từ hồng cầu chảy trong mao mạch, khoảng cách khuếch tán trở thành yếu tố hạn chế. Do đó, ở cấp độ vi tuần hoàn, mật độ của các mạch được tưới máu có liên quan đến oxy hóa mô hơn là tốc độ mà các tế bào hồng cầu đang chảy trong mao mạch được tưới máu.
Các cơ quan như thận và ruột có cấu trúc vi mạch khác nhau, liên quan đến các nối tắt tiền mao mạch hoặc trao đổi ngược dòng, khiến các cơ quan này dễ bị thiếu oxy hơn các cơ quan khác.
Việc kiểm soát tưới máu vi mạch bị ảnh hưởng bởi các yếu tố địa phương, với sự giao tiếp ngược qua các kênh khác nhau, cho phép thích ứng tưới máu với chuyển hóa cục bộ.
Một yếu tố quan trọng khác để cung cấp oxy ở cấp độ vi tuần hoàn là hematocrit mao mạch. Vì hiệu ứng thể tích của lớp plasma ở bề mặt nội mạc mạch máu lớn hơn tương đối ở mức mao mạch so với trong các mạch lớn, hematocrit mao mạch thấp hơn nhiều so với hệ thống. Ngoài ra, hematocrit thấp hơn ở các mạch nhánh bên so với mạch thẳng, do quán tính động học của hồng cầu. Theo đó, hematocrit mao mạch rất khó dự đoán từ các phép đo hematocrit toàn thân.
Tất cả các yếu tố này làm cho khó dự đoán tưới máu vi mạch và cung cấp oxy mô từ các phép đo huyết động học toàn thân. Ngoài ra, các biện pháp can thiệp trị liệu nhằm tăng cường cung cấp oxy toàn thân có thể không làm tăng việc cung cấp oxy ở cấp độ vi tuần hoàn.
Thay đổi vi tuần hoàn trong bệnh lý
Nhiễm trùng huyết
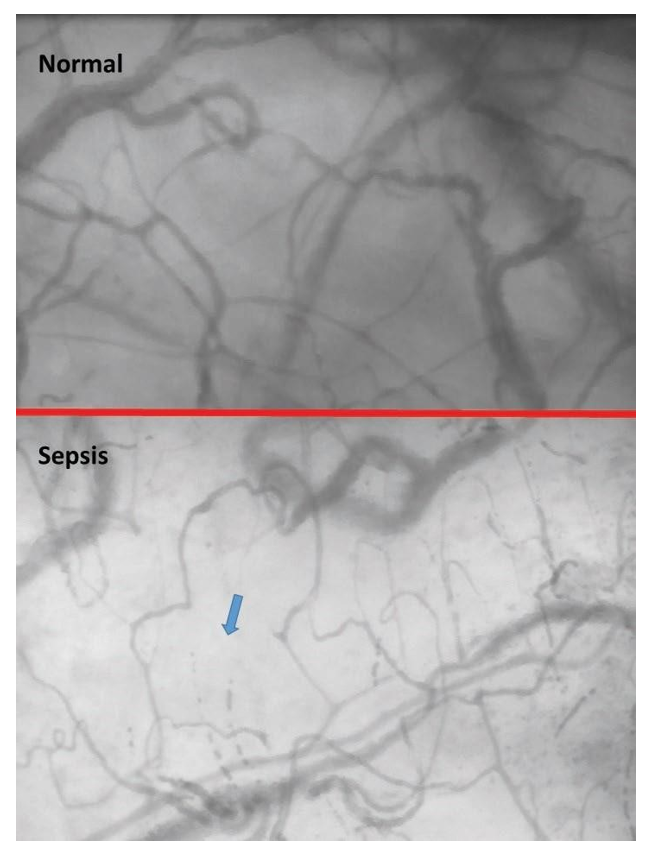
Trong một bài báo “bước ngoặt” xuất bản năm 2002, De Backer et al. [1] đã chứng minh rằng vi tuần hoàn dưới lưỡi của bệnh nhân nhiễm trùng huyết và sốc nhiễm trùng đã thay đổi rõ rệt so với tình nguyện viên khỏe mạnh và đối chứng ICU. Bệnh nhân bị nhiễm trùng đã giảm mật độ của các mạch máu được tưới máu, do sự gia tăng kết hợp của dòng chảy bị dừng cũng như trong các mạch máu được tưới máu không liên tục, với các mạch máu được tưới máu ở gần các mạch được tưới máu (Hình 14.1). Những thay đổi này chỉ được quan sát thấy trong các mạch máu nhỏ hơn 20 micron, đại diện cho hầu hết các mao mạch. Một yếu tố chính của những thay đổi vi tuần hoàn này là sự không đồng nhất bên trong trường quan sát mà còn giữa một số trường được đóng bởi một vài micron. Điều quan trọng là những bất thường này đã không được cố định, vì việc sử dụng acetylcholine tại chỗ đã bình thường hóa hoàn toàn việc vi tuần hoàn dưới lưỡi của những bệnh nhân bị nhiễm trùng này. Những kết quả này đã được sao chép trong hơn 40 bài báo từ các đội khác nhau trên thế giới.
Sự liên quan của những thay đổi này là gì? Trong các mô hình thực nghiệm, các khu vực tưới máu vi tuần hoàn bị suy yếu được đồng nhất hóa với các khu vực thiếu oxy và thậm chí là chết tế bào [2]. Ở người, điều này phức tạp hơn để chứng minh, nhưng những cải thiện trong tưới máu vi tuần hoàn có liên quan đến sự cải thiện nồng độ lactate. Một số nghiên cứu đã chỉ ra rằng sự thay đổi vi tuần hoàn dưới lưỡi có liên quan đến kết quả [1, 3, 4]. Trong số các biến số vi tuần hoàn liên quan đến kết quả, mật độ mao mạch được tưới máu và tỷ lệ mao mạch được tưới máu có liên quan tích cực đến tỷ lệ sống, trong khi chỉ số không đồng nhất có liên quan nghịch với tỷ lệ sống [1, 3, 5]. Ngược lại, tốc độ của các tế bào hồng cầu trong các mạch được tưới máu không khác nhau giữa những người sống sót và không sống sót [6], minh họa rằng khuếch tán và không đối lưu là rất quan trọng đối với quá trình oxy hóa mô. Do đó, sự thay đổi vi tuần hoàn có liên quan đến sinh lý bệnh của rối loạn chức năng cơ quan và tử vong.
Hình 14.1 Ví dụ về đánh giá vi mô của vi tuần hoàn dưới lưỡi. Hình ảnh SDF được ghi lại ở một bệnh nhân đối chứng (bình thường) và ở một bệnh nhân bị sốc nhiễm trùng (nhiễm trùng huyết).
Điều gì có thể là các cơ chế tiềm năng chịu trách nhiệm cho những thay đổi này? Các mô hình thực nghiệm nhiễm trùng huyết nhấn mạnh rằng một số cơ chế có liên quan, bao gồm rối loạn chức năng nội mô, phản hồi ngược bị suy giảm, độ nhạy cảm với các chất gây co mạch và giãn mạch, thay đổi glycocalyx và sự kết dính của các tế bào lưu thông [7].
Có phải là những thay đổi liên quan đến thay đổi trong huyết động học hệ thống? Mối quan hệ giữa tưới máu vi tuần hoàn và áp lực động mạch hoặc cung lượng tim ở mức tốt nhất, là lỏng lẻo [8, 9]. Sự thay đổi vi mạch là tương tự ở những bệnh nhân bị nhiễm trùng có cung lượng tim thấp và cao [10]. Do đó những điều này không thể được phát hiện bằng cách xem xét huyết động học toàn thân. Có thể bỏ qua huyết động hệ thống? Rõ ràng là không, tưới máu vi mạch không thể được duy trì nếu không đạt được cung lượng tim tối thiểu hoặc huyết áp, nhưng giá trị này là khá. Mũi tên màu xanh biểu thị một biến khu vực không được tưới máu giữa các cá nhân do đó khá khó để xác định giá trị ngưỡng rõ ràng. Vì lý do này, tăng áp lực tưới máu và cung lượng tim đều liên quan đến một phản ứng thay đổi và không thể đoán trước [8, 11].
Suy chức năng vi tuần hoàn trong các bệnh lý khác.
Sự thay đổi vi mạch tương đối giống nhau (mặc dù thường ít nghiêm trọng hơn) so với những trường hợp được báo cáo trong sốc nhiễm trùng cũng đã được quan sát thấy trong các điều kiện khác. Ở những bệnh nhân bị sốc tim, mật độ vi mạch và tưới máu mao mạch bị giảm, cùng với sự gia tăng không đồng nhất tưới máu [12, 13]. Những thay đổi này có liên quan đến kết cuộc [12, 13].
Ở những bệnh nhân được cấp cứu sau chấn thương, mức độ nghiêm trọng và thời gian tưới máu vi mạch có liên quan đến rối loạn chức năng cơ quan [14]. Tương tự như vậy, bệnh nhân phẫu thuật có nguy cơ cao xuất hiện các biến chứng sau phẫu thuật có rối loạn chức năng vi mạch xung quanh phẫu thuật nghiêm trọng hơn và kéo dài hơn so với nhóm không có rối loạn với cuộc mổ không biến chứng [15].
Rối loạn chức năng vi tuần hoàn cũng đã được quan sát thấy trong sản giật [16] hoặc sau khi ngừng tim [17].
Đánh giá vi tuần hoàn như thế nào
Như đã trình bày ở trên, sự thay đổi vi tuần hoàn không thể được phát hiện bằng cách theo dõi huyết động cổ điển. Tốt nhất, những điều này có thể được đề xuất ở một bệnh nhân có cung lượng tim và giá trị áp lực động mạch trong các mục tiêu và độ bão hòa oxy tĩnh mạch cao (SvO2) cho thấy các dấu hiệu lâm sàng của giảm tưới máu mô hoặc tăng mức độ lactate máu. Biomarkers như lactate có thể chỉ ra tình trạng thiếu oxy mô, nhưng nguồn gốc của nó không thể nằm trong vi tuần hoàn. Ngoài ra, việc giảm lactate máu có thể mất thời gian sau khi tưới máu được phục hồi.
Dấu hiệu lâm sàng có thể xuất hiện hấp dẫn. Lốm đốm da, thời gian làm đầy mao mạch và nhiệt độ da là những chỉ số tuyệt vời của tưới máu vi tuần hoàn ở da [18]. Đó là các biện pháp dễ dàng đo lường và thường không tốn kém. Ngoài ra, thay đổi tưới máu da có liên quan đến kết cuộc [19, 20]. Thật không may, những dấu hiệu lâm sàng này chỉ tiếp cận cho tưới máu vi tuần hoàn da và bị ảnh hưởng rất nhiều bởi các điều kiện tại chỗ (nhiệt độ môi trường) hoặc tình trạng bệnh nhân (bệnh động mạch ngoại biên, hiện tượng Raynaud, v.v.) hoặc sử dụng thuốc vận mạch. Ngoài ra, vi tuần hoàn da có thể không phản ánh nhiều khu vực vi tuần hoàn trung tâm hơn, đặc biệt là khi tình trạng co mạch da là một phản ứng sinh lý quan trọng giúp bảo tồn tưới máu đến các cơ quan quan trọng hơn. Do đó, đánh giá tưới máu vi tuần hoàn da rất hữu ích như một công cụ xử lý nhưng thiếu tính đặc hiệu. Theo đuổi bình thường hóa tưới máu vi tuần hoàn da do đó có nguy cơ điều trị quá mức một số bệnh nhân hoặc thậm chí chuyển dòng máu từ cơ quan quan trọng sang tưới máu da (vì nó có thể xảy ra với một số thuốc giãn mạch).
Nhìn trực tiếp của vi tuần hoàn
Hai kính hiển vi cầm tay khác nhau hiện đang được sử dụng để trực quan hóa vi tuần hoàn ở bệnh nhân bị bệnh nghiêm trọng (trường tối sidestream (SDF) và hình ảnh liên quan trường tối (IDF)) [21]. Về cơ bản, những trường chiếu sáng này bằng cách sử dụng sự phản xạ ánh sáng từ các lớp sâu hơn và các mạch được hiển thị bởi vì ánh sáng được hấp thụ ở bước sóng chọn lọc bởi hemoglobin có trong các tế bào hồng cầu. Những kính hiển vi này hầu hết được áp dụng trên vùng dưới lưỡi (Hình 14.1), vì da được bao phủ bởi một biểu mô dày biểu hiện khó hình dung của vi tuần hoàn. Vi tuần hoàn dưới lưỡi có ưu điểm là tương đối trung tâm và ở nhiệt độ lõi, ít bị ảnh hưởng bởi nhiệt độ môi trường và co mạch ngoại vi. Thật không may, rất khó để áp dụng các thiết bị này trên vùng dưới lưỡi ở bệnh nhân không đặt nội khí quản. Ngoài ra, cần hết sức cẩn thận để loại bỏ dịch tiết và hạn chế tạo tác áp lực. Các khuyến nghị về thu thập và phân tích hình ảnh gần đây đã được công bố [21]. Hình ảnh vi tuần hoàn hầu hết được phân tích bằng phân tích thủ công ngoại tuyến bằng cách sử dụng lưới để đếm các mạch máu. Nhãn cầu là khả thi và đáng tin cậy để đánh giá các biến đơn giản. Phân tích hỗ trợ phần mềm đang trở nên sẵn sàng.
Đánh giá gián tiếp tưới máu vi tuần hoàn
Test hoạt động mạch
Do sự không đồng nhất của tưới máu vi tuần hoàn trong bệnh lý, vi tuần hoàn có thể được đánh giá trực tiếp bằng Doppler laser hoặc cảm biến oxy. Thật vậy, những biện pháp đo lường tưới máu hoặc oxy hóa này trong một thể tích tương đối lớn (ít nhất 1 mm3) có chứa nhiều mạch bao gồm tiểu động mạch, mao mạch và tĩnh mạch. Theo đó, giá trị đo được biểu thị mức trung bình của lưu lượng / PO2 trong các mạch máu khác nhau và không tính đến các mạch máu không được sử dụng. Tuy nhiên, vi tuần hoàn có thể được đánh giá gián tiếp bằng cách ước tính độ hoạt động mạch sau khi tắc tạm thời. Phân tích sự thay đổi lưu lượng máu / độ bão hòa O2 trong một giai đoạn ngắn của thiếu máu cục bộ cẳng tay cho phép định lượng dự trữ vi mạch. Một số chỉ số có thể được đo, nhưng độ dốc tăng dần, hoặc độ dốc phục hồi, là dễ đo nhất và có thể lặp lại nhiều nhất.
Iontophoresis [22] và thử thách nhiệt [23], cả hai được kết hợp với Doppler laser, đều có thể được sử dụng để đánh giá phản ứng của da với các loại thuốc giãn mạch khác nhau hoặc sưởi ấm tiêu chuẩn, tương ứng. So với tắc tạm thời, chúng có lợi thế để khám phá nhiều vùng da trung tâm hơn và không nhạy cảm với co mạch ngoại vi xảy ra khi đáp ứng với bệnh cũng như dùng thuốc vận mạch.
Độ chênh PCO2
PCO2 mô tăng trong điều kiện dòng chảy thấp. Để thoát khỏi ảnh hưởng của PCO2 động mạch, gradient PCO2 động mạch của mô, hoặc khoảng cách PCO2, được tính toán. Các phép đo PCO2 mô đã được sử dụng để phản ánh tưới máu vi tuần hoàn ở vùng dưới lưỡi hoặc thậm chí vùng dạ dày. Thật không may, những kỹ thuật này không còn nữa.
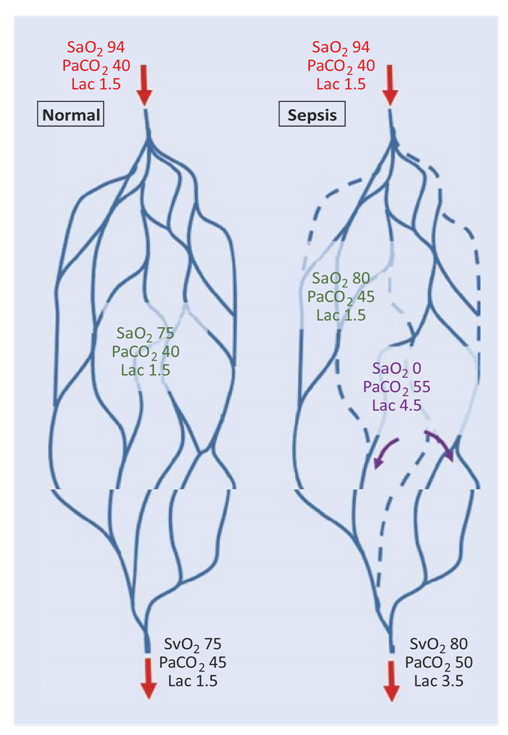
Độ chênh PCO2 trong tĩnh mạch có thể được sử dụng để đánh giá gián tiếp tưới máu vi tuần hoàn[24]. PCO2 tĩnh mạch được đo trên khí máu tĩnh mạch thu được trong catheter tĩnh mạch trung tâm hoặc động mạch phổi, đồng thời với khí máu động mạch. Vì PCO2 có thể khuếch tán khoảng cách xa hơn PO2, sự tích lũy PCO2 ở các khu vực không được tưới máu đang dần khuếch tán đến các tĩnh mạch dẫn thoát (Hình 14.2) do đó độ chênh PCO2 tĩnh mạch -động mạch cũng tăng trong trường hợp thay đổi vi tuần hoàn, mặc dù ít hơn đáng kể so với trong mô chính nó. Độ chênh PCO2 tĩnh mạch-động mạch phải được giải thích kết hợp với độ bão hòa O2 tĩnh mạch: độ chênh PCO2 tĩnh mạch-động mạch chủ yếu thể hiện cung lượng tim thay đổi khi độ bão hòa O2 tĩnh mạch thấp, trong khi nó chủ yếu đại diện cho sự thay đổi của vi mạch máu khi độ bão hòa O2 tĩnh mạch là bình thường hoặc tăng [25].
Hình 14.2 Mối quan hệ giữa độ chênh PCO2 tĩnh mạch-động mạch và thay đổi vi tuần hoàn. Trong điều kiện bình thường, hầu hết các khu vực được tưới máu đầy đủ và do đó được oxy hóa. Yêu cầu trao đổi chất được đáp ứng với nhu cầu và không có sự đình trệ dòng chảy. Sản xuất CO2 nhanh chóng bị “rửa trôi”, và độ chênh PCO2 tĩnh mạchđộng mạch là tối thiểu. Trong điều kiện nhiễm trùng huyết, vi tuần hoàn không đồng nhất, với các khu vực được tưới máu kém ở gần khu vực được tưới máu tốt. Ở những khu vực không được tưới máu, có sự gia tăng CO2 do ứ đọng dòng chảy và tạo ra CO2 kỵ khí gián tiếp do môi trường đệm H + được tạo ra bởi quá trình thủy phân ATP. Điều thú vị là CO2 có khả năng khuếch tán khoảng cách xa hơn so với O2 để có thể đến các tĩnh mạch dẫn thoát. Ở những khu vực được tưới máu tốt, dòng chảy trở nên dư thừa, do đó SO2 tĩnh mạch của khu vực này bị dư thừa, góp phần làm cho SvO2 cao. Do đó, phía tĩnh mạch của vi tuần hoàn bị bệnh được đặc trưng bởi SvO2, PCO2 và lactate cao.
Giới hạn
Một trong những hạn chế quan trọng nhất là chúng tôi đang xem xét vi tuần hoàn trong một cơ quan hy vọng rằng nó có thể đại diện cho vi tuần hoàn của các cơ quan khác. Trong khi quá trình dẫn đến rối loạn chức năng nội mô đang ảnh hưởng đến vi tuần hoàn ở các cơ quan khác nhau (nó đã được chứng minh một cách độc đáo trong trường hợp nhiễm trùng huyết, vi tuần hoàn cũng bị ảnh hưởng tương tự ở tất cả các cơ quan, bao gồm não, gan và thận), một số đặc điểm giải phẫu hoặc yếu tố tại chỗ có thể làm cho một số cơ quan thậm chí còn nhạy cảm hơn những cơ quan khác. Theo đó, người ta thường cho rằng những thay đổi vi tuần hoàn được phát hiện ở vùng dưới lưỡi có khả năng phản ánh những thay đổi tối thiểu có thể quan sát được ở các cơ quan khác, trong khi các cơ quan khác có thể có những thay đổi nghiêm trọng hơn hoặc đáp ứng khác nhau với các can thiệp điều trị do yếu tố tại chỗ.
Ý nghĩa thực hành
Vi tuần hoàn là một yếu tố quyết định quan trọng của tưới máu cơ quan. Một khi cung lượng tim thỏa đáng và áp lực động mạch được tạo ra, sự thay đổi vi tuần hoàn trở thành yếu tố quyết định chính của tưới máu mô.
Thay đổi vi tuần hoàn đã được chứng minh chủ yếu ở nhiễm trùng huyết mà còn trong suy tim nặng, chấn thương và phẫu thuật có nguy cơ cao. Những thay đổi này được đặc trưng bởi sự giảm mật độ của các mạch máu được tưới máu và sự không đồng nhất của các khu vực gần một vài micron.
Thay đổi vi tuần hoàn không thể được phát hiện bằng các công cụ huyết động cổ điển. Mối liên hệ giữa áp lực động mạch / cung lượng tim và tưới máu vi tuần hoàn tốt nhất là tương đối lỏng lẻo.
Đánh giá lâm sàng của vi tuần hoàn thường không đóng góp vì ghi nhận sự phân ly từ ngoại vi đến tuần hoàn trung tâm hơn.
Vi tuần hoàn phải được đo trực tiếp (kính hiển vi cầm tay áp trên vùng dưới lưỡi) hoặc được đánh giá gián tiếp bằng cách đo độ chênh PCO2 tĩnh mạch.
Với các đặc điểm của sự thay đổi vi tuần hoàn, những điều này thường không thành công trong các can thiệp huyết động học cổ điển (dịch truyền / tác nhân gây tăng co bóp cơ tim/ thuốc vận mạch). Trong khi các nghiên cứu thực nghiệm đã báo cáo kết quả đầy hứa hẹn với một số can thiệp, tác dụng có lợi của những điều này cần phải được xác nhận trong khu vực lâm sàng.
Mặc dù việc đánh giá vi tuần hoàn vẫn còn trong khu vực nghiên cứu, sự hiểu biết về các thay đổi vi tuần hoàn vẫn rất quan trọng đối với sự hiểu biết về thay đổi tưới máu kéo dài mặc dù đã điều chỉnh các thay đổi về huyết động học toàn thân.
Kết luận
Các vi tuần hoàn là một yếu tố chính quyết định tưới máu mô và các thay đổi vi tuần hoàn thường tồn tại sau khi điều chỉnh các thay đổi toàn thân. Mặc dù điều tra về vi tuần hoàn vẫn thuộc về khu vực nghiên cứu, điều quan trọng là phải hiểu những điều này có thể tồn tại và góp phần vào rối loạn chức năng cơ quan.
Thông tin mang về
Thay đổi vi tuần hoàn xuất hiện ở nhiều bệnh nhân bị bệnh nặng, và đặc biệt là nhiễm trùng huyết, và góp phần gây rối loạn chức năng nội tạng và kết cuộc nghèo nàn.
Ngay cả khi không phải lúc nào cũng có thể trực tiếp hình dung những thay đổi này cũng như không thể kiểm soát những thay đổi này, điều quan trọng là phải hiểu rằng những điều này có thể tồn tại để đảm bảo kiểm soát tốt hơn nguồn nhiễm trùng huyết hoặc để nỗ lực ngăn chặn để tăng tưới máu mô bằng cách thúc đẩy hơn hệ thống huyết động trong khi vi tuần hoàn không đáp ứng với các can thiệp này.
Tài liệu tham khảo
De Backer D, Creteur J, Preiser JC, Dubois MJ, Vincent JL. Microvascular blood flow is altered in patients with sepsis. Am J Respir Crit Care Med. 2002;166(1):98–104.
Wu L, Mayeux PR. Effects of the inducible nitric-oxide synthase inhibitor L-N(6)(1-iminoethyl)-lysine on microcirculation and reactive nitrogen species generation in the kidney following lipopolysaccharide administration in mice. J Pharmacol Exp Ther. 2007;320(3):1061–7.
De Backer D, Donadello K, Sakr Y, Ospina-Tascon GA, Salgado DR, Scolletta S, et al. Microcirculatory alterations in patients with severe sepsis: impact of time of assessment and relationship with outcome. Crit Care Med. 2013;41(3):791–9.
Hernandez G, Boerma EC, Dubin A, Bruhn A, Koopmans M, Edul VK, et al. Severe abnormalities in microvascular perfused vessel density are associated to organ dysfunctions and mortality and can be predicted by hyperlactatemia and norepinephrine requirements in septic shock patients. J Crit Care. 2013;28(4):538–14.
Sakr Y, Dubois MJ, De Backer D, Creteur J, Vincent JL. Persistant microvasculatory alterations are associated with organ failure and death in patients with septic shock. Crit Care Med. 2004;32:1825–31.
Edul VS, Enrico C, Laviolle B, Vazquez AR, Ince C, Dubin A. Quantitative assessment of the microcirculation in healthy volunteers and in patients with septic shock. Crit Care Med. 2012;40:1443–8.
De Backer D, Donadello K, Taccone FS, Ospina-Tascon G, Salgado D, Vincent JL. Microcirculatory alterations: potential mechanisms and implications for therapy. Ann Intensive Care. 2011;1(1):27.
De Backer D, Creteur J, Dubois MJ, Sakr Y, koch M, Verdant C, et al. The effects of dobutamine on microcirculatory alterations in patients with septic shock are independent of its systemic effects. Crit Care Med. 2006;34(2):403–8.
Ospina-Tascon G, Neves AP, Occhipinti G, Donadello K, Buchele G, Simion D, et al. Effects of fluids on microvascular perfusion in patients with severe sepsis. Intensive Care Med. 2010;36(6):949–55.
Edul VS, Ince C, Vazquez AR, Rubatto PN, Espinoza ED, Welsh S, et al. Similar microcirculatory alterations in patients with normodynamic and hyperdynamic septic shock. Ann Am Thorac Soc. 2016;13(2):240–7.
Dubin A, Pozo MO, Casabella CA, Palizas F Jr, Murias G, Moseinco MC, et al. Increasing arterial blood pressure with norepinephrine does not improve microcirculatory blood flow: a prospective study. Crit Care. 2009;13(3):R92.
De Backer D, Creteur J, Dubois MJ, Sakr Y, Vincent JL. Microvascular alterations in patients with acute severe heart failure and cardiogenic shock. Am Heart J. 2004;147:91–9.
den Uil CA, Lagrand WK, van der EM, Jewbali LS, Cheng JM, Spronk PE, et al. Impaired microcirculation predicts poor outcome of patients with acute myocardial infarction complicated by cardiogenic shock. Eur Heart J. 2010;31:3032–9.
Tachon G, Harrois A, Tanaka S, Kato H, Huet O, Pottecher J, et al. Microcirculatory alterations in traumatic hemorrhagic shock. Crit Care Med. 2014;42(6):1433–41.
Jhanji S, Lee C, Watson D, Hinds C, Pearse RM. Microvascular flow and tissue oxygenation after major abdominal surgery: association with post-operative complications. Intensive Care Med. 2009;35(4):671–7.
Ospina-Tascon GA, Nieto Calvache AJ, Quinones E, Madrinan HJ, Valencia JD, Bermudez WF, et al. Microcirculatory blood flow derangements during severe preeclampsia and HELLP syndrome. Pregnancy Hypertens. 2017;10:124–30.
Donadello K, Favory R, Salgado-Ribeiro D, Vincent JL, Gottin L, Scolletta S, et al. Sublingual and muscular microcirculatory alterations after cardiac arrest: a pilot study. Resuscitation. 2011;82(6):690–5.
Ait-Oufella H, Bakker J. Understanding clinical signs of poor tissue perfusion during septic shock. Intensive Care Med. 2016;42(12):2070–2.
Ait-Oufella H, Lemoinne S, Boelle PY, Galbois A, Baudel JL, Lemant J, et al. Mottling score predicts survival in septic shock. Intensive Care Med. 2011;37(5):801–7.
Hernandez G, Pedreros C, Veas E, Bruhn A, Romero C, Rovegno M, et al. Evolution of peripheral vs metabolic perfusion parameters during septic shock resuscitation. A clinical-physiologic study. J Crit Care. 2012;27(3):283–8.
Ince C, Boerma EC, Cecconi M, De Backer D, Shapiro NI, Duranteau J, et al. Second consensus on the assessment of sublingual microcirculation in critically ill patients: results from a task force of the European Society of Intensive Care Medicine. Intensive Care Med. 2018;44:281.
Kubli S, Boegli Y, Ave AD, Liaudet L, Revelly JP, Golay S, et al. Endotheliumdependent vasodilation in the skin microcirculation of patients with septic shock. Shock. 2003;19:274–80.
Orbegozo D, Mongkolpun W, Stringari G, Markou N, Creteur J, Vincent JL, et al. Skin microcirculatory reactivity assessed using a thermal challenge is decreased in patients with circulatory shock and associated with outcome. Ann Intensive Care. 2018;8(1):60.
Ospina-Tascon GA, Umana M, Bermudez WF, Bautista-Rincon DF, Valencia JD, Madrinan HJ, et al. Can venous-to-arterial carbon dioxide differences reflect microcirculatory alterations in patients with septic shock? Intensive Care Med. 2016;42(2):211–21.
Perner A, Gordon AC, De Backer D, Dimopoulos G, Russell JA, Lipman J, et al. Sepsis: frontiers in diagnosis, resuscitation and antibiotic therapy. Intensive Care Med. 2016;42(12):1958–69.