Robert A. Solomon, M.D., and E. Sander Connolly, Jr., M.D.
N Engl J Med 2017; 376:1859-1866May 11, 2017DOI: 10.1056/NEJMra1607407
Người dịch: TS. BS. Ngô Mạnh Hùng
Phó Trưởng khoa Phẫu thuật Thần kinh 2, Trung tâm Phẫu thuật Thần kinh, Bệnh viện Việt Đức
Dị dạng động tĩnh mạch não (AVM) là bất thường bẩm sinh mạch máu trong não, xuất hiện do quá trình phát triển bất thường của hệ thống mạch máu, tạo ra sự thông thương trực tiếp giữa các động mạch não với tĩnh mạch não1. Triệu chứng lâm sàng thường gặp nhất là chảy máu não và động kinh. Dấu hiệu thần kinh khu trú và đau đầu có thể tiến triển độc lập với chảy máu não2. Cùng với việc ứng dụng rộng rãi chẩn đoán hình ảnh thần kinh ở não, AVM ngày càng được phát hiện nhiều3.
Có bốn phương pháp điều trị đã được đồng thuận trong điều trị AVM: phẫu thuật, xạ phẫu (radisurgery), nút mạch và điều trị bảo tồn. Vẫn chưa có đồng thuận (concesus) về phương pháp điều trị tốt nhất, và tuỳ thuộc vào việc bệnh nhân đến khám ở chuyên khoa nào mà có quyết định điều trị theo hướng của chuyên khoa đó4. Quyết định điều trị trên lâm sàng phụ thuộc vào nhiều yếu tố khác nhau như kích thước, vị trí và chi tiết giải phẫu5.
Bài này tổng kết về dị dạng động tĩnh mạch não, với đặc trưng là một nidus với các mạch máu bất thường nối thông trực tiếp giữa động mạch và tĩnh mạch mà không có giường mạch máu nối tiếp. Bài này đã loại trừ các dò động tĩnh mạch vỏ não (cortical arterovenous fistula), dị dạng tĩnh mạch, cavernoma malformation, và các dò động tĩnh mạch màng cứng (dural arterovenous fistula).
Nguy cơ chảy máu
Nguy cơ chảy máu hàng năm của AVM là khoảng 3%, song phụ thuộc vào tình trạng lâm sàng và giải phẫu của khối dị dạng, nguy cơ này có thể thấp khoảng 1% hoặc rất cao khoảng 33%. Nguy cơ chảy máu tăng lên nếu bệnh nhân đã có đợt chảy máu trước đó (HR, 3.2; 95% CI, 2.4-4.3) hoặc nếu dị dạng nằm sâu trong não hoặc thân não (HR, 2.4; 95% CI, 1.1-3.8) hoặc đặc điểm dẫn lưu vào hệ thống tĩnh mạch sâu (HR, 2.4; 95%CI, 1.1-3.8)6. Dựa trên những tiêu chí đó, bệnh nhân nếu không có yếu tố nguy cơ nào có tỉ lệ chảy máu rất thấp ( máu trung bình (8-10%/năm) và những bệnh nhân có cả ba yếu tố nguy cơ ở trên có tỉ lệ chảy máu cao (>30%/năm).
Các đặc điểm giải phẫu khác đi kèm với chảy máu bao gồm các phình mạch dạng quả dâu nằm ở động mạch nuôi khối AVM (HR 1.8; 95%CI, 1.6-2.0) và các tĩnh mạch dẫn lưu đi ra khỏi khối AVM rất hẹp5. Hẹp tĩnh mạch dẫn lưu thường ở dạng hẹp hoặc thắt của một hoặc nhiều tĩnh mạch dẫn lưu chính của khối dị dạng động tĩnh mạch. Hậu quả của hiện tượng hẹp tĩnh mạch dẫn lưu là nguy cơ chảy máu cao, và nguy cơ này cao nhất khi chỉ có một tĩnh mạch dẫn lưu khối máu tụ7.
Biểu hiện lâm sàng của chảy máu não từ khối AVM phụ thuộc vào mức độ tổn thương các cấu trúc não lân cận. Tổn thương các vùng của não chi phối vận động, cảm giác, thị giác và chức năng ngôn ngữ (thuật ngữ “eloquent”), tổn thương các đường dẫn truyền thần kinh ở sâu trong chất trắng và các hạch xám trung tâm, và thứ phát là tăng áp lực nội sọ thường dẫn đến kết quả điều trị tồi. Với những bệnh nhân sống sót sau lần chảy máu đầu tiên, khoảng 25% hoàn toàn không có tổn thương thần kinh, 30% có tổn thương mức độ nhẹ-vừa và 45% có tổn thương nặng8. 3 tháng sau chảy máu, khoảng 20% số bệnh nhân sống được sau chảy máu tử vong, và 1/3 số bệnh nhân còn lại tàn phế mức độ vừa8.
Đặc điểm giải phẫu của khối AVM tạo thành một số tiêu chí được sử dụng trong thang điểm được sử dụng để tiên lượng kết quả điều trị AVM. Thang điểm được sử dụng rộng rãi nhất cho mục đích này là phân độ Spetzler-Martin (bảng 1), ban đầu dùng để tiên lượng kết quả điều trị phẫu thuật song cũng có thể được sử dụng trong tiên lượng kết quả điều trị xạ phẫu9. Phân độ thay đổi từ 1-5 điểm với 3 tiêu chí của khối AVM: đường kính của khối AVM ( 6cm [3điểm]), tĩnh mạch hồi lưu (hệ tĩnh mạch nông [0 điểm], hệ tĩnh mạch sâu [1điểm]), và khối AVM nằm ở vùng eloquent (vận động, cảm giác, ngôn ngữ, thị giác, nhân xám trung ương [1 điểm]). Điểm phân độ càng thấp thì nguy cơ điều trị càng thấp. Bảng phân độ tiên lượng chi tiết hơn đối với kết quả điều trị xạ phẫu đã được đưa ra là VRAS (Virginia Radiosurgery AVM
Scale)10,11. VRAS gắn vào 1 trong 5 độ dựa vào các tiêu chí: thể tích khối AVM ( 3 [0đ], 2-4cm3 [1đ], > 4cm3 [2đ]), vị trí eloquent (1đ), tiền sử chảy máu (1đ). AVM độ I có 0đ và AVM độ V: 4 điểm.
Bảng 1. Phân độ AVM theo Spetzler-Martin
| Đặc điểm của khối AVM | Điểm |
| Kích thước (đường kính) | |
| Nhỏ ( | 1 |
| Trung bình (3-6cm) | 2 |
| Lớn (> 6cm) | 3 |
| Vị trí | |
| Eloquent | 1 |
| Non-eloquent | 0 |
| Tĩnh mạch dẫn lưu | |
| Hệ tĩnh mạch nông | 0 |
| Hệ tĩnh mạch sâu | 1 |
Điều trị dị dạng động tĩnh mạch não
Xạ phẫu (stereotactic radiosurgery)
Xạ phẫu là phương pháp điều trị đã được nghiên cứu rất nhiều đối với các AVM12. Các kỹ thuật như gamma knife, cyber knife, proton beam, hội tụ, đưa một liều chiếu xạ lớn đến khối dị dạng, nhằm kích hoạt quá trình tạo xơ của mạch máu và làm huyết khối tắc mạch của tổn thương. Khả năng tắc hoàn toàn khối dị dạng mạch được tiên lượng dựa trên kích thước của khối dị dạng và liều chiếu xạ tính ở mép của tổn thương (liều chiếu xạ viền: marginal dose).
Các tổn thương đáp ứng hiệu quả nhất với xạ phẫu là các tổn thương rất nhỏ, VRAS grade 1 hoặc 2 (3), thường được điều trị với liều chiếu xạ là 18Gy hoặc hơn. Với phương pháp điều trị này, tỉ lệ tắc mạch tổn thương, đánh giá bởi MRI hoặc chụp mạch não, lên đến 80%. Các tổn thương lớn hơn (grade 3,4,hoặc 5) được điều trị với liều chiếu xạ viền thấp hơn và tỉ lệ điều trị thành công là dưới ½ (48%), và thường có các yếu tố nguy cơ đáng kể như hoại tử do tia xạ ở các vùng não lân cận (3%) (hình 1)11.
Một trong những hạn chế lớn nhất của xạ phẫu đối với AVM là sự tắc nghẽn mạch máu của tổn thương diễn ra rất muộn, trung bình thường kéo dài 2-4 năm. Hầu hết các số liệu đều cho thấy rằng nguy cơ chảy máu trong thời gian này chỉ hơi thấp hơn so với nguy cơ trong giai đoạn trước điều trị13.
Trong một nghiên cứu ca bệnh với số lượng lớn, điều trị xạ phẫu trong AVM, 2236 bệnh nhân đã được theo dõi từ 8 trung tâm với thời gian trung bình là 89 tháng. Nguy cơ chảy máu hàng năm sau xạ phẫu là 1%. Tỉ lệ bít tắc hoàn toàn AVM mà không có chảy máu sau điều trị hoặc tổn thương não ổn định, đạt 60% só bệnh nhân11. Các tổn thương Spetzler-Martin 1 hoặc 2 (hầu hết có đường kính dưới 3cm) có kết quả điều trị tốt nhất, với 70% tổn thương biến mất mà không để lại biến chứng, so với 56% đối với grade 3 (đường kính > 3cm) và 35% ở nhóm grade 4 (hầu như toàn bộ trên 3cm, một số > 6cm) (bảng 2).
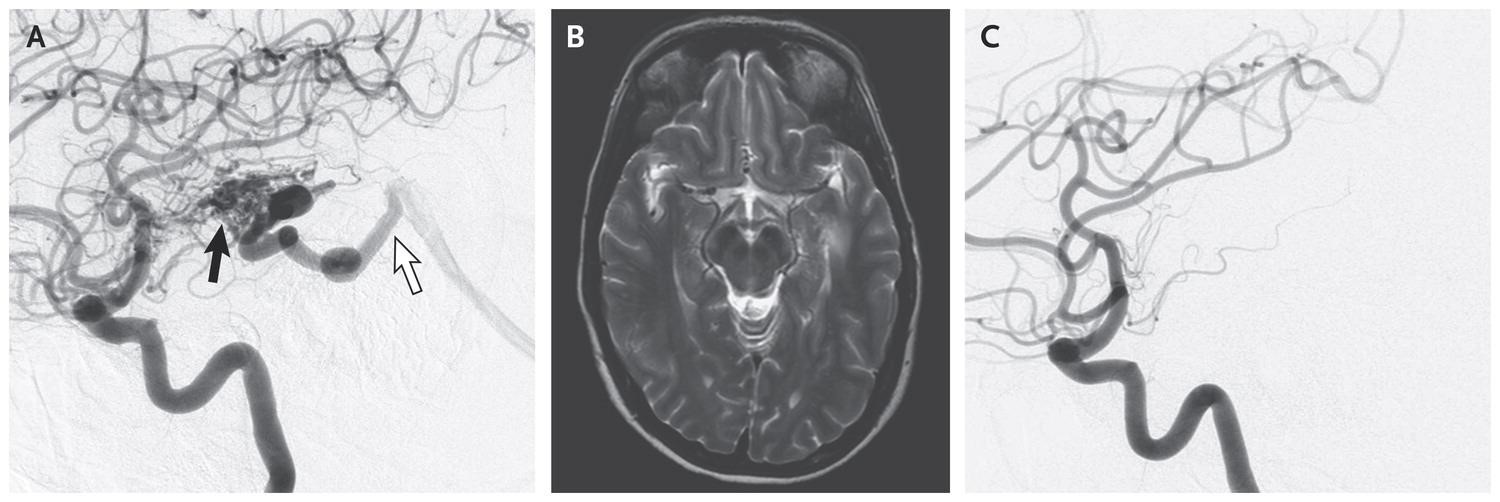
Hình 1. AVM grade 3
Bởi sự đáp ứng kém ở diện rộng, các tổn thương AVM grade 4, 5 đối với điều trị xạ phẫu, cũng như trở ngại trong việc sử dụng các phương pháp tiếp cận khác mô tả dưới đây, “điều trị xạ trị tập trung, phân đoạn” được đề nghị như một phương pháp tiếp cận khác. Với phương pháp này, toàn bộ khối AVM được điều trị ban đầu với liều chiếu xạ thấp (12-16Gy) để hạn chế các biến chứng liên quan đến xạ trị và điều trị lần thứ hai với thời gian ngắt quãng là 2-4 năm17. Một phương pháp tương tự khác là “progressive, staged-volume radiotherapy”, chia tổn thương thành các phần thể tích tương đương với nhau, xạ trị từng phần với thời gian ngắt quãng là từ 2-9 tháng18-20. Một phương pháp thực nghiệm thứ ba là “xạ phẫu đích liều thấp: hypofractionated stereotactic radisurgery”, trong đó bệnh nhân được điều trị với liều 6-7 Gy đế toàn bộ mép của khối AVM trong 5 liệu trình, với tổng liều là 30-35Gy21. Mặc dù các nghiên cứu lâm sàng đánh giá kết quả điều trị xạ trị này vẫn còn nhỏ và không có đối chứng, song tỉ lệ tắc mạch trong tổn thương hoặc gần tắc của tổn thương ở thời điểm 5 năm mà không có biến chứng thần kinh mới xuất hiện là khoảng 50%22. Hơn nữa, tỉ lệ chảy máu não sau điều trị lên đến 31% ở thời điểm 10 năm, và các tác động do xạ trị vĩnh viễn không hồi phục gặp ở 4-28% số bệnh nhân.
Điều trị can thiệp nội mạch
Điều trị can thiệp nội mạch khối AVM được tiến hành bằng cách đặt catheter để đưa các chất chẳng hạn như N-butyl-2-cyanoacrylate hoặc các ethylene vinyl alcohol copolymer không dính. Kỹ thuật này đòi hỏi phải đặt catheter siêu chọn lọc vào động mạch nuôi khối AVM, với mục tiêu là lấp đầy nidus và làm tắc các mạch máu nuôi trong khi vẫn bảo tồn các mạch máu phụ đi đến vùng não bình thường. Thường thường, nút mạch một phần được tiến hành để chuẩn bị cho phẫu thuật lấy bỏ khối dị dạng. Với các AVM lớn, làm tắc mạch ban đầu gây ra tình trạng giảm lưu lượng máu và kích hoạt cơ chế làm rối loạn dòng máu tại vùng, điều này có thể gây ra chảy máu vào tổ chức não bình thường xung quanh trong và sau khi phẫu thuật, một hiện tượng gọi là “ phá vỡ áp lực tưới máu” (“perfusion pressure breakthrough”)23. Nút mạch trước mổ cũng làm giảm tử vong phẫu thuật do làm tắc các động mạch nuôi ở sâu, giảm thiểu sự cần thiết phải phẫu tích đến chất trắng ở sâu, nằm quanh khối AVM24. Tuy nhiên, nút mạch trước mổ lại để lại di chứng thần kinh vĩnh viễn ở 2,5% số bệnh nhân24.
Nút mạch trước xạ phẫu cũng được đề xuất để làm giảm kích thước các khối AVM lớn đến kích thước cho phép tiến hành xạ phẫu25. Nút mạch trước xạ phẫu cũng làm tắc các phình mạch ở động mạch nuôi và các phình mạch trong nidus cua rkhoosi AVM. Với những bệnh nhân có biểu hiện chảy máu từ các khối phình mạch này, mục tiêu của nút các khối phình mạch trước xạ phẫu có thể làm giảm nguy cơ chảy máu tái phát trong thời gian nghỉ giữa hai lần xạ phẫu và sự biến mất của khối AVM26. Cách tiếp cận này đặc biệt có hiệu quả trong trường hợp túi phình nguy cơ cao ở động mạch nuôi ở hố sau.
Hạn chế của nút mạch trước xạ phẫu đích là các chất liệu nút mạch trong khối dị dạng có thể cản trở khả năng hấp thu tia xạ của nidus và làm giảm ranh giới của khối dị dạng, khiến cho việc xác định đích của xạ trị khó khăn27. Đi kèm với những hạn chế này, hầu như toàn bộ các nghiên cứu đã chỉ ra rằng nút mạch trước xạ phẫu giảm hiệu quả về sau của xạ phẫu11,27,28.
Khi giới thiệu các hoạt chất nút mạch dạng lỏng thế hệ hai, có thể đi đến chính xác hơn trong nidus của khối AVM, các kỹ thuật nút mạch tiên tiến ngày càng được phát triển để có thể nút được toàn bộ tổnt hương mà không cần xạ phẫu hay vi phẫu bổ trợ. Trong nghiên cứu BRAVO đa trung tâm (Brain Arterovenous Malformation Embolization with Onyx), 117 bệnh nhân đã được điều trị với hoạt chất mới hơn với mục đích điều trị triệt để tổn thương29. Tỉ lệ tử vong của điều trị là 4,3% và tàn phế là 5,1%; tỉ lệ nút hoàn toàn tổn thương (100%) đạt đưuocj chỉ ở 23,5% số bệnh nhân, với 82% số trường hợp còn sống sau điều trị đã chỉ được điều trị một phần, cần thêm xạ phẫu hoặc phẫu thuật. Một nghiên cứu đơn trung tâm với những bệnh nhân được lựa chọn có kích thước khối AVM > 3cm cho thấy tỉ lệ bít tắc cao hơn khi tiến hành nút toàn bộ khối AVM (50%) song cái giá phải trả là tỉ lệ tử vong cao (2%) và tàn phế (11%)30. Kết quả này đưa ra một câu hỏi rằng cách tiếp cận này liệu có thể cải thiện tiến triển tự nhiên của tổn thương này hơn so với việc điều trị bảo tồn, không điều trị.
Hình 2. Khối AVM grade 1
Điều trị vi phẫu thuật
Mở nắp sọ trong phẫu thuật lấy bỏ khối AVM được tiến hành lần đầu năm 1920, song phẫu thuật được hoàn thiện hơn về sau với việc sử dụng kính vi phẫu thuật, hệ thống dẫn đường, và các trang thiết bị hiện đại31. Đốt điện vi phẫu các động mạch nuôi và tĩnh mạch hồi lưu cho phép lấy bỏ toàn bộ khối AVM thành một khối song cần phải chấp nhận một số rủi ro khi tác động vào nhu mô não lân cận, trong khi tiến hành phẫu tích khối AVM ra khỏi não. Biểu hiện lâm sàng của tổn thương tổ chức lân cận phụ thuộc vào vị trí của khối AVM và chức năng của vùng não lân cận ở mép của tổn thương, và những biểu hiện này cần phải được quan tâm trong việc đánh giá trước mổ và lập kế hoạch phẫu thuật.
Hệ thống phân độ của Spetzler-Martin (SM) đã được sử dụng để xác định nguy cơ tổn thương thần kinh hoặc tử vong sau mổ khối AVM trong não14. Trong một nghiên cứu lớn, đơn trung tâm với những bệnh nhân AVM chưa vỡ, nguy cơ xuất hiện tổn thương mới và vĩnh viễn sau vi phẫu thuật chỉ là 2% với SM độ 1 hoặc độ 2, so với nguy cơ 17% ở độ 3 và 45% ở độ 4 hoặc độ 515. Một vài nghiên cứu đã cho kết quả tương tự và chỉ ra rằng tỉ lệ tàn phế là 2% đối với bệnh nhân SM1 hoặc SM2 (hình 2) và tỉ lệ tử vong là 0,3%14,16.
Sự đa dạng trong kết quả phẫu thuật của các nghiên cứu đã được công bố, đặc biệt là SM 3 hoặc cao hơn, có thể là do sai số lựa chọn (selection bias) và sự khác biệt ở tình trạng trước mổ của bệnh nhân15. Kết quả của AVM chưa vỡ nhìn chung tốt hơn kết quả của AVM đã chảy máu hoặc đã có di chứng thần kinh trước mổ. Hơn nữa, các kết quả đã công bố cho thấy kinh nghiệm ở những trung tâm chuyên khoa và có thể không phản ánh được các nguy cơ ở các trung tâm với số lượng bệnh nhân ít hơn.
Điều trị bảo tồn hay điều trị can thiệp
Những nguy cơ của điều trị AVM não cần phải được cân bằng với những nguy cơ nếu không điều trị. Nghiên cứu ARUBA (the Randomized Trial of Unrupture Brain Arteriovenous Malformation)32 đã phân tích ngẫu nhiên 226 bệnh nhân AVM chưa vỡ để bảo tồn hoặc điều trị (xạ phẫu, nút mạch hoặc phẫu thuật), đã dừng lại sớm bởi thông cáo của viện sức khoẻ quốc gia (National Institutes of Health) bởi sự vượt quá những quan sát can thiệp. Thử nghiệm này bị chỉ trích bởi số liệu không được phân tích theo các dạng can thiệp, các yếu tố đặc biệt của bệnh nhân tiên lượng nguy cơ đi kèm với dạng can thiệp, hoặc các nguy cơ đoán trước của tình trạng vỡ dựa trên các đặc điểm của tổn thương7. Thử nghiệm xác nhận tỉ lệ vỡ hàng năm là 2,3% ở nhóm bảo tồn, song không đưa ra được kết quả phẫu thuật đối với bệnh nhân SM 1 hoặc 2, các nhóm bệnh nhân có chỉ định phẫu thuật tốt nhất14,15. Sự phản biện mạnh nhất đối với thử nghiệm này là thời gian theo dõi trung bình chỉ có 33 tháng, một khoảng thời gian rất ngắn để có thể đánh giá được nguy cơ lâu dài của tình trạng vỡ hoặc các tác động điều trị của xạ phẫu.
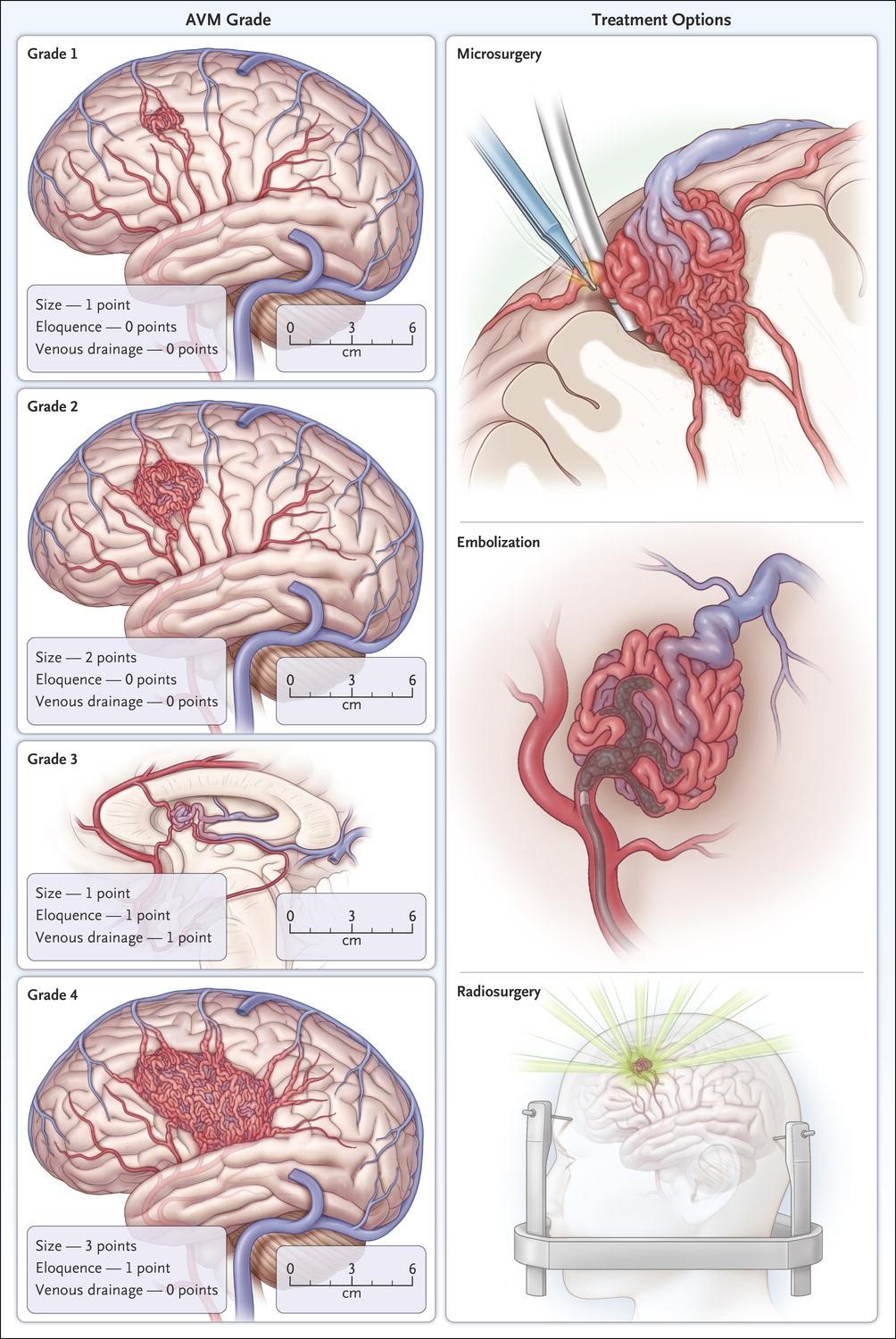
Lựa chọn phương pháp điều trị đối với AVM là rất phức tạp và nên được hướng dẫn bởi các đặc điểm đặc hiệu của tổn thương mạch máu (bảng 1 và 2). Phân độ Spetzler-Martin tổng kết các đặc điểm này, chúng liên quan đến kết quả có thể đạt được với mỗi phương pháp điều trị (hình 3).
Avm grade 1 hoặc 2
Trong một phân tích meta-analysis 137 nghiên cứu quan sát với 13.398 bệnh nhân và 46.314 năm-bệnh nhân theo dõi, biến chứng liên quan đến điều trị dẫn đến các tổn thương thần kinh vĩnh viễn hoặc tử vong gặp ở 7% số bệnh nhân đã điều trị phẫu thuật hoặc nút mạch và ở 5% số bệnh nhân điều trị xạ phẫu33. Bít tắc tổn thương, ghi nhận trên MRI hoặc DSA, đạt được ở 96% số bệnh nhân sau phẫu thuật, 38% ở xạ phẫu và 13% ở nút mạch đơn thuần. Dựa trên những kết quả này, phẫu thuật nhìn chung là lựa chọn tốt nhất đối với những bệnh nhân AVM có nguy cơ thấp, cụ thể là SM grade 1 hoặc 2. Ở những trung tâm với số lượng bệnh nhân mổ lớn, phẫu thuật lấy bỏ hoàn toàn hoặc làm tắc tổn thương mà không có biến chứng đạt được với phẫu thuật là trên 95% và với xạ phẫu là 70%34.
Avm grade 3
Lựa chọn phương pháp điều trị phức tạp hơn đối với AVM grade 3. Ví dụ, một số AVM grade 3 rất nhỏ, nằm ở sâu ở vùng eloquent ở não. Các dị dạng này có tĩnh mạch dẫn lưu sâu, thường đi kèm với nguy cơ chảy máu cao nếu không điều trị10. Xạ trị điều trị không có biến chứng thường được áp dụng với tổn thương grade 3, bất kể các tác nhân khác như vùng eloquent hay tĩnh mạch dẫn lưu sâu. Vì vậy, những bệnh nhân có tổn thương AVM này, đặc biệt là những bệnh nhân chưa chảy máu, nên được điều trị với xạ phẫu.
Điều trị các khối AVM grade 3 lớn hơn nằm ở vùng vỏ não eloquent hiện nay vẫn còn đang có nhiều tranh luận. Với các tổn thương chưa vỡ trong vùng này, có rất ít bằng chứng cho thấy rằng kết quả của phương pháp này tốt hơn các phương pháp bảo tồn. Tỉ lệ tàn phế sau phẫu thuật ít nhất là 15% song những nghiên cứu ca bệnh đã công bố về AVM grade 3 điều trị phẫu thuật không phản ánh chính xác các nguy cơ do sai số lựa chọn, bởi những nghiên cứu này thường loại trừ những bệnh nhân AVM lớn hoặc ở những vùng vỏ não có chứng năng34. Kết quả xạ phẫu làm tắc toàn bộ khối AVM mà khong có chảy máu sau điều trị và không có các tổn thương não vĩnh viễn, có triệu chứng liên quan đến xạ trị nhỏ hơn 50% số bệnh nhân AVM grade 3 với kích thước lớn hơn 3cm. Ngay cả khi sử dụng phương pháp nút mạch thì đầu để giảm kích thước của tổn thương, sau đó xạ phẫu, kết quả cho thấy là cũng không tốt hơn nhóm bệnh nhân không điều trị. Tuy nhiên, tuổi của bệnh nhân, các ảnh hưởng tâm lý về nguy cơ vỡ của khối AVM và mức độ nặng của các tổn thương thần kinh có thể xuất hiện sau điều trị là các yếu tố cần phải cân nhắc khi đưa ra quyết định điều trị đối với từng bệnh nhân.
Các AVM grade 3 vỡ đặc biệt nghiêm trọng bởi tỉ lệ chảy máu tái phát cao nếu không điều trị5,6. Khi chúng đi kèm với phình mạch vỡ, nguy cơ chảy máu thậm chí còn cao hơn, và can thiệp nội mạch cấp cứu để bít tắc các mạch nuôi túi phình cần phải được tiến hành. AVM vỡ mà không doc điểm chảy máu thường được cân nhắc điều trị đa mô thức, với nút mạch trước mổ, sau đó là điều trị phẫu thuật hoặc xạ phẫu.
Avm grade 4, 5 và ở thân não
Nỗ lực điều trị triệt để AVM grade 4 và grade 5 và hầu hết các AVM ở thân não- với sự loại trừ các nguy cơ chảy máu đe doạ cuộc sống và các triệu chứng thần kinh tàn phế xuất hiện dần dần, đặc biệt là ở người trẻ tuổi-nhìn chung thường có kết cục thất bại và kết quả tồi. Các nghiên cứu phẫu thuật chỉ ra rằng tỉ lệ tàn phế liên quan đến điều trị lên đến gần 50% và can thiệp nội mạch và xạ phẫu cũng thất bại trong việc điều trị các dị dạng này ở hầu hết các trường hợp34. Khi bệnh nhân có AVM grade 4 hoặc 5 và chảy máu não, điều trị can thiệp nội mạch triệu chứng được đưa ra để làm tắc một phần khối dị dạng là nguyên nhân chảy máu, hoặc điều trị nút các túi phình của động mạch nuôi, có thể làm giảm nguy cơ chảy máu về sau.
Bảng 2. Kết quả khả quan của điều trị phẫu thuật và xạ phẫu các AVM theo phân độ Spertzler-Martin
| Độ SM | Kết quả khả quan (% bệnh nhân) | |
| Vi phẫu thuật | Xạ phẫu | |
| 1 | 95 | 70 |
| 2 | 95 | 70 |
| 3 | 80 | 56 |
| 4 | 30 | 35 |
| 5 | 30 | 35 |
Tóm tắt
Các số liệu hiện này không đủ để đưa ra một guideline về điều trị, song chúng củng cố quan điểm hầu hết bệnh nhân AVM vỡ và một số bệnh nhân AVM chưa vỡ chọn lọc nên được điều trị hơn là không điều trị. Kết quả của nghiên cứu ARUBA cung cấp một viễn cảnh khác về cách tiếp cận này; tuy nhiên, sự hạn chế của nghiên cứu, như đã nói ở trên, cần phải được cân nhắc. Các nghiên cứu so sánh tương tự có thể chỉ ra những nguy cơ biết trước đi kèm với các đặc điểm cụ thể của AVM là cần thiết. Các bệnh nhân Spetzler-Martin 1 hoặc 2 hiện nay được điều trị phẫu thuật, song xạ phẫu và can thiệp nội mạch cũng là các lựa chọn đối với một số bệnh nhân. AVM grade 4 hoặc 5 dường như tốt hơn với điều trị bảo tồn song đôi khi lợi ích từ điều trị can thiệp nội mạch một phần cũng cần cân nhắc với những tổn thương có nguy cơ chảy máu cao, chẳng hạn như phình mạch ở động mạch nuôi hoặc ở trong nidus. Các tổn thương AVM grade 3 nằm sâu và nhỏ, đặc biệt là không vỡ, nên được điều trị với xạ phẫu.
Một số lựa chọn điều trị khác cũng đã được đưa ra với các tổn thương grade 3 kích thước lớn, bao gồm cả điều trị bảo tồn. Sự phức tạp của AVM khiến cho việc điều trị tổn thương này cần phải theo nhóm đa chuyên khoa và quyết định điều trị dựa trên từng bệnh nhân cụ thể.
Tài liệu tham khảo
Friedlander RM. Arteriovenous malfor- mations of the brain. N Engl J Med 2007; 356:2704-12.
Berman MF, Sciacca RR, Pile-Spell- man J, et al. The epidemiology of brain ar- teriovenous malformations. Neurosurgery 2000;47:389-97.
Stapf C, Mohr JP, Pile-Spellman J, Solo- mon RA, Sacco RL, Connolly ES Jr. Epide- miology and natural history of arteriove- nous malformations. Neurosurg Focus 2001;11(5):e1.
Cockroft KM, Jayaraman MV, Amin- Hanjani S, Derdeyn CP, McDougall CG, Wilson JA. A perfect storm: how A Ran- domized Trial of Unruptured Brain Arte- riovenous Malformations’ (ARUBA’s) trial design challenges notions of external va- lidity. Stroke 2012;43:1979-81.
Gross BA, Du R. Natural history of ce- rebral arteriovenous malformations: a meta- analysis. J Neurosurg 2013;118:437-43.
Stapf C, Mast H, Sciacca RR, et al. Pre- dictors of hemorrhage in patients with un-treated brain arteriovenous malformation. Neurology 2006;66:1350- 5.
Sahlein DH, Mora P, Becske T, et al. Features predictive of brain arteriovenous malformation hemorrhage: extrapolation to a physiologic model. Stroke 2014;45:1964-70.
Fukuda K, Majumdar M, Masoud H, et al. Multicenter assessment of morbidity associated with cerebral arteriovenous mal- formation hemorrhages. J Neurointerv Surg 2016 June 22 (Epub ahead of print).
Spetzler RF, Martin NA. A proposed grading system for arteriovenous malfor- mations. J Neurosurg 1986;65:476-83.
Pollock BE, Storlie CB, Link MJ, Staf- ford SL, Garces YI, Foote RL. Comparative analysis of arteriovenous malformation grading scales in predicting outcomes after stereotactic radiosurgery. J Neurosurg 2017;126:852-8.
Starke RM, Kano H, Ding D, et al. Ste- reotactic radiosurgery for cerebral arterio- venous malformations: evaluation of long- term outcomes in a multicenter cohort. J Neurosurg 2017;126:36-44.
Ajiboye N, Chalouhi N, Starke RM, Zanaty M, Bell R. Cerebral arteriovenous malformations: evaluation and manage- ment. ScientificWorldJournal 2014;2014: 649036.
Maruyama K, Kawahara N, Shin M, et al. The risk of hemorrhage after radio- surgery for cerebral arteriovenous malfor- mations. N Engl J Med 2005;352:146-53.
Spetzler RF, Ponce FA. A 3-tier classifi- cation of cerebral arteriovenous malforma- tions: clinical article. J Neurosurg 2011; 114:842-9.
Bervini D, Morgan MK, Ritson EA, Heller G. Surgery for unruptured arteriove- nous malformations of the brain is better than conservative management for selected cases: a prospective cohort study. J Neuro- surg 2014;121:878-90.
Potts MB, Lau D, Abla AA, Kim H, Young WL, Lawton MT. Current surgical re- sults with low-grade brain arteriovenous malformations. J Neurosurg 2015;122:912- 20.
Yamamoto M, Akabane A, Matsumaru Y, Higuchi Y, Kasuya H, Urakawa Y. Long- term follow-up results of intentional 2-stage Gamma Knife surgery with an interval of at least 3 years for arteriovenous malformations larger than 10cm3. J.Neurosurg 2012; 117: Suppl: 126-34.
Seymour ZA, Sneed PK, Gupta N, et al. Volume-staged radiosurgery for large arte- riovenous malformations: an evolving para- digm. J Neurosurg 2016;124:163-74.
Nagy G, Grainger A, Hodgson TJ, et al. Staged-volume radiosurgery of large arterio- venous malformations improves outcome by reducing the rate of adverse radiation effects. Neurosurgery 2016 February 15 (Epub ahead of print).
Hanakita S, Shin M, Koga T, Igaki H, Saito N. Outcomes of volume-staged radio- surgery for cerebral arteriovenous malfor- mations larger than 20 cm3 with more than 3 years of follow-up. World Neurosurg 2016;87:242-9.
Lindvall P, Grayson D, Bergström P, Bergenheim AT. Hypofractionated stereo- tactic radiotherapy in medium-sized to large arteriovenous malformations. J Clin Neurosci 2015;22:955-8.
Chen JC, Mariscal L, Girvigian MR, et al. Hypofractionated stereotactic radiosur- gery for treatment of cerebral arteriove- nous malformations: outcome analysis with use of the modified Arteriovenous Malfor- mation Scoring System. J Clin Neurosci 2016;29:155-61.
Young WL, Kader A, Ornstein E, et al. Cerebral hyperemia after arteriovenous mal- formation resection is related to “break- through” complications but not to feeding artery pressure. Neurosurgery 1996;38: 1085-93.
Starke RM, Komotar RJ, Otten ML, et al. Adjuvant embolization with Nbutyl cyanoacrylate in the treatment of cerebral arte- riovenous malformations: outcomes, com- plications, and predictors of neurologic deficits. Stroke 2009;40:2783-90.
Lee CC, Chen CJ, Ball B, et al. Stereo- tactic radiosurgery for arteriovenous mal- formations after Onyx embolization: a case- control study. J Neurosurg 2015;123:126-35. 26. Alexander MD, Cooke DL, Hallam DK, Kim H, Hetts SW, Ghodke BV. Less can be more: targeted embolization of aneurysms associated with arteriovenous malforma- tions unsuitable for surgical resection. In- terv Neuroradiol 2016;22:445-51.
Ding D, Starke RM, Kano H, et al. Ste- reotactic radiosurgery for SpetzlerMartin Grade III arteriovenous malformations: an international multicenter study. J Neuro- surg 2017;126:859-71.
Cohen-Inbar O, Lee CC, Xu Z, Schle- singer D, Sheehan JP. A quantitative analy- sis of adverse radiation effects following Gamma Knife radiosurgery for arteriove- nous malformations. J Neurosurg 2015;123: 945-53.
Pierot L, Cognard C, Herbreteau D, et al. Endovascular treatment of brain arte- riovenous malformations using a liquid em- bolic agent: results of a prospective, multi- centre study (BRAVO). Eur Radiol 2013;23: 2838-45.
Saatci I, Geyik S, Yavuz K, Cekirge HS. Endovascular treatment of brain arteriove- nous malformations with prolonged intra- nidal Onyx injection technique: long-term results in 350 consecutive patients with completed endovascular treatment course. J Neurosurg 2011;115:78-88.
Kretzer RM, Coon AL, Tamargo RJ. Walter E. Dandy’s contributions to vascular neurosurgery. J Neurosurg 2010;112:1182- 91.
Mohr JP, Parides MK, Stapf C, et al. Medical management with or without inter- ventional therapy for unruptured brain ar- teriovenous malformations (ARUBA): a mul- ticentre, non-blinded, randomised trial. Lancet 2014;383:614-21.
van Beijnum J, van der Worp HB, Buis DR, et al. Treatment of brain arteriovenous malformations: a systematic review and meta-analysis. JAMA 2011;306:2011-9.
Morgan MK, Stoodley MA, Fuller JW. Comparison between surgery and Gamma Knife radiosurgery for brain AVMs. J Neuro- surg 2017;126:33841.



