Consensus for the management of analgesia, sedation and delirium in adults with COVID-19-associated acute respiratory distress syndrome
Manuel Donato, Federico Carlos Carini, María Julia Meschini, Ignacio López Saubidet, Adela Goldberg, Marisol García Sarubio, Daniela Olmos, Rosa Reina
Rev. bras. ter. intensiva 33 (1) • Jan-Mar 2021 • https://doi.org/10.5935/0103-507X.20210005
Dịch bởi: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
Đối tượng:
Để đề xuất các chiến lược nhanh chóng cho một cách tiếp cận toàn diện để giảm đau, an thần, chống sảng, vận động sớm và sự tham gia của gia đình cho bệnh nhân mắc hội chứng suy hô hấp cấp do COVID-19, xét đến nguy cơ lây nhiễm cao ở các nhân viên y tế, thì phương pháp điều trị nhân đạo mà chúng tôi phải cung cấp cho bệnh nhân và sự bao gồm của gia đình bệnh nhân, trong bối cảnh thiếu các chiến lược điều trị cụ thể chống lại virus trên toàn cầu cho đến nay và sự thiếu hụt tiềm năng về nguồn lực y tế.
Phương pháp:
Một đánh giá không hệ thống về bằng chứng khoa học trong cơ sở dữ liệu thư mục chính đã được thực hiện, cùng với kinh nghiệm và đánh giá lâm sàng trong nước và quốc tế. Cuối cùng, các thành viên của Ủy ban Giảm đau, An thần và Sảng của Sociedad Argentina de Terapia Intensiva đã thống nhất được các khuyến cáo.
Kết quả:
Các khuyến cáo đã được thống nhất và các công cụ đã được phát triển để đảm bảo một cách tiếp cận toàn diện để giảm đau, an thần, chống sảng, vận động sớm và sự tham gia của gia đình cho bệnh nhân người lớn bị hội chứng suy hô hấp cấp do COVID-19.
Thảo luận:
Với thứ tự mới được tạo ra trong các liệu pháp điều trị chuyên sâu do đại dịch COVID-19 đang tiến triển, chúng tôi đề xuất không bỏ qua các phương pháp thực hành tốt thông thường mà hãy điều chỉnh chúng cho phù hợp với bối cảnh cụ thể được tạo ra. Sự đồng thuận của chúng tôi được hỗ trợ bởi bằng chứng khoa học và kinh nghiệm trong nước và quốc tế và sẽ là một công cụ tham vấn hấp dẫn trong các liệu pháp chuyên sâu.
Giới thiệu
Bệnh Coronavirus 2019 (COVID-19) là một bệnh lý đường hô hấp ở người do nhiễm loại coronavirus mới được xác định bằng từ viết tắt SARS-CoV-2. (1) Vào ngày 11 tháng 3 năm 2020, Tổ chức Y tế Thế giới (WHO) đã công bố COVID-19 một đại dịch, và kể từ thời điểm đó cho đến ngày 10 tháng 10, khoảng 36.754.395 trường hợp được xác nhận và 1.064.838 trường hợp tử vong đã được báo cáo trên toàn thế giới. Các nước Châu Mỹ. (2,3)
Không có loại thuốc cụ thể chống lại loại vi rút này hoặc một loại vắc xin có sẵn trên toàn cầu. Mặc dù dexamethasone và hydrocortisone đã được chứng minh là cải thiện khả năng sống sót trong những trường hợp nghiêm trọng của COVID-19 và heparin đóng vai trò quan trọng trong việc ngăn ngừa huyết khối tĩnh mạch sâu (cũng trong những trường hợp nghiêm trọng), hiện nay chiến lược tốt nhất để đối phó với đại dịch là phòng ngừa lây nhiễm qua công các biện pháp chính sách. (4) Thời gian ủ bệnh của nhiễm SARS-CoV-2 là 2 đến 14 ngày, và hầu hết các bệnh nhiễm trùng đều lây từ người sang người, có khả năng lây truyền cao. (5) Bệnh viện Brigham và Phụ nữ, Khoa Nội tổng quát, của Trường Y Harvard đã đề xuất một phân loại điều trị-lâm sàng của bệnh chia quá trình của bệnh thành các giai đoạn khác nhau và lần lượt xác định 2 nhóm bệnh lý chồng chéo nhưng khác nhau: nhóm thứ nhất do vi rút gây ra và nhóm thứ hai do phản ứng của vật chủ đối với vi rút. (6) Giai đoạn I hoặc bệnh nhẹ xảy ra tại thời điểm được tiêm chủng và giai đoạn đầu của bệnh; Giai đoạn II xảy ra khi tổn thương phổi được thiết lập trong người; và Giai đoạn III hoặc bệnh nặng có biểu hiện như viêm quá phát toàn thân ngoài phổi.
Tỷ lệ mắc và tử vong do COVID-19 gia tăng phần lớn là do viêm phổi cấp tính do vi rút tiến triển thành hội chứng suy hô hấp cấp tính (ARDS). hầu hết các trường hợp ở bệnh nhân cao tuổi có bệnh đi kèm (béo phì, tiểu đường, bệnh thận mãn tính, tăng huyết áp, bệnh tim và bệnh phổi mãn tính). (ICU). (7-11) Ở nước ta, một chính sách công sớm đã tạo ra thời gian để hệ thống y tế chuẩn bị về năng lực ứng phó với đại dịch, đặc biệt quản lý để tăng nguồn cung cấp vật tư cần thiết cho bệnh viện và 12.450 giường bệnh, nhiều hơn gần 50% so với điều kiện ICU trước đại dịch. ở tất cả các tỉnh nơi thực tế không có sự lưu hành của vi rút trong cộng đồng. Thực tế này đã làm cho việc áp dụng các quy trình khác nhau trong ICU trở nên cần thiết, chủ yếu là do việc sử dụng các nguồn lực và chăm sóc y tế tăng theo cấp số nhân để giảm nguy cơ lây nhiễm ở nhân viên y tế.
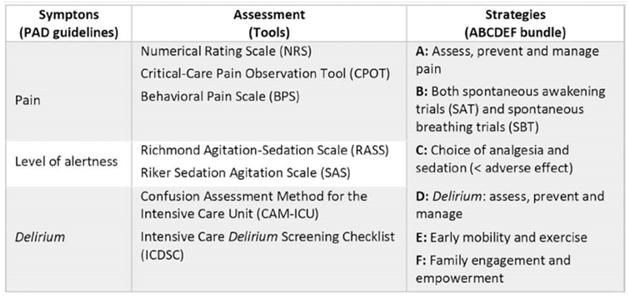
Trong ICU, cách tiếp cận toàn diện nhằm đạt được sự thoải mái, an toàn và tạo điều kiện cho các can thiệp hỗ trợ sự sống cho những bệnh nhân nguy kịch với COVID-19 ARDS chủ yếu bao gồm đánh giá có hệ thống về giảm đau, an thần và sảng (ASD) trong chăm sóc quan trọng, ngoài khả năng vận động sớm và gắn kết gia đình. Tất cả điều này được phản ánh trong hướng dẫn thực hành lâm sàng năm 2018 về phòng ngừa và quản lý cơn đau, kích động/an thần, sảng, bất động và gián đoạn giấc ngủ (PADIS) ở bệnh nhân người lớn trong ICU và gói biện pháp ABCDEF (Hình 1), được xuất bản bởi The Society of Critical Care Medicine. (14,15) ARDS nghiêm trọng do SARS-CoV-2 tạo ra trong đại dịch COVID-19 đã thách thức khả năng của chúng tôi trong việc tạo, thích ứng và duy trì các giao thức làm việc, chẳng hạn như các giao thức được đề xuất trong gói ABCDEF. Ngoài ra, bằng chứng tốt nhất hiện có cho việc quản lý những bệnh nhân này đến từ các quốc gia có thu nhập cao với hệ thống y tế được chuẩn bị tốt hơn, nơi mà các giao thức thường có tỷ lệ chấp nhận cao và thường không thiếu nguồn lực y tế.
Hình 1 Các thành phần của gói ABCDEF. (14)
Mục tiêu của sự đồng thuận này là đề xuất các chiến lược và công cụ mục tiêu để quản lý tối ưu ASD ở nhóm dân số này, có tính đến nguy cơ lây nhiễm cao tồn tại trong các nhân viên y tế, phương pháp điều trị nhân đạo mà chúng tôi phải cung cấp cho bệnh nhân và sự bao gồm của gia đình bệnh nhân nhưng trong bối cảnh thiếu các chiến lược điều trị cụ thể có sẵn trên toàn cầu để chống lại vi rút và thiếu nguồn lực y tế tiềm ẩn có thể xảy ra khi hệ thống y tế bão hòa. (16)
Phương pháp
Tài liệu này được tạo ra bởi sự đồng thuận của các nhóm danh nghĩa. Tài liệu thu được dựa trên đánh giá không hệ thống về bằng chứng khoa học, được bổ sung vào đánh giá và kinh nghiệm lâm sàng của nhóm chuyên gia tham gia và các nhóm khác trên toàn thế giới.
Các tìm kiếm tài liệu do các tác giả thiết kế được thực hiện trong Cơ sở dữ liệu Cochrane về các Tổng quan Hệ thống (CDSR), Sổ đăng ký Thử nghiệm Có Kiểm soát Trung tâm Cochrane (CENTRAL), Cơ sở Dữ liệu Tóm tắt Tổng quan về Hiệu ứng (DARE), MEDLINE, và EMBASE. Chiến lược tìm kiếm cơ bản được thiết kế cho Medline (PubMed) bao gồm các thuật ngữ sau. Analgesia: (Coronavirus OR Spike glycoprotein, COVID-19 virus OR Severe Acute Respiratory Syndrome Coronavirus 2 OR COVID-19 OR Corona Virus OR COVID-19 OR COVID19 OR 2019-nCoV OR SARS-CoV-2 OR SARS-CoV2 OR (Pneumonia AND Wuhan AND 2019) OR (Coronavir* AND 2019)) AND (Critical Care OR Care, Critical OR Intensive Care OR Care, Intensive) AND (Analgesic OR Analgesic* OR Anodynes OR Antinociceptive Agents). Sedación: (Coronavirus OR Spike glycoprotein, COVID-19 virus OR Severe Acute Respiratory Syndrome Coronavirus 2 OR COVID-19 OR Corona Virus OR COVID-19 OR COVID19 OR 2019-nCoV OR SARS-CoV-2 OR SARS-CoV2 OR (Pneumonia AND Wuhan AND 2019) OR (Coronavir* AND 2019)) AND (Critical Care OR Care, Critical OR Intensive Care OR Care, Intensive) AND (Hypnotics and Sedatives OR Sedatives and Hypnotic* OR Hypnotic* OR Sedative*). Delirium: (Coronavirus OR Spike glycoprotein, COVID-19 virus OR Severe Acute Respiratory Syndrome Coronavirus 2 OR COVID-19 OR Corona Virus OR COVID-19 OR COVID19 OR 2019-nCoV OR SARS-CoV-2 OR SARS-CoV2 OR (Pneumonia AND Wuhan AND 2019) OR (Coronavir* AND 2019)) AND (Critical Care OR Care, Critical OR Intensive Care OR Care, Intensive) AND (Delirium OR Delirium*).
Việc đưa vào các đánh giá có hệ thống các thử nghiệm lâm sàng có đối chứng ngẫu nhiên và các hướng dẫn thực hành lâm sàng được ưu tiên. Ban biên tập bao gồm các bác sĩ hồi sức, dược sĩ và bác sĩ dược động học, những người đã đề cập đến một quy trình quản lý ASD ở người lớn mắc ARDS do COVID-19 gây ra. Chúng tôi sẽ xem xét các giai đoạn khác nhau mà bệnh nhân nguy kịch phải trải qua, từ cách tiếp cận ban đầu với đường thở, đến cách tiếp cận thở máy trong các giai đoạn khác nhau và đến quá trình cai nghiện. Đối với mỗi giai đoạn, các nguồn thông tin thư mục được đề cập đã được phân tích và đưa ra các khuyến cáo.
Một nhóm các chuyên gia độc lập đã thành lập Ủy ban Đánh giá. Nhóm này đã phân tích tài liệu và đề xuất các sửa đổi, được thảo luận cho đến khi đạt được đồng thuận cuối cùng.
Kết quả
Quá trình đặt nội khí quản chuỗi nhanh ở người lớn bị ards do covid-19
Chúng tôi khuyến cáo chỉ đặt nội khí quản (OTI) ở người lớn có COVID-19 và suy hô hấp trung bình đến nặng, những người có gắng sức hô hấp tăng lên với tần số hô hấp > 30 lần/phút và PaO2/FiO2 2 > 50%. Một thuật toán được các thành viên của Sociedad Argentina de Terapia Intensiva điều chỉnh để đặt nội khí quản được đề xuất.
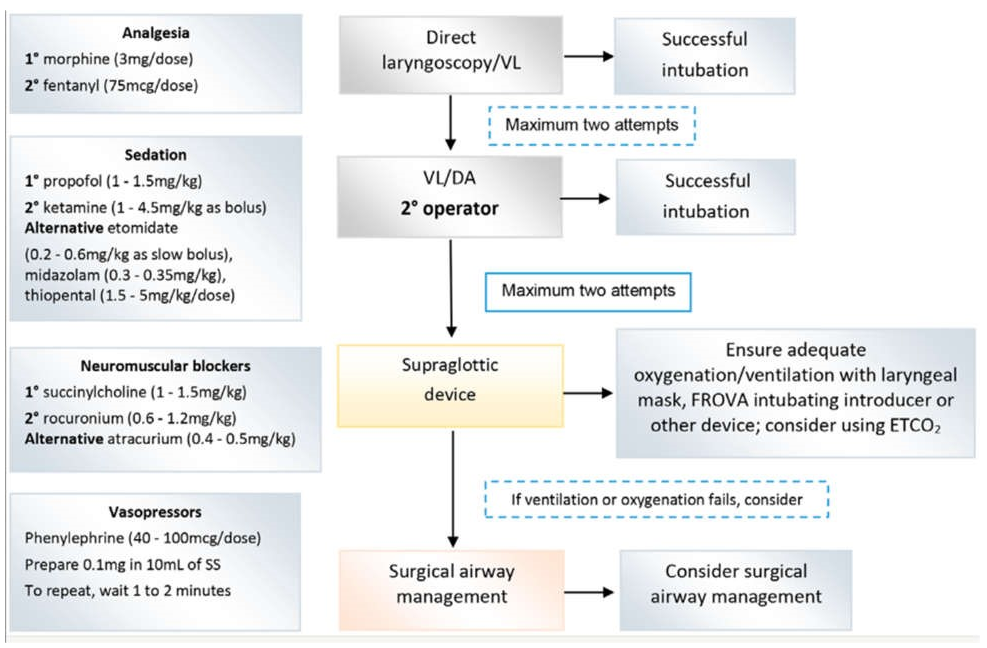
Một số trung tâm y tế trên toàn thế giới đã báo cáo rằng phần lớn bệnh nhân mắc COVID-19 ARDS phải đặt nội khí quản trong vòng 24 giờ đầu tiên sau khi được đưa vào ICU và trong vòng dưới 8 giờ đối với những bệnh nhân có các yếu tố nguy cơ liên quan, phải thở máy kéo dài, tức là từ 3 đến 4 tuần, với tỷ lệ tử vong rất cao. (17-19) Do đó, quyết định đặt nội khí quản phải luôn được đưa ra có tính đến những kết quả này và đánh giá khả năng hồi phục tiềm năng của bệnh nhân. Nguy cơ khí dung trong bất kỳ thao tác nào trong đường thở là cao đến rất cao và yêu cầu sử dụng phương tiện bảo vệ cá nhân bảo vệ tối đa (khẩu trang loại N95, áo choàng cách ly, găng tay, kính bảo vệ mắt và khẩu trang) luôn đi kèm với vệ sinh tay đầy đủ.(20,21) Nên sử dụng các loại thuốc tác dụng nhanh để giảm nhu cầu thông khí bằng bóng qua mặt nạ và hậu quả là nguy cơ tạo ra khí dung dịch tiết của bệnh nhân. Kế hoạch phải luôn bao gồm, và theo thứ tự tiếp theo, giảm đau, an thần và thuốc chẹn thần kinh cơ (NMB). Một giải pháp thay thế là sử dụng ketamine, có tác dụng giảm đau và an thần; nơi có thể tránh sử dụng opioid. Hình 2 tóm tắt quy trình mà chúng tôi đề xuất cho quy trình này, với một định dạng hữu ích để sử dụng làm danh sách kiểm tra ở đầu giường. (22)
Các công cụ đánh giá và giám sát
Đau
Chúng tôi khuyến cáo nên sử dụng một cách có hệ thống Thang điểm đau hành vi (BPS, Behavioral Pain Scale) hoặc Công cụ quan sát cơn đau do chăm sóc nghiêm trọng (CPOT, Critical-Care Pain Observation Tool) ở người lớn không giao tiếp được dựa trên giai đoạn phát triển của COVID-19 ARDS.
Chúng tôi khuyến cáo, bất kể giai đoạn phát triển hoặc độ sâu của thuốc an thần, ở những bệnh nhân này đạt được và duy trì mục tiêu giảm đau
Hình 2 Trình tự cho chuỗi đặt nội khí quản thích ứng. (22)
SS – dung dịch muối 0,9%; VL – videolaryngoscopy; DA – đường thở khó; ETCO2 – carbon dioxide cuối thở ra.
Chiến lược tốt nhất để đạt được kết quả lâm sàng phù hợp ở bệnh nhân trong khi bảo quản thuốc đầu tay là tuân thủ gói ABCDEF.(14) Đánh giá liên tục và có hệ thống về cơn đau, kích động và sảng ở người lớn mắc COVID-19 ARDS là biện pháp hiệu quả, an toàn, nhanh chóng và rẻ tiền nhất để tiết kiệm thuốc. Đó là lý do tại sao chúng tôi nhấn mạnh tầm quan trọng của nó một cách rõ ràng trong tài liệu này bằng ngôn ngữ của chúng tôi tại giường bệnh nhân.
Dựa trên khả năng giao tiếp của bệnh nhân, các thang điểm báo cáo cơn đau, chẳng hạn như thang đánh giá số (NRS, numerical rating scale), có thể được sử dụng ở những bệnh nhân có khả năng giao tiếp hoặc thang quan sát dựa trên hành vi, chẳng hạn như BPS và CPOT, có thể được sử dụng khi bệnh nhân không thể giao tiếp.(14,23) Tuy nhiên, không thể áp dụng cho bệnh nhân được an thần sâu, được định nghĩa theo thang điểm kích động-an thần Richmond (RASS, Richmond agitation-sedation scale) là -3 đến -5, hoặc với NMBs; Hạn chế sử dụng chúng ở người lớn mắc ARDS COVID-19 vừa/nặng.(15) Ngoài ra, trong những trường hợp này, Chúng tôi khuyến cáo nên bắt đầu và luôn duy trì giảm đau phòng ngừa.
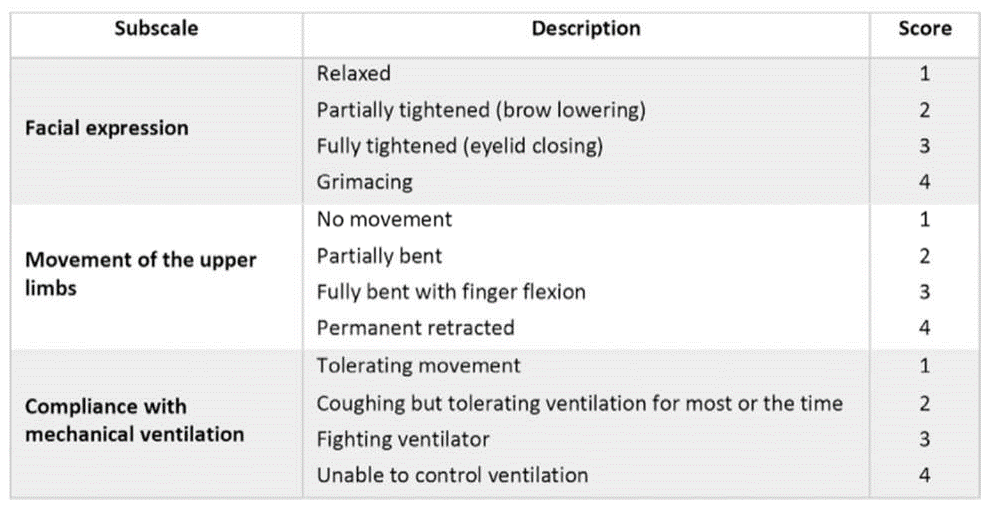
Công cụ BPS đánh giá 3 thang điểm, tức là biểu hiện trên khuôn mặt, cử động chi trên và tuân thủ thở máy, và có thể được sử dụng cho những bệnh nhân đang trong tình trạng an thần sâu không thể tự biểu hiện (Hình 3). (24) Mỗi thang điểm phụ được cho điểm từ 1 đến 4, cho tổng điểm có thể từ 3 đến 12.
Hình 3 Thang đo mức độ đau về hành vi. (24)
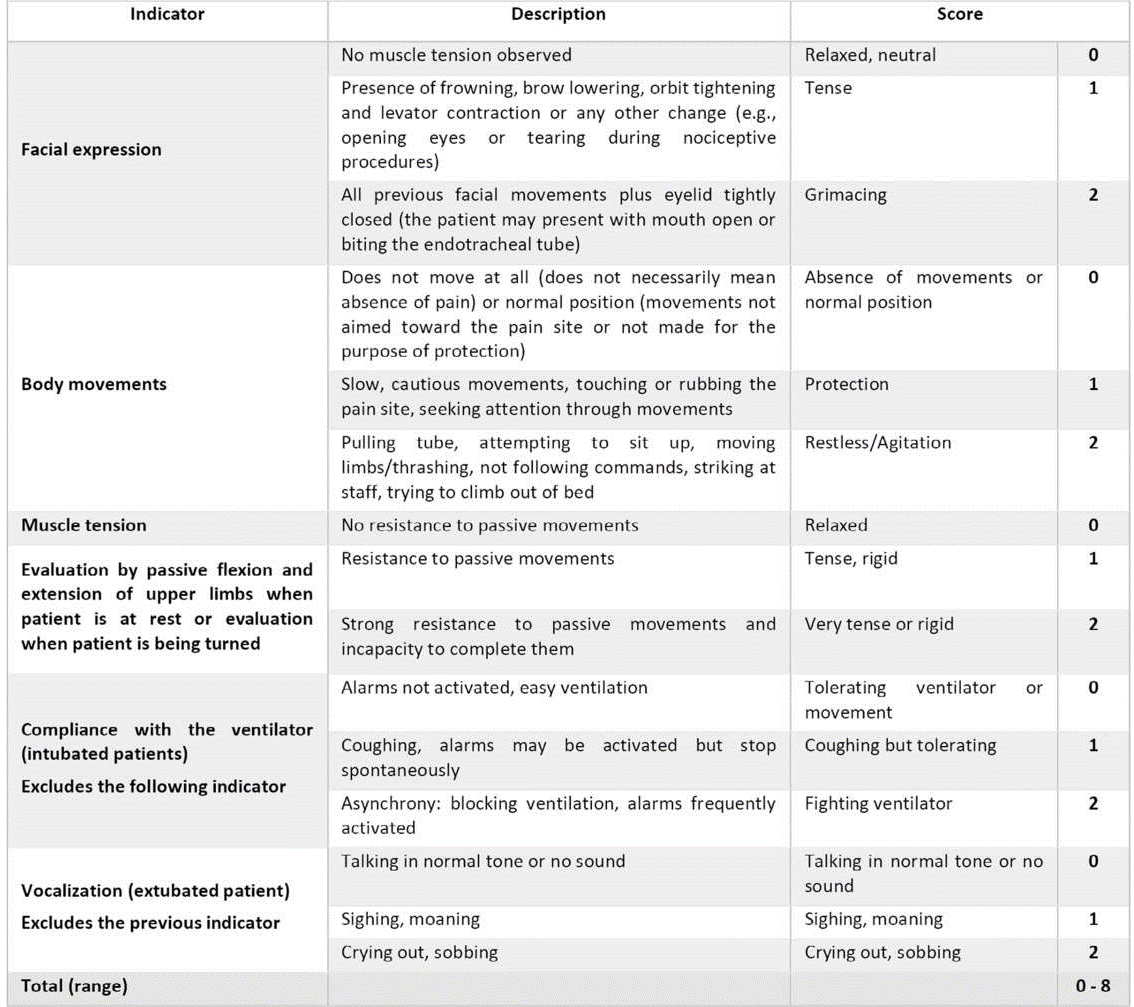
Mặt khác, CPOT dựa trên điểm số của 4 thành phần: Nét mặt; Vận động cơ thể; Tuân thủ máy thở (hoặc phát âm ở bệnh nhân rút nội khí quản); và sự căng cơ.(25) Mỗi thành phần được cho điểm từ 0 đến 2, với tổng điểm có thể từ 0 đến 8 (Hình 4). Ưu điểm của nó là nó cho điểm cường độ của các phản ứng hành vi của bệnh nhân chứ không phải là cường độ của chính cơn đau; nó cũng cho phép đánh giá những bệnh nhân không thể tự báo cáo.
Trong trường hợp bệnh nhân giao tiếp được, cơn đau có thể được đánh giá bằng cách trả lời một câu hỏi đơn giản (Bạn có đau không? Có/Không) hoặc bằng cách đánh giá cường độ đau bằng thang điểm từ 0 (không đau) đến 10 (mức đau tối đa có thể tưởng tượng được). Cả NRS và nhận thức chủ quan đều có thể được sử dụng như nhau. (26)
Kích động hoặc mức độ tỉnh táo
Chúng tôi khuyến cáo sử dụng RASS có hệ thống ở người lớn theo các mục tiêu theo giai đoạn phát triển của COVID-19 ARDS:
Giai đoạn sớm hoặc ARDS vừa/nặng (an thần sâu): Mức an thần RASS mục tiêu -4/-5. Với sự sẵn có của điện não đồ đã xử lý (pEEG), chúng tôi luôn khuyến cáo sử dụng chúng trong giai đoạn này với mục tiêu thang đo chỉ số kép (BIS ©) từ 40 đến 60;
Giai đoạn trung gian hoặc ARDS nhẹ (an thần nhẹ): Mức an thần RASS mục tiêu 0 đến -3. Ở những mức độ an thần này, việc sử dụng pEEG có thể không cần thiết; nếu nó được sử dụng, chúng tôi đề xuất mục tiêu BIS © từ 60 đến 80; và
Giai đoạn tiến triển hoặc cai máy (an thần nhẹ hoặc không dùng thuốc an thần): Mục tiêu an thần RASS cấp độ 1 đến -1.
Hình 4 Công cụ quan sát cơn đau trong chăm sóc tích cực. (25)
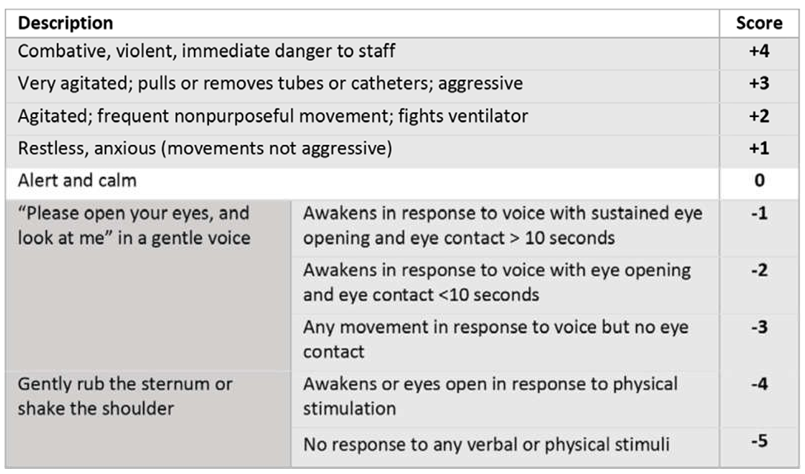
Một đánh giá hệ thống của Cochrane với phân tích tổng hợp được công bố vào năm 2018 cho thấy việc thực hiện các phác đồ an thần ở người lớn và trẻ sơ sinh trong ICU không vượt trội so với các phương pháp chăm sóc thông thường về tỷ lệ tử vong, thời gian thở máy và thời gian nằm viện. (27) (28) Mặc dù vậy, việc giám sát thường xuyên và liên tục mức độ tỉnh táo bằng các công cụ đã được xác thực là lý tưởng trong ICU. Tuy nhiên, do nhân viên y tế có nguy cơ lây nhiễm cao và bệnh nhân nhiễm COVID-19 thường phải an thần sâu nên nhiệm vụ này gặp nhiều khó khăn. Chúng tôi đề xuất sử dụng các công cụ đã được xác nhận tùy thuộc vào giai đoạn lâm sàng của bệnh nhân và có tính đến mức độ an thần và yêu cầu của NMB. Thông qua RASS (Hình 5), một đánh giá chủ quan có thể được thực hiện với 10 giá trị có thể, với giá trị dương tương ứng với các mức độ kích động khác nhau và giá trị âm tương ứng với an thần. (29,30)
Đánh giá khách quan thông qua máy đo độ sâu gây mê dựa trên điện não đồ dựa trên việc đo hoạt động điện não ở 2 hoặc 4 kênh. Theo tính khả dụng hạn chế của nó, việc sử dụng nó chỉ được đề xuất cho những bệnh nhân đang dùng thuốc an thần sâu (RASS -4 /-5) khi không thể đánh giá lâm sàng. Để sử dụng, các khuyến cáo sau được cung cấp: đảm bảo rằng các điện cực được đặt đúng cách, để ít nhất 3-5 phút để đạt được tín hiệu ổn định, tìm kiếm sự hiện diện của các tín hiệu nhiễu và đánh giá chất lượng tín hiệu, hoạt động của điện cơ đồ, mức độ an thần (mục tiêu phải từ 40 đến 60 trong màn hình BIS © và CoNoxTM, ở giá trị thấp hơn, mức độ an thần sẽ sâu hơn), tỷ lệ ức chế (càng gần 0 càng tốt) và sóng điện não đồ để xác nhận rằng các trị số phù hợp với từng giá trị riêng biệt. Chúng tôi khuyến cáo nên xem lại các khuyến cáo của Hiệp hội Quốc tế về Đào tạo Bác sĩ Gây mê Hồi sức điện não. Ngoài ra, nó cũng nổi bật Thang đo An thần-Kích động Riker (SAS, Riker Sedation-Agitation Scale) bao gồm đánh giá chủ quan với 7 cấp độ riêng lẻ, với số điểm 5 – 7 tương ứng với kích động, 1-3 tương ứng với an thần và 4 tương ứng với bệnh nhân bình tĩnh và hợp tác. Không giống như RASS, Riker SAS đánh giá phản ứng với các kích thích đau đớn. (32) Cuối cùng, đánh giá chủ quan cho phép đánh giá phản ứng của bệnh nhân với các kích thích khác nhau: thính giác, xúc giác hoặc đau đớn; tuy nhiên, những đánh giá như vậy không thể được sử dụng khi bệnh nhân đang chịu tác dụng của NMB.
Thuốc ức chế thần kinh cơ
Chúng tôi khuyến cáo sử dụng đánh giá lâm sàng và bổ sung lý tưởng, dựa trên tình trạng sẵn có, với sự theo dõi khách quan bằng máy kích thích thần kinh ngoại vi nhóm bốn (TOF, train-of-four) ở người lớn mắc ARDS COVID-19 vừa/nặng.
Hình 5 Thang kích động-an thần Richmond. (29)
Mặc dù không có thang điểm để đánh giá mức độ phong tỏa thần kinh cơ, các hướng dẫn thực hành lâm sàng về việc sử dụng lâu dài NMBs đề xuất hướng dẫn chuẩn độ các thuốc này dựa trên hiệu quả lâm sàng mong muốn. (33-35) Đối với bệnh nhân ARDS tuân thủ thở máy và trong trường hợp không có ho trước khi hút, chúng tôi khuyến cáo, nếu có, theo dõi khách quan độ sâu của thuốc an thần (EEG). TOF cung cấp 4 xung điện cực đại đến dây thần kinh ngoại vi và đánh giá sự tuyển dụng của sợi cơ. (33,35) Các dây thần kinh thường được sử dụng là nhánh thái dương của dây thần kinh mặt, quan sát sự co giật ở cơ hoặc dây thần kinh mi hoặc dây thần kinh trụ và quan sát phản ứng ở cơ dang của ngón tay cái. Điểm số có thể có trong khoảng từ 0 đến 4, với giá trị từ 0 đến 2 cho thấy một biện pháp phong tỏa thần kinh thích hợp. (33) Công cụ này phải luôn được bổ sung với đánh giá lâm sàng. Cuối cùng, nếu bệnh nhân đã được sử dụng NMB, không thể thực hiện các đánh giá theo thang điểm hành vi và chủ quan về an thần và giảm đau.
Sảng (Delirium)
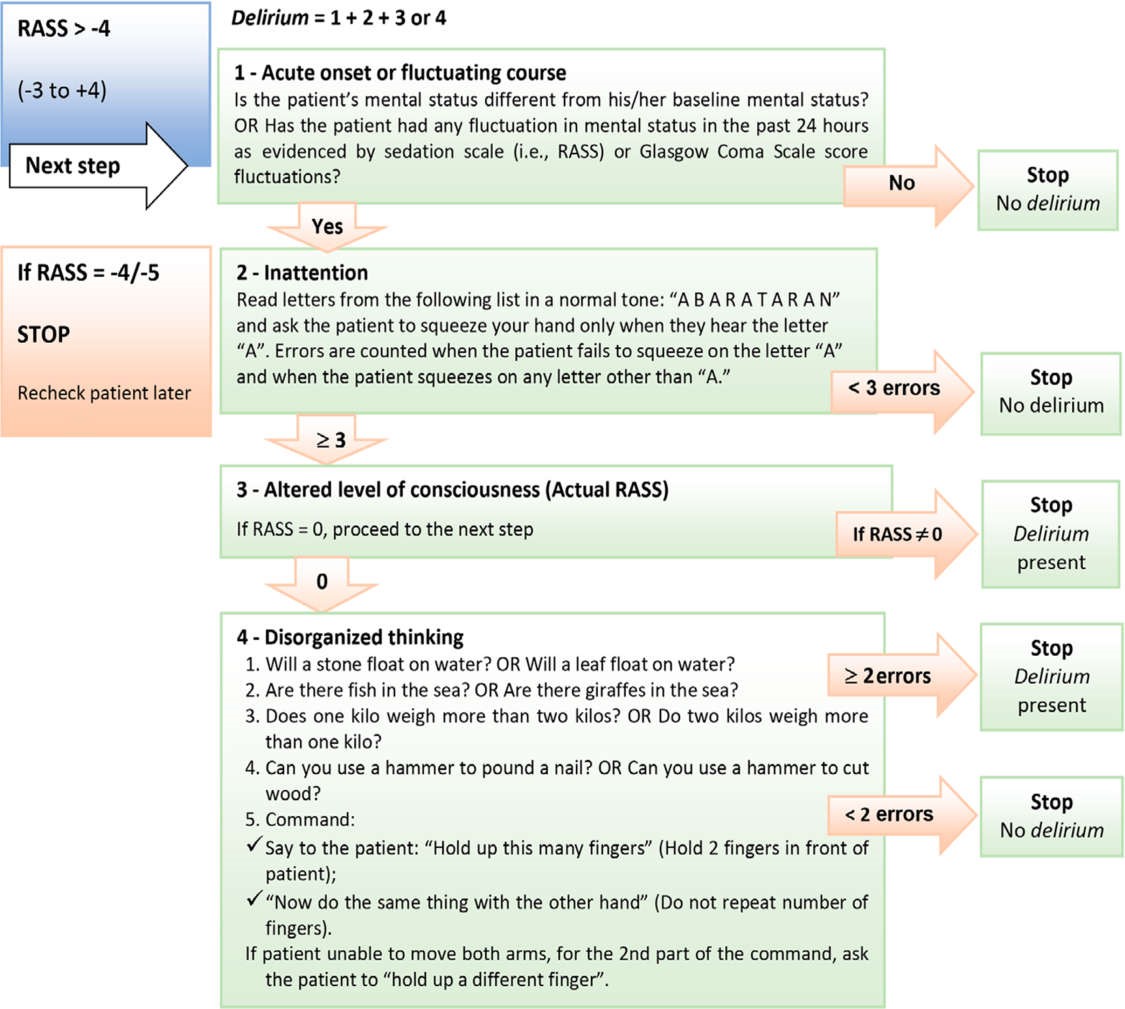
Chúng tôi khuyến cáo nên sử dụng Phương pháp Đánh giá Sảng cho Đơn vị Chăm sóc Đặc biệt (CAM-ICU, Confusion Assessment Method for the Intensive Care Unit) để đánh giá sự hiện diện của sảng ở người lớn dựa trên giai đoạn phát triển của COVID-19 ARDS.
CAM-ICU đánh giá 4 triệu chứng cơ bản của sảng, được định nghĩa là “rối loạn ý thức được đặc trưng bởi sự khởi phát cấp tính và quá trình mất chú ý dao động” kèm theo suy nghĩ vô tổ chức (Hình 6). (3638)
Ngoài ra, bảng kiểm sàng lọc sảng trong chăm sóc đặc biệt (ICDSC), bao gồm 8 mục dựa trên định nghĩa về sảng trong Sổ tay chẩn đoán và thống kê các rối loạn tâm thần IV (DSM-IV) của Hiệp hội Tâm thần Hoa Kỳ, (36,39) có thể được dùng. Nó tính đến nhiều biểu hiện hơn và cho phép mô tả tốt hơn các đặc điểm của sảng cận lâm sàng, mặc dù một số điểm được đánh giá không có định nghĩa hoạt động rõ ràng. Mỗi mục nhận được điểm 1 nếu bệnh nhân đáp ứng rõ ràng các tiêu chí được xác định trong hướng dẫn tính điểm, trong khi điểm 0 được cho nếu không có biểu hiện hoặc nếu mục đó không thể cho điểm. Sảng được chẩn đoán dựa trên tổng điểm lớn hơn 4 và đánh giá lâm sàng. (36,39)
Covid-19 trong bối cảnh khủng hoảng
Tổng quát
Chúng tôi khuyến cáo nên sử dụng thuốc qua đường truyền liên tục, thay vì truyền ngắt quãng, để giảm số người vào phòng và nguy cơ tiếp xúc lây truyền cho nhân viên điều trị ARDS ở người lớn với COVID-19.
Chúng tôi khuyến cáo nên phát triển và áp dụng các chiến lược để tiết kiệm các loại thuốc được lựa chọn khi có thể.
Chúng tôi khuyến cáo nên xem xét và cân nhắc với Dịch vụ Dược phẩm về các tác dụng lâm sàng tiềm ẩn của các tương tác dược lý có thể xảy ra giữa các loại thuốc giảm đau-an thần và sảng và các loại thuốc thử nghiệm hiện được khuyến cáo là hỗ trợ điều trị cho bệnh nhân COVID-19.
Bước đầu tiên trước khi bắt đầu truyền thuốc để cắt cơn là đánh giá rủi ro của chính bệnh nhân và các yếu tố nguy cơ bên ngoài có thể làm thay đổi dược động học và dược lực học của thuốc. Người lớn tuổi có xu hướng ít mô cơ hơn và rối loạn chức năng cơ quan nhiều hơn so với người trẻ tuổi, có khả năng dẫn đến giảm chuyển hóa và bài tiết thuốc với nguy cơ tích lũy thuốc.(40,41) Tiền sử lạm dụng thuốc bất hợp pháp, opioid, thuốc chống loạn thần, benzodiazepine hoặc rượu làm giảm ái lực của thuốc với các thụ thể của chúng, do đó làm giảm hiệu quả ở liều bình thường.
Hình 6 Phương pháp đánh giá sảng trong khoa chăm sóc đặc biệt. (38)
Ở những bệnh nhân có chỉ số khối cơ thể cao, các thuốc ưa mỡ qua đường truyền liên tục, chẳng hạn như propofol, sẽ dẫn đến nguy cơ tích tụ và kéo dài cả tác dụng mong muốn và không mong muốn. Ngoài ra còn có các yếu tố đặc trưng cho thực hành lâm sàng có thể dẫn đến những thay đổi trong việc lựa chọn thuốc và điều chỉnh liều lượng; các yếu tố đó bao gồm tương tác giữa các loại thuốc được sử dụng, sự tuân thủ của bệnh nhân với thở máy, có thể dẫn đến tình trạng kích động mạnh và hậu quả là gây ngủ sâu, phụ thuộc vào thuốc vận mạch do hạ huyết áp do thuốc giảm đau an thần, v.v. (15,28,42) Ngoài việc cách ly nghiêm ngặt, nguy cơ lây truyền do tiếp xúc với dịch tiết và khí dung cần có cách tiếp cận tích cực với thuốc an thần và kiểm soát cơn đau để ngăn ngừa kích động đột ngột không kiểm soát và/hoặc tự rút nội khí quản. Một đánh giá báo cáo rằng tỷ lệ rút nội khí quản ngoài kế hoạch được báo cáo trong các thử nghiệm an thần khác nhau lên đến 12%, cao không thể chấp nhận được trong bối cảnh này. Một khía cạnh cần ưu tiên trong việc quản lý người lớn mắc COVID-19 ARDS là việc sử dụng các loại thuốc được dùng qua đường truyền liên tục thay vì ngắt quãng (được đề xuất cho các loại thuốc như morphin, lorazepam, diazepam, v.v.) vì làm như vậy làm giảm số lần vào phòng và do đó làm tăng nguy cơ tiếp xúc với bệnh truyền nhiễm của nhân viên y tế. Một hạn chế đối với việc chuẩn bị dịch truyền bị mất là bằng chứng liên quan đến loại chất pha loãng, độ pha loãng tối đa, loại vật liệu đóng gói và điều kiện môi trường. Những điều kiện này làm thay đổi tính ổn định hóa học và vi sinh của các dung dịch pha loãng và hạn chế khả năng tạo dịch truyền lâu dài, do đó làm tăng thay đổi dịch truyền và tiếp xúc với bệnh nhân. Tất cả các khía cạnh này đã được tính đến trong các khuyến cáo về việc pha loãng và sử dụng thuốc của Sociedad Argentina de Terapia Intensiva (SATI) cho Bộ Y tế Quốc gia.
Do có thể thiếu các loại thuốc được lựa chọn, thường có giá thành cao và phải nhập khẩu, nên trong thời kỳ đại dịch, cần phải ghi nhớ và áp dụng các chiến lược tiết kiệm thuốc, luôn giữ gói biện pháp ABCDEF làm tài liệu tham khảo và tránh thu thập thuốc trong phòng không cần thiết, để Dịch vụ nhà thuốc có thể quản lý các nguồn lực dựa trên hồ sơ tiêu thụ theo thời gian thực. (14,43) Một khía cạnh quan trọng khác là hậu quả lâm sàng có thể xảy ra của sự tương tác giữa thuốc được sử dụng để giảm đau và sảng và các loại thuốc thử nghiệm hiện được khuyến cáo là điều trị hỗ trợ cho COVID-19. (44)
Giảm đau
Chúng tôi khuyến cáo nên duy trì chiến lược giảm đau trước tiên, luôn luôn đánh giá sự hiện diện của cơn đau và cách xử trí, trước khi sử dụng hoặc tăng lượng thuốc an thần ở người lớn với COVID-19 ARDS.
Chúng tôi khuyến cáo sử dụng opioid để kiểm soát cơn đau ở người lớn với COVID-19 ARDS, bất kể tiến triển của bệnh. Bất cứ khi nào có thể, Chúntôi khuyến cáo nên đánh giá việc thực hiện các chiến lược tiết kiệm opioid đã chọn.
Dòng đầu tiên: Fentanyl
Dòng thứ hai: Morphine
Thay thế: Remifentanil (ưu tiên trong giai đoạn phục hồi)
Một trụ cột của phương pháp này là trước tiên phải duy trì chiến lược giảm đau, luôn đánh giá sự hiện diện của cơn đau và cách xử trí trước khi sử dụng hoặc gia tăng thuốc an thần. (15) Một khía cạnh lâm sàng quan trọng cần nhấn mạnh liên quan đến fentanyl và morphin là tương tác dược lý đã được ghi nhận đầy đủ của chúng với các thuốc benzodiazepin (midazolam và lorazepam), dexmedetomidine và propofol trong thời gian ở gan. chuyển hóa, có khả năng gây suy hô hấp, hạ huyết áp và an thần sâu (Bảng 1). Ngoài ra còn có bằng chứng liên quan về mặt lâm sàng về tương tác giữa Remfentanil và benzodiazepine, dexmedetomidine và propofol có thể dẫn đến các đợt giảm thông khí, tắc nghẽn đường thở, tụt độ bão hòa hoặc ngưng thở. điều chỉnh đến liều hiệu quả tối thiểu của thuốc an thần và opioid thông qua việc đánh giá liên tục các mục tiêu được cá nhân hóa đề xuất cho việc giảm đau của từng bệnh nhân.
Bảng 1 Liều lượng, các tác dụng ngoại ý và tương tác của các loại thuốc giảm đau được đề xuất
|
Thuốc |
Pha loãng Nồng độ ổn định/tương thích Chất pha loãng |
Liều ban đầu và truyền duy trì |
Điều chỉnh liều lượng |
Các biện pháp phòng ngừa/tương tác với quản lý COVID-19/các tác dụng phụ nghiêm trọng |
|
Ống Fentanyl 250mcg/5mL |
CS: tính bằng SS, tối đa 20mcg/mL (bằng PVC hoặcPP) Trong DX5%, 5mcg/mL(trong PVC hoặc PP) Tinh khiết (trong hộp nhựaPVC hoặc PP) Ví dụ: 10 ống (2500mcg) + 100mL SS (thể tích cuối cùng 150mL) |
Liều ban đầu: 1mcg/kg Duy trì: CI 0,7 – 2,5mcg/kg/giờ Không quá 10mcg/kg/giờ |
LF nặng: sử dụng liều thay thế hoặc liều thấp hơn có hiệuquả |
Các tác dụng phụ: hạ huyết áp – giải phóng histamine – suy hô hấp Tương tác: LPV/r: tương tác tiềm tàng, nguy cơ tích lũy. Sử dụng liều hiệu quả tối thiểu |
|
Remifentanil lọ 5mg |
Hoàn nguyên lọ bằng 5mL DW CS: tính bằng SS/DX5%, 5 – 20mcg/mL Giới hạn thể tích tối đa: 400mcg/mL Thận trọng! Trong RL, nó chỉ ổn định trong 4 giờ Ví dụ: 2 lọ + 100mL SS(thể tích cuối cùng 110mL) |
Liều ban đầu: không áp dụng Duy trì: CI 0,5 -15mcg/kg/giờ |
RF hoặc LF: không điều chỉnh |
Tác dụng ngoại ý: tăng nồng độ sau khi ngưng sử dụng. Tụt huyết áp, suy hô hấp Tương tác: không có |
|
Morphine ống 10mg/1mL |
CS: tính bằng SS, 0,14 – 1,5mg/mL Tối đa 2,5mg/mL Trong DX5%, 0,1 – 1mg/mL Ví dụ: 10 ống (100mg) + 100mL SS (thể tích cuối cùng 110mL) |
Liều ban đầu: 0,05 – 0,1mg/kg Duy trì: CI 0,07 đến 0,5mg/kg/giờ |
RF: rủi ro tích lũy Điều chỉnh: GF> 50mL/phút: 0,02 – 0,15mg/kg IV c/4 giờ; GF 20 – 50mL/phút: 75% liều dùng; GF: 10 – 20mL/phút: 50% liều LF: khuyến cáo không nên, nguy cơ mắc bệnh não gan |
Các tác dụng phụ: hạ huyết áp – giải phóng histamine Tương tác: LPV/r: tương tác vừa phải, nồng độ morphin có thể giảm, tiềm ẩn nguy cơ hội chứng cai |
CS – concentration stable for 24 hours; SS – 0.9% saline solution; DX5% – 5% dextrose; RL – Ringer’s lactate; LF – liver failure; DW – distilled water; RF – renal failure; GF – glomerular filtration; CI – continuous infusion; PRIS – propofol infusion syndrome; HR – heart rate; PP – polypropylene; PE – polyethylene; PVC – polyvinyl chloride; LPV/r – lopinavir/ritonavir; HCQ – hydroxychloroquine; NA – not applicable
Fentanyl là loại thuốc được sử dụng rộng rãi nhất trong bối cảnh của chúng ta, cũng như ở phần còn lại của thế giới, với đặc điểm dược động học, chống chỉ định và các tác dụng ngoại ý đã biết.(46) Cần thận trọng đặc biệt khi dùng truyền liên tục và kéo
dài do tích lũy chủ yếu ở bệnh nhân suy gan nặng; Cơn đau nên được đánh giá thường xuyên và điều chỉnh tốc độ truyền định kỳ để đạt được liều hiệu quả thấp nhất ở những bệnh nhân này. (15,45) Morphine thường được sử dụng ở mức độ thấp hơn fentanyl ở bệnh nhân thở máy do hiệu lực thấp hơn, đặc điểm dược động học kém hơn và nhiều tác dụng ngoại ý hơn; tuy nhiên, nó là một giải pháp thay thế kinh tế và nổi tiếng khi fentanyl không hiệu quả hoặc khi thiếu hụt. (43) Một trong những chất chuyển hóa có hoạt tính của nó, morphin 6glucuronid, tích tụ ở bệnh nhân suy thận và gan; do đó phải điều chỉnh liều hoặc đình chỉ truyền định kỳ ở những quần thể này. Ngoài ra, việc sử dụng nó thường liên quan đến các đợt hạ huyết áp và giải phóng histamine.(42,45,46) Trong giai đoạn trung gian hoặc ARDS nhẹ, việc sử dụng bolus morphine ngắt quãng có thể là một lựa chọn.
Không có nhiều lựa chọn thay thế khác trong bối cảnh của chúng tôi, Remfentanil có tác dụng khởi phát nhanh, không tích lũy đến mức cao và không cần điều chỉnh liều trong trường hợp suy thận hoặc gan; tuy nhiên, chi phí cao và tính sẵn có dao động trong ICU của chúng tôi, quá trình nhanh chóng qua cơ thể do dược động học và các tác dụng phụ liên quan, chẳng hạn như hạ huyết áp, suy hô hấp và tăng nồng độ do dùng thuốc bị gián đoạn, làm cho nó trở thành một chiến lược kém hấp dẫn hơn đối với bệnh nhân COVID -19 ARDS.(45,47) Vì vậy, không nên sử dụng Remfentanil như một tác nhân duy nhất hoặc ở liều cao.(45,48) Khi có thể, việc sử dụng nó nên được dành cho giai đoạn phục hồi, khi khuyến cáo sử dụng thuốc an thần nhẹ hơn hoặc trong thời gian ngắn.
Do có thể có sự thiếu hụt các loại thuốc được lựa chọn trong đại dịch, một chiến lược mà chúng ta nên luôn đánh giá và cố gắng thực hiện trong thời gian an thần nhẹ hoặc phục hồi, cùng với gói ABCDEF, là sự kết hợp của các thuốc nonopioid để giảm liều opioid được lựa chọn. Sự kết hợp của các loại thuốc giảm đau với các cơ chế hoạt động khác nhau, chẳng hạn như trong giảm đau đa phương thức, rất quan trọng để tạo ra tác dụng hiệp đồng và để giảm các tác dụng phụ thường gặp liên quan đến opioid. và ung thư; cho đến nay, không có bằng chứng chất lượng tốt về việc sử dụng nó thường quy trong các ICU. (15,42,49) Bảng 2 cho thấy các thuốc nonopioid được sử dụng phổ biến nhất trong ICU trong trường hợp chiến lược này được thực hiện.
Sự kết hợp giữa opioid tiêm tĩnh mạch và uống có thể cho thấy nhu cầu thuốc tiêm tĩnh mạch thấp hơn và thời gian cai máy ngắn hơn cho những bệnh nhân bị bệnh nặng, mặc dù cần có bằng chứng tốt hơn để có thể đưa ra khuyến cáo thuận lợi. (50) Rào cản chính đối với việc sử dụng opioid đường uống trong ICU là sinh khả dụng bị thay đổi do giảm hấp thu theo đường này ở những bệnh nhân bị bệnh nặng.
Thuốc an thần
Chúng tôi khuyến cáo nên sử dụng lịch trình an thần năng động và tuần tự theo nhu cầu của người lớn với COVID-19 ARDS để tránh quá tải.
Chúng tôi khuyến cáo nên “nghỉ” hoặc ngắt quãng thuốc an thần hàng ngày ở người lớn với COVID19 ARDS chỉ khi điều kiện lâm sàng cụ thể của bệnh nhân cho phép và đội ngũ y tế có thể đảm bảo được sự bảo vệ thích hợp.
Chúng tôi khuyến cáo nên sử dụng một lịch trình điều trị dược lý để an thần dựa trên mục tiêu và sự tiến triển của bệnh ở người lớn với COVID-19 ARDS:
Giai đoạn sớm hoặc ARDS trung bình/nặng (an thần sâu)
Dòng đầu tiên: Midazolam
Dòng thứ hai: Propofol
Thay thế: Benzodiazepines (lorazepam và diazepam) và ketamine.
Bảng 2 Liều lượng, các tác dụng ngoại ý và tương tác thuốc để giảm đau đa phương thức
|
Thuốc |
Pha loãng Nồng độ ổn định/tương thích Chất pha loãng |
Liều ban đầu và truyền duy trì |
Điều chỉnh liều lượng |
Các biện pháp phòng ngừa/tương tác với quản lý COVID-19/các tác dụng phụ nghiêm trọng |
|
Lọ paracetamol 10mg/mL |
Tương thích với SS và DX5% CS: 1mg/mL (sử dụng ngay) Có thể dùng trực tiếp mà không cần pha loãng trước |
Duy trì: 650mg mỗi 4 giờ – 1000mg mỗi 6 giờ Liều tối đa ≤ 4000mg/ngày |
LF: chống chỉ định ở những bệnh nhân bị LF nặng RF: CrCl ≤ 30mL/phút Cân nhắc việc tăng khoảng cách giữa các liều và giảm liều |
Các tác dụng phụ: buồn nôn, nôn, nhức đầu, mất ngủ Tương tác: không có |
|
Ketamine lọ 500mg/10mL |
CS: tính bằng SS, 1mg/mL (pha loãng 500mg trong 500mL) |
Liều ban đầu: 0,1 – 0,5mg/kg Khuyến nghị: 0,15mg/kg Duy trì: CI 0,1 – 0,4mg/kg/giờ Không vượt quá 2mg/kg/giờ |
RF hoặc LF: không cần điều chỉnh |
Các sự kiện có hại: các triệu chứng tâm thần (ảo giác); suy hô hấp; huyết áp thấp Tương tác: LPV/r: tương tác tiềm tàng, nguy cơ tích lũy. Sử dụng liều hiệu quả tối thiểu |
|
Dexmedetomidine lọ 200mcg/2mL |
CS: tính bằng SS, 4mcg/mL Ví dụ: 2 lọ trong 100mL SS (thể tích cuối cùng là 104mL) |
Duy trì: CI 0,2 – 0,7 mcg/kg/giờ Khuyến nghị sử dụng trong 24 giờ |
LF: sử dụng 0,2 – 0,7 mcg/kg/giờ |
Các tác dụng phụ: nhịp tim chậm và hạ huyết áp Tương tác vừa phải với LPV/r (giám sát) và với HCQ Theo dõi khoảng QT |
|
Ketorolac ống 30mg/mL |
CS: tính bằng SS, 0,3 – 0,6mg/mL (trong hộp nhựa PVC) Trong RL và DX5%, 0,6mg/mL (trong hộp nhựa PVC). |
Liều khởi đầu: 30mg, sau đó 1530mg mỗi 6 giờ trong 5 ngày Liều tối đa: 120mg/ngày trong 5 ngày Truyền tĩnh mạch trực tiếp, tiêm trong vòng không dưới 15 giây |
RF: 15mg mỗi 6 giờ Liều tối đa: 60mg/ngày |
Tác dụng ngoại ý: tăng huyết áp, phù nề, phản ứng có hại trên da Tương tác: Không có |
|
Diclofenac ống 75mg/3mL |
CI: pha 100mL – 500mL SS hoặc DX5% với dung dịch natri bicacbonat tiêm (0,5mL dung dịch 8,4% hoặc 1mL dung dịch 4,2%) Truyền ngắt quãng: pha 1 ống với 50mL SS |
Duy trì: 75 mg mỗi 12 giờ Liều khuyến cáo tối đa: 150mg/ngày |
LF và RF nghiêm trọng: việc sử dụng nó không được khuyến khích |
Tác dụng phụ: suy thận, phù, ngừng tim, phản ứng da Tương tác: không xảy ra với dexamethasone và hydrocortisone |
|
Tramadol ống 50mg/mL |
CS: tính bằng SS và DX5%, 0,4 – 0,5mg/mL (PVC) Tính bằng RL, 0,4mg/mL (PVC) |
Duy trì: 50 – 100mg sau mỗi 6 giờ |
RF: CrCl Liều tối đa: 200mg/ngày CrCl LF nặng: 50mg mỗi 12 giờ |
Biến cố có hại: phản ứng da và đường tiêu hóa Tương tác: tiềm năng với LPV/r và với HCQ Theo dõi khoảng QT |
|
Carbamazepine viên 200mg |
CS: tính bằng SS và DX5%, 0,4 – 0,5mg/mL (PVC) Tính bằng RL, 0,4mg/mL (PVC) |
Liều ban đầu: 50 – 100mg Duy trì: 100 – 200mg sau mỗi 4 – 6 giờ Liều tối đa: 1200mg/ngày |
LF và RF nghiêm trọng: việc sử dụng nó không được khuyến khích |
Biến cố có hại: phản ứng da và đường tiêu hóa, hạ huyết áp, blốc nhĩ thất Tương tác: không dùng với LPV/r và HCQ Tương tác có thể xảy ra với dexamethasone và hydrocortisone, ivermectin và ít khả năng hơn với remdesivir |
|
Gabapentin viên 100, 300, 600mg |
NA |
Liều ban đầu: 100 mg cứ 8 giờ một lần Duy trì: 900 – 3600mg 3 lần mỗingày |
RF: CrCl 30 – 59mL/phút: 400 – 1400mg/ngày 2 lần mỗi ngày CrCl 15 – 29mL/phút 200 – 700mg/ngày x 1 lần/ngày CrCl 15mL/phút: 100 – 300mg/ngày CrCl |
Các tác dụng phụ: phản ứng da và đường tiêu hóa, chóng mặt, buồn ngủ Tương tác: không có |
|
Viên Pregabalin 25,50,75,150,300 mg |
NA |
Liều khởi đầu: 75 – 150mg Duy trì: 150 – 600mg/ngày x 2 lần/ngày Liều thông thường: 300 – 600mg/ngày |
RF: CrCl 30 – 60mL/phút: 75 đến 300mg/ngày chia làm 2 hoặc 3 lần CrCl 15 – 30mL/phút 25 150mg/ngày một lần hoặc hai lần mỗi ngày CrCl dưới 5mL/phút 2550mg một lần mỗi ngày |
Tác dụng ngoại ý: có thể gây an thần quá mức và hạ huyết áp. Tương tác: Không có |
Giai đoạn trung gian hoặc ARDS nhẹ (an thần nhẹ) và giai đoạn tiến triển hoặc cai máy (an thần nhẹ hoặc không dùng thuốc an thần)
Dòng đầu tiên: Propofol
Dòng thứ hai: Dexmedetomidine
Thay thế: Benzodiazepines (midazolam, lorazepam và diazepam) và clonidine
Những bệnh nhân mắc COVID-19 nặng vào ICU hầu hết đều có biểu hiện giảm oxy máu nặng và/hoặc ARDS cần thở máy, an thần sâu và đôi khi NMBs.(11,51-53) Thách thức là duy trì an thần sâu nghiêm ngặt khi cần thiết và, đồng thời xác định thời điểm sớm nhất có thể bắt đầu dùng thuốc an thần nhẹ. Điều quan trọng là phải nhận ra lợi ích của việc tránh dùng thuốc an thần sâu và kéo dài, cùng với lợi ích của việc an thần nhẹ với sự tham gia tích cực của gia đình, mặc dù không phải lúc nào cũng có thể triển khai tham gia trong thời gian đại dịch do nguy cơ phơi nhiễm và lây nhiễm. (36,54,55) Ví dụ, và mặc dù lợi ích của nó đã được chứng minh, việc áp dụng thời gian nghỉ thuốc an thần hàng ngày là khó khăn và tiềm ẩn nhiều rủi ro ở những bệnh nhân này. Do đó, phải đặc biệt lưu ý và luôn ưu tiên bảo vệ đội ngũ y tế, ngay cả khi điều đó gây bất lợi cho chiến lược này.(56) Trước khi thực hiện thử nghiệm nghỉ an thần và do đó đánh giá tình trạng an thần nhẹ, cần đáp ứng tất cả các tiêu chí sau: PaO2/FiO2 > 175mmHg, áp lực dương cuối thở ra (PEEP) 2O, FiO2
Giai đoạn đầu
Các hướng dẫn hiện hành về ASD trong điều kiện bình thường ưu tiên sử dụng các thuốc an thần có thời gian bán hủy ngắn và dược động học hai phân khu và các thuốc nonbenzodiazepin.(15) Tuy nhiên, trong trường hợp này và cho các trường hợp trên, chúng tôi có thể ưu tiên các loại thuốc có thời gian bán hủy dài hơn (midazolam, lorazepam, v.v.), luôn luôn điều chỉnh đến liều tối thiểu có hiệu quả, làm giảm chi phí và được cung cấp rộng rãi trong các ICU trong thời gian đầu thở máy (Bảng 3). Việc truyền liên tục ketamine kết hợp, trong các chiến lược an thần sâu, có thể giúp những bệnh nhân khó điều trị tiếp cận với phương pháp điều trị thông thường và giảm nhu cầu sử dụng thuốc để giảm đau. (57,58) Một đánh giá có hệ thống gần đây với phân tích tổng hợp đã báo cáo rằng việc sử dụng ketamine như một chất bổ trợ trong lịch sử dụng thuốc an thần-giảm đau cho bệnh nhân thở máy sẽ làm giảm nhu cầu về propofol; tuy nhiên, có sự không chắc chắn về kết quả lâm sàng, khả năng dung nạp và hồ sơ an toàn. (59)
Diazepam có thời gian bán hủy dài và hầu như chỉ được chuyển hóa ở gan, tạo ra các chất chuyển hóa có hoạt tính có nguy cơ tích tụ rất cao ở những bệnh nhân bị suy giảm chức năng thận. Dễ gây sảng và có tá dược (propylene glycol) tích tụ ở bệnh nhân suy thận và có thể rất độc, dẫn đến toan chuyển hóa và tổn thương thận. Không có bằng chứng chất lượng tốt về việc truyền liên tục cho những bệnh nhân nguy kịch; do đó, nó chỉ nên được sử dụng trong thời gian thiếu các loại thuốc thông thường, và nên tránh truyền quá lâu. do đó, liều lượng và giám sát của chúng cần được đánh giá nghiêm ngặt.
Bảng 3 Liều lượng, các tác dụng ngoại ý và tương tác của các loại thuốc an thần được đề xuất
|
Thuốc |
Pha loãng Nồng độ ổn định/tương thích Chất pha loãng |
Liều ban đầu và truyền duy trì |
Điều chỉnh liều lượng |
Các biện pháp phòng ngừa/tương tác với quản lý COVID-19/các tác dụng phụ nghiêm trọng |
|
Midazolam ống 5mg/mL |
CS: 0,035 -1mg/mL trong thùng PCV và lên đến 2mg/mL trong thùng PP cho SS và DX5% Không tương thích với RL; có thể được quản lý tinh khiết Ví dụ: 8 ống (120mg) + 100 mL SS (thể tích cuối cùng 124mL) |
Liều ban đầu: 0,01 – 0,05 mg/kg Duy trì: CI 0,02 -0,1 mg/kg/giờ Không vượt quá 0,2 mg/kg/giờ |
RF: bắt đầu với liều hiệu quả thấp nhất CrCl LF: Child-pug B-C không được khuyến cáo để truyền liên tục |
Biến cố có hại: suy hô hấp-hạ huyết áp. Tương tác: LPV/r: Tương tác tiềm năng Giám sát chặt chẽ; sử dụng liều hiệu quả tối thiểu |
|
Lorazepam ống 4mg/mL |
Độ ổn định của dung dịch khó Tránh ánh sáng CS: tính bằng DX5%, 1 – 2mg/mL (bằng polyolefin hoặc PVC) Tính bằng SS, 1mg/mL trong PP; 0,04mg/mL trong PVC; 0,1 và 0,038mg/mL trong PE Trong RL, 0,1mg/mL trong PE Ví dụ: 10 ống (40mg) + 30mL DX5% (khối lượng cuối cùng 40mL) |
Liều ban đầu: 0,02 – 0,04 mg/kg ‘(≤ 2mg) Duy trì: CI 0,01 – 0,1mg/kg/giờ Tốc độ truyền ≤ 10mg/giờ |
RF hoặc LF nặng: sử dụng thay thế Nguy cơ tích tụ tá dược |
Thận trọng: nguy cơ tích tụ tá dược độc (propylene glycol) ở người suy thận, hạn chế truyền dịch Tác dụng ngoại ý: suy hô hấp hạ huyết áp Tương tác: không có |
|
Diazepam ống 10mg/2mL |
Độ ổn định của dung dịch khó Tránh ánh sáng SS, 0,01mg/mL, 0,05 mg/mL, 0,08 mg/mL và 0,2mg/mL; DX5%, 0,04 mg/mL và 0,2 mg/mL Các dung dịch pha loãng tương thích trong PE và hộp thủy tinh Tương thích với RL trong hộp thủy tinh CS 0,05mg/mL |
Liều ban đầu: 5 – 10mg Duy trì: 0,03 – 0,1mg/kg cứ 0,5 – 6 giờ một lần CI: 0,05 – 0,2 mg/kg/giờ |
RF hoặc LF: không yêu cầu điều chỉnh cụ thể, giám sát chặt chẽ do nguy cơ tích tụ tá dược |
Biện pháp phòng ngừa: tích tụ tá dược propylene glycol có thể tạo ra độc tính Giám sát chặt chẽ, nguy cơ quá tải. Biến cố có hại: suy hô hấp Tương tác: Có thể xảy ra với LPV/r |
|
Propofol ống 200mg/20mL (1%) Propofol lọ 1000mg/50mL (2%) |
Đặt ống vào một túi PP hoặc PVC rỗng 6 giờ ổn định Ví dụ: 4 ống (800mg) trong thùng rỗng (thể tích cuối cùng là 80mL) Sử dụng trực tiếp từ lọ mà không cần chuyển/pha loãng. Sau khi mở, độ ổn định 12 giờ |
Liều khởi đầu: 5μg/kg/phút Chỉ khi không có khả năng hạ huyết áp Duy trì: CI 0,3 -3 mg/kg/giờ Không quá 4,5mg/kg/giờ |
RF hoặc LF: dùng liều thấp hơn 0,3 – 2,4mg/kg/giờ |
Đề phòng: nguy cơ tích tụ khi truyền kéo dài; sử dụng liều hiệu quả tối thiểu. Các tác dụng ngoại ý: suy hô hấp, hạ huyết áp, tăng triglycerid máu; nguy cơ mắc PRIS tăng khi dùng liều lớn hơn 3 mg/kg/h; giám sát chặt chẽ. Tương tác: tiềm năng với LPV/r và với HCQ Theo dõi khoảng QT |
|
Dexmedetomidine lọ 200mcg/2 mL |
CS: tính bằng SS, 4mcg/mL Ví dụ: 2 lọ + 100mL SS (thể tích cuối cùng là 104mL) |
Liều ban đầu: (không khuyến khích) 0,5 mcg/kg trong 15 phút – theo dõi nhịp tim nghiêm ngặt Duy trì: CI 0,2 -1,4mcg/kg/giờ |
LF: theo dõi, dùng liều thấp hơn 0,2 – 0,7mg/kg/giờ |
Các tác dụng phụ: nhịp tim chậm và hạ huyết áp Tương tác: tiềm năng với LPV/r và với HCQ theo dõi khoảng QT |
|
Clonidine ống 150mcg/mL |
Tránh ánh sáng CS: 9mcg/mL tính bằng SS Ví dụ: 6 ống + 100mL SS (khối lượng cuối cùng 106mL) |
Bolus: 0,5mcg/kg (chỉ ở bệnh nhân huyết động ổn định) Duy trì: CI 0,5 2mcg/kg/giờ Lên đến 3mcg/kg/giờ |
RF hoặc LF: không điều chỉnh |
Tác dụng ngoại ý: hạ huyết áp, nhịp tim chậm, blốc nhĩ thất Tương tác: không |
Giai đoạn trung gian và giai đoạn nâng cao
Trong giai đoạn hồi phục, với việc dùng thuốc an thần nhẹ hơn và không cần thuốc NMB và các phiên điều trị nằm sấp, chúng ta có thể ưu tiên các thuốc có dược động học thuận lợi hơn, thời gian bán hủy ngắn hơn và ít tích lũy hơn (propofol và dexmedetomidine). (42,60) Nếu tình hình huyết động cho phép, việc sử dụng propofol đơn độc hoặc kết hợp với benzodiazepine (thường là midazolam) nên được xem xét vì cách tiếp cận này đã được chứng minh là dẫn đến thời gian lưu lại ICU ngắn hơn và tỷ lệ sảng thấp hơn so với benzodiazepine đơn thuần. Tuy nhiên, để truyền propofol liên tục, cần theo dõi liên tục do nguy cơ suy hô hấp, hạ huyết áp, tăng triglycerid máu và sau thời gian dài truyền và dùng liều tối đa, xuất hiện hội chứng truyền propofol (PRIS). (45,61)
Sự kết hợp của dexmedetomidine với các thuốc giảm đau khác đã được chứng minh là làm giảm liều midazolam, propofol và opioid. (62) So với propofol, dexmedetomidine có liên quan đến thời gian nằm ICU ngắn hơn và tỷ lệ mê sảng thấp hơn, trong khi ở những bệnh nhân thở máy kéo dài, nó có thể làm giảm số ngày thở máy và giữ cho bệnh nhân ở trạng thái giao tiếp. (63-65) Một chất thay thế dexmedetomidine là clonidine; tuy nhiên, bằng chứng hỗ trợ việc sử dụng nó trong điều kiện bệnh nhân nguy kịch rất khan hiếm và có chất lượng thấp; do đó, nó chỉ nên được sử dụng trong những trường hợp thiếu các liệu pháp thông thường. (65) Thuốc tác động alpha-2 (như dexmedetomidine), chi phí thấp và tính an toàn phù hợp ở những bệnh nhân ổn định về huyết động làm cho nó trở thành một lựa chọn thay thế hấp dẫn khi dexmedetomidine không phải là một lựa chọn. Ngược lại, ở những bệnh nhân đang dùng dexmedetomidine, trong giai đoạn cai máy, nên chuyển đổi dần dần để tránh các hiện tượng ngừng thuốc và lo lắng trước khi ngừng sử dụng. (66-68)
Mặc dù việc sử dụng ketamine không phổ biến trong ICU của chúng tôi, việc sử dụng nó có thể hữu ích như một biện pháp thay thế trong an thần nhẹ và do đặc tính giảm đau của nó, như một chiến lược tiết kiệm opioid hoặc benzodiazepine khi kết hợp với các lựa chọn thuốc đó. (69, 70) Việc sử dụng ketamine có liên quan đến các biến cố thần kinh thường xuyên và nghiêm trọng, chẳng hạn như suy hô hấp và hạ huyết áp, làm hạn chế khả năng hồi phục của bệnh nhân ARDS COVID-19. Nó không được khuyến cáo cho những bệnh nhân nghi ngờ đau thắt ngực không ổn định, huyết áp cao không kiểm soát được hoặc tăng huyết áp nội sọ. Quan trọng là, việc đánh giá độ sâu của thuốc mê bằng BIS làm mất giá trị và mối tương quan đối với bệnh nhân dùng ketamine.
Khi bệnh cảnh hô hấp của bệnh nhân được duy trì trong 48 giờ (PaO2/FiO2> 200, FiO2 2O), không có NMBs và không cần định vị nằm sấp, có thể tiến tới thời gian bán thải ngắn hơn, với các chiến lược tiết kiệm opioid. Trong giai đoạn thứ ba này, mục tiêu là đạt được RASS từ 1 đến -1, đặc biệt chú ý đến việc quản lý cơn đau và lo lắng bằng thuốc và không dùng thuốc và theo dõi hàng ngày sự hiện diện của sảng. Nếu dexmedetomidine đã được sử dụng cho những bệnh nhân đã được an thần trước đó, thì không nên tiến hành dẫn đầu, vì sẽ mất 6 giờ để đạt được hiệu quả mong muốn. Nếu sử dụng dẫn đầu, nên dùng 0,5mcg/kg trong 15 phút với theo dõi nhịp tim, vì có thể xảy ra tăng huyết áp thoáng qua.
Các chất ngăn chặn thần kinh cơ
Chúng tôi khuyến cáo nên sử dụng các chất ngăn chặn thần kinh cơ, bắt đầu bằng việc truyền không liên tục, chỉ trong điều kiện lâm sàng chính xác của bệnh nhân, và theo mục tiêu và sự tiến triển của bệnh ở người lớn với COVID-19 ARDS:
Giai đoạn sớm hoặc ARDS trung bình/nặng (an thần sâu)
Dòng đầu tiên: Atracurium
Dòng thứ hai: Vecuronium hoặc rocuronium
Thay thế: Pancuronium
Bệnh nhân ARDS COVID-19 yêu cầu thở máy kéo dài và an thần sâu, thường liên quan đến việc sử dụng NMBs liên tục, dẫn đến nguy cơ di chứng cao trong và sau thời gian điều trị ICU của họ. (71) Việc sử dụng NMB được khuyến cáo cho những bệnh nhân nặng ARDS, với PaO2/FiO2
Về lợi ích lâm sàng của chiến lược này trong giai đoạn đầu của ARDS, có bằng chứng mâu thuẫn về sự cải thiện kết quả lâm sàng ở nhóm dân số này, mặc dù nó có thể giúp hạn chế tổn thương phổi do bệnh nhân tự gây ra (P-SILI) và tổn thương phổi liên quan đến không đồng bộ máy thở – bệnh nhân do kích hoạt kép và kích hoạt ngược, và có thể tránh tạo khí dung. (22,74-76) Ở những bệnh nhân quyết định sử dụng NMBs (ví dụ, ARDS nặng với thông khí nằm sấp), Chúng tôi khuyến cáo nên dùng thuốc chẹn không phân cực với truyền bolus ngắt quãng để tạo điều kiện thông khí bảo vệ phổi và tư thế nằm sấp, chỉ chuyển sang truyền liên tục nếu có mất đồng bộ dai dẳng hoặc tổn thương huyết động nặng, đánh giá lại sau mỗi 24 giờ. (22,77)
Các hướng dẫn thực hành lâm sàng và sự đồng thuận của các bác sĩ chuyên khoa trên toàn thế giới khuyến cáo cisatracurium là lựa chọn hàng đầu cho bệnh nhân ARDS, cũng là loại được nghiên cứu nhiều nhất ở nhóm dân số này. (15,43,76) Bởi vì nó không có sẵn ở Argentina, khuyến nghị lựa chọn đầu tiên của chúng tôi là atracurium. Atracurium, giống như cisatracurium, có cấu trúc benzylisoquinoline và là một NMB tác dụng trung gian được chuyển hóa bởi các esterase huyết tương và thải trừ Hofmann, điều này có lợi cho việc sử dụng nó ở bệnh nhân suy thận hoặc gan (Bảng 4). (76,78) Tuy nhiên, do đối với tác dụng histaminergic của nó, nó có thể tạo ra sự gia tăng chất bài tiết ở đường hô hấp và, khi sử dụng kéo dài, sự tích tụ của laudanosine, một chất chuyển hóa có khả năng gây độc cho thần kinh. (45,73)
Bảng 4 Liều lượng, các tác dụng ngoại ý và tương tác của các loại thuốc được đề xuất cho phong bế thần kinh cơ
|
Thuốc |
Pha loãng Nồng độ ổn định/tương thích Chất pha loãng |
Liều ban đầu và truyền duy trì |
Điều chỉnh liều lượng |
Các biện pháp phòng ngừa/tương tác với quản lý COVID-19/các tác dụng phụ nghiêm trọng |
|
Atracurium ống 50mg / 5mL |
CS: tính bằng SS / DX5%. 0,2 – 1mg / mL Tối đa 5mg / mL; không tương thích với RL Ví dụ: 10 ống (500mg) + 100mL SS (thể tích cuối cùng 150mL) |
Liều ban đầu: 0,4 – 0,5mg / kg Duy trì: 5 – 20mcg / kg / phút |
RF hoặc LF: không cần điều chỉnh |
Sự kiện có hại: nguy cơ giải phóng histamine (tối thiểu) Sốc phản vệ (nếu truyền liên tục trong thời gian dài) Tương tác: không có |
|
Vecuronium lọ 10mg |
Pha lại mỗi lọ bằng 10mL nước cất Tương thích với SS, DX5%, RL Ví dụ: 5 ống (50mg) + 100mL SS (thể tích cuối cùng 150mL) |
Liều ban đầu: 0,08 – 0,1mg / kg Duy trì: 0,8 – 1,7mcg / kg / phút |
RF hoặc RF khẩn cấp cấp tính: sử dụng liều hiệu dụng tối thiểu do nguy cơ tích lũy |
Tác dụng ngoại ý: tắc nghẽn phế vị với liều cao Tương tác: không có |
|
Rocuronium ống 50mg / 5mL |
Tương thích với SS, DX5% và RL CS: SS, RL và DX5%, 0,5 và 2mg / mL Ví dụ: 4 ống (200mg) + 100mL SS (thể tích cuối cùng 120mL) |
Liều ban đầu: 0,06 – 1mg / kg Duy trì: 8 – 12mcg / kg / phút |
RF hoặc LF: không cần điều chỉnh, đánh giá đáp ứng liều |
Các tác dụng ngoại ý: nhịp tim chậm, tắc nghẽn phế vị với liều cao Tương tác: tiềm năng với LPV / r hoặc với HCQ, theo dõi khoảng QT |
|
Ống Pancuronium 4mg / 2mL |
Tương thích với SS, DX5%, RL Ví dụ: 10 ống (40mg) + 100mL SS (khối lượng cuối cùng 120mL) |
Liều ban đầu: 0,04 – 0,1mg / kg Duy trì: 1 – 2mcg / kg / phút |
RF: sử dụng liều hiệu quả tối thiểu, do nguy cơ tích lũy Tránh sử dụng nó ở những bệnh nhân có RF nặng, CrCl |
Các tác dụng phụ: suy hô hấp, tăng huyết áp, tắc nghẽn phế vị với liều cao Tương tác: không có |
Đối với dòng thứ hai, vecuronium hoặc rocuronium, với tác dụng trung gian, có thể được xem xét và cũng có thể được sử dụng qua đường tiêm truyền liên tục. Những loại thuốc này được chuyển hóa ở gan và có thể dẫn đến suy thận và gan, nhưng ưu điểm của chúng so với pancuronium là có chất giải độc (sugammadex) giúp đảo ngược nhanh chóng quá trình phong tỏa thần kinh cơ. Pancuronium, có tác dụng kéo dài, là một giải pháp thay thế có dược động học không thuận lợi hơn, có thể được xem xét sử dụng liên tục hoặc ngắt quãng. (35)
Thuật toán giảm đau ở người lớn với COVID19 ARDS trong bối cảnh thiếu hụt
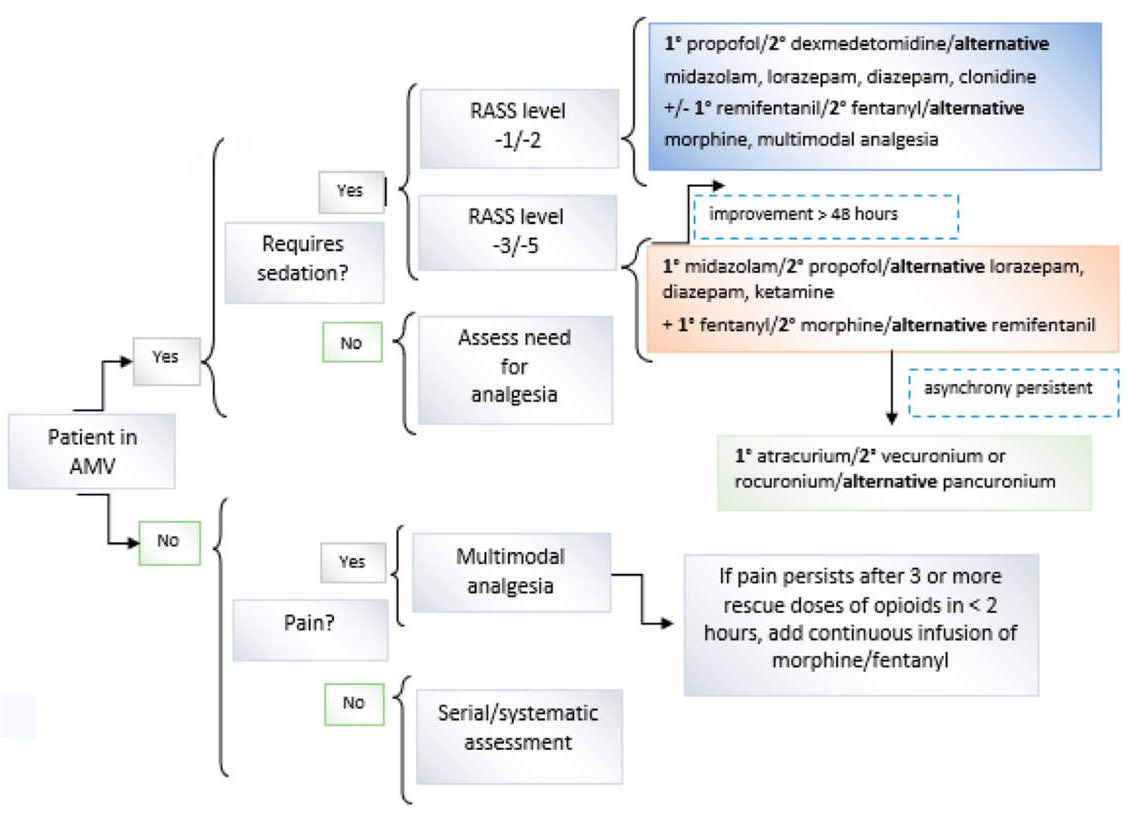
Hình 7 cho thấy một thuật toán được đề xuất, theo các khuyến cáo thông thường, với mục tiêu duy trì các loại thuốc đã chọn, giảm kích động và/hoặc sảng và tạo điều kiện cho việc cai thở máy với tình trạng sức khỏe thể chất và nhận thức tối đa có thể. Có khả năng là khi đối mặt với đại dịch COVID-19, sẽ cần phải sử dụng lịch trình thay đổi do thiếu thuốc lựa chọn, thiết bị y tế hoặc nhân viên y tế, có thể dẫn đến thời gian thở máy bảo vệ kéo dài do ARDS nghiêm trọng và các quy trình khôi phục chậm hơn. (22) Tài liệu này sẽ xem xét các sai lệch có thể có của thuật toán được đề xuất và sẽ trình bày các giải pháp thay thế để giải quyết chúng.
Phương pháp điều trị toàn diện cho bệnh nhân sảng trong phòng chăm sóc đặc biệt
Chúng tôi khuyến cáo không sử dụng điều trị thuốc thông thường để phòng ngừa hoặc kiểm soát chứng sảng ở người lớn với COVID-19 ARDS.
Chúng tôi khuyến cáo, nếu có thể, áp dụng các biện pháp không dùng thuốc, chẳng hạn như tạo cảm giác thoải mái sớm bằng cách sử dụng thuốc giảm đau, thuốc an thần tối thiểu và chăm sóc con người tối đa (eCASH), để ngăn ngừa và giảm tình trạng sảng ở người lớn với COVID-19 ARDS.
Sảng là kết quả của suy cơ quan cấp tính và được đặc trưng bởi sự khởi đầu cấp tính của sự thay đổi ý thức và chú ý với một diễn biến dao động. Điều quan trọng là, sự xuất hiện của nó ở những bệnh nhân nhập viện ICU có liên quan đến tỷ lệ tử vong cao hơn. do đó, việc phòng ngừa là rất cần thiết. Có tính đến các yếu tố khuynh hướng (ốm yếu, suy giảm nhận thức, v.v.) và các yếu tố kết thúc (có thể được phân thành 3 lĩnh vực: mức độ nghiêm trọng của bệnh, tiếp xúc với thuốc và các yếu tố môi trường), có khả năng sự gia tăng tỷ lệ sảng này không phải là một sản phẩm của một tình trạng dinh dưỡng não cụ thể của virus mà thay vào đó là gánh nặng lớn của các yếu tố kết tủa (liên quan đến an thần, bất động, cô lập, v.v.). (81,83) Khái niệm eCASH do Vincent và cộng sự đề xuất. là một điểm khởi đầu tốt để thảo luận về các biện pháp điều trị không dùng thuốc. Dựa trên khái niệm này, gói ABCDEF có thể được hiểu là “con đường” để đạt được lý tưởng này. (14)
Hình 7 Thuật toán đề xuất để xử lý người lớn mắc hội chứng suy hô hấp cấp COVID-19 trong bối cảnh thiếu thuốc. AMV – thở máy hỗ trợ; RASS – Thang kích động-an thần Richmond.
Tương tự như hướng dẫn thực hành lâm sàng PADIS, chúng tôi không khuyến cáo, do thiếu bằng chứng và lợi ích lâm sàng, thường xuyên sử dụng haloperidol, thuốc chống loạn thần điển hình hoặc không điển hình hoặc các loại thuốc khác để ngăn ngừa hoặc kiểm soát cơn sảng. (15,84-89) Trong trường hợp quyết định sử dụng chiến lược này, chúng tôi đề nghị sử dụng nó cho bệnh nhân kích động (RASS > 1) và ở liều thấp và ưu tiên các thuốc có thời gian bán hủy ngắn và nguy cơ tích lũy thấp hơn (Bảng 5). Việc sử dụng biện pháp kiềm chế vật lý chỉ nên được sử dụng trong những trường hợp ngoại lệ, lưu ý rằng nó không ngăn chặn được các tác dụng phụ, gây chấn thương cho bệnh nhân và làm trầm trọng thêm tình trạng sảng. Trong nghiên cứu MENDS (Tối đa hóa hiệu quả của thuốc an thần mục tiêu và giảm rối loạn chức năng thần kinh), việc sử dụng dexmedetomidine dẫn đến nhiều ngày không sảng hoặc hôn mê và thời gian an thần nhiều hơn so với việc sử dụng lorazepam ở bệnh nhân thở máy. (90) Những tác dụng này cũng đã được báo cáo khi so sánh thuốc này với propofol hoặc midazolam. như chúng tôi đã đề cập trước đây, chìa khóa nằm ở việc sử dụng các gói biện pháp có tổ chức (ABCDEF) chứ không phải trong việc sử dụng một loại thuốc duy nhất. (93)
Khả năng vận động sớm và sự tham gia của gia đình
Chúng tôi khuyến cáo, nếu có thể, duy trì ít nhất một vận động thụ động kể từ khi bắt đầu thở máy và áp dụng các quy trình cho phép bao gồm toàn bộ nhóm làm việc và gia đình người lớn có COVID-19 ARDS.
Sự tiếp xúc của nhân viên y tế và nguy cơ lây nhiễm thực hiện sử dụng hợp lý PPE (khẩu trang loại N95, áo choàng cách ly, găng tay, kính bảo vệ mắt và mặt nạ), vệ sinh tay đầy đủ và giảm thiểu tất cả các nguy cơ lây nhiễm tiềm ẩn, chẳng hạn như tự rút nội khí quản và sự kích động, trong số những người khác, là một ưu tiên. Một ví dụ là làn sóng nhiễm trùng đầu tiên ở vùng Lombardy của Ý, nơi có khoảng 9% ca nhiễm SARS-CoV-2 là ở nhân viên y tế. (94) Do đó, xung đột nảy sinh giữa những gì được đề xuất bởi gói ABCDEF và khái niệm về eCASH (bệnh nhân tỉnh táo và bình tĩnh đi cùng với gia đình của họ) và sự liên hợp do đại dịch gây ra với những bệnh nhân cần thở máy bảo vệ, an thần sâu trong nhiều trường hợp, và cách ly nghiêm ngặt cho cả gia đình và nhóm điều trị. (20,54) Như một kết quả của việc gia tăng nguy cơ lây nhiễm trong ICU và để bảo vệ sức khỏe của các nhóm làm việc và bệnh nhân, nhiều trung tâm đã giảm trước sự gia nhập của nhân viên y tế, chẳng hạn như bác sĩ vận động học, nhà trị liệu nghề nghiệp, nhà tâm lý học, nhân viên xã hội và gia đình. Khi các điều kiện về dịch tễ và ICU được cải thiện, chúng tôi tin rằng điều cần thiết là phải ưu tiên tổ chức lại toàn bộ nhóm chăm sóc sức khỏe thông qua các quy trình đơn giản và rõ ràng.
Bảng 5 Liều lượng, các tác dụng ngoại ý và tương tác của các loại thuốc được đề xuất cho chứng sảng
|
Thuốc |
Pha loãng Nồng độ ổn định /chất pha loãng tương thích |
Liều ban đầu và truyền duy trì |
Điều chỉnh liều lượng |
Các biện pháp phòng ngừa / tương tác với quản lý COVID-19 / các tác dụng phụ nghiêm trọng |
|
Quetiapine viên 25, 50, 100, 200mg |
NA |
Duy trì: 50mg mỗi 12 giờ (liều tối đa 200mg mỗi 12 giờ) |
LF: bắt đầu ở mức 25mg / ngày |
Các tác dụng phụ: kéo dài khoảng QT, tăng huyết áp, nhịp tim nhanh Tương tác: LPV / r: Tương tác tiềm năng. Có thể làm tăng nồng độ quetiapine |
|
Viên nén Olanzapine 2,5, 5, 10mg |
NA |
Duy trì: 5mg / ngày |
RF: không điều chỉnh LF: không điều chỉnh |
Tác dụng ngoại ý: hạ huyết áp thế đứng, phù ngoại vi, tăng cholesterol máu Tương tác: không thể xảy ra với LPV / r |
|
Viên nén Risperidone 0,5, 1, 2, 3, 4mg |
NA |
Duy trì: 0,5mg mỗi 12 giờ (liều tối đa 4mg / ngày) |
RF nặng: sử dụng liều tối thiểu LF nặng: sử dụng liều tối thiểu |
Các tác dụng phụ: kéo dài khoảng QT, rối loạn chức năng máu Tương tác: LPV / r: khả năng kéo dài khoảng QT; HCQ: tiềm năng tăng nồng độ risperidone |
|
Haloperidol ống 5mg / mL |
CS: 0,1mg / mL DX5% trong hộp thủy tinh Không được thử nghiệm trong các dung dịch pha loãng hoặc vật chứa khác |
Duy trì: 2,5mg mỗi 8 giờ (liều tối đa 20mg / ngày) |
Ở người lớn tuổi, sử dụng liều tối thiểu |
Các tác dụng phụ: kéo dài khoảng QT, hạ huyết áp, xoắn đỉnh Tương tác: không dùng với LPV / r hoặc HCQ |
|
Viên nén Haloperidol 1, 5 và 10mg |
NA |
Duy trì: 2,5 đến 5mg mỗi 8 giờ |
Ở người lớn tuổi, sử dụng liều tối thiểu |
Các tác dụng phụ: kéo dài khoảng QT, hạ huyết áp, xoắn đỉnh Tương tác: không dùng với LPV / r hoặc HCQ |
Đối với khả năng vận động sớm, điều quan trọng là phải duy trì ít nhất vận động thụ động ngay từ thời điểm đầu thở máy, đánh giá tính khả thi của tiến trình đó khi tình trạng lâm sàng của bệnh nhân cho phép. Việc vận động sớm của bệnh nhân được thở máy bởi một nhóm đa ngành đã được chứng minh là một thủ thuật khả thi, an toàn và đã được chứng minh là có tác động liên quan đến lâm sàng đối với các tình trạng trước đại dịch. (95-97) Trong một nghiên cứu gần đây, sự tham gia linh hoạt của gia đình như được đề xuất trong gói ABCDEF, khi so sánh với một phác đồ hạn chế hơn, không ảnh hưởng đến kết quả lâm sàng ở bệnh nhân và nhân viên nhưng đã làm giảm lo lắng và trầm cảm ở người thân của họ. (98) Bất chấp kết quả này, đại dịch và sự cô lập, trước kinh nghiệm của bệnh nhân và gia đình, chúng tôi tin rằng cần đưa bệnh nhân về gần gia đình hơn. Trước khi thực hiện các biện pháp này, đối với Argentina, chúng tôi khuyến cáo nên đọc luật về thông tin và cung cấp tư vấn pháp lý, để luôn bảo vệ quyền lợi của bệnh nhân và tuân thủ trách nhiệm chuyên môn của nhóm làm việc. (99)
Thảo luận
Việc quản lý ASD ở những bệnh nhân nguy kịch đã thay đổi sâu sắc trong 20 năm qua, từ những bệnh nhân chủ yếu được an thần sâu sang những bệnh nhân có mục tiêu an thần nhẹ hơn, kiểm soát cơn đau tốt hơn, khả năng vận động sớm và sự tham gia của gia đình như một phần của điều trị. Tuy nhiên, các tình huống bắt buộc của đại dịch liên quan đến những bệnh nhân không hợp tác, những người bị đa bệnh lý và cách ly với gia đình và nhân viên y tế của họ. Sự đồng thuận này tiến bộ các hướng dẫn về giảm đau ở bệnh nhân nguy kịch với COVID-19 ARDS do các chuyên gia thực hiện với bằng chứng tốt nhất hiện có ở các nước có thu nhập cao nhưng theo kinh nghiệm và quan điểm về tình hình của ICU ở nước ta và Mỹ Latinh. (22,43, 58, 71, 77, 83, 100)
Một hạn chế là kết quả của việc điều chỉnh các hướng dẫn quốc tế cho phù hợp với bối cảnh của chúng ta là mức độ ưu tiên trong các giai đoạn nhất định của các loại thuốc đã được loại bỏ trong các phác đồ điều trị. Biện pháp này chủ yếu được hình thành như một chiến lược để tiết kiệm các loại thuốc được lựa chọn, mà ở nước ta thường đắt tiền và thường phải nhập khẩu. Tuy nhiên, các loại thuốc được ưu tiên trong sự đồng thuận này có mặt trong các hướng dẫn thực hành lâm sàng quốc tế có liên quan và khi được sử dụng thích hợp, như được nêu chi tiết trong tài liệu này, có thể là đồng minh tuyệt vời để bảo vệ các loại thuốc được lựa chọn và vẫn tạo ra lợi ích lâm sàng ở bệnh nhân. (15,101)
Đối mặt với thực tế mới trong các ICU được tạo ra bởi đại dịch COVID-19 đang diễn ra, chúng ta không nên từ bỏ các “thực hành tốt” thông thường mà hãy điều chỉnh chúng. Cuộc khủng hoảng này nên được sử dụng như một cơ hội để thực hiện một cách tiếp cận có hệ thống dựa trên bằng chứng tốt nhất hiện có, ưu tiên các chiến lược có mục tiêu với việc kiểm soát cơn đau đầy đủ và giảm dần thuốc an thần và các tác dụng phụ của nó trong thời gian ngắn và trung hạn. Tương tự như vậy, nó sẽ cho phép chúng tôi điều chỉnh hệ thống trong trường hợp khan hiếm nguồn lực y tế do đại dịch. Hiệu suất của nhóm đa ngành trong và ngoài ICU và khả năng của họ trong việc xác định, đánh giá và điều chỉnh các giao thức dựa trên bằng chứng tốt nhất hiện có, ngay cả trước khi các cơ quan chức năng ở cấp khu vực hoặc quốc gia có thể kết hợp các thay đổi trong các giao thức chung, là những ví dụ về tính linh hoạt và cam kết về sự thay đổi đó.
Sự đồng thuận của chúng ta có mục tiêu cuối cùng là giải quyết những vấn đề mà đại dịch thường đặt ra trong khu vực của chúng ta; do đó, chúng tôi xem xét việc phân chia tiến triển của bệnh thành các giai đoạn khác nhau để lập kế hoạch xử trí ASD cho bệnh nhân thở máy là phù hợp. Bất kể loại thuốc được sử dụng là gì, chúng tôi tin rằng điều cần thiết là mỗi ICU phải thiết kế lịch trình quản lý an thần, giảm đau, sảng, khả năng vận động và sự tham gia của gia đình để đạt được cách tiếp cận nhất quán trong việc quản lý bệnh nhân và do đó cải thiện kết quả lâm sàng. (102)
References
World Health Organization (WHO) Coronavirus disease (COVID-19) pandemic. 2020. [2020 Nov 11]. Available from: https://www.who.int/emergencies/diseases/novel-coronavirus-2019.
World Health Organization (WHO) WHO Coronavirus Disease (COVID-19) Dashboard. 2020. [2020 Nov 11]. Available from: https://covid19.who.int/
Argentina. Ministerio de Salud Nuevo coronavirus COVID-19. Jul, 2020. [2020 Nov 11]. Informe diario. Available from: https://www.argentina.gob.ar/coronavirus/informe-diario/julio2020.
Falavigna M, Colpani V, Stein C, Azevedo LC, Bagattini AM, Brito GV, et al. Diretrizes para o tratamento farmacológico da COVID-19. Consenso da Associação de Medicina Intensiva Brasileira, da Sociedade Brasileira de Infectologia e da Sociedade Brasileira de Pneumologia e Tisiologia. Rev Bras Ter Intensiva. 2020;32(2):166–196. [PMC free article] [PubMed] [Google Scholar]
Centers for Disease Control and Prevention Interim Clinical Guidance for Management of Patients with Confirmed Coronavirus Disease (COVID-19) 2020. [2020 Nov 11]. Available from: https://www.cdc.gov/coronavirus/2019ncov/hcp/clinical-guidance-management-patients.html.
Siddiqi HK, Mehra MR. COVID-19 illness in native and immunosuppressed states: a clinical-therapeutic staging proposal. J Heart Lung Transplant. 2020;39(5):405–407. [PMC free article] [PubMed] [Google Scholar]
Mahase E. Covid-19: most patients require mechanical ventilation in first 24 hours of critical care. BMJ. 2020;368:m1201–m1201. [PubMed] [Google Scholar]
Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72?314 Cases From the Chinese Center for Disease Control and Prevention. JAMA. 2020;323(13):1239–1242. [PubMed] [Google Scholar]
Liu K, Fang YY, Deng Y, Liu W, Wang MF, Ma JP, et al. Clinical characteristics of novel coronavirus cases in tertiary hospitals in Hubei Province. Chin Med J (Engl) 2020;133(9):1025–1031. [PMC free article] [PubMed] [Google Scholar]
Young BE, Ong SW, Kalimuddin S, Low JG, Tan SY, Loh J, Ng OT, Marimuthu K, Ang LW, Mak TM, Lau SK, Anderson DE, Chan KS, Tan TY, Ng TY, Cui L, Said Z, Kurupatham L, Chen MI, Chan M, Vasoo S, Wang LF, Tan BH, Lin RTP, Lee VJ, Leo YS, Lye DC, Singapore 2019 Novel Coronavirus Outbreak Research Team Epidemiologic features and clinical course of patients infected with SARS-CoV-2 in Singapore. JAMA. 2020;323(15):1488–1494. [PMC free article] [PubMed] [Google Scholar]
Richardson S, Hirsch JS, Narasimhan M, Crawford JM, McGinn T, Davidson KW, et al. Presenting characteristics, comorbidities, and outcomes among 5700 patients hospitalized with COVID-19 in the New York City Area. JAMA. 2020;323(20):2052–2059. [PMC free article] [PubMed] [Google Scholar]
Argentina. Ministerio de Salud Nación invirtió 42 mil millones de pesos en la expansión del sistema de salud para responder a la pandemia de COVID-19. [2020 Nov 11]. Available from: https://www.argentina.gob.ar/noticias/nacioninvirtio-42-mil-millones-de-pesos-en-la-expansion-del-sistema-de-salud-para.
Ministerio de Salud de la Nación . Análisis de situación de salud: Republica Argentina. Ciudad Autónoma de Buenos Aires: Ministerio de Salud de la Nación; 2018. [2020 Nov 11]. Available from: https://bancos.salud.gob.ar/sites/default/files/2019-12/0000001392cnt-anlisis_de_situacin_de_salud__repblica_argentina_-_asis_2018_compressed.pdf. [Google Scholar]
Marra A, Ely EW, Pandharipande PP, Patel MB. The ABCDEF Bundle in Critical Care. Crit Care Clin. 2017;33(2):225–243. [PMC free article] [PubMed] [Google Scholar]
Devlin JW, Skrobik Y, Gélinas C, Needham DM, Slooter AJC, Pandharipande PP, et al. Clinical Practice Guidelines for the Prevention and Management of Pain, Agitation/Sedation, Delirium, Immobility, and Sleep Disruption in Adult Patients in the ICU. Crit Care Med. 2018;46(9):e825–e873. [PubMed] [Google Scholar]
Emanuel EJ, Persad G, Upshur R, Thome B, Parker M, Glickman A, et al. Fair allocation of scarce medical resources in the time of Covid-19. N Engl J Med. 2020;382(21):2049–2055. [PubMed] [Google Scholar]
Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054–1062. [PMC free article] [PubMed] [Google Scholar]
Wunsch H. Mechanical ventilation in COVID-19: interpreting the current epidemiology. Am J Respir Crit Care Med. 2020;202(1):1–4. [PMC free article] [PubMed] [Google Scholar]
Hernandez-Romieu AC, Adelman MW, Hockstein MA, Robichaux CJ, Edwards JA, Fazio JC, Blum JM, Jabaley CS, Caridi-Scheible M, Martin GS, Murphy DJ, Auld SC, Emory COVID-19 Quality and Clinical Research Collaborative Timing of intubation and mortality among critically ill coronavirus disease 2019 patients: a single-center cohort study. Crit Care Med. 2020;48(11):e1045–e1053. [PMC free article] [PubMed] [Google Scholar]
Argentina. Ministerio de Salud Recomendaciones para el uso de los EPP. 2020. [2020 Nov 11]. Available from: https://www.sati.org.ar/images/MSN_19-03_EPP_Recomendaciones_uso_.pdf.
Argentina. Ministerio de Salud Nuevo coronavirus COVID-19. Tratamiento de sostén. [2020 Nov 11]. Available from: https://www.argentina.gob.ar/salud/coronavirus-COVID-19/tratamiento-sosten.
Carini F, Cassabella C, Garcia Sarubio M. Analgosedación en el paciente crítico en ventilación mecánica: el bundle ABCDEF en la pandemia de COVID-19. Rev Argentina Ter Intensiva. 2020;(Supl 1):47–53. [Google Scholar]
Georgiou E, Paikousis L, Lambrinou E, Merkouris A, Papathanassoglou ED. The effectiveness of systematic pain assessment on critically ill patient outcomes: a randomised controlled trial. Aust Crit Care. 2020;33(5):412–419. [PubMed] [Google Scholar]
Payen JF, Bru O, Bosson JL, Lagrasta A, Novel E, Deschaux I, et al. Assessing pain in critically ill sedated patients by using a behavioral pain scale. Crit Care Med. 2001;29(12):2258–2263. [PubMed] [Google Scholar]
Gélinas C, Fillion L, Puntillo KA, Viens C, Fortier M. Validation of the critical-care pain observation tool in adult patients. Am J Crit Care. 2006;15(4):420–427. [PubMed] [Google Scholar]
Markman JD, Gewandter JS, Frazer ME. Comparison of a pain tolerability question with the numeric rating scale for assessment of self-reported chronic pain. JAMA Netw Open. 2020;3(4):e203155. [PMC free article] [PubMed] [Google Scholar]
Aitken LM, Bucknall T, Kent B, Mitchell M, Burmeister E, Keogh SJ, Cochrane Emergency and Critical Care Group Protocol-directed sedation versus non-protocol-directed sedation in mechanically ventilated intensive care adults and children. Cochrane Database Syst Rev. 2018;(11):CD009771–CD009771. [PMC free article] [PubMed] [Google Scholar]
Shehabi Y, Al-Bassam W, Pakavakis A, Murfin B, Howe B. Optimal sedation and pain management: a patient- and symptom-oriented paradigm. Semin Respir Crit Care Med. 2020 Sep 21; [PubMed] [Google Scholar]
Sessler CN, Gosnell MS, Grap MJ, Brophy GM, O’Neal PV, Keane KA, et al. The Richmond Agitation-Sedation Scale: validity and reliability in adult intensive care unit patients. Am J Respir Crit Care Med. 2002;166(10):1338–1344. [PubMed] [Google Scholar]
Ely EW, Truman B, Shintani A, Thomason JW, Wheeler AP, Gordon S, et al. Monitoring sedation status over time in ICU patients: reliability and validity of the Richmond Agitation-Sedation Scale (RASS) JAMA. 2003;289(22):2983– 2991. [PubMed] [Google Scholar]
International Consortium for EEG Training of Anesthesia Practitioners (ICE-TAP) 2020. [2020 Jul 10]. Available from: https://icetap.org/
Riker RR, Picard JT, Fraser GL. Prospective evaluation of the Sedation-Agitation Scale for adult critically ill patients. Crit Care Med. 1999;27(7):1325–1329. [PubMed] [Google Scholar]
Bouju P, Tadié JM, Barbarot N, Letheulle J, Uhel F, Fillatre P, et al. Clinical assessment and train-of-four measurements in critically ill patients treated with recommended doses of cisatracurium or atracurium for neuromuscular blockade: a prospective descriptive study. Ann Intensive Care. 2017;7(1):10–10. [PMC free article] [PubMed] [Google Scholar]
Baumann MH, McAlpin BW, Brown K, Patel P, Ahmad I, Stewart R, et al. A prospective randomized comparison of train-of-four monitoring and clinical assessment during continuous ICU cisatracurium paralysis. Chest. 2004;126(4):1267–1273. [PubMed] [Google Scholar]
Jacobi J, Fraser GL, Coursin DB, Riker RR, Fontaine D, Wittbrodt ET, Chalfin DB, Masica MF, Bjerke HS, Coplin WM, Crippen DW, Fuchs BD, Kelleher RM, Marik PE, Nasraway SA Jr, Murray MJ, Peruzzi WT, Lumb PD, Task Force of the American College of Critical Care Medicine of the Society of Critical Care Medicine.American Society of HealthSystem Pharmacists.American College of Chest Physicians Clinical practice guidelines for the sustained use of sedatives and analgesics in the critically ill adult. Crit Care Med. 2002;30(1):119–141. [PubMed] [Google Scholar]
Haenggi M, Blum S, Brechbuehl R, Brunello A, Jakob SM, Takala J. Effect of sedation level on the prevalence of delirium when assessed with CAM-ICU and ICDSC. Intensive Care Med. 2013;39(12):2171–2179. [PubMed] [Google Scholar]
Ely EW, Inouye SK, Bernard GR, Gordon S, Francis J, May L, et al. Delirium in mechanically ventilated patients: validity and reliability of the Confusion Assessment Method for the intensive care unit (CAM-ICU) JAMA. 2001;286(21):2703–2710. [PubMed] [Google Scholar]
Critical Illness. Brain Dysfunction, and Survivorship (CIBS) Center Confusion Assessment Method for the Intensive Care Unit (CAM-ICU) 2020. [2020 Nov 11]. Available from: https://www.icudelirium.org/medicalprofessionals/downloads/resources-by-category.
Bergeron N, Dubois MJ, Dumont M, Dial S, Skrobik Y. Intensive Care Delirium Screening Checklist: evaluation of a new screening tool. Intensive Care Med. 2001;27(5):859–864. [PubMed] [Google Scholar]
Hutchison LC, O’Brien CE Changes in pharmacokinetics and pharmacodynamics in the elderly patient. J Pharm Pract. 2007;20(1):4–12. [Google Scholar]
Montmeat D, Gard C, Raux M, Constantin JM, Tilleul P. Shortage of sedatives and neuromuscular blockers during COVID-19 pandemic: the result of an overstocking procedure in French hospitals? Anaesth Crit Care Pain Med. 2020;39(5):585–586. [PMC free article] [PubMed] [Google Scholar]
Barr J, Fraser GL, Puntillo K, Ely EW, Gélinas C, Dasta JF, Davidson JE, Devlin JW, Kress JP, Joffe AM, Coursin DB, Herr DL, Tung A, Robinson BR, Fontaine DK, Ramsay MA, Riker RR, Sessler CN, Pun B, Skrobik Y, Jaeschke R, American College of Critical Care Medicine Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Crit Care Med. 2013;41(1):263–306. [PubMed] [Google Scholar]
Ammar MA, Sacha GL, Welch SC, Bass SN, Kane-Gill SL, Duggal A, et al. Sedation, analgesia, and paralysis in COVID-19 patients in the setting of drug shortages. J Intensive Care Med. 2021;36(2):157–174. [PubMed] [Google Scholar]
University of Liverpool. COVID-19 Drug Interactions. 2020. [2020 Jul 10]. Available from: https://www.covid19druginteractions.org/checker.
IBM Mcromedex. [2020 Nov 11]. Available from: www.micromedexsolutions.com.
Devlin JW, Roberts RJ. Pharmacology of commonly used analgesics and sedatives in the ICU: benzodiazepines, propofol, and opioids. Crit Care Clin. 2009;25(3):431-49, vii. [PubMed] [Google Scholar]
Muellejans B, López A, Cross MH, Bonome C, Morrison L, Kirkham AJT. Remifentanil versus fentanyl for analgesia based sedation to provide patient comfort in the intensive care unit: a randomized, double-blind controlled trial [ISRCTN43755713] Crit Care. 2004;8(1):R1–11. [PMC free article] [PubMed] [Google Scholar]
Yu EHY, Tran DH, Lam SW, Irwin MG. Remifentanil tolerance and hyperalgesia: short-term gain, long-term pain? Anaesthesia. 2016;71(11):1347–1362. [PubMed] [Google Scholar]
Wheeler KE, Grilli R, Centofanti JE, Martin J, Gelinas C, Szumita PM, et al. Adjuvant analgesic use in the critically ill: a systematic review and meta-analysis. Crit Care Explor. 2020;2(7):e0157. [PMC free article] [PubMed] [Google Scholar]
Wanzuita R, Poli-de-Figueiredo LF, Pfuetzenreiter F, Cavalcanti AB, Westphal GA. Replacement of fentanyl infusion by enteral methadone decreases the weaning time from mechanical ventilation: a randomized controlled trial. Crit Care. 2012;16(2):R49–R49. [PMC free article] [PubMed] [Google Scholar]
Bhatraju PK, Ghassemieh BJ, Nichols M, Kim R, Jerome KR, Nalla AK, et al. Covid-19 in critically ill patients in the Seattle Region – Case series. N Engl J Med. 2020;382(21):2012–2022. [PMC free article] [PubMed] [Google Scholar]
Gandhi RT. Large COVID-19 case series from the New York City Area. NEJM J Watch; Apr 29, 2020. [CrossRef] [Google Scholar]
Guan WJ, Ni ZY, Hu Y, Liang WH, Ou CQ, He JX, Liu L, Shan H, Lei CL, Hui DSC, Du B, Li LJ, Zeng G, Yuen KY, Chen RC, Tang CL, Wang T, Chen PY, Xiang J, Li SY, Wang JL, Liang ZJ, Peng YX, Wei L, Liu Y, Hu YH, Peng P, Wang JM, Liu JY, Chen Z, Li G, Zheng ZJ, Qiu SQ, Luo J, Ye CJ, Zhu SY, Zhong NS, China Medical Treatment Expert Group for Covid-19 Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med. 2020;382(18):1708–1720. [PMC free article] [PubMed] [Google Scholar]
Vincent JL, Shehabi Y, Walsh TS, Pandharipande PP, Ball JA, Spronk P, et al. Comfort and patient-centred care without excessive sedation: the eCASH concept. Intensive Care Med. 2016;42(6):962–971. [PMC free article] [PubMed] [Google Scholar]
Shehabi Y, Chan L, Kadiman S, Alias A, Ismail WN, Tan MA, Khoo TM, Ali SB, Saman MA, Shaltut A, Tan CC, Yong CY, Bailey M, Sedation Practice in Intensive Care Evaluation Study Group investigators Sedation depth and longterm mortality in mechanically ventilated critically ill adults: a prospective longitudinal multicentre cohort study. Intensive Care Med. 2013;39(5):910–918. [PMC free article] [PubMed] [Google Scholar]
Kress JP, Pohlman AS, O’Connor MF, Hall JB. Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. N Engl J Med. 2000;342(20):1471–1477. [PubMed] [Google Scholar]
Garber PM, Droege CA, Carter KE, Harger NJ, Mueller EW. Continuous infusion ketamine for adjunctive analgosedation in mechanically ventilated, critically ill patients. Pharmacotherapy. 2019;39(3):288–296. [PubMed] [Google Scholar]
Grupo de Trabajo de Sedación, Analgésia y Delirium de Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronrias (SEMICYUC) Protocolos de analgosedación en pacientes con infección por SARS-CoV-2 (COVID-19) en caso de desabastecimiento. 2020. [2020 Nov 11]. Available from: https://semicyuc.org/wpcontent/uploads/2020/03/PROTOCOLO-ANALGOSED-COVID-SEMICYUC.pdf.
Manasco AT, Stephens RJ, Yaeger LH, Roberts BW, Fuller BM. Ketamine sedation in mechanically ventilated patients: a systematic review and meta-analysis. J Crit Care. 2020;56:80–88. [PubMed] [Google Scholar]
Zhou Y, Jin X, Kang Y, Liang G, Liu T, Deng N. Midazolam and propofol used alone or sequentially for long-term sedation in critically ill, mechanically ventilated patients: a prospective, randomized study. Crit Care. 2014;18(3):R122– R122. [PMC free article] [PubMed] [Google Scholar]
Wang H, Wang C, Wang Y, Tong H, Feng Y, Li M, et al. Sedative drugs used for mechanically ventilated patients in intensive care units: a systematic review and network meta-analysis. Curr Med Res Opin. 2019;35(3):435–446. [PubMed] [Google Scholar]
Le Guen M, Liu N, Tounou F, Augé M, Tuil O, Chazot T, et al. Dexmedetomidine reduces propofol and remifentanil requirements during bispectral index-guided closed-loop anesthesia: a double-blind, placebo-controlled trial. Anesth Analg. 2014;118(5):946–955. [PubMed] [Google Scholar]
Xia ZQ, Chen SQ, Yao X, Xie CB, Wen SH, Liu KX. Clinical benefits of dexmedetomidine versus propofol in adult intensive care unit patients: a meta-analysis of randomized clinical trials. J Surg Res. 2013;185(2):833–843. [PubMed] [Google Scholar]
Conti G, Ranieri VM, Costa R, Garratt C, Wighton A, Spinazzola G, et al. Effects of dexmedetomidine and propofol on patient-ventilator interaction in difficult-to-wean, mechanically ventilated patients: a prospective, open-label, randomised, multicentre study. Crit Care. 2016;20(1):206–206. [PMC free article] [PubMed] [Google Scholar]
Cruickshank M, Henderson L, MacLennan G, Fraser C, Campbell M, Blackwood B, et al. Alpha-2 agonists for sedation of mechanically ventilated adults in intensive care units: a systematic review. Health Technol Assess. 2016;20(25):v–xx. [PMC free article] [PubMed] [Google Scholar]
Terry K, Blum R, Szumita P. Evaluating the transition from dexmedetomidine to clonidine for agitation management in the intensive care unit. SAGE Open Med. 2015;3:2050312115621767–2050312115621767. [PMC free article] [PubMed] [Google Scholar]
Gagnon DJ, Riker RR, Glisic EK, Kelner A, Perrey HM, Fraser GL. Transition from dexmedetomidine to enteral clonidine for ICU sedation: an observational pilot study. Pharmacotherapy. 2015;35(3):251–259. [PubMed] [Google Scholar]
Wang JG, Belley-Coté E, Burry L, Duffett M, Karachi T, Perri D, et al. Clonidine for sedation in the critically ill: a systematic review and meta-analysis. Crit Care. 2017;21(1):75–75. [PMC free article] [PubMed] [Google Scholar]
Mion G. Ketamine infusions for sedation in ICU. Anaesth Crit Care Pain Med. 2019;38(4):397–398. [PubMed] [Google Scholar]
Groetzinger LM, Rivosecchi RM, Bain W, Bahr M, Chin K, McVerry BJ, et al. Ketamine infusion for adjunct sedation in mechanically ventilated adults. Pharmacotherapy. 2018;38(2):181–188. [PubMed] [Google Scholar]
Devlin JW, O’Neal HR Jr, Thomas C., Barnes Daly MA., Stollings JL., Janz DR, et al. Strategies to Optimize ICU Liberation (A to F) Bundle Performance in Critically Ill Adults With Coronavirus Disease 2019. Crit Care Explor. 2020;2(6):e0139. [PMC free article] [PubMed] [Google Scholar]
Katoh N, Ohya Y, Ikeda M, Ebihara T, Katayama I, Saeki H, et al. Clinical practice guidelines for the management of atopic dermatitis 2018. J Dermatol. 2019;46(12):1053–1101. [PubMed] [Google Scholar]
Greenberg SB, Vender J. The use of neuromuscular blocking agents in the ICU: where are we now? Crit Care Med. 2013;41(5):1332–1344. [PubMed] [Google Scholar]
Papazian L, Forel JM, Gacouin A, Penot-Ragon C, Perrin G, Loundou A, Jaber S, Arnal JM, Perez D, Seghboyan JM, Constantin JM, Courant P, Lefrant JY, Guérin C, Prat G, Morange S, Roch A, ACURASYS Study Investigators Neuromuscular blockers in early acute respiratory distress syndrome. N Engl J Med. 2010;363(12):1107–1116. [PubMed] [Google Scholar]
National Heart, Lung, and Blood Institute PETAL Clinical Trials Network. Moss M, Huang DT, Brower RG, Ferguson ND, Ginde AA, Gong MN, et al. Early neuromuscular blockade in the acute respiratory distress syndrome. N Engl J Med. 2019;380(21):1997–2008. [PMC free article] [PubMed] [Google Scholar]
deBacker J, Hart N, Fan E. Neuromuscular Blockade in the 21st Century Management of the Critically Ill Patient. Chest. 2017;151(3):697–706. [PubMed] [Google Scholar]
Alhazzani W, Møller MH, Arabi YM, Loeb M, Gong MN, Fan E, et al. Surviving Sepsis Campaign: Guidelines on the management of critically ill adults with coronavirus disease 2019 (COVID-19) Intensive Care Med. 2020;46(5):854–887. [PMC free article] [PubMed] [Google Scholar]
Moore L, Kramer CJ, Delcoix-Lopes S, Modrykamien AM. Comparison of cisatracurium versus atracurium in early ARDS. Respir Care. 2017;62(7):947–952. [PubMed] [Google Scholar]
Aung Thein MZ, Pereira J V, Nitchingham A, Caplan GA. A call to action for delirium research: meta-analysis and regression of delirium associated mortality. BMC Geriatr. 2020;20(1):325–325. [PMC free article] [PubMed] [Google Scholar]
Garcez FB, Aliberti MJ, Poco PC, Hiratsuka M, Takahashi SF, Coelho VA, et al. Delirium and adverse outcomes in hospitalized patients with COVID-19. J Am Geriatr Soc. 2020;68(11):2440–2446. [PMC free article] [PubMed] [Google Scholar]
Khan SH, Lindroth H, Perkins AJ, Yasser J, Wang S, Roberts S, et al. Delirium Incidence, Duration and Severity in Critically Ill Patients with COVID-19. Crit Care Explor. 2020;2(12):e0290. [PMC free article] [PubMed] [Google Scholar]
Docherty AB, Harrison EM, Green CA, Hardwick HE, Pius R, Norman L, Holden KA, Read JM, Dondelinger F, Carson G, Merson L, Lee J, Plotkin D, Sigfrid L, Halpin S, Jackson C, Gamble C, Horby PW, Nguyen-Van-Tam JS, Ho A, Russell CD, Dunning J, Openshaw PJ, Baillie JK, Semple MG, ISARIC4C investigators Features of 20 133 UK patients in hospital with covid-19 using the ISARIC WHO Clinical Characterisation Protocol: prospective observational cohort study. BMJ. 2020;369:m1985–m1985. [PMC free article] [PubMed] [Google Scholar]
Kotfis K, Williams Roberson S, Wilson JE, Dabrowski W, Pun BT, Ely EW. COVID-19: ICU delirium management during SARS-CoV-2 pandemic. Crit Care. 2020;24(1):176–176. [PMC free article] [PubMed] [Google Scholar]
Santos E, Cardoso D, Neves H, Cunha M, Rodrigues M, Apóstolo J. Effectiveness of haloperidol prophylaxis in critically ill patients with a high risk of delirium: a systematic review. JBI Database Syst Rev Implement Rep. 2017;15(5):1440–1472. [PubMed] [Google Scholar]
Schrijver EJ, de Graaf K, de Vries OJ, Maier AB, Nanayakkara PW. Efficacy and safety of haloperidol for in-hospital delirium prevention and treatment: a systematic review of current evidence. Eur J Intern Med. 2016;27:14–23. [PubMed] [Google Scholar]
Girard TD, Exline MC, Carson SS, Hough CL, Rock P, Gong MN, Douglas IS, Malhotra A, Owens RL, Feinstein DJ, Khan B, Pisani MA, Hyzy RC, Schmidt GA, Schweickert WD, Hite RD, Bowton DL, Masica AL, Thompson JL, Chandrasekhar R, Pun BT, Strength C, Boehm LM, Jackson JC, Pandharipande PP, Brummel NE, Hughes CG, Patel MB, Stollings JL, Bernard GR, Dittus RS, Ely EW, MIND-USA Investigators Haloperidol and ziprasidone for treatment of delirium in critical illness. N Engl J Med. 2018;379(26):2506–2516. [PMC free article] [PubMed] [Google Scholar]
Choi M, Barra ME, Newman K, Sin JH. Safety and effectiveness of intravenous chlorpromazine for agitation in critically ill patients. J Intensive Care Med. 2018;35(10):1118–1122. [PubMed] [Google Scholar]
Herling SF, Greve IE, Vasilevskis EE, Egerod I, Bekker Mortensen C, Moller AM, et al. Interventions for preventing intensive care unit delirium in adults. Cochrane Database Syst Rev. 2018;11(11):CD009783–CD009783. [PMC free article] [PubMed] [Google Scholar]
Burry L, Hutton B, Williamson DR, Mehta S, Adhikari NK, Cheng W, et al. Pharmacological interventions for the treatment of delirium in critically ill adults. Cochrane Database Syst Rev. 2019;9(9):CD011749–CD011749. [PMC free article] [PubMed] [Google Scholar]
Pandharipande PP, Sanders RD, Girard TD, McGrane S, Thompson JL, Shintani AK, Herr DL, Maze M, Ely EW, MENDS investigators Effect of dexmedetomidine versus lorazepam on outcome in patients with sepsis: an a prioridesigned analysis of the MENDS randomized controlled trial. Crit Care. 2010;14(2):R38–R38. [PMC free article] [PubMed] [Google Scholar]
Jakob SM, Ruokonen E, Grounds RM, Sarapohja T, Garratt C, Pocock SJ, Bratty JR, Takala J, Dexmedetomidine for Long-Term Sedation Investigators Dexmedetomidine vs midazolam or propofol for sedation during prolonged mechanical ventilation: two randomized controlled trials. JAMA. 2012;307(11):1151–1160. [PubMed] [Google Scholar]
Reade MC, O’Sullivan K, Bates S, Goldsmith D, Ainslie WR, Bellomo R. Dexmedetomidine vs. haloperidol in delirious, agitated, intubated patients: a randomised open-label trial. Crit Care. 2009;13(3):R75–R75. [PMC free article] [PubMed] [Google Scholar]
Pun BT, Balas MC, Barnes-Daly MA, Thompson JL, Aldrich JM, Barr J, et al. Caring for Critically Ill Patients with the ABCDEF Bundle: Results of the ICU Liberation Collaborative in Over 15,000 Adults. Crit Care Med. 2019;47(1):3– 14. [PMC free article] [PubMed] [Google Scholar]
HealthManagement.org COVID-19 Pandemic: Lessons from Italy. 2020. [2020 Jul 10]. Available from: https://healthmanagement.org/c/icu/news/covid-19-pandemic-lessons-from-italy.
Hodgson CL, Stiller K, Needham DM, Tipping CJ, Harrold M, Baldwin CE, et al. Expert consensus and recommendations on safety criteria for active mobilization of mechanically ventilated critically ill adults. Crit Care Med. 2014;18(6):658–658. [PMC free article] [PubMed] [Google Scholar]
Schweickert WD, Pohlman MC, Pohlman AS, Nigos C, Pawlik AJ, Esbrook CL, et al. Early physical and occupational therapy in mechanically ventilated, critically ill patients: a randomised controlled trial. Lancet. 2009;373(9678):1874–1882. [PubMed] [Google Scholar]
Ely EW. The ABCDEF bundle: science and philosophy of how ICU liberation serves patients and families. Crit Care Med. 2017;45(2):321–330. [PMC free article] [PubMed] [Google Scholar]
Rosa RG, Falavigna M, da Silva DB, Sganzerla D, Santos MMS, Kochhann R, de Moura RM, Eugênio CS, Haack TDSR, Barbosa MG, Robinson CC, Schneider D, de Oliveira DM, Jeffman RW, Cavalcanti AB, Machado FR, Azevedo LCP, Salluh JIF, Pellegrini JAS, Moraes RB, Foernges RB, Torelly AP, Ayres LO, Duarte PAD, Lovato WJ, Sampaio PHS, de Oliveira Júnior LC, Paranhos JLDR, Dantas ADS, de Brito PIPGG, Paulo EAP, Gallindo MAC, Pilau J, Valentim HM, Meira Teles JM, Nobre V, Birriel DC, Corrêa E, Castro L, Specht AM, Medeiros GS, Tonietto TF, Mesquita EC, da Silva NB, Korte JE, Hammes LS, Giannini A, Bozza FA, Teixeira CICU, Visits Study Group Investigators. Brazilian Research in Intensive Care Network Effect of flexible family visitation on delirium among patients in the intensive care unit: the ICU visits randomized clinical trial. JAMA. 2019;322(3):216–228. [PMC free article] [PubMed] [Google Scholar]
Argentina. Senado y Cámara de Diputados de la Nación Argentina Ley 27.553. Boletin Oficial de la República Argentina. 11/08/2020. [2020 Nov 11]. Available from: https://www.boletinoficial.gob.ar/detalleAviso/primera/233439/20200811.
Ballesteros Sanz MA, Hernández-Tejedor A, Estella A, Jiménes Rivera JJ, Gonzáles de Molina Ortiz FJ, Sandiumenge Camps A, et al. Recomendaciones de “hacer” y “no hacer” en el tratamiento de los pacientes críticos ante la pandemia por coronavirus causante de COVID-19 de los Grupos de Trabajo de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC) Med Intensiva. 2020;44(6):371–388. [PMC free article] [PubMed] [Google Scholar]
Celis-Rodríguez E, Birchenall C, de la Cal MA, Castorena Arellano G, Hernández A, Ceraso D, et al. Guía de práctica clínica basada en la evidencia para el manejo de la sedoanalgesia en el paciente adulto críticamente enfermo. Med Intensiva. 2013;37(8):519–574. [PubMed] [Google Scholar]
Davidson JE, Harvey MA, Bemis-Dougherty A, Smith JM, Hopkins RO. Implementation of the Pain, Agitation, and Delirium Clinical Practice Guidelines and promoting patient mobility to prevent post-intensive care syndrome. Crit Care Med. 2013;41(9) Suppl 1:S136–S145. [PubMed] [Google Scholar]