Dịch: BS. Trần Quang Dư , BS. Lê Nguyễn Minh Luân
Blalock–taussig shunt (bt shunt)
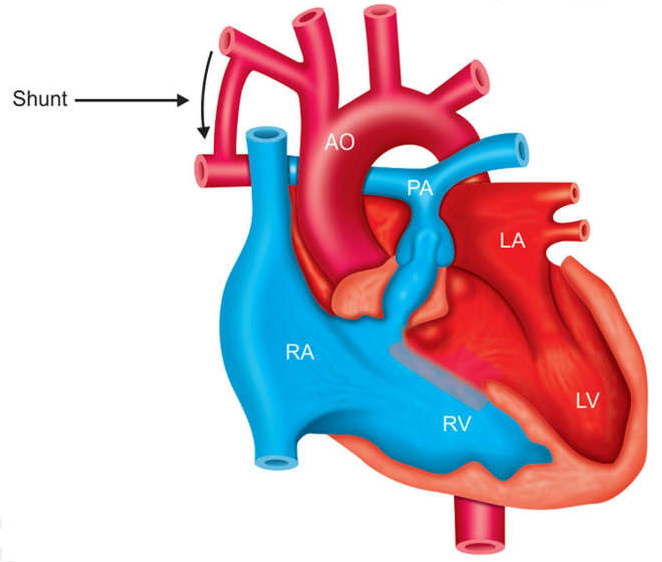
Là shunt từ hệ thống sang phổi, được tạo ra để đảm bảo dòng máu lên phổi ở những bệnh nhân có tắc nghẽn dòng máu lên phổi. Shunt này có thể được xem như là “ống động mạch nhân tạo” và điển hình ở trẻ sơ sinh (không van ĐMP, tứ chứng Fallot nặng) cần được hỗ trợ trước phẫu thuật bằng cách duy trì sự tồn tại của ống động mạch với truyền prostaglandin E1 hoặc E2. Shunt cũng có thể ở những trẻ nhũ nhi và trẻ lớn chưa thích hợp để sữa chữa tim hoàn toàn hay triệt để.
Hình 23-1: Blalock-Taussig (BT) shunt
Tiền phẫu- tiếp cận mạch máu
Tránh đặt catheter TMTT ở tĩnh mạch chủ trên (SVC), bên ĐM phổi dự định sẽ đặt shunt vì có thể tạo hematom sẽ gây khó khăn cho phẫu thuật.
Tránh đặt catheter động mạch bên tay tạo shunt vì sẽ không theo dõi được HA cả trong và sau phẫu thuật.
Thay đổi sinh lý:
Máu từ động mạch chủ được lấy 1 phần sang động mạch phổi.
Tăng lượng máu lên phổi cùng bên.
Lưu lượng máu qua động mạch phổi tùy thuộc vào kích thước của ống ghép mạch máu (kích thước ống tạo shunt).
Xử trí sau mổ:
Duy trì cung lượng tim thích hợp với inotropes như Dopamin.
Nhu cầu dịch: 80-100 ml/kg/ngày
Bắt đầu Heparin: 5–10 ui/kg/h.
Aspirin: 5 mg/kg/ngày.
Giữ mức FiO2 thấp – khí trời (0,25%).
Trẻ nhỏ cần được thở máy trong 24 giờ đầu vì thường có xu hướng giảm cung lượng tim và phù phổi cùng bên với shunt.
Giữ cân bằng tuần hoàn hệ thống và tuần hoàn phổi.
Chăm sóc đường thở: Hút đàm qua NKQ, áp lực hút thấp, VLTL hô hấp.
Độ bão hòa oxy thấp
Nếu độ bão hòa oxy thấp (
Thông báo cho phẫu thuật viên, siêu âm tim khẩn cấp đánh giá dòng máu qua shunt.
Truyền Heparin 10- 20 UI/kg/h khi shunt có nguy cơ bị tắc nghẽn.
Có thể sử dụng Noradrenalin để tăng huyết áp hệ thống tạm thời.
Nếu hematorite của bệnh nhân tăng quá cao cần trích máu.
Độ bão hòa oxy cao
Xảy ra nếu dòng máu qua shunt lên phổi quá nhiều do truyền dư dịch và tuần hoàn không được cân bằng.
Nghi ngờ shunt quá mức nếu:
Độ bão hòa oxy cao hơn 85% với mức FiO2 thấp.
Phù phổi (có thể 1 bên).
Suy tim.
HA tâm trương thấp do máu “run off’ qua phổi.
Tình trạng toan chuyển hóa kéo dài ở bệnh nhân “hồng” (Giảm máu hệ thống).
Xử trí “over shunting”
Cần hạn chế dịch ± lợi tiểu và inotropes (hỗ trợ tải thể tích của thất)
Trong vài trường hợp, chấp nhận pH (toan hô hấp cho phép) và Fi02 thấp làm tăng kháng lực mạch máu phổi và làm giảm lượng máu qua shunt lên phổi.
Siêu âm tim hoặc thông tim để xác định dòng máu qua shunt và xác định các nguồn máu khác lên phổi như PDA, tuần hoàn bàng hệ chủ phổi (MAPCAs).
Phẫu thuật cấp cứu sửa lại shunt đôi khi được đặt ra đối với shunt có kích thước quá lớn (chèn shunt có đường kính nhỏ hơn). Và bắt buộc phải làm lại khi HA tâm trương quá thấp và toan kéo dài mặc dù đã điều trị với các biện pháp để nâng kháng lực mạch máu phổi lên.
Seroma (tụ dịch)
Shunt Gortex có thể “ướt” (ngấm nước), do tụ dịch, được phát hiện bằng siêu âm hoặc X quang.
Bidirectional glenn shunt (bdg)
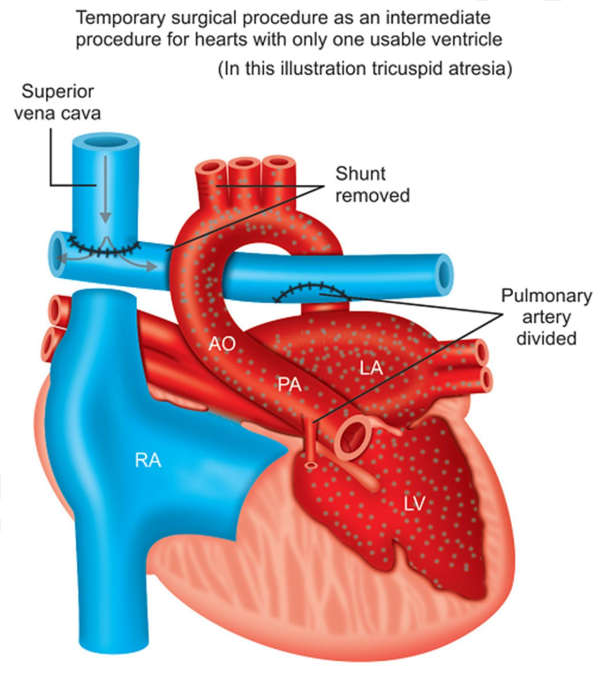
Shunt được tạo ra giữa tĩnh mạch chủ trên và động mạch phổi.
Chỉ định trong những trường hợp sinh lý tim một thất có hẹp động nạch phổi.
Kiểm soát gây mê
Hình 23-2: Bidirectional Glenn shunt
Đặt đường line ở tĩnh mạch cảnh ngắn.
Động mạch bẹn yêu cầu phải đo được áp lực nhĩ phải và nhĩ trái.
Kiểm soát hậu phẫu thuật
Giữ đầu cao, giúp tăng dòng máu lên phổi.
Cài thông số máy thở với áp lực đường thở trung bình thấp và PEEP thấp.
Cai máy thở sớm.
Tăng máu từ tĩnh mạch về.
Áp lực âm khoang màng phổi – áp lực động mạch phổi thấp – cải thiện dòng máu qua shunt tới động mạch phổi.
Tránh để PCO2 cao và PO2 thấp vì làm co mạch máu phổi.
Heparin 5 – 10 U/kg/h bắt đầu sau phẫu thuật 4 giờ.
Aspirin 5 mg/kg/ngày được bắt đầu vào ngày kế tiếp – sau 2 liều aspirin ngưng truyền heparin.
Rút catheter tĩnh mạch cảnh sớm.
Nếu bệnh nhân bị phù mặt, sung huyết hoặc kích thích nhiều phải siêu âm kiểm lại flow qua shunt.
Các trường hợp tim một thất khi tiêm truyền phải thật cẩn thận tránh làm tắc mạch do khí.
Bdg nguy cơ cao
Những bệnh nhân cao áp phổi (trung bình > 18).
Kích thước động mạch phổi giới hạn.
Những bệnh nhân có CVP cao, được kiểm soát bằng các thuốc giãn mạch máu phổi như truyền Milrinone hoặc uống Sildenafil.
Tăng thông khí ngắt quãng với nồng độ oxy 100% có thể cải thiện dòng máu qua shunt.
Pulmonary artery banding
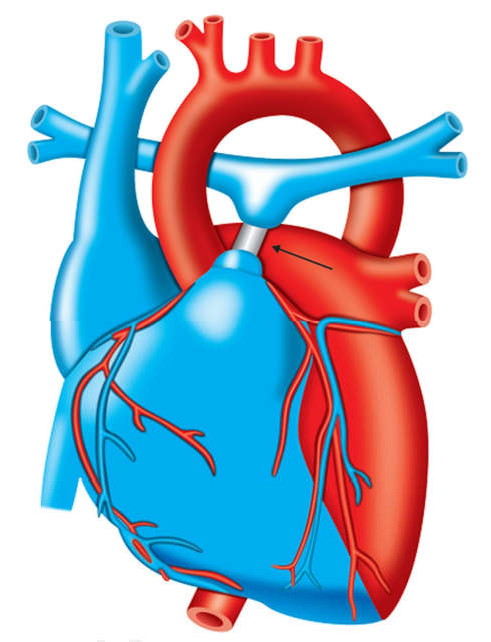
Làm hẹp động mạch phổi để giảm dòng máu lên động mạch phổi trong các tổn thương gây ra suy tim sung huyết do dòng máu lên động mạch phổi quá mức.
Chỉ định của PA band:
Tim một thất có tăng dòng máu lên phổi.
VSD có nhiều lỗ dạng phô mai.
D-TGA với vách liên thất còn nguyên vẹn sau 3 tuần với BT shunt training thất trái.
Thay đổi sinh lý sau phẫu thuật
Giảm máu lên ĐM phổi – độ bão hòa oxy thấp
Máu chuyển từ các ĐM phổi sang ĐM chủ làm tăng HA hệ thống.
Làm tăng hậu tải thất phải.
Đôi khi làm hở van nhĩ thất đã có trước đó trở nên nhiều hơn.
Trong suốt thời gian phẫu thuật, hỗ trợ thông khí với Fi02 như khí trời và thể tích lưu thông Vt thấp.
Thu nhỏ khẩu kính của ĐMP còn 75 – 80% thường không gây rố loạn nhịp nhanh và huyết áp tốt.
Xử trí hậu phẫu
Hình 23-3: Pulmonary artery band
Bệnh nhân cần được thông khí nhân tạo trong 24 giờ đầu vì thường sẽ có giảm cung lượng tim xảy ra.
Inotropes cần được sử dụng để hỗ trợ cho thất.
Chăm sóc hô hấp cẩn thận rất quan trọng cho nhóm bệnh nhân tiếp tục theo dõi nhịp tim và SpO2 là bắt buộc khi bệnh nhân đột ngột chậm nhịp tim và giảm SpO2.
Thêm Captoril có thể hỗ trợ thất nếu HA tốt vào ngày 2-3 của hậu phẫu.
Nếu SpO2 cao, nghi ngờ tình trạng band không chặt – kiểm tra siêu âm và làm siết band lại.
Điều trị lợi tiểu tích cực là cần thiết.
Fontan procedure
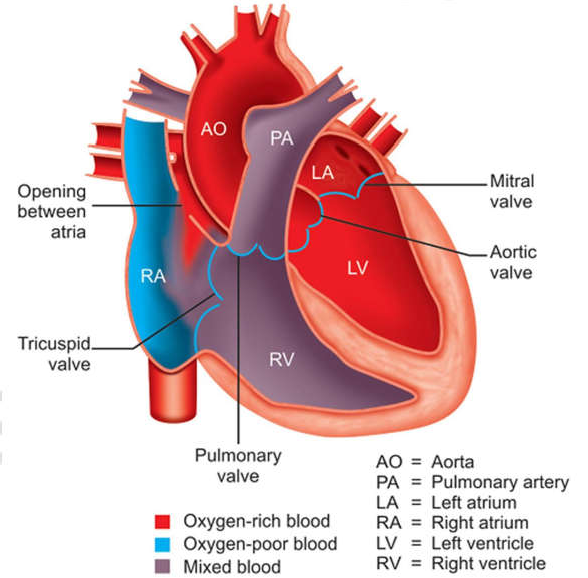
Hình 23-4: Extracardiac Fontan
Là phẫu thuật nối tĩnh mạch hệ thống vào động mạch phổi.
Bao gồm Fontan ngoài tim nối trực tiếp bằng ống dẫn PTFE hoặc Fontan đi xuyên qua nhĩ phải (đường hầm Fontan bên) (Lateral tunnel Fontan).
Máu lên động mạch phổi phụ thuộc vào độ chênh áp giữa áp lực tĩnh mạch hệ thống và áp lực động mạch phổi.
Trong trường hợp cao áp phổi hoặc áp lực nhĩ trái cao sẽ dẫn đến tràn dịch màng phổi.
Tạo cửa sổ làm giảm áp lực tĩnh mạch hệ thống, cải thiện được cung lượng tim nhưng làm giảm SpO2.
Xử trí hậu phẫu
Nằm đầu cao và nâng chân cao.
Thông khí nhân tạo giống như trong phẫu thuật Glen – PEEP thấp và rút NKQ sớm
Duy trì áp lực đổ đầy thất bằng cách truyền cao phân tử.
Tập VLTL hô hấp là cần thiết vì giúp làm giảm kháng lực mạch máu phổi.
Tối ưu hóa sức co bóp cơ tim bằng các inotropes (inodilators).
Trong Fontan bên, giữ nhịp xoang là bắt buộc.
Trong Fontan ngoài tim, khởi đầu truyền Heparin và sau khi rút NKQ chuyển sang uống Warfarin, giữ INR 2,5-3.
Theo dõi áp lực tĩnh mạch chủ trên, cũng là áp lực Fontan, nếu SP02 giảm và áp lực Fontan cao, kiểm tra siêu âm khẩn để loại trừ tắc nghẽn hệ thống Fontan.
Tràn dịch màng phổi có thể được phát hiện và tồn tại trong một khoảng thời gian dài.
Tràn dịch màng bụng có thể xuất hiện trong các trường hợp Fontan nguy cơ cao.
Các tình huống đặc biệt
Bởi vì sự thay đổi đột ngột thể tích và hình thể của thất, dẫn đến suy thất nên phải hỗ trợ bằng inotrope liều cao.
Nên bắt đầu với một mình Milrinon hơn là kết hợp với inotropes.
Sildenafil đường uống.
FiO2 cao nếu có chỉ định.
Tạo cửa sổ giúp làm giảm áp hệ thống Fontan.
Nếu áp lực Fontan của bệnh nhân vẫn còn cao, mở rộng cửa sổ hơn nữa hoặc tháo bỏ hệ thống Fontan.
Atrial septal defect (asd)
Là bệnh tim bẩm sinh không tím, tăng lưu lượng máu lên phổi.
Nhĩ phải lớn, thất phải lớn, hẹp ĐMP (PAS) và nhĩ trái tương đối nhỏ.
Kiểm soát hậu phẫu
Hình 23-5: Atrial septal defect (ASD)
Thường hồi phục không có vấn đề nghiêm trọng, rút NKQ sớm.
Kiểm soát tình trạng quá tải vì nhĩ trái nhỏ, có thể dẫn đến phù phổi.
Theo dõi liên tục SpO2 – nếu tình trạng giảm SpO2 kéo dài, có thể do phù phổi hoặc TMC dưới hướng qua nhĩ trái.
Loạn nhịp nhĩ có thể xảy ra.
Atrioventricular canal defect
Hình 23-6: Atrioventricular canal defect
Ventricular septal defect
Hình 23-7: Ventricular septal defect (VSD)
Total anomalous pulmonary venous connection (tapvc)
Xử trí hậu phẫu
Hình 23-8: Supracardiac TAPVC
Kiểm soát tùy vào mức độ nghiêm trọng của thương tổn, áp lực động mạch phổi trước mổ và tình trạng van nhĩ thất.
Những bệnh nhân có tăng áp phổi nặng xử trí bao gồm:
Thở máy có thể khoảng 48 giờ.
Cần an thần sâu khi thở máy.
Tránh hút đàm thường xuyên, khi hút đàm phải cho an thần đầy đủ.
Giữ độ bão hòa oxy cao và mức CO2 thấp vì CO2 cao có thể làm co mạch máu phổi.
Bất cứ khi nào độ bão hòa oxy giảm xuống phải tăng thông khí với Fi02 100%.
Sau 4 giờ tiếp nhận bệnh nhân, bắt đầu tiêm Phenoxybezamine 0,5 – 1 mg/kg/24 giờ.
Có thể sử dụng Mirinone.
Uống Sildenafil trong ngày đầu.
Giữ phổi trong tình trạng tốt, xẹp phổi, tràn, tràn khí màng phổi, tràn dịch màng phổi có thể gây ra cơn cao áp phổi.
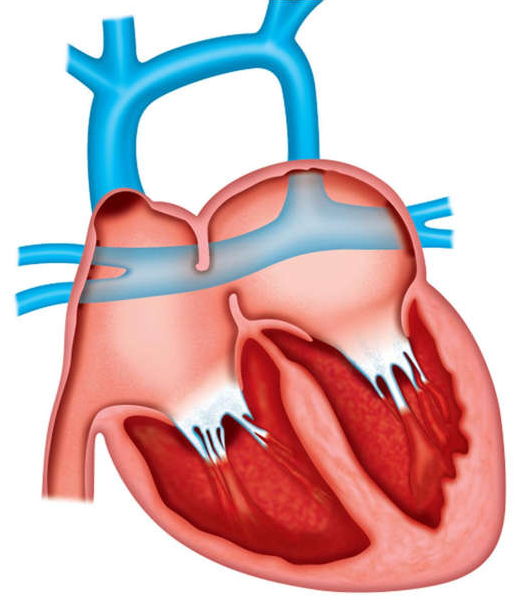
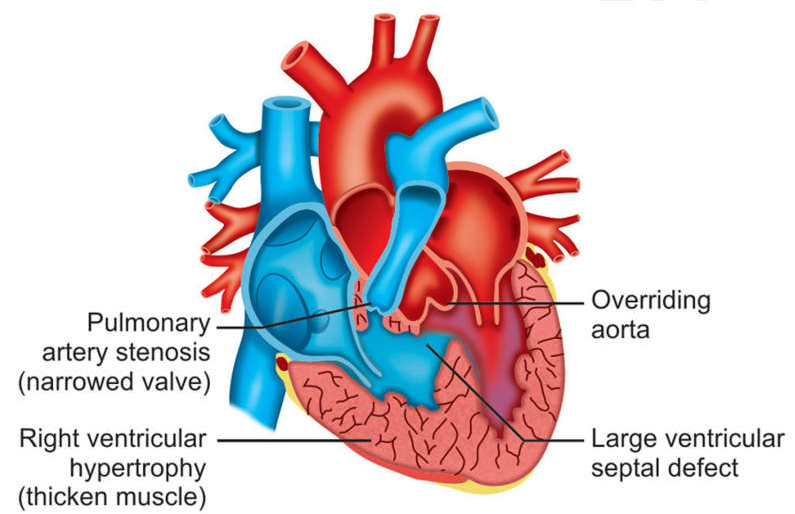
Tetralogy of fallot
Bệnh tim bẩm sinh tím.
TOF gồm 4 tổn thương:
Thông liên thất.
Hẹp đường thoát thất phải (RVOT).
Động mạch chủ cưỡi ngựa.
Phì đại thất phải.
Trước khi sữa chữa
Trẻ nhũ nhi có TOF dung nạp kém với thuốc giãn mạch và thuốc chủ vận beta.
Cơn tím thiếu oxy thường xảy ra do sự co thắt đường thoát thất phải và được điều trị bằng:
Oxy
Tăng thể tích tuần hoàn: truyền dịch 10 – 30 ml/kg
An thần (Morphine)
Tư thế gối ngực
Thuốc co mạch
Metaraminol: khởi đầu 0.01 μg/kg, sau đó truyền 0.1–1 μg/kg/min.
Noradrenaline truyền tĩnh mạch: 0.1–0.5 μg/kg/min.
Beta-blocker—propranolol: 0.1 mg/kg IV.
Đặt NKQ giúp thở
Giai đoạn phẫu thuật
Giảm cung lượng tim do rối loạn chức năng thất phải, CPB và hẹp tồn lưu đường thoát thất phải.
Tràn dịch qua khoang thứ 3 – đòi hỏi lọc màng bụng hoặc đặt ống dẫn lưu ngực để dẫn lưu.
Duy trì một áp lực nhĩ phải cao trong giai đoạn hậu phẫu để cải thiện cung lượng tim và giúp lưu lượng máu từ thất phải vượt qua nơi tắc nghẽn.
Truyền máu hoặc cao phân tử để cải thiện cung lượng tim và duy trì CVP với cao phân tử.
Áp lực nhĩ phải duy trì khoảng 16 – 18 mmHg.
Sử dụng inotropes một cách cẩn thận. Không giảm liều inotropes trong 48 giờ vì có thể xảy ra tình trạng giảm cung lượng tim sau 12 – 24 giờ.
Rút NKQ khi huyết động ổn định với sự hỗ trợ tối thiểu và Fi02
Giới hạn dịch bằng 2/3 nhu cầu.
Digoxin được sử dụng để ngưng dần các thuốc vận mạch truyền.
Block nhánh phải (Right bundle branch block, RBBB) có thể xảy ra do sự cắt thất phải có hoặc không có tổn thương nhánh phải hoặc hệ thống dẫn truyền.
RBBB có liên quan với block phân nhánh trái trước.
LAH có liên quan với block tim hoàn toàn (CHB, complete heart block).
Máy tạo nhịp tạm thời được đặt trong lúc phẫu thuật ở tất cả bệnh nhân.
Nếu block tim hoàn toàn vẫn còn tồn tại sau hơn 2 – 3 tuần thì cần PPI.
Biến chứng muộn là loạn nhịp thất.
Trẻ được phẫu thuật sớm có tỉ lệ ngoại tâm thu thất ít hơn.
Nếu giảm cung lượng tim xảy ra dù đã dung vận mạch liều cao, cần siêu âm để tìm thông liên thất tồn lưu, hẹp đường thoát thất phải, tuần hoàn bàng hệ phế chủ và nhiễm trùng.
Giai đoạn hậu phẫu cần đảm bảo lợi tiểu tốt, theo dõi những dấu hiệu đánh giá chức năng của thất phải như gan to và tràn dịch màng phổi.
Hình 23-9: Tetralogy of Fallot
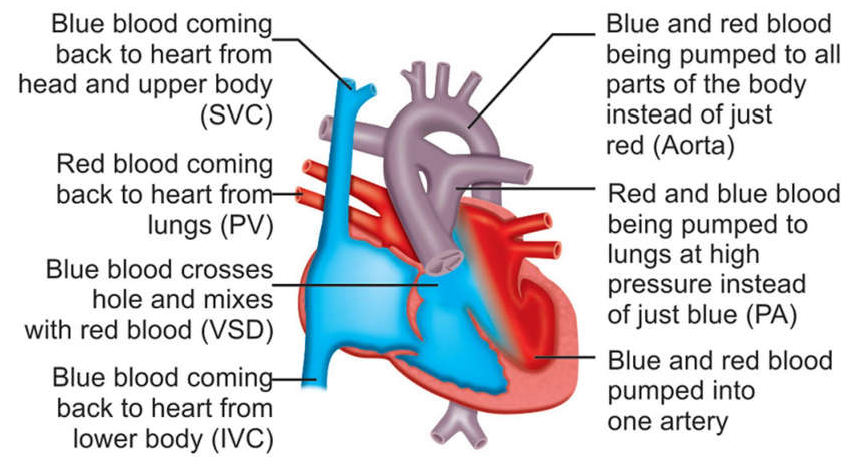
Truncus arteriosus
Đặc trưng bởi một đường thoát chung cho thất với thông liên thất kèm theo.
Trẻ có dòng máu lên phổi tốt thường không cần phải can thiệp cho đến khi áp lực mạch máu phổi giảm xuống lúc 3 tháng tuổi, khi các dấu hiệu sung huyết phổi tăng lên.
Dòng máu lên phổi tăng cao vì vậy tình trạng cao áp phổi sớm xảy ra.
Chăm sóc hậu phẫu
Hình 23-10: Truncus arteriosus
Biến chứng sớm trong giai đoạn hậu phẫu bao gồm giảm cung lượng tim và cao áp phổi.
Tất cả các điều trị dự phòng cơn cao áp phổi phải được tiến hành sớm.
CVP nên để ở mức cao để duy trì cung lượng tim.
Dịch truyền khoảng 2/3 nhu cầu.
Theo dõi cơn cao áp phổi.
Trẻ bệnh nặng có hở van thân động mạch chung và cần phải sữa chữa van.
Thông tim và siêu âm để loại trừ thông liên thất tồn lưu và tắc nghẽn đường ống dẫn máu lên phổi.
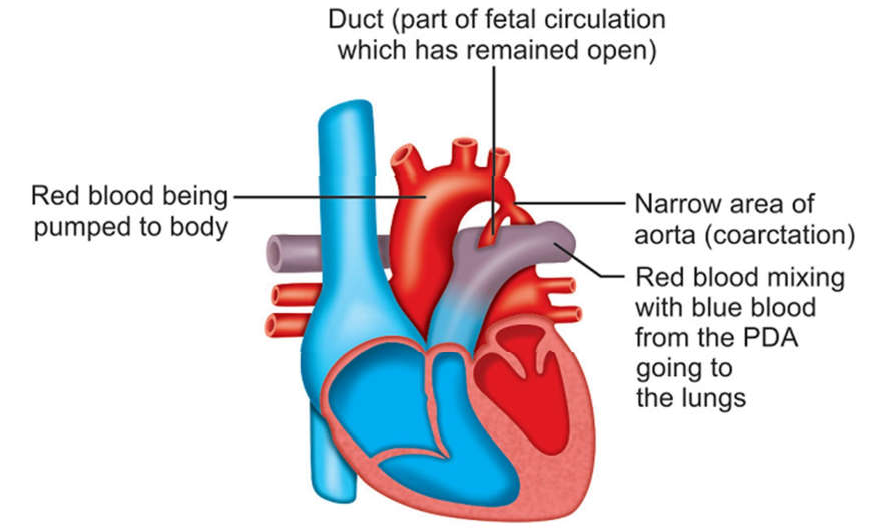
Coarctation of aorta
Xảy ra trong đoạn xuống của ĐMC ngực, đối diện với nơi ống động mạch đổ vào và gần kề nơi xuất phát của ĐM dưới đòn trái.
Phẫu thuật sửa chữa bao gồm:
Tạo hình động mạch dưới đòn T
Nối tận – tận.
Sự lựa chọn phụ thuộc vào tuổi của bệnh nhân.
Trong suốt thời gian kẹp ĐMC lúc phẫu thuật, truyền dịch phụ thuộc vào mức độ của tuần hoàn bàng hệ.
Truyền dịch không đủ có thể gây thiếu máu cục bộ tủy sống, thận, dạ dày ruột.
Sự gia tăng đột ngột hậu tải của thất trái có thể làm giảm sức chịu đựng ở bệnh nhân có suy tim sung huyết trước đó
Giảm hậu tải với các thuốc giãn mạch như Nitroprusside có thể gây nguy hiểm với huyết áp dưới nơi kẹp động mạch bị thấp.
Biến chứng trầm trọng nhất là liệt hai chi dưới vì hội chứng động mạch tủy sống trước do kẹp động mạch chủ.
Hình 23-11: Coarctation of aorta
Xẹp phổi trong giai đoạn hậu phẫu do xẹp phổi trái lúc mở xương ức.
Cai máy thở và rút NKQ có thể trì hoãn vì thần kinh hoành và thần kinh quặt ngược thanh quản bị tổn thương.
Tràn dịch dưỡng trấp do tổn thương ống ngực có thể xảy ra.
Tăng huyết áp kéo dài sau khi sữa chữa CoA vì mức catecholamine và renin cao.
Nếu không điều trị, làm căng vết khâu cung ĐMC làm chảy máu nhiều đòi hỏi phải truyền máu và mở xương ức.
Không điều trị tăng huyết áp có thể dẫn đến hội chứng sau phẫu thuật eo ĐMC – phản xạ co thắt mạch máu mạc treo giảm tưới máu nội tạng dẫn đến thiếu máu cục bộ và thủng ruột, tăng tỉ lệ tử vong.
Dẫn lưu dạ dày và không nuôi ăn đường miệng trong 2-3 ngày đầu.
Kiểm soát tăng huyết áp với Nitroprusside, ức chế Beta, Captoril 1-2 mg/kg/liều/mỗi 8 giờ.
Nên kiểm tra huyết áp chi dưới để tìm sự hiện diện của sự chênh áp tồn lưu.
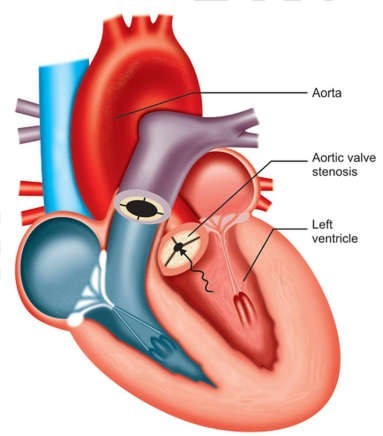
Hẹp van động mạch chủ
Những trẻ lớn có thể không có triệu chứng suy tim nặng vì đã thích nghi với tình trạng hẹp nặng dần của van.
Bệnh có nguyên nhân bẩm sinh, tương tự trường hợp van 2 lá.
Hẹp van động mạch chủ nặng có thể làm giảm tưới máu mạch vành, dẫn đến cơn đau thắt ngực và thiếu máu cơ tim cục bộ.
Phẫu thuật có thể là sửa chữa hoặc thay thế van động mạch chủ.
Lựa chọn sửa chữa van ở những trẻ nhỏ, thay thế van ở những trẻ lớn hơn.
Thay van tim cơ học đòi hỏi phải có thuốc chống đông kéo dài.
Ghép van tim (từ người khác) không cần thuốc chống đông nhưng van được thay có khuynh hướng xấu đi theo thời gian.
Sửa chữa van có thể theo sau phẫu thuật phục hồi động mạch chủ.
Van cơ học có thể phải thay mới sau một thời gian.
Phẫu thuật Ross (ghép van tự thân): van và thân động mạch phổi được cắt luôn cả khối rồi thay vào vị trí của van động mạch chủ đồng thời cắm lại hai động mạch vành. Chỗ van động mạch phổi bị cắt sẽ được thay thế bằng một van động mạch phổi đồng loài.
Hậu phẫu
Hình 23-12: Aortic stenosis
Hậu phẫu ở những bệnh nhân này đòi hỏi áp lực đổ đầy cao, nên giữ CVP lớn hơn 10.
Rút nội khí quản có thể được lựa chọn, không bắt buộc.
Giảm hậu tải.
Bắt đầu sử dụng thuốc ức chế men chuyển sau mổ.
Nếu phẫu thuật thay van nhân tạo, bắt đầu truyền tĩnh mạch Heparin 10 u/kg/h.
Wafarin 5 mg/ngày, giữ INR 2.5 – 3.
Aspirin 5 mg/kg/ngày.
Sau phẫu thuật Ross: tránh tập vật lý trị liệu hô hấp.
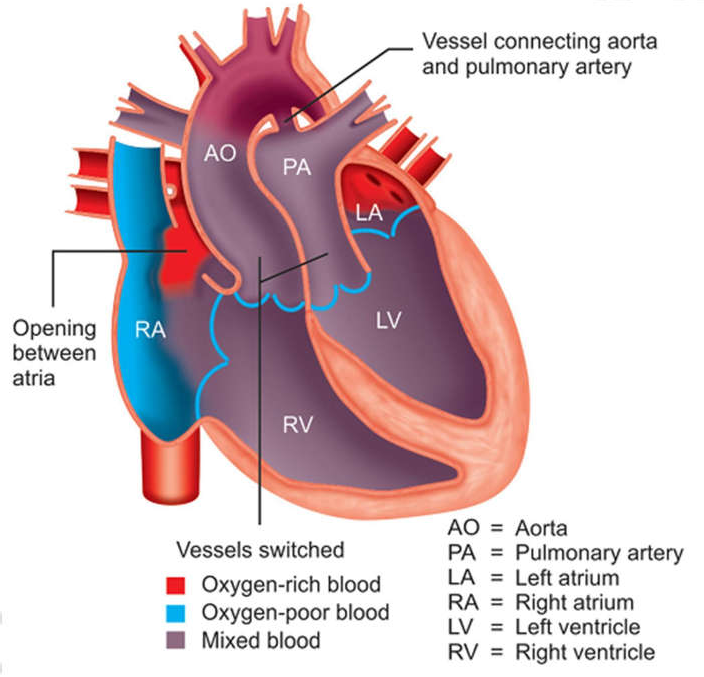
Chuyển vị đại động mạch
Phẫu thuật hoàn chỉnh hiện nay là chuyển đổi động mạch (JATENE) hay chuyển đổi tâm nhĩ (Mustard hay Senning).
Phẫu thuật Jatene bao gồm cắm lại cả 2 động mạch chủ vào đúng vị trí ở tâm nhĩ tương ứng và cắm lại động mạch vào vào vị trí mới trên động mạch vừa chuyển đổi.
Hình 23-13: Transposition of great arteries (TGA)
Phẫu thuật trên chỉ có thể hoàn thành khi thất trái có thể bơm máu thắng được kháng lực mạch máu hệ thống. Điều đó chỉ xảy ra trong 3 trường hợp sau:
Phẫu thuật ở trẻ sơ sinh vài ngày tuổi, khi thất trái tiếp xúc với áp lực cao của hệ mạch máu phổi (trước 3 tuần).
Ở trẻ lớn hơn có sự hiện hiện lỗ thông liên thất không giới hạn, với áp lực thất trái cao và do đó cơ tim tập trung dày lên.
Ở những trẻ lớn mà vách liên thất nguyên vẹn, khối cơ thất phát triển phì đại lên thông qua đặt một vòng xiết ở động mạch phổi (banding động mạch phổi).
Biến chứng phẫu thuật: bao gồm mất máu nhiều, tăng áp lực động mạch phổi và thiếu máu cơ tim liên quan đến việc cắm lại động mạch vành.
Xuất huyết do rất nhiều yếu tố.
Thể tích mồi lớn trong khi chạy tim phổi nhân tạo
Giảm số lượng và chức năng tiểu cầu trong trong lúc chạy tim phổi nhân tạo và bị hạ thân nhiệt.
Đường khâu vết mổ rộng và kéo dài có thể trở nên không an toàn.
Tăng áp phổi ở trẻ sơ sinh có thể dẫn đến giảm chức năng thất phải. Điều này có thể phòng tránh bằng cách tránh làm tăng CO2 và giảm Oxy máu. Tăng áp phổi đòi hỏi phải sử dụng thuốc giãn mạch và hít khí NO.
Thiếu máu cơ tim có thể liên quan đến khí hay tổn thương vi phẫu của động mạch vành.
Sự hình thành cục máu đông lớn có thể dẫn đến suy chức năng thất.
Xoắn thắt mạch vành trong khi nối cũng có thể gây giảm tưới máu và thiếu máu thất.
Nitroglycerin có thể được sử dụng để làm giãn mạch vành.
Biến chứng lâu dài tương tự phẫu thuật phục hồi động mạch chủ.
Những biến chứng khác bao gồm tắc động mạch vành, tăng huyết áp và hẹp động động mạch phổi chính.
Rối loạn nhịp bao gồm nhịp nhanh kịch phát trên thất và block tim hoàn hoàn được ghi nhận trong 20% các trường hợp.
Phẫu thuật chuyển đổi tâm nhĩ (Mustard hay Senning) trong đó tĩnh mạch hệ thống hướng vào thất trái và tĩnh mạch phổi chệch sang thất phải.
Màng tim hay miếng Dacron được sử dụng trong Mustard và mô nhĩ tự nhiên được dùng trong Senning.
Sự tắc nghẽn hồi lưu tĩnh mạch về nhĩ có thể có nguyên nhân từ sự tắc nghẽn trong tim.
Nghi ngờ tắc chỗ nối tĩnh mạch và nhĩ phải khi CVP tăng không giải thích được, biểu hiện lâm sàng là sự ứ máu trên mặt và ứ máu tĩnh mạch cổ.
Tắc các tĩnh mạch phổi về nhĩ trái biểu hiện như phù phổi. Nó có thể gây suy tim sớm cũng như trễ.
Thông khí giới hạn tương tự như Glenn sau phẫu thuật Senning.
Đo điện tim Holter 24 giờ có thể phát hiện 95% các trường hợp tổn thương hệ thống dẫn truyền của tim khi chuyển đổi tâm nhĩ.
Nút xoang và cơ tâm nhĩ cũng có thể bị tổn thương.
Điều hòa hoạt động điện tim có thể được chỉ định.
Hội chứng suy nút xoang với giai đoạn ngắn ngưng xoang cần máy tạo nhịp vĩnh viễn.
Xử trí hậu phẫu
Hầu hết những bệnh nhi được phẫu thuật chuyển đổi ở độ tuổi sơ sinh và các bé được nhập khoa PICU (hồi sức nhi) với ngực hở.
Chăm sóc bệnh nhi ngực hở phòng ngừa nhiễm trùng từ bên ngoài (xem phụ lục 4).
Những bệnh nhi này đều có LA và PA line, theo dõi chúng thật cẩn thận, giữ LAP từ 10-12, cân bằng dịch với dịch keo, FFP, PCV.
Adrenaline, dopamine và milrinone là những lựa chọn vận mạch tốt.
Lọc màng bụng có thể giúp thải dịch tốt.
Nếu thấy băng ngực phồng lên và các dấu hiệu khác của chèn ép tim – gọi phẫu thuật viên.
Thông khí thích hợp, nếu thông khí với VT lớn có thể gây hiện tượng chèn ép và làm hạ huyết áp.
Phòng ngừa sớm cơn tăng áp phổi.
Giữ nhịp tim trong khoảng 140-160. Nếu cần, phải điều hòa nhịp nhĩ cũng như nhĩ-thất.
Giữ thân nhiệt bằng warmer.
Cảnh giác với dấu hiệu giảm cung lượng tim.
Nếu huyết áp đang ở ngưỡng hạ, nhìn ngay xem băng ngực có phồng lên không.
Khi đóng ngực phải quan sát thông khí và độ bão hòa oxy.
Sau đóng ngực có nguy cơ bệnh nhi bị hạ huyết áp, thế nên cần chú ý tăng vận mạch nếu cần và cai máy sớm nếu các thông số máy thở trong giới hạn chấp nhận được.
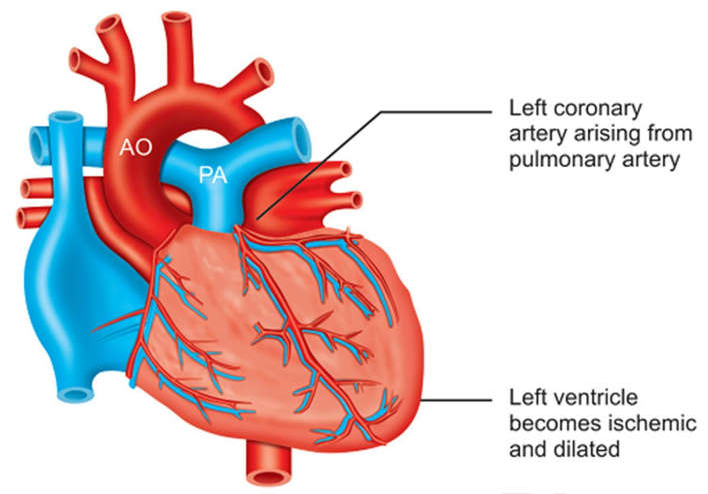
Bất thường động mạch vành trái từ động mạch phổi (alcapa)
Chăm sóc hậu phẫu tùy thuộc vào tuổi xuất hiện, thay đổi thứ phát của thất trái và kiểu phẫu thuật.
Ở những ca chuyển đổi mạch vành, luôn thận trọng với bất kì thay đổi ECG nào, đó có thể là cảnh báo của sự xoắn thắt mạch vành hoặc tắc nghẽn đường hầm.
Theo dõi men tim bệnh nhân mỗi 24 giờ.
Milrinone tĩnh mạch hay adrenaline tĩnh mạch là những lựa chọn vận mạch tốt.
Ở những ca suy tim trái nặng, bóng nội động mạch chủ (IABP) hay dụng cụ hỗ trợ thất trái là những lựa chọn tốt trong giai đoạn đầu hậu phẫu.
Hình 23-14: Anomalous left coronary artery from pulmonary artery (ALCAPA)
Hội chứng thiểu sản thất trái (hlhs)
Xử trí giai đoạn sớm
Thiểu sản thất trái là tật tim bẩm sinh gây tử vong nhiều nhất trong tháng đầu sau sinh. Hội chứng này bao gồm một loạt các tật của tim trái bao gồm: teo hay hẹp van động mạch chủ, thiểu sản nhánh lên cung động mạch chủ và thiểu sản hay thiếu mất thất trái. Tiên lượng lâu dài của những trẻ mắc hội chứng này hiện nay rất xấu, nhưng hiện có 2 phương án có hi vọng: một là ghép tim, hai là phẫu thuật tái tạo tim được tiên phong bởi Norwood để tái tạo hệ tuần hoàn có thể giúp bệnh nhi sống sót.
Ghép tim sơ sinh hiện nay được thực hiện ở rất ít trung tâm trên thế giới; nó bị hạn chế không phải bởi cơ sở vật chất hay kĩ năng chuyên môn, mà bởi số lượng tạng hiến cực kì ít ỏi. Do đó mà phẫu thuật Norwood trở thành lựa chọn khả dĩ ở hầu hết các bệnh nhi bị mắc hội chứng này.
Giai đoạn đầu tiên trong chuỗi phẫu thuật Norwood hướng tới tái tạo cung động mạch chủ, đảm bảo phối hợp đầy đủ mở thông vách liên nhĩ và lưu lương máu lên phổi bằng shunt Blalock-Taussig hay ống thông thất phải-động mạch phổi. Mục tiêu của bác sĩ hồi sức để chuẩn bị bệnh nhi cho phẫu thuật này là đưa tỷ lệ Qp/Qs về gần 1.0 nhất có thể. Ống động mạch phải được mở bằng prostaglandin E1 hoặc E2 (xem bên dưới).
Giai đoạn tiếp theo sau đó thực hiện lúc trẻ được 4-9 tháng tuổi, bằng cách tạo luồng thông 2 chiều giữa tĩnh mạch chủ và động mạch phổi (Norwood giai đoạn 2), giảm thể tích máu đổ vào thất phải. Cuối cùng phẫu thuật Fortan được thực hiện (Norwood giai đoạn 3) khi trẻ được 12-24 tháng tuổi.
Thời điểm khám chẩn đoán bệnh
Chẩn đoán trước sanh
Thiểu sản thất trái thường được chẩn đoán trước sanh dựa vào siêu âm thai tầm soát. Yêu cầu sau đó là thiết lập liên lạc giữa bác sĩ sản khoa, bác sĩ sơ sinh và bác sĩ tim mạch nhi để đảm bảo trẻ được mới sinh ra sẽ được chăm sóc phù hợp và chuyển ngay đến đơn vị tim mạch nhi.
Chẩn đoán sau sanh
Nếu không được chẩn đoán trước sanh, trẻ bị thiểu sản thất trái thường sẽ rơi vào tình trạng sốc nặng, toan chuyển hóa, mất mạch đùi cùng thời điểm ống động mạch đóng lại. Triệu chứng lâm sàng khi đó rất khó phân biệt với hẹp cung động mạch chủ. Chẩn đoán chi tiết chỉ có khi siêu âm tim sau hồi sức bệnh nhân.
Chẩn đoán bằng siêu âm tim
Ngoại trừ thông tin về giải phẫu của tật tim – chìa khóa bắt buộc phải có từ siêu âm tim giúp cho công việc hồi sức- những điểm chính mà bác sĩ hồi sức cần chú ý là tình trạng của ống động mạch, mức độ cản trở của bất kì sự cản trở nào nếu có của dòng máu đi ra từ thất trái.
Sự cản trở lỗ thông liên nhĩ có thể xử trí bằng cách phẫu thuật sớm (phương án tốt nhất) hoặc đặt bóng nong lỗ thông liên nhĩ (để trì hoãn phẫu thuật).
Xử trí khi tiếp cận bệnh nhân
Sự sống còn của bệnh nhân được quyết định trước tiên bởi các yếu tố sau:
Sự tồn tại ống động mạch mở, đảm cho cho máu từ động mạch phổi có thể đến được động mạch chủ.
Máu từ tĩnh mạch phổi đổ về nhĩ trái có thể chảy qua tim phải bằng lỗ bầu dục hay lỗ thông liên nhĩ.
Sự cân bằng đạt được giữa kháng lực hệ phổi và hệ chủ (Qp:Qs ~ 1:1).
Prostaglandin tiêm giữ ống động mạch mở.
Hồi sức theo “ABC”
Nên thiết lập chiến lược điều trị đầy đủ khi trẻ được chẩn đoán thiểu sản thất trái trước sanh hoặc ngay khi chẩn đoán sau sanh.
Đường thở và thông khí
Rất nhiều trẻ bị thiểu sản thất trái chịu đựng tốt với thở khí trời khi được cho PGE1 liều thấp mà không cần đặt nội khí quản hay thông khí cơ học.
Nếu cần phải đặt nội khí quản, sử dụng ketamine và dãn cơ, giới hạn FiO2 ở mức 21-30%.
Cho trẻ thở khí trời hoặc thở trong thiết trị chụp lên đầu ở mức FiO2 thấp nhất có thể, giữ độ bão hòa oxy trong động mạch hệ thống trong khoảng từ 70-80%.
Thiết bị cung cấp khí trộn nên có khi thông khí bằng tay hoặc bằng thiếp bị chụp lên đầu.
Không cung cấp oxy bằng đường mũi qua cannula hoặc mặt nạ vì % oxy không thể biết chính xác.
Thiết lập thông khí ban đầu:
FiO2: 21-30%
Tần số thở: 20 lần/phút
Vt: 10 ml/kg
Mục tiêu khí máu:
PaO2: 30-45 mmHg
PaCO2: 37,5-45 mmHg
SaO2: 70-80% hướng tới điều chỉnh Qp:Qs bằng 1
Tim mạch:
Tiếp tục truyền prostaglandin (PGE1 hay PGE2 5-20 ng/kg/phút).
Mục tiêu huyết áp động mạch khoảng 45-60 mmHg và tưới máu hệ thống “tốt” (chi ấm, không thiếu hụt máu, lactate
Sử dụng dung dịch keo có thể được cân nhắc.
Cân nhắc hỗ trợ vận mạch nếu chức năng thất phải kém trên siêu âm hoặc cung lượng tim thấp kéo dài trên bệnh nhân bị toan chuyển hóa (dopamine 5-15 mcg/kg/phút), nhưng phải cảnh giác sự thay đổi cân bằng kháng lực mạch máu phổi/kháng lực mạch máu hệ thống. Nếu dopamine làm tăng kháng lực mạch máu phổi, dobutamine sẽ là lựa chọn thay thấy. Adrenaline vẫn là lựa chọn hàng thứ 2.
Đường truyền:
Những đứa bé mắc phải hội chứng này sẽ phải trải qua quá trình phẫu thuật với ít nhất 3 cuộc phẫu thuật. Do đó tất cả những đường truyền phải được chăm sóc thật tốt.
Catheter đa nòng đặt ở tĩnh mạch chủ trên nên tránh nếu có thể. Nếu phải đặt catheter ở vùng này, nên có kế hoạch rút sớm sau phẫu thuật.
Tuy nhiên, một catheter nhỏ đặt ở tĩnh mạch chủ trên rất có ý nghĩa để theo dõi nồng độ oxy “tĩnh mạch trộn”, qua đó, thể hiện được sự cân bằng các luồng thông trong và sau phẫu thuật Norwood giai đoạn 1.
Đường động mạch cánh tay trái nên tránh. Những trẻ bị hội chứng thiểu sản thất trái thường có kèm hẹp động mạch chủ, do đó đo huyết áp dựa vào đường động mạch này không đáng tin cậy do áp suất không chính xác.
Cân bằng các shunt trước phẫu thuật
Tăng lưu lượng máu phổi
Độ bão hòa oxy > 80% và PaO2> 45 mmHg gợi ý Qp:Qs>1.
Giảm huyết áp tâm trương:
Thở khí trời
Cân nhắc đặt nội khí quản giảm thông khí nhằm tăng CO2 để giảm Qp.
Giảm lưu lượng máu phổi
Độ bão hòa oxy
Điều này khá hiếm gặp trước giai đoạn 1 phẫu thuật sửa chữa.
Kiểm tra đường truyền prostaglandin:
Kiểm tra lại ống động mạch và lỗ thông liên nhĩ bằng siêu âm.
Thử sử dụng thuốc co mạch (noradrenalin 0,05-0,4 mcg/kg/phút) trong khi chuẩn bị phẫu thuật cấp cứu nếu độ bão hòa oxy máu không cải thiện nhanh chóng.
Thời điểm phẫu thuật
Nếu tình trạng bé tương đối ổn định, giai đoạn I phẫu thuật Norwood có thể tiến hành vào ngày nhập viện hoặc sáng hôm sau (nếu nhập viện ban đêm).
Nếu bé không ổn định, mặc dù tình trạng nội khoa và phẫu thuật có chống chỉ định do những vấn đề chính chưa được giải quyết thì cũng phải tiến hành phẫu thuật khẩn cấp.
Phẫu thuật đôi khi cũng có thể hoãn để tiện cho việc đánh giá thần kinh nếu trẻ biểu hiện bệnh về thần kinh khi đến khám.
Phẫu thuật và gây mê
Dù gây mê kiểu nào, có những điểm chính sau đây:
Cân bằng shunt nên được giữ thăng bằng (SaO2 70-80%). Thở khí trời hoặc FiO2 thấp thường được yêu cầu trong quá trình di chuyển bệnh nhân đến phòng mổ và từ phòng mổ ra đơn vị hồi sức.
Các đường truyền nên được đảm bảo tốt nhất có thể.
Một đường truyền 1 nòng đặt ở tĩnh mạch chủ trên nên được đặt để đo độ bão hòa oxy tĩnh mạch trộn.
Những thông số sinh lý hữu ích được sử dụng khi ống shunt/PA được tháo kẹp khi kết thúc tuần hoàn ngoài cơ thể. Sự tăng áp suất tưới máu cao hơn 25-30 mmHg gợi ý Qp tăng cao, và bước tiếp theo cần làm là làm tăng kháng lực mạch phổi bằng cách giảm FiO2 ngay lập tức và cho phép CO2 tăng trong quá trình ngưng tuần hoàn ngoài cơ thể.
Siêu âm tim nên được thực hiện nếu tình trạng không ổn định.
Hậu phẫu giai đoạn 1 norwood
Sinh lý của những đứa bé thường tương tự sau sau giai đoạn 1 phẫu thuật Norwood. Ống động mạch được thay thế bằng shunt động mạch phổi-chủ nhưng cả hệ phổi lẫn chủ đều được cấp máu từ cùng một nguồn và sự cân bằng kháng lực hệ phổi-chủ tiếp tục quyết định tỷ lệ lưu lượng máu phổi-chủ.
Cân bằng shunt sau phẫu thuật
Tăng lưu lượng máu phổi:
Độ bão hòa oxy > 80% và PaO2> 45 mmHg gợi ý Qp:Qs>1.
Giảm huyết áp tâm trương:
Thở khí trời
Điều chỉnh bất kì kiềm chuyển hóa nào (dùng acetazolamic hay arginine hydrochloride).
Lựa chọn giảm thông khí nhằm tăng CO2 để làm giảm Qp.
Giảm tần số thở nhưng vẫn giữ Vt.
Thêm khoảng chết thông khí để tăng CO2 thở lại.
Tăng PEEP.
Thêm CO2 tiềm ẩn nguy hiểm và không được khuyến cáo.
Nếu có bằng chứng lưu lượng máu lên phổi vẫn tăng dù đã áp dụng những biện pháp trên, ta nên xem xét nhanh chóng thay ống thông/PA kích cỡ nhỏ hơn.
Giảm lưu lượng máu phổi:
Độ bão hòa oxy
Siêu âm kiểm tra tình trạng mở shunt.
Loại trừ nguyên nhân giảm oxy máu do phổi.
Kiểm tra và điều chỉnh độ bão hòa oxy/giảm cung lượng tim.
Giữ kháng lực mạch máu hệ thống cao bằng thuốc co mạch (noradrenaline 0,05-0,4 mcg/kg/ph) để đẩy máu qua shunt/phổi.
Tăng FiO2 để giảm kháng lực mạch máu phổi.
Giảm kiềm chuyển hóa.
Hủy tác động co mạch.
Xem xét phẫu thuật cấp cứu lại khi cần nếu lưu lượng máu quá ít.
Để mở thông shunt, độ bão hòa oxy thấp (60-70%) có thể được chấp nhận ở giai đoạn sớm hậu phẫu, nhưng độ bão hòa oxy quá thấp (dưới 60%) thì không được, đặc biệt khi nó liên quan đến tình trạng toan máu hay giảm tưới máu hệ thống.
Sự giải thích tỉ lệ Qp:Qs chỉ bằng độ bão hòa oxy hệ thống giả định rằng máu tĩnh mạch trộn về tim chỉ được bão hòa khoảng 50% oxy và không thay đổi bằng những điều chỉnh “cân bằng”. Điều này thì hiếm xảy ra. Ta vẫn sử dụng những hiểu biết tốt hơn về sự phân phối lưu lượng các shunt và lưu lượng máu hệ thống thông qua đánh giá độ bão hòa oxy máu tĩnh mạch chủ trên.
Cách tính shunt
Có thể giả định SaO2 = SpaO2 khoảng 95%-100%.
Với một cung lượng tim và nhu cầu chuyển hóa thông thường, SaO2 –SsvcO2 xấp xỉ khoảng 25- 30%.
Chăm sóc tổng quát hậu phẫu
Những trẻ này rất yếu ớt. Chăm sóc những gì cần thiết và quan sát cẩn thận tình trạng lâm sàng ở mỗi bước.
Siêu âm kiểm tra thường quy sau mổ.
Ở những trẻ có nguy cơ tăng áp phổi, cần phải cho an thần trước khi hút đàm hoặc thực hiện các chăm sóc gây stress cho trẻ.
Cẩn thận ở những trẻ huyết động không ổn định.
Sử dụng lợi tiểu nếu cần.