Neven Stevic, Emeric Chatelain, Auguste Dargent, Laurent Argaud, Martin Cour, and Claude Guérin
American Journal of Respiratory and Critical Care Medicine Volume 203 Number 8 | April 15 2021
Dịch bởi: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Gửi tới Người biên tập:
Một tỷ lệ đáng kể bệnh nhân mắc bệnh coronavirus (COVID-19) nhập viện ICU yêu cầu thở máy xâm nhập do hội chứng suy hô hấp cấp (ARDS), vẫn còn liên quan đến tỷ lệ tử vong cao (1). Áp dụng áp lực dương cuối kỳ thở ra (PEEP) tối ưu để đảm bảo huy động phổi trong khi hạn chế siêu bơm phồng phổi vẫn còn là thách thức trong ARDS (2, 3). Tuy nhiên, có một số công cụ đơn giản có thể giúp cá nhân hóa mức độ PEEP ở những bệnh nhân tại giường bệnh. Trong số đó, điểm thông khí qua siêu âm phổi (LUS, lung ultrasound) và tỷ lệ huy động trên bơm phồng (R/I ratio, recruitment-to-inflation ratio) có khả năng xác định những bệnh nhân có nhiều khả năng được hưởng lợi từ PEEP hơn (2). Các nghiên cứu trước đây thực sự cho thấy rằng LUS có thể đánh giá sự phân bố không gian của quá trình huy động phổi do PEEP gây ra nhưng không phát hiện ra siêu bơm phồng một cách đáng tin cậy (4, 5). Tỷ lệ R/I là một công cụ đã được phát triển gần đây để đánh giá cả tiềm năng huy động phổi và nguy cơ siêu bơm phồng, nhưng nó không cung cấp thông tin khu vực về huy động phổi (6–8). Do đó, hai công cụ này, luôn sẵn có ở đầu giường trong hầu hết các ICU, có thể cung cấp thông tin bổ sung và bổ sung về việc huy động phổi.
Trong nghiên cứu này, chúng tôi nhằm đánh giá khả năng thu nhận phổi đồng thời bằng tỷ lệ R/I và LUS ở bệnh nhân ARDS liên quan đến COVID-19.
Phương pháp
Chúng tôi đã thực hiện một nghiên cứu quan sát tiền cứu trong khoảng thời gian từ ngày 31 tháng 3 đến ngày 29 tháng 10 năm 2020, trong một ICU gồm 26 trường đại học trực thuộc ở Lyon, Pháp, đã được ủy ban đạo đức thể chế của chúng tôi phê duyệt.
Những bệnh nhân trưởng thành liên tiếp mắc ARDS liên quan đến COVID-19 trong đó có sự huy động phổi do PEEP được đánh giá đồng thời với cả tỷ lệ LUS và R/I trong vòng 48 giờ đầu tiên sau khi đặt nội khí quản. COVID-19 đã được xác nhận về mặt sinh học và chẩn đoán ARDS dựa trên các tiêu chí Berlin.
Cài đặt máy thở và cơ học hô hấp đã được ghi lại ở những bệnh nhân được an thần và quản lý, được thở kiểm soát thể tích với máy thở Evita XL (Dräger Medical). Tất cả các phép đo được thực hiện ở bệnh nhân ở tư thế nữa nằm nữa ngồi. Sự hiện diện của việc đóng hoàn toàn đường thở được đánh giá bằng cách đo áp lực mở đường thở (AOP, airway opening pressure), như đã mô tả trước đây (6).
Sự huy động phổi do PEEP gây ra được đánh giá bằng tỷ lệ R/I với PEEP cao và thấp lần lượt là 15 cm H2O (trong 30 phút) và 5 cm H2O; trong trường hợp AOP> 5 cm H2O, R/I được tính bằng AOP thay vì 5 cm H2O (6–8). Tóm lại, khối lượng PEEP được huy động từ thấp đến cao chia cho sự thay đổi áplực hiệu quả cho thấy độ giãn nở của phổi được huy động; tỷ lệ giữa độ giãn nở này so với độ giãn nở ở PEEP thấp cho ra tỷ lệ R/I (6–8). Trong trường hợp không có giá trị giới hạn được xác nhận rộng rãi, tỷ lệ R/I trung bình của nhóm thuần tập được sử dụng để phân loại bệnh nhân thành những người huy động cao và thấp.
Điểm LUS được tính ở PEEP 15 cm H2O và PEEP 5 cm H2O, bằng cách tổng điểm vùng (0–3 điểm) thu được ở sáu vùng của mỗi phổi (tức là trên và dưới thành ngực trước, giữa và sau) (4, 5, 9, 10). Điểm delta LUS (ΔLUS) được định nghĩa là sự khác biệt thu được giữa PEEP thấp và cao. Điểm đánh giá lại LUS cũng được xác định theo phương pháp được xác nhận bởi Bouhemad và cộng sự (5). Tất cả các nhà nghiên cứu đã được thử nghiệm (> 100 quy trình LUS) và bị mù kết quả tỷ lệ R/I.
Dữ liệu liên tục được biểu thị dưới dạng trung vị (phần tư thứ nhất đến phần tư thứ ba). Các phép so sánh được thực hiện bằng cách sử dụng các bài kiểm tra không đối xứng. Các mối tương quan được đánh giá bằng thử nghiệm tương quan rho Spearman và khoảng tin cậy (CI) 95% của nó.
Kết quả
Có 24 bệnh nhân (tuổi: 69 [63–73] tuổi; tỷ số giới tính: 5) được đưa vào (Bảng 1). Thời gian từ khi có triệu chứng đầu tiên đến khi nhập viện ICU là 8 (7– 10) ngày. Hai mươi hai bệnh nhân (88%) được điều trị bằng liệu pháp oxy qua mũi dòng cao hoặc thông khí không xâm lấn trước khi đặt nội khí quản.
Hầu hết bệnh nhân (n = 22/24, 92%) có ARDS từ trung bình đến nặng (Bảng 1). Việc đóng đường thở hoàn toàn xuất hiện trong một phần ba trường hợp; không ai trong số họ có AOP trên PEEP cao (Bảng 1). Tỷ lệ R/I trung bình là 0,7, do đó xác định 12 người huy động cao (0,8 [0,8–1,1]) và 12 người huy động thấp (0,5 [0,3–0,6]) (Bảng 1). Điểm LUS đo được ở PEEP thấp và cao không có sự khác biệt đáng kể giữa hai phân nhóm, trong khi cả điểm ΔLUS và LUS lại cao hơn đáng kể ở những người huy động cao (Bảng 1). Sự khác biệt về điểm số tái thông khí LUS chủ yếu được thúc đẩy bởi sự tái thông khí nhiều hơn ở các vùng phổi bên và phổi sau ở những người huy động (Bảng 1). Chúng tôi nhận thấy mối tương quan có ý nghĩa (P 2O (Hình 1)
Thảo luận
Phát hiện chính và mới của nghiên cứu này là tỷ lệ R/I ở ngưỡng 0,7 tương quan với điểm tái chứng LUS, đặc biệt ở những bệnh nhân không đóng hoàn toàn đường thở. Theo hiểu biết tốt nhất của chúng tôi, đây là báo cáo đầu tiên kết hợp tỷ lệ R/I và LUS để đánh giá sự huy động của phổi, ngay cả khi xem xét những bệnh nhân có ARDS không COVID-19.
Kết quả của chúng tôi mở rộng sự xác nhận trước đó của điểm đo lại LUS so với thể tích được thu nhận được đo bằng đường cong thể tích – áp lực (4), bằng cách nhấn mạnh nhất quán sự cần thiết phải xem xét AOP khi đánh giá huy động phổi bằng phương pháp đo phế dung (spirometric methods).
Trong nghiên cứu của chúng tôi, điểm tái xác nhận LUS ở vùng phổi sau của những người huy động cao hơn đáng kể so với những người không huy động nhưng không ở vùng phổi trước. Phát hiện quan trọng này cho thấy rằng việc huy động phổi xảy ra ở các vùng phổi phụ thuộc, đây là hiệu quả mong muốn của PEEP hoặc của bất kỳ phương pháp nào khác được sử dụng để khơi gợi quá trình này.
Bảng 1. Đặc điểm bệnh nhân, cơ học hô hấp và khả năng huy động của phổi
|
|
All (n = 24) |
High Recruiters (n = 12) |
Low Recruiters (n = 12) |
P Value |
|
Age, yr |
69 (62 to 73) |
67 (60 to 73) |
70 (63 to 74) |
0.325 |
|
Sex, M, n (%) |
20 (83) |
11 (92) |
9 (75) |
0.590 |
|
Body mass index, kg/m2 |
31 (27 to 34) |
31 (29 to 33) |
29 (25 to 34) |
0.347 |
|
Preexisting conditions, n (%) |
|
|
|
|
|
COPD |
3 (13) |
2 (17) |
1 (8) |
>0.999 |
|
Hypertension |
11 (46) |
6 (50) |
5 (42) |
>0.999 |
|
Diabetes |
12 (46) |
6 (50) |
6 (50) |
>0.999 |
|
Ischemic heart disease |
2 (8) |
1 (8) |
1 (8) |
>0.999 |
|
SAPS II score |
40 (31 to 44) |
37 (31 to 43) |
41 (31 to 46) |
0.840 |
|
Delay between intubation and inclusion, h |
8 (4 to 16) |
9 (4 to 16) |
8 (5 to 13) |
0.728 |
|
PaO2/FIO2 at inclusion, mm Hg |
136 (99 to 166) |
111 (92 to 160) |
144 (117 to 179) |
0.141 |
|
Severity of ARDS, n (%) |
|
|
|
0.187 |
|
Mild |
2 (8) |
0 (0) |
2 (17) |
— |
|
Moderate |
15 (63) |
7 (58) |
8 (67) |
— |
|
Severe |
7 (29) |
5 (42) |
2 (17) |
— |
|
Fluid balance from admission, L |
−2.0 (−2.0 to 1.1) |
0.8 (−1.7 to 1.2) |
−0.2 (−2.3 to 0.1) |
0.219 |
|
Baseline respiratory data |
|
|
|
|
|
VT, ml/kg (PBW) |
6.0 (5.8 to 6.1) |
5.9 (5.8 to 6.1) |
6.0 (5.8 to 6.1) |
0.620 |
|
Respiratory rate, cycles/min |
25 (22 to 28) |
25 (23 to 28) |
25 (22 to 28) |
0.726 |
|
PEEP, cm H2O |
12 (10 to 15) |
15 (10 to 15) |
12 (10 to 13) |
0.272 |
|
Auto-PEEP, cm H2O |
1.0 (0.6 to 1.0) |
1.0 (0.5 to 1.0) |
1.0 (0.6 to 1.0) |
0.650 |
|
Pplat, cm H2O |
24 (22 to 27) |
24 (22 to 27) |
24 (21 to 27) |
0.907 |
|
Crs, ml/cm H2O |
34 (29 to 48) |
42 (33 to 47) |
32 (29 to 36) |
0.076 |
|
Ventilatory ratio† |
1.47 (1.24 to 1.88) |
1.58 (1.40 to 2.16) |
1.29 (1.17 to 1.53) |
0.198 |
|
Respiratory data at PEEP 5 and 15 cm H2O |
|
|
|
|
|
AOP > 5 cm H2O, n (%) |
8 (33) |
4 (33) |
4 (33) |
1.000 |
|
ΔSpO2/FIO2‡ |
11 (4 to 16) |
11 (4 to 16) |
10 (2 to 16) |
0.788 |
|
Vrec, ml |
226 (117 to 356) |
347 (227 to 546) |
120 (76 to 212) |
|
|
Vrec, ml/kg(PBW) |
3.9 (1.9 to 4.6) |
4.5 (3.5 to 7.3) |
2.1 (1.3 to 3.4) |
|
|
Crs at PEEP 5 cm H2O |
37 (29 to 42) |
39 (31 to 47) |
35 (26 to 40) |
0.311 |
|
Crs at PEEP 15 cm H2O |
31 (24 to 40) |
39 (29 to 47) |
26 (23 to 31) |
0.012 |
|
Crec, ml/cm H2O |
22 (11 to 32) |
32 (24 to 50) |
12 (8 to 21) |
|
|
R/I ratio |
0.70 (0.49 to 0.81) |
0.80 (0.74 to 1.20) |
0.48 (0.20 to 0.57) |
|
|
LUS score at PEEP 5 cm H2O |
24 (22 to 25) |
24 (23 to 25) |
24 (22 to 26) |
0.594 |
|
LUS score at PEEP 15 cm H2O |
21 (20 to 23) |
20 (19 to 22) |
22 (21 to 23) |
0.170 |
|
ΔLUS score§ |
3 (1 to 4) |
4 (3 to 6) |
2 (0 to 3) |
0.012 |
|
Anterior lung regions |
1 (0 to 2) |
2 (0 to 2) |
1 (0 to 2) |
0.633 |
|
Lateral lung regions |
0 (0 to 1) |
1 (0 to 2) |
0 (0 to 1) |
0.077 |
|
Posterior lung regions |
1 (0 to 1) |
1 (1 to 2) |
0 (0 to 1) |
0.009 |
|
LUS reaeration score |
3 (1 to 5) |
4 (3 to 6) |
2 (0 to 3) |
0.017 |
|
Anterior lung regions |
1 (0 to 2) |
2 (0 to 3) |
1 (0 to 2) |
0.593 |
|
Lateral lung regions |
0 (0 to 1) |
1 (0 to 3) |
0 (0 to 1) |
0.084 |
|
Posterior lung regions |
1 (0 to 1) |
1 (1 to 2) |
0 (0 to 1) |
0.009 |
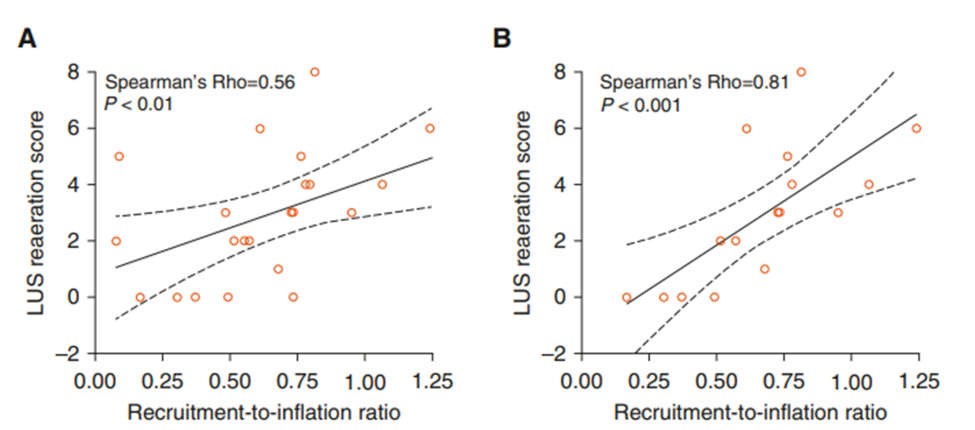
Hình 1. Tương quan giữa tỷ lệ huy động trên bơm phồng (R/I) và điểm tái thông khí trên siêu âm phổi (LUS). (A và B) Đường liên tục cho thấy hồi quy tuyến tính (với khoảng tin cậy 95% ở các đường đứt nét) giữa tỷ lệ R/I và điểm tái thông khí LUS ở 24 bệnh nhân mắc bệnh coronavirus (COVID-19) – hội chứng suy hô hấp cấp tính gây ra có và không có áp lực mở đường thở (AOP)> 5 cm H2O (A) và ở 16 bệnh nhân không có AOP> 5 cm H2O (B). Lưu ý, tỷ lệ R/I là một biến số liên tục, trong khi điểm số hiệu chỉnh lại LUS là một biến số rời rạc trong hồi quy tuyến tính.
Thực tế là độ giãn nở của hệ thống hô hấp ở nhóm trước cao hơn so với nhóm sau, và tỷ lệ thông khí, một dấu hiệu của khoảng chết, không khác nhau giữa hai nhóm, lập luận chống lại một siêu bơm phồng đáng kể.
Trong nghiên cứu của Chen và các đồng nghiệp ở ARDS không COVID-19, tỷ lệ R/I phân biệt người huy động với người không huy động, tương ứng với giá trị trung bình của nhóm thuần tập của họ, là 0,5. Trong nghiên cứu này, giá trị trung bình của tỷ lệ R/I là 0,7, được sử dụng để phân tích. Tuy nhiên, chúng tôi đã tìm thấy kết quả tương tự ở ngưỡng 0,5 (dữ liệu không được hiển thị).
Nghiên cứu của chúng tôi bị hạn chế bởi thực tế là nó chỉ tập trung vào một trung tâm và phương pháp tiêu chuẩn vàng để đánh giá huy động phổi (tức là, chụp cắt lớp vi tính định lượng) đã không được sử dụng. Ngoài ra, chúng tôi không thể loại trừ rằng PEEP lớn hơn 15 cm H2O có thể đã huy động phổi ở một số người huy động thấp. Tuy nhiên, phát hiện của chúng tôi xác nhận các báo cáo trước đây về tính khả thi của phép đo tỷ số R/I trong COVID-19 (6–8). Hơn nữa, các phép đo không được lặp lại theo thời gian vì có thể khả năng huy động sẽ thay đổi. Đây sẽ là mục đích của các nghiên cứu sâu hơn.
References
COVID-ICU Group on behalf of the REVA Network and the COVID-ICU Investigators. Clinical characteristics and day-90 outcomes of 4244 critically ill adults with COVID-19: a prospective cohort study. Intensive Care Med 2021;47:60–73.
Turbil E, Terzi N, Cour M, Argaud L, Einav S, Guérin C. Positive end-expiratory pressure-induced recruited lung volume measured by volume-pressure curves in acute respiratory distress syndrome: a physiologic systematic review and meta-analysis. Intensive Care Med 2020;46:2212–2225.
Schultz MJ. High versus low PEEP in non-recruitable collapsed lung tissue: possible implications for patients with COVID-19. Lancet Respir Med 2020;8:e44.
Bouhemad B, Brisson H, Le-Guen M, Arbelot C, Lu Q, Rouby JJ. Bedside ultrasound assessment of positive endexpiratory pressure-induced lung recruitment. Am J Respir Crit Care Med 2011;183:341–347.
Chiumello D, Mongodi S, Algieri I, Vergani GL, Orlando A, Via G, et al. Assessment of lung aeration and recruitment by CT scan and ultrasound in acute respiratory distress syndrome patients. Crit Care Med 2018;46:1761– 1768.
Chen L, Del Sorbo L, Grieco DL, Junhasavasdikul D, Rittayamai N, Soliman I, et al. Potential for lung recruitment estimated by the recruitment-to-inflation ratio in acute respiratory distress syndrome: a clinical trial. Am J Respir Crit Care Med 2020;201:178–187.
Pan C, Chen L, Lu C, Zhang W, Xia JA, Sklar MC, et al. Lung recruitability in COVID-19-associated acute respiratory distress syndrome: a single-center observational study. Am J Respir Crit Care Med 2020;201:1294–1297.
Beloncle FM, Pavlovsky B, Desprez C, Fage N, Olivier PY, Asfar P, et al. Recruitability and effect of PEEP in SARS-Cov-2-associated acute respiratory distress syndrome. Ann Intensive Care 2020;10:55.
Ranieri VM, Rubenfeld GD, Thompson BT, Ferguson ND, Caldwell E, Fan E, et al.; ARDS Definition Task Force. Acute respiratory distress syndrome: the Berlin definition. JAMA 2012;307:2526–2533.
Zieleskiewicz L, Markarian T, Lopez A, Taguet C, Mohammedi N, Boucekine M, et al.; AZUREA Network. Comparative study of lung ultrasound and chest computed tomography scan in the assessment of severity of confirmed COVID-19 pneumonia. Intensive Care Med 2020;46:1707–1713.