Case 41
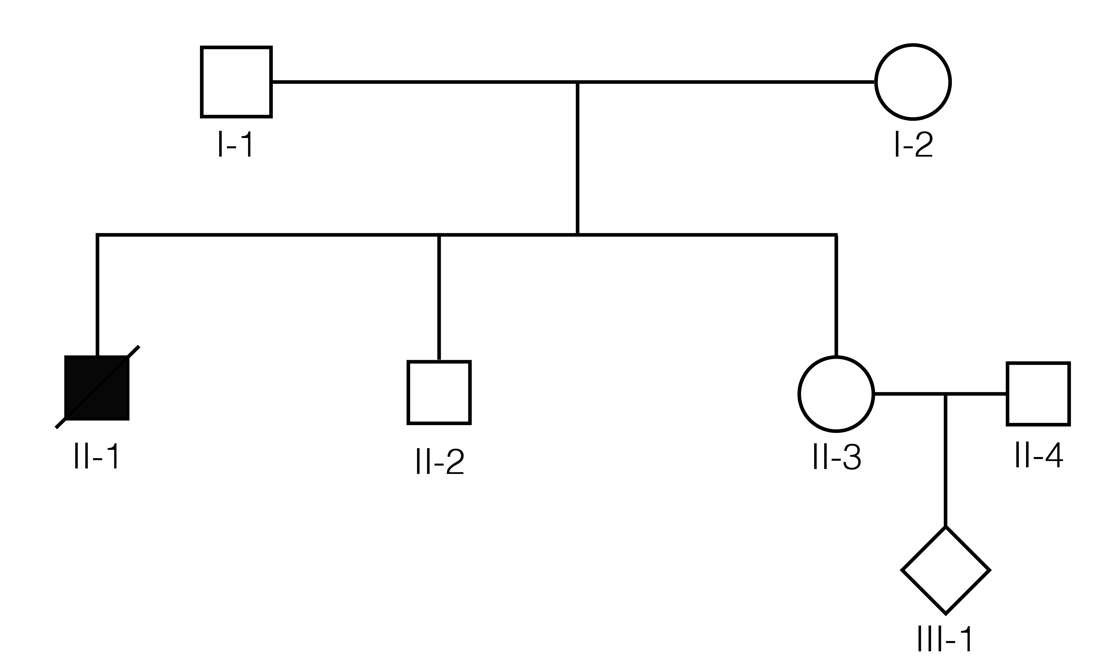
Bệnh nhân nữ 34 tuổi (II-3 trong phả hệ sau) mang thai 12 tuần. Cô ấy có người anh trai (II-1) chết do xuất huyết sơ sinh và hiện tượng đó được cho rằng do thiếu hụt Protein C.
Dưới đây là phả hệ gia đình:
Kết quả định lượng Protein C của các thành viên trong gia đình như sau:
|
Bệnh nhân |
Protein C (Chromogenic) |
Khoảng tham chiếu |
|
I-1 |
54 U/dL |
65 – 135 U/dL |
|
I-2 |
79 U/dL |
|
|
II-1 |
54 U/dL |
|
|
II-2 |
53 U/dL |
|
|
II-3 |
75 U/dL |
|
|
II-4 |
82 U/dL |
Câu hỏi 1: Nhận xét các kết quả trên. Bạn cần thêm xét nghiệm gì?
Bạn yêu cầu xét nghiệm Protein C bằng phương pháp cục đông, có kết quả như sau:
|
Bệnh nhân |
Protien C (Chromogenic) |
Protein C (Clotting) |
Khoảng tham chiếu |
|
|
I-1 |
54 U/dL |
51 U/dL |
|
|
|
I-2 |
79 U/dL |
53 U/dL |
||
|
II-1 |
54 U/dL |
|||
|
65 – 135 U/dL |
||||
|
II-2 |
53 U/dL |
51 U/dL |
||
|
|
||||
|
II-3 |
75 U/dL |
50 U/dL |
||
|
II-4 |
82 U/dL |
85 U/dL |
Câu hỏi 2: Tại sao có sự khác biệt kết quả Protein C giữa 2 phương pháp?
Câu hỏi 3: Xác suất em bé III-1 sinh ra với bệnh thiếu hụt Protein C đồng hợp tử là bao nhiêu?
Mẹ em bé và người bạn đơi không có quan hệ huyết thống và tỉ lệ thiếu hụt Protein C dị hợp tử là 1/1000 (giả dụ).
Câu hỏi 4: Xác suất em bé III- 1 bị thiếu hụt Protein C đồng hợp tử là bao nhiêu nếu II -4 có Protein C giảm thấp do dị hợp tử đột biến gây thiếu Protein C.
Đáp án
Câu hỏi 1: Nhận xét các kết quả trên. Bạn cần thêm xét nghiệm gì?
Kết quả định lượng Protein C bằng phương pháp Chromogenic không ủng hộ cho chẩn đoán thiếu hụt Protein C ở bệnh nhân tử vong do xuất huyết sơ sinh (II-1).
Bạn nên chỉ định:
a/Định lượng Protein C bằng phương pháp cục đông.
b/Protein S.
Câu hỏi 2: Tại sao có sự khác biệt kết quả Protein C giữa 2 phương pháp?
Xét nghiệm cục đông cho kết quả ủng hộ cho chẩn đoán thiếu hụt Protein C ở II-1. Xét nghiệm Chromogenic không xác định được các đột biến ở vùng GLA của Protein C (hoặc các serine proteases tương tự khác).
Câu hỏi 3: Xác suất em bé III-1 sinh ra với bệnh thiếu hụt Protein C đồng hợp tử là bao nhiêu?
Mẹ em bé và người bạn đơi không có quan hệ huyết thống và tỉ lệ thiếu hụt Protein C dị hợp tử là 1/1000 (giả dụ).
Từ phân tích phả hệ, suy ra khả năng II-3 mang gen dị hợp tử bệnh thiếu hụt Protein C là 2/3. Kết quả Protein C của II-3 có vẻ phù hợp với giả thuyết II-3 mang gen dị hợp tử. Bởi vì kết quả Protein C thấp ở phương pháp cục đông nhưng bình thường ở phương pháp GLA cho nên đột biến có thể nằm trên miền GLA của gen Protein C (PROC).
Do vậy khả năng có em bé bị đồng hợp tử Protein C là 1/2 x 1/1000 = 1/2000.
Câu hỏi 4: Xác suất em bé III- 1 bị thiếu hụt Protein C đồng hợp tử la bao nhiêu nếu II -4 có Protein C giảm thấp do dị hợp tử đột biến gây thiếu Protein C.
Trong trường hợp này, xác xuất III-1 đồng hợp tử gen gây thiếu hụt Protein C là 1/2 x 1/2 = 1/4.
|
Tóm tắt: Đây là trường hợp thiếu hụt Protein C, nguyên nhân do 2 đột biến riêng biệt trên gen PROC (2 đột biến dị hợp tử) dẫn đến sự khác biệt kết quả Protein C bằng phương pháp Chromogenic và phương pháp cục đông |
Case 42
Bệnh nhân nữ 23 tuổi được đưa tới bạn với tiền sử thuyên tắc mạch phổi xuất hiện sau một chuyến bay đường dài 6 tháng trước.
Kết quả sàng lọc đông máu như sau (bệnh nhân không sử dụng thuốc kháng đông trong thời gian xét nghiệm)
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
AT act |
92 U/dL |
>78 U/dL |
|
Protein C act |
34 U/dL |
>63 U/dL |
|
Protein S act |
35 U/dL |
>60 U/dL |
|
Lupus anticoagulant |
Not detected |
– |
|
IgG anti-β2 GP1 antibody |
2.9 units/mL |
1-6 units/mL |
|
IgG Anticardiolipin antibody |
6.2 units/mL |
|
|
PT |
13 s |
11 -14 s |
|
APTT |
33 s |
23 -35 s |
|
Fibrinogen |
2.7 g/L |
1.5 -4.0 g/L |
Câu hỏi 1: Chẩn đoán là gì?
Câu hỏi 2: Bạn cần thêm xét nghiệm gì và tại sao?
Đáp án
Câu hỏi 1: Chẩn đoán là gì?
Xét nghiệm đông máu thấy giảm nồng độ Protein C và Protein S. Điều quan trọng cần lưu ý: đây là xét nghiệm Protein C và Protein S hoạt tính. Thiếu hụt kết hợp Protein C và Protein S hiếm gặp và có một số nguyên nhân sau:
a/Thiếu vitamin K, tuy nhiên PT bình thường do vậy nguyên nhân này có thể loại trừ. Hơn nữa, bệnh nhân đang không sử dụng các thuốc chống đông máu.
b/Thiếu Protein C và Protein S thật sự.
c/Kết quả dương tính giả do đột biến FV Leiden.
Câu hỏi 2: Bạn cần thêm xét nghiệm gì và tại sao?
Sàng lọc kháng Protein C hoạt hóa (APCr) và Factor V Leiden. Trong thực hành, hầu hết các phòng xét nghiệm cũng sàng lọc đột biến Prothrombin G20210A bởi vì xét nghiệm này thường kết hợp với xét nghiệm Factor V Leiden.
Xét nghiệm cho kết quả đồng hợp tử đột biến Factor V Leiden và dẫn đến giảm Protein C và Protein S. Xét nghiệm Chromogenic Protein C và xét nghiệm miễn dịch Protein S cho kết quả bình thường.
|
Tóm tắt: Đây là trường hợp đồng hợp tử đột biến Factor V Leiden dẫn đến nồng độ Protein C và Protein hoạt tính S giảm giả. |
Case 43
Bệnh nhân nam 34 tuổi tới khám tại khoa cấp cứu với triệu chứng đau chân trái 2 ngày. Bạn nghi ngờ bệnh nhân có huyết khối tĩnh mạch sâu (DVT) và chỉ định cho bệnh nhân được siêu âm, kết quả siêu âm khẳng định tình trạng DVT.
Trước khi kê thuốc chống đông, bạn yêu cầu các xét nghiệm đông máu và có kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
PT |
13 s |
11.5 – 13 s |
|
APTT |
22 s |
28 – 34 s |
|
Fibrinogen (Clauss) |
4.1 g/L |
2.0 – 4.0 g/L |
|
PLT |
356 x 109/L |
150 – 400 x 109/L |
Câu hỏi 1: Bạn cần hỏi thêm ở bệnh nhân những thông tin gì?
Câu hỏi 2: Bạn sẽ chỉ định thêm các xét nghiệm gì?
Không có yếu tố nguy cơ nào rõ ràng có thể gợi ra lý do tại sao xuất hiện DVT. Tuy nhiên anh trai của bệnh nhân và cậu (anh/em của mẹ) có tiền sử unprovoked DVTs.
Bạn nghi ngờ kết quả APTT ngắn (22 s) cho chỉ định xét nghiệm lại, có kết quả tương tự (21.5 s).
Câu hỏi 3: Bạn sẽ chỉ định thêm xét nghiệm gì để làm rõ nguyên nhân APTT ngắn?
Bạn yêu cầu xét nghiệm FVIII, FIX, FXI và FXII.
Kết quả FIX tăng cao (6.56 IU/mL – bình thường là 0.5 -1.5 IU/mL). Các yếu tố khác bình thường.
Câu hỏi 4: Bạn nghĩ trường hợp này có thể giải thích như thế nào?
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Đáp án
Câu hỏi 1: Bạn cần hỏi thêm ở bệnh nhân những thông tin gì?
Bạn cần tìm hiểu liệu có các yếu tố nguy cơ thúc đẩy phát triển DVT ở bệnh nhân hay không. Điều này rất quan trọng để xác định bệnh nhân có cần dùng thuốc chống đông máu kéo dài hay không?
Câu hỏi 2: Bạn sẽ chỉ định thêm các xét nghiệm gì?
Bạn nên xác định xem có tiền sử gia đình về bệnh huyết khối tĩnh mạch hay tiềm ẩn bệnh huyết khối tĩnh mạch hay không. Điều này sẽ giúp bạn xác định liệu có bất thường di truyền trong gia đình hay không.
Bạn cần chú ý rằng APTT ngắn và nên yêu cầu lặp lại xét nghiệm này để khẳng định kết quả.
Câu hỏi 3: Bạn sẽ chỉ định thêm xét nghiệm gì để làm rõ nguyên nhân APTT ngắn?
APTT ngắn thường do tăng nồng độ FVIII hoặc FIX, bạn nên chỉ định xét nghiệm yếu tố đông máu.
Câu hỏi 4: Bạn nghĩ trường hợp này có thể giải thích như thế nào?
Xét nghiệm FIX tăng cao rõ rệt và xét nghiệm này nên được lặp lại để khẳng định kết quả. Nguyên nhân của hiện tượng FIX tăng cao có thể được giải thích bằng phân tích đột biến gen F9.
Phân tích trình tự gen F9 ở bệnh nhân này và sau đó là các thành viên trong gia đình có biểu hiện, xác định đột biến tại vị trí 338 trong đó Arginine bị thay bằng Leucine (R338L). Xét nghiệm FIX bằng phương pháp miễn dịch (FIX: Antigen) bình thường và do vậy đây là đột biến tăng chức năng, được gọi là FIX Padua. Vùng này của FIX rất quan trọng trong việc gắn với FX và đột biến này làm tăng hiệu quả của việc gắn này.
Câu hỏi 5: Bạn sẽ điều trị bệnh nhân này như thế nào?
Bệnh nhân này có unprovoked DVT và nguyên nhân là bất thường tiền yếu tố đông máu. Nguy cơ tái phát DVT tăng rõ ràng và bệnh nhân nên được duy trì thuốc chống đông suốt đời.
|
Tóm tắt: Đây là trường hợp huyết khối tĩnh mạch sâu (DVT) do đột biến tăng chức năng trên gen F9. |
Case 44
Bệnh nhân nữ 42 tuổi có tiền sử 5 lần sảy thai liên tiếp trong quý đầu thai kỳ. Bệnh nhân được sàng lọc kháng thể kháng phospholoipid và có kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
Silica Clotting time |
1.12 |
|
|
dRVVT |
1.09 |
|
|
IgG antiCardiolipin antibidy |
3.2 GPLU/mL |
1-12 GPLU/mL |
|
IgM antiCardiolipin antibidy |
5.3 GPLU/mL |
1-9 GPLU/mL |
Câu hỏi 1: Bạn cần chỉ định thêm xét nghiệm gì?
Bạn yêu cầu xét nghiệm kháng thể IgG anti-β2 glycoprotein. Kết quả là 221 units/mL với khoảng tham chiếu là 1-6 units/mL.
Câu hỏi 2 : Bạn giải thích các kết quả này như thế nào ?
Câu hỏi 3 : Bạn sẽ kiểm soát lần mang thai tiếp theo cho bệnh nhân như thế nào ?
Đáp án
Câu hỏi 1: Bạn cần chỉ định thêm xét nghiệm gì?
Tiền sử của bệnh nhân gợi ý hội chứng kháng phosphilid (APS) và do vậy, nên chỉ định các xét nghiệm sàng lọc kháng đông Lupus bằng 2 phương pháp : phương pháp dựa trên APTT và phương pháp dựa vào dRVVT. Các xét nghiệm này đều cho kết quả âm tính.
Nồng độ kháng thể Anti-Cardiolipin không tăng. Tuy nhiên anti-β2 glycoprotein chưa được thực hiện, do vậy cần chỉ định xét nghiệm này.
Câu hỏi 2 : Bạn giải thích các kết quả này như thế nào ?
Nồng độ IgG anti-β2 glycoprotein tăng cao và cần được xét nghiệm lại để khẳng định. Xét nghiệm lặp lại cho kết quả tương tự. Xét nghiệm kháng thể anti-Cardiolipin sử dụng một kháng nguyên có nguồn gốc từ bò trong khi xét nghiệm anti-β2 glycoprotein sử dụng β2 glycoprotein người tái tổ hợp, và có sự khác nhau chút ít về epitope giữa 2 loại này. Trong một số trường hợp, như ở bệnh nhân này, có thể có kháng thể kháng lại β2 glycoprotein người nhưng không kháng lại anti-β2 glycoprotein bò như trong xét nghiệm antiCardiolipin.
Câu hỏi 3 : Bạn sẽ kiểm soát lần mang thai tiếp theo cho bệnh nhân như thế nào ?
Sẽ có giá trị nếu ANA và ENA được xét nghiệm đê loại trừ sự có mặt của kháng thể Anti_Ro. Kháng thể này có thể liên quan đến tim bẩm sinh ở trẻ nhỏ.
Bệnh nhân này cần được điều trị Heparin trọng lượng phân tử thấp (LMWH) và Aspirin liều thấp trong thời gian mang thai, phù hợp với các hướng dẫn điều trị APS ở phụ nữ mang thai. Cần có sự kết hợp chặt chẽ giữa bác sĩ sản khoa và bác sĩ nhi sơ sinh khi bệnh nhân sinh con.
|
Tóm tắt: Đây là trường hợp sảy thai nhiều lần do sự có mặt của kháng thể anti-β2 glycoprotein. |
Case 45
Bệnh nhân nam 83 tuổi được làm xét nghiệm do nghi ngờ bệnh lý ác tính đại tràng. Tiền sử y khoa của bệnh nhân và tiền sử gia đình không có gì đặc biệt.
Bệnh nhân được làm xét nghiệm đông máu và cho kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
PT |
13 s |
11 – 14 s |
|
APTT |
66 s |
25 – 35 s |
|
Fibrinogen (Clauss) |
2.7 g/L |
1.5 – 4.0 g/L |
|
PLT |
204 x 109/L |
150 – 400 x 109/L |
Câu hỏi 1: Nhân xét các kết quả trên và bạn cần chỉ định thêm xét nghiệm nào?
Kết quả xét nghiệm FVIII, IX, XI, XII bình thường.
Bạn yêu cầu xét nghiệm kháng đông Lupus, kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
Silica Clotting time (SCT) |
2.77 |
|
|
SCT + PL |
39% |
|
|
dRVVT |
2.01 |
|
|
dRVVT + PL |
44.1% |
Câu hỏi 2: Nhận xét các kết quả trên?
Bác sĩ ngoại khoa băn khoăn về nguy cơ chảy máu do APTT kéo dài.
Câu hỏi 3: Bạn đưa ra lời khuyên gì cho bác sĩ ngoại khoa?
Câu hỏi 4: Các bệnh nhân có kháng đông Lupus có nguy cơ chảy máu không và tại sao?
Câu hỏi 5: Tiêu chuẩn sử dụng để xác định kháng đông Lupus?
Đáp án
Câu hỏi 1: Nhân xét các kết quả trên và bạn cần chỉ định thêm xét nghiệm nào?
Có hiện tượng APTT kéo dài nhưng bệnh nhân không có tiền sử y khoa hoặc tiền sử gia đình nào đáng chú ý. Có vẻ như không phải là các bất thường bẩm sinh, tuy nhiên sẽ có giá trị nếu thực hiện các đánh giá chuẩn. Trong trườn hợp APTT kéo dài và không có tiền sử chảy máu có ý nghĩa, có thể nghĩ tới các nguyên nhân sau: a/ Bệnh lý chảy máu mắc phải, ví dụ có chất ức chế FVIII. b/ Kháng đông Lupus.
Sẽ là phù hợp nếu bạn nên chỉ định xét nghiệm yếu tố VIII, IX, XI, XII và kháng đông Lupus. Mặc dù thiếu FXII thường không liên quan với các biểu hiện chảy máu, tuy nhiên nó có thể làm APTT kéo dài, và vì vậy nên xét nghiệm để loại trừ.
Một số phòng xét nghiệm có thể lặp lại xét nghiệm APTT sử dụng hóa chất không nhạy với Lupus. Nếu có mặt kháng đông Lupus thì APTT sẽ trở về bình thường – sau đó các xét nghiệm sàng lọc kháng đông Lupus nên được thực hiện. Phòng xét nghiệm nên sử dụng thuốc thử APTT nhạy với kháng đông Lupus khi sàng lọc kháng thể này, đó là thuốc thử APTT có nồng độ thấp phospholipid.
Câu hỏi 2: Nhận xét các kết quả trên?
Các xét nghiệm sàng lọc kháng đông Lupus cho thấy SCT kéo dài và dRVVT kéo dài kể cả sau khi đã bổ sung phospholipid ngoại sinh, khẳng định sự có mặt của kháng thể kháng phospholipid, đó là kháng đông Lupus.
Sẽ rất có ích nếu sàng lọc kháng thể Anti-Cardiolipin và kháng thể Anti2GPI và các nguyên nhân khác gây kháng đông Lupus (ví dụ ANA), tuy nhiên nguyên nhân ác tính cũng được xác định là nguyên nhân gây kháng đông Lupus.
Câu hỏi 3: Bạn đưa ra lời khuyên gì cho bác sĩ ngoại khoa?
Nguy cơ chảy máu rất thấp nhưng nguy cơ tăng đông tiềm ẩn rất đáng chú ý do khả năng bệnh đại tràng ác tính. Điều trị dự phòng chống đông nên được thực hiện ở bệnh nhân này.
Câu hỏi 4: Các bệnh nhân có kháng đông Lupus có nguy cơ chảy máu không và tại sao?
Các bệnh nhân có kháng đông Lupus nói chung sẽ tăng nguy cơ tắc mạch (cả động mạch và tĩnh mạch) nhiều hơn là nguy cơ chảy máu. Tuy nhiên, các bệnh nhân này cũng thường có tiểu cầu giảm và trong một số trường hợp có giảm FII, và chảy máu nếu có là do lý do này. Xét nghiệm PT của bệnh nhân bình thường, tuy nhiên thuốc thử PT thường có nồng độ cao Phospholipid và có thể trung hòa các kháng đông Lupus yếu. Nếu có bất kể vấn đề gì gợi ý các rối loạn chảy máu hoặc bất kỳ băn khoăn nào khác thì xét nghiệm FII nên được thực hiện.
Câu hỏi 5: Tiêu chuẩn sử dụng để xác định kháng đông Lupus?
Tiêu chuẩn để định nghĩa sự có mặt của kháng đông Lupus là:
a/Kéo dài các xét nghiệm đông máu phụ thuộc phospholipid.
b/Chứng minh sự có mặt của chất ức chế ở xét nghiệm Mixtest.
c/Chứng minh sưj phụ thuộc phospholipid của chất ức chế.
|
Tóm tắt: Đây là trường hợp APTT kéo dài do sự có mặt của kháng đông Lupus |
Case 46
Bệnh nhân nam 4 tuổi nhập viện do Purpura Fulminans.
Trẻ được làm các xét nghiệm đông máu và cho kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
AT act |
109 U/dL |
>78 U/dL |
|
Protein C act |
82 U/dL |
>63 U/dL |
|
Protein S act |
2 U/dL |
>60 U/dL |
|
Free Protein S Antigen |
3 U/dL |
>61 U/dL |
|
APCr |
2.3 |
>2.20 |
|
Prothrombin G20210A |
G/G (Wild Type Sequence) |
– |
|
PT |
19 s |
11 – 14 s |
|
APTT |
42 s |
25 – 35 s |
|
Fibrinogen (Clauss) |
1.1 g/L |
1.5 – 4.0 g/L |
|
PLT |
82 x 109/L |
150 – 400 x 109/L |
Câu hỏi 1: Các kết quả xét nghiệm trên gợi ý điều gì?
Câu hỏi 2 : Bạn cần thêm thông tin hoặc xét nghiệm gì?
Tiền sử duy nhất đáng chú ý là gần đây bệnh nhân có ban dạng phỏng nước, phù hợp với chẩn đoán thủy đậu (Varicella Zoster).
Câu hỏi 3: Điều này có ý nghĩa gì không?
Đáp án
Câu hỏi 1: Các kết quả xét nghiệm trên gợi ý điều gì?
Xét nghiệm đông máu cho thấy giảm Protein S antigen tự do đồng thời giảm Protein S hoạt tính, phù hợp với tình trạng thiếu hụt Protein S. Thêm nữa, PT và APTT kéo dài cùng với giảm Fibrinogen và giảm tiểu cầu – các xét nghiệm này phù hợp với chẩn đoán DIC.
Câu hỏi 2 : Bạn cần thêm thông tin hoặc xét nghiệm gì?
Lặp lại xét nghiệm Protein S. Sàng lọc chất ức chế Protein S nên được thực hiện. Điều này tương tự như sàng lọc chất ức chế FVIII, trộn huyết tương bệnh nhân và huyết tương bình thường tỉ lệ tương đương , ủ và đo nồng độ Protein S trên hỗn hợp MIX. Nếu nồng độ Protein S của MIX giảm thì gợi ý có chất ức chế Protein S. Nồng độ chất ức chế có thể định lượng bằng xét nghiệm tương tự xét nghiệm Bethesda nhưng là đo nồng độ Protein S chứ không phải nồng độ FVIII.
Mức Protein S thấp không có nghĩa là bệnh thiếu hụt Protein S bẩm sinh nhưng có thể quan trọng, định hướng việc tìm hiểu tiền sử gia đình hoặc tiền sử y khoa của bệnh nhân có gì đáng chú ý hay không.
Câu hỏi 3: Điều này có ý nghĩa gì không?
Thiếu hụt Protein S thứ phát sau nhiễm trùng virus thủy đậu (Varicella Zoster) đã được báo cáo mặc dù đây là một biến chứng hiếm gặp. Điều trị rất đa dạng bao gồm truyền plasma hoặc trao đổi huyết tương, thuốc chống đông và thuốc kháng virus.
|
Tóm tắt: Đây là trường hợp thiếu hụt Protein S thứ phát sau nhiễm virus thủy đậu (Varicella Zoster). |
Case 47
Một luật sư 39 tuổi được nhập viện do DVT. Một bác sĩ rất nhiệt tình kiểm tra nồng độ Homocysteine tổng của cô ấy và kết quả tăng cao 220µmol/L (khoảng tham chiếu là
Câu hỏi 1: Giải thích hiện tượng này?
Câu hỏi 2: Bạn sẽ hỏi bệnh nhân thêm thông tin gì?
Câu hỏi 3: Bạn cần chỉ định thêm xét nghiệm nào?
Câu hỏi 4: Bạn sẽ điều trị bệnh nhân này như thế nào?
Đáp án
Câu hỏi 1: Giải thích hiện tượng này?
Total Homocysteine (tHcy) tăng cao, việc đầu tiên là lặp lại xét nghiệm này để khẳng định kết quả. Mẫu phân tích Homocysteine cần được thực hiện ngay lập tức sau khi lấy mẫu bởi vì nồng độ chất này có thể tăng cao nếu quá trình xét nghiệm bị trì hoãn.
Câu hỏi 2: Bạn sẽ hỏi bệnh nhân thêm thông tin gì?
Tiền sử gia đình là điều cần chú ý. Bệnh nhân đang sử dụng thuốc gì? Bệnh nhân thuộc dân tộc nào?
Câu hỏi 3: Bạn cần chỉ định thêm xét nghiệm nào?
Bạn cần chỉ định lại xét nghiệm Hcy để khẳng định tình trạng bất thường. Bạn cũng nên xét nghiệm nồng độ vitamin B12, Folate và có thể là vitamin B6. Bạn cũng cần kiểm tra chức năng thận. Các xét nghiệm đặc hiệu hơn của enzym (hoặc xét nghiệm gen) liên quan đến chuyển hóa Hcy cũng nên được cân nhắc, nó có thể cần thiết để xác định nguyên nhân Hcy tăng cao.
Câu hỏi 4: Bạn sẽ điều trị bệnh nhân này như thế nào?
Bạn nên điều trị DVT bằng thuốc chống đông.
Bạn có thể bổ sung Vitamin B12, Folate và B6 cho bệnh nhân bởi vì những vitamin này có thể làm giảm nồng độ Hcy. Trong một số trường hợp, bổ sung chế độ ăn có Betaine có thể làm giảm nồng độ Hcy.
Có thể là Hcy tăng cao do khiếm khuyết một trong các enzym tham gia vào chuyển hóa Hcy. Xét nghiệm gen nên được thực hiện để xác định các bất thường di truyền và thông tin này có thể sử dụng để tư vấn cho các thành viên có liên quan trong gia đình. Có thể là nồng độ Hcy không trở về bình thường sau khi bổ sung vitamin, nếu vậy thì bệnh nhân này nên được điều trị thuốc chống đông lâu dài.
|
Tóm tắt: Đây là trường hợp huyết khối tĩnh mạch sau do tăng Homosysteine máu. |
Case 48
Bệnh nhân nam 45 tuổi tới khoa cấp cứu với triệu chứng sưng đau chân trái. Ông ta được chỉ định siêu âm, xác nhận tình trạng DVT. Bệnh nhân được kê đơn sử dụng Warfarin.
Không có yếu tố nguy cơ nào rõ ràng của việc xuất hiện DVT. Xét nghiệm công thức máu và chức năng thận bình thường.
3 tháng sau bệnh nhân tới phòng khám ngoại trú để xác định xem ông ta có phải sử dụng thuốc chống đông kéo dài hay không. Trong quá trình điều trị, bệnh nhân không có tác dụng phụ nào với Warfarin và đặc biệt, không có chảy máu.
BBệnh nhân đồng ý ngừng Warfarin 4 tuần và được thực hiện xét nghiệm D -dimer. Kết quả D dimer của bệnh nhân là 750ng/ml (khoảng tham chiếu là
Câu hỏi 1: Bệnh nhân có khả năng tái phát DVT hay không?
Câu hỏi 2: Nguy cơ chảy máu trong khi duy trì Warfarin?
Đáp án
Câu hỏi 1: Bệnh nhân có khả năng tái phát DVT hay không?
Điểm DASH ở bệnh nhân này là 4 dựa trên tuổi, giới và D dimer sau 4 tuần ngừng sử dụng Warfarin. Bệnh nhân có 19,9% nguy cơ tái phát VTE hàng năm và lời khuyên là nên duy trì sử dụng Warfarin.
Câu hỏi 2: Nguy cơ chảy máu trong khi duy trì Warfarin?
Nguy cơ chảy máu rất thấp (
|
Tóm tắt: Đây là trường hợp bệnh nhân nam 45 tuổi có tình trạng unprovoked DVT. Nguy cơ tái phát cao, nên sử dụng kháng đông lâu dài. |
Case 49
Bệnh nhân nữ 46 tuổi nhập viện do yêu cầu của bác sĩ phẫu thuật với chẩn đoán huyết khối tĩnh mạch mạc treo. Bệnh nhân được chỉ định các xét nghiệm đông máu, không có thuốc chống đông nào được sử dụng khi bệnh nhân làm xét nghiệm.
Kết quả như sau:
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
PT |
13 s |
11.5 – 13 s |
|
APTT |
33 s |
28 – 34 s |
|
Fibrinogen (Clauss) |
4.1 g/L |
2.0 – 4.0 g/L |
|
PLT |
689 x 109/L |
150 – 400 x 109/L |
Câu hỏi 1: Nhận xét các kết quả trên? Bạn có cần chỉ định thêm xét nghiệm nào nữa không?
Bạn yêu cầu xét nghiệm gen JAK2 và có kêt quả đột biến dị hợp đột biến gen JAK2V617F.
Câu hỏi 2: Điều này có ý nghĩa gì?
Câu hỏi 3: Bạn sẽ điều trị huyết khối tĩnh mạch mạc treo như thế nào?
Đáp án
Câu hỏi 1: Nhận xét các kết quả trên? Bạn có cần chỉ định thêm xét nghiệm nào nữa không?
Các xét nghiệm ban đầu cho thấy số lượng tiểu cầu tăng có thể tiên phát hoặc thứ phát. Ở những bệnh nhân có huyết khối ở các vị trí không thường gặp, đặc biệt huyết khối tĩnh mạch mạc treo, điều quan trọng là sàng lọc các bệnh tăng sinh tủy. Do vậy sàng lọc đột biến gen JAK2 và CALR cần được thực hiện. Trong một số ít trường hợp, bất thường có thể gây ra bởi đột biến gen MPL, THPO và TET2.
Câu hỏi 2: Điều này có ý nghĩa gì?
Các xét nghiệm sau đó tìm thấy đột biến JAK2V617F.
Đột biến JAK2 đã được coi là đột biến nguy cơ cao cho huyết khối tĩnh mạch mạc treo. Trong một số trường hợp, đột biên JAK2 có số lượng tiểu cầu bình thường.
YYếu tố nguy cơ cho việc xuất hiện huyết khối tĩnh mạch mạc treo ở bệnh nhân có tăng sinh tủy bao gồm đột biến JAK2 V617F, tuổi trẻ, giới nữ, và sự có mặt của những bệnh lý huyết khối khác.
Câu hỏi 3: Bạn sẽ điều trị huyết khối tĩnh mạch mạc treo như thế nào? Điều trị thuốc chống đông được chỉ định ở bệnh nhân có rối loạn tăng sinh tủy. Tỉ lệ tái phát cao mặc dù đã sử dụng thuốc chống đông.
|
Tóm tắt: Đây là trường hợp huyết khối tĩnh mạch mạc treo do di hợp tử đột biến JAK2 V617F |
Case 50
Bệnh nhân nam 65 tuổi được nhập viện thay van động mạch chủ sinh học (AVR). Bệnh nhân ổn định trong thời gian sử dụng tuần hoàn ngoài cơ thể, nhưng 3 ngày sau thì có xuất hiện huyết khỗi tĩnh mạch chậu. Bệnh nhân được điều trị Heparin không phân đoạn (UFH) nhưng tiểu cầu bắt đầu giảm và 5 ngày sau điều trị, bệnh nhân có số lượng tiểu cầu 28 x 109/L. Tiểu cầu của bệnh nhân thời điểm sau mổ là 228 x 109/L.
|
Xét nghiệm |
Bệnh nhân |
Khoảng tham chiếu |
|
INR |
1.2 |
1.0 |
|
APTT |
65 s |
28 – 34 s |
|
Fibrinogen (Clauss) |
3.4 g/L |
2.0 – 4.0 g/L |
|
Thrombin time |
>60 s |
11.5 – 13 s |
|
PLT |
28 x 109/L |
150 – 400 x 109/L |
Câu hỏi 1: Điểm 4T của bệnh nhân là bao nhiêu?
Câu hỏi 2: Bạn cần thêm những xét nghiệm gì?
Điểm 4T của bệnh nhân tăng (7) chỉ ra khả năng cao của HIT và bệnh phẩm nên được chuyển ngay lập tức để sàng lọc HIT.
Câu hỏi 3: Các xét nghiệm nào có thể sử dụng để sàng lọc HIT?
Câu hỏi 4: Bạn sẽ điều trị bệnh nhân này như thế nào?
Đáp án
Câu hỏi 1: Điểm 4T của bệnh nhân là bao nhiêu?
Tính điểm 4T dựa vào:
a/Hiện tượng giảm số lượng tiểu cầu (+2)
b/Sử dụng Heparin trong vòng 30 ngày (+2)
c/Tắc mạch mới (+2)
d/Nguyên nhân khác gây giảm tiểu cầu (+1)
Điểm 4T của bệnh nhân là 7. Điểm 4T có giá trị tiên đoán âm cao nhưng có giá trị tiên đoán dương thấp. Khoảng điểm 6 – 8 chỉ ra khả năng cao HIT (≈ 64%).
Câu hỏi 2: Bạn cần thêm những xét nghiệm gì?
Lý giải phù hợp nhất cho tình trạng giảm tiểu cầu và huyết khối tĩnh mạch cậu là HIT (Heparin Induced Thrombocytopaenia) và điều này được ủng hộ bằng việc tăng điểm 4T. Mẫu bệnh phẩm nên được gửi đi để sàng lọc HIT.
Câu hỏi 3: Các xét nghiệm nào có thể sử dụng để sàng lọc HIT?
Ngưng tập tiểu cầu do Heparin :
a/Ngưng tập tiểu cầu bằng phương pháp LTA: Đây là xét nghiệm chức năng tiểu cầu bằng phương pháp LTA tiêu chuẩn sử dụng tiểu cầu bình thường với huyết tương bệnh nhân và Heparin. Tuy nhiên, đô nhạy của xét nghiệm này rất khác nhau (35 – 85%).
Lựa chọn người cho cho xét nghiệm này rất quan trọng bởi vì tiểu cầu đáp ứng với kháng thể HIT rất khác nhau. Kháng thể HIT gây hoạt hóa tiểu cầu tại nồng độ Heparin 0.1 – 0.3 IU/ml và biến mất tại nồng độ Heparin cao (100IU/mL).
Độ nhạy của xét nghiệm có thể tăng khi sử dụng tiểu cầu rửa nhưng yêu cầu kỹ thuật phức tạp
Xét nghiệm này không được khuyến nghị để sàng lọc HIT rộng rãi do độ nhạy không cao.
b/Phương pháp multi-plate cho ngưng tập tiểu cầu trở kháng sử dụng máu toàn phần, là phương pháp cao cấp hơn phương pháp LTA, tương tự xét nghiệm giải phóng Serotonin và được báo cáo có độ nhạy khoảng 90%.
[14C] – Serotonin Release Assay (SRA). Trong xét nghiệm này, tiểu cầu cầu của người cho tải [14C] serotonin được ủ với Heparin và huyết tương bệnh nhân, sau đó đo tỉ lệ Serotonin giải phóng ra. SRA có độ nhạy và độ đặc hiệu 95% nhưng kỹ thuật rất phức tạp và không được khuyến nghị sử dụng.
Xét nghiệm Heparin-Induced Platelet Activation (HIPA). Đây là xét nghiệm chức năng phát hiện kháng Heparin có ý nghĩa lâm sàng. HIPA có độ nhạy tương tự SRA nhưng không được sử dụng rộng rãi.
Xét nghiệm kháng nguyên. Có rất nhiều xét nghiệm sẵn có để đo lượng kháng thể IgG hoặc IgG/IgA/IgM trong các trường hợp nghi ngờ HIT. Nếu dương tính, xét nghiệm Elisa có thể lặp lại sử dụng liều cao Heparin (100 U/ml). Độ ức chế – kết quả dương tính (giảm >50% mật độ quang) là đặc điểm của kháng thể HIT.
Xét nghiệm miễn dịch có độ nhạy cao nhưng độ đặc hiệu thấp và xét nghiệm dương tính mạnh có ý nghĩa hơn dương tính yếu và do vây, khuyến nghị các phòng xét nghiệm trả kết quả dưới dạng OD (mật độ quang), độ ức chế bởi Heparin, điểm cắt của xét nghiệm dương tính, chứ không chỉ đơn thuần báo cáo kết quả dương tính hay âm tính.
Câu hỏi 4: Bạn sẽ điều trị bệnh nhân này như thế nào?
Cần dừng UFH và bệnh nhân có thể sử dụng chất chống đông khác thay thế, có thể là Argatroban và Danaparoid.
|
Tóm tắt: Đây là trường hợp bệnh nhân sau khi sử dụng tuần hoàn ngoài cơ thể thì xuất hiện biến chứng HIT gây ra huyết khỗi tĩnh mạch chậu. |