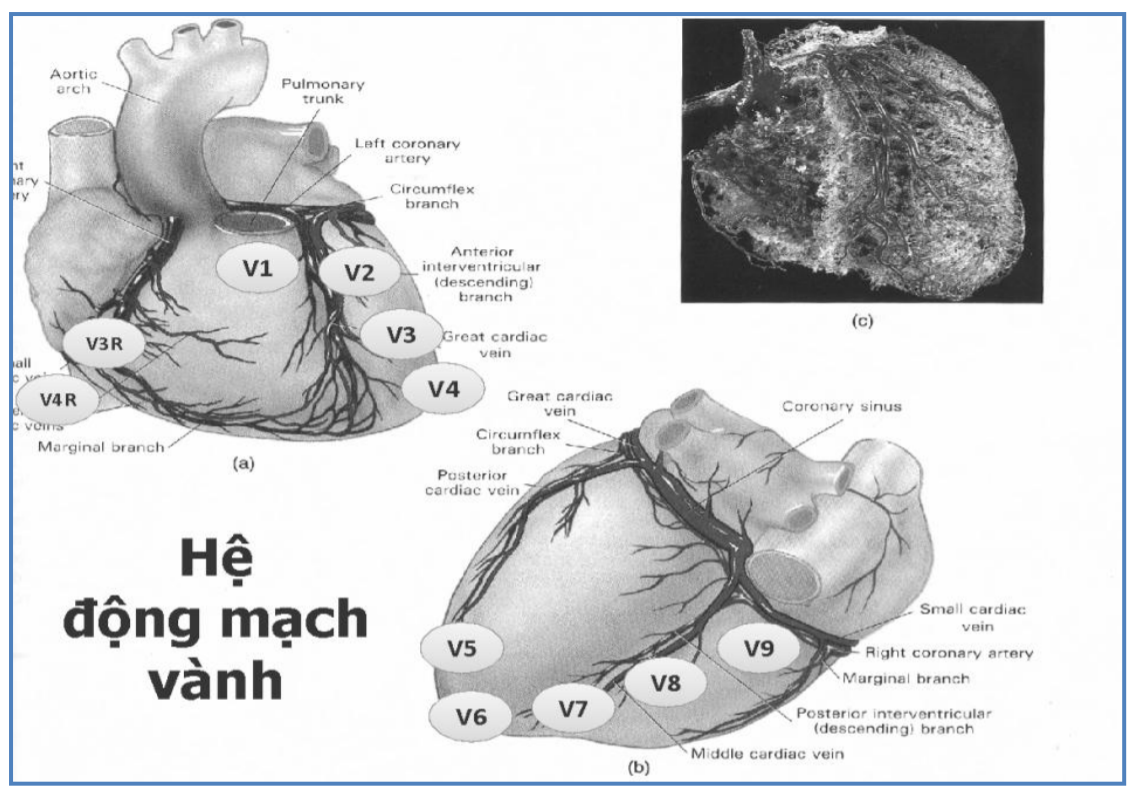
Điện tâm đồ trong bệnh mạch vành
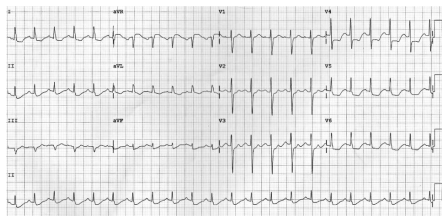
Các chuyển đạo điện tim giúp khảo sát tình trạng thiếu máu cục bộ các vùng cơ tim khác nhau
Mỗi chuyển đạo điện tâm đồ (ngoại biên hay trước tim) đều “nhìn vào” và giúp khảo sát tình trạng thiếu máu cục bộ các vùng cơ tim tương ứng mà nó phản ánh.
Ngoài 12 chuyển đạo điện tâm đồ thông dụng, trong trường hợp cần thiết, chúng ta có thể ghi thêm các chuyển đạo trước tim phải (V3R-V4R) hoặc các chuyển đạo thành sau (V7-V9) để giúp khảo sát rõ hơn tình trạng thiếu máu cục bộ cơ tim.
V1, V2: “nhìn vào” và khảo sát điện học vách liên thất
V3, V4: “nhìn vào” và khảo sát điện học thành trước thất trái
V5, V6: “nhìn vào” và khảo sát điện học thành bên thấp (mỏm) thất trái
DI, aVL: “nhìn vào” và khảo sát điện học thành bên cao thất trái
V7, V8, V9: “nhìn vào” và khảo sát điện học thành sau thất trái
DII, DIII, aVF: “nhìn vào” và khảo sát điện học thành dưới thất trái
V1, V3R, V4R: “nhìn vào” và khảo sát điện học thất phải
Hình 2.1. Lược đồ các chuyển đạo trước tim và vùng cơ tim được khảo sát
Biến đổi điện tâm đồ trong thiếu máu cục bộ cơ tim
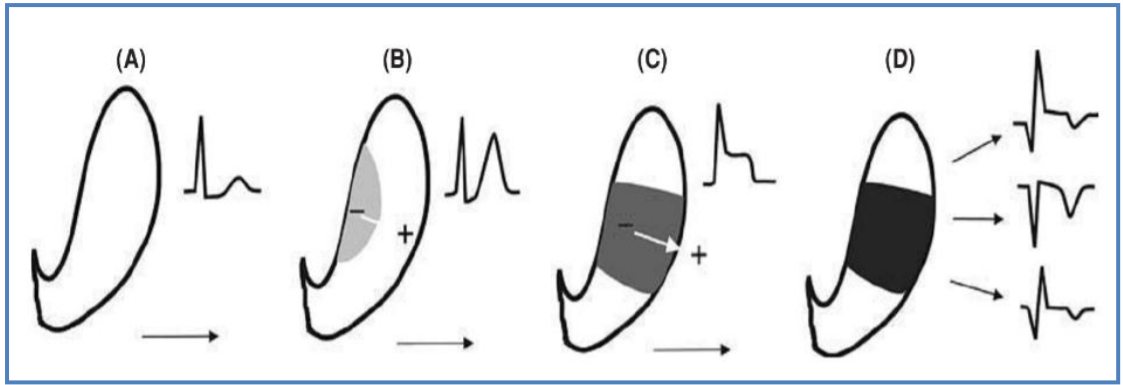
Biến đổi các sóng điện tâm đồ trong thiếu máu cục bộ cơ tim phụ thuộc vào vị trí vùng cơ tim bị tác động (dưới nội tâm mạc, dưới thượng tâm mạc, xuyên thành) và bản chất hay mức độ thiếu máu cục bộ (thiếu máu, tổn thương, hoại tử).
Các biến đổi điện tâm đồ càng có ý nghĩa chẩn đoán bệnh mạch vành khi biến đổi theo thời gian và đặc biệt là xuất hiện trong bệnh cảnh lâm sàng gợi ý (triệu chứng đau thắt ngực/ tăng các enzym sinh học tim như troponin).
Hình 2.2. A: cơ tim bình thường; B: thiếu máu dưới nội tâm mạc; C: tổn thương xuyên thành; D: hoại tử xuyên thành.
ST chênh
Đoạn ST bắt đầu từ điểm J (junction) tới khởi đầu sóng T. Đoạn ST bình thường dài khoảng 80 ms (độ rộng của 2 ô nhỏ). Đoạn ST bình thường đẳng điện, có thể khả năng và đi dốc lên ở các chuyển đạo trước tim (nhưng không quá 1 mm).
Trong các hình thái thiếu máu cục bộ cơ tim, đoạn ST có thể khả năng (elevation), hoặc chênh xuống (depression) so với đường đẳng điện. Xác định mức độ ST chênh dựa vào sự chuyển dịch của điểm J (điểm nối, được coi là điểm cuối sóng S hay điểm đầu đoạn ST) và điểm nằm ở khoảng thời gian 80 ms sau điểm J (tương đương với độ rộng 2 ô nhỏ trên điện tâm đồ, tức 2 mm).
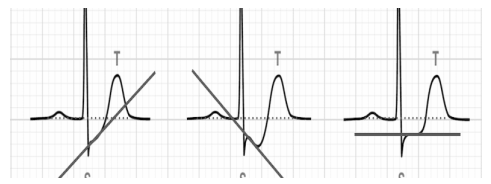
Hình 2.3. 1: ST đẳng điện bình thường; 2: ST chênh xuống 4 mm tại điểm J và 5 mm khoảng 80 ms sau điểm J; 3: ST khả năng 4 mm tại điểm J và 6 mm khoảng 80 ms sau điểm J
Cơ chế của ST chênh:
Hình 2.4. Cơ chế của ST chênh
ST chênh xuống hay khả năng tùy thuộc vào sự biến đổi hướng vector khử cực bị dịch chuyển về phía nội tâm mạc hay thượng tâm mạc trong hoàn cảnh thiếu máu cục bộ.
Thiếu máu dưới nội tâm mạc (subendocardial) sẽ làm chậm trễ tái cực ở lớp gần nội mạc, dẫn đến vector tái cực hướng từ ngoài vào trong tim buồng tim khiến đoạn ST chênh xuống tại vùng chuyển đạo tương ứng.
Thiếu máu dưới thượng tâm mạc hay xuyên thành (epicardial hay transmural), thường gặp trong nhồi máu cơ tim cấp, vector khử cực sẽ biến đổi theo chiều ngược lại, hướng từ trong ra ngoài buồng tim làm cho ST khả năng.
Thông thường, sự chênh của đoạn ST có ý nghĩa chẩn đoán khi mức độ chênh lớn hơn 0,5-1 mm và xảy ra trên các chuyển đạo liên tiếp hoặc trong một miền chuyển đạo.
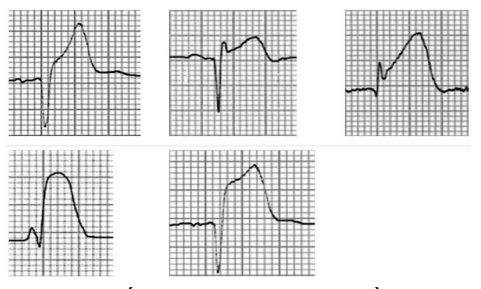
ST khả năng trong nhồi máu cơ tim có thể biểu hiện qua nhiều hình dạng khác nhau. Do đó cần chẩn đoán phân biệt với các dạng ST khả năng trong các bệnh lý khác như tăng gánh thất trái, viêm cơ tim – màng ngoài tim, hội chứng Brugada, block nhánh trái hoặc phải, …
Hình 2.5. Một số dạng ST khả năng trong nhồi máu cơ tim
Hình 2.6. Đoạn ST – T chênh hình mộ. Đoạn ST – T chênh cao, đoạn ST và T hòa nhập thành 1 khối và 1 pha dương duy nhất. Đoạn ST – T hình mộ dự báo nguy cơ tử vong cao.
Hình 2.7. Một số dạng ST khả năng trong các bệnh lý khác như: tăng gánh thất trái, block nhánh trái hoàn toàn, viêm màng ngoài tim, tăng kali máu, hội chứng Brugada.
Trong một số trường hợp khó chẩn đoán, cần thực hiện nhiều điện tâm đồ khác nhau tại các thời điểm khác nhau. Trong bệnh cảnh nhồi máu cơ tim, đoạn ST – T khả năng và thay đổi theo giờ phụ thuộc vào tiến triển của bệnh. Các vùng cơ tim bị thiếu máu và hoại tử lan rộng nếu không được điều trị tái tưới máu khiến cho biểu hiện trên điện tâm đồ cũng thay đổi. Theo hướng dẫn chẩn đoán Nhồi máu cơ tim cấp của Hội Tim mạch Châu Âu – ESC, cần làm điện tâm đồ tại nhiều thời điểm hoặc cần mắc monitor để theo dõi điện tâm đồ liên tục nhằm đánh giá động học của điện tâm đồ trong những trường hợp không rõ ràng về chẩn đoán.
Hình 2.8. Động học đoạn ST-T theo thời gian trong NMCT cấp
Một đặc điểm khác giúp chẩn đoán phân biệt ST khả năng do nhồi máu cơ tim với các nguyên nhân khác đó là hình ảnh ST chênh xuống “soi gương” ở các chuyển đạo có hướng đối diện với các chuyển đạo có đoạn ST khả năng. Ví dụ như ST khả năng ở chuyển đạo aVL (-30 độ) thì sẽ chênh xuống ở chuyển đạo DIII (+120 độ)
Hình 2.9. Hình ảnh ST chênh xuống “soi gương” ở aVL
Hình 2.10. NMCT cấp thành dưới. ST khả năng ở DII DIII aVF, và ST chênh xuống soi gương ở aVL.
Trong hội chứng vành cấp, điện tâm đồ có thể biểu hiện ST chênh xuống với nhiều hình dạng khác nhau. Đoạn ST chênh xuống đại biểu cho vùng thiếu máu ở dưới nội tâm mạc, hoặc trong trường hợp khác do tổn thương nhiều thân động mạch vành dẫn đến những vùng tổn thương cơ tim lan rộng làm thay đổi vector tái cực tâm thất khiến cho biểu hiện trên điện tâm đồ là đoạn ST – T chênh xuống thay vì khả năng như nhồi máu cơ tim cấp xuyên thành.
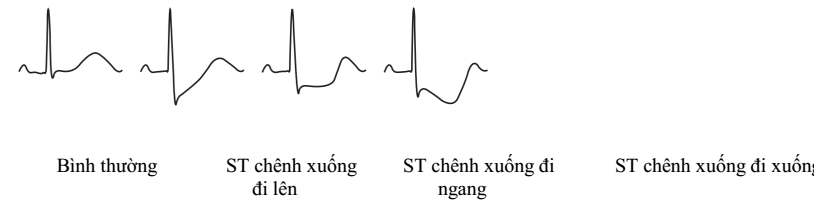
Hình 2.11. Một số hình thái đoạn ST chênh xuống. Đoạn ST chênh xuống đi dốc lên, chênh xuống đi dốc xuống và chênh xuống đi ngang.
Hình 2.12. Đoạn ST chênh xuống trên nhiều chuyển đạo
Các minh họa về ST chênh:
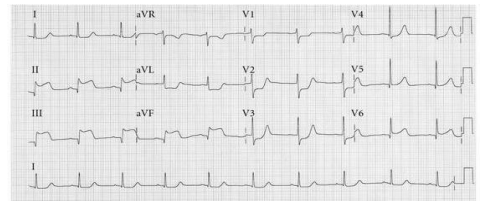
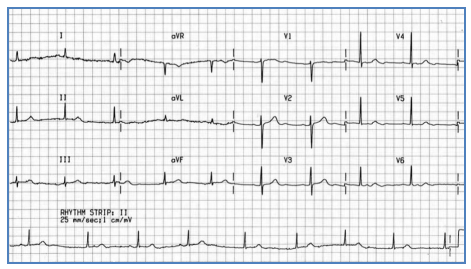
Hình 2.13. Điện tâm đồ của một bệnh nhân có cơn đau thắt ngực điển hình. Nhịp xoang 75 ck/ph, trục xu hướng trái, ST chênh xuống khoảng 1 mm V5, V6 và D2, gợi thiếu máu dưới nội tâm mạc vùng trước bên và vùng thành dưới cơ thất trái.
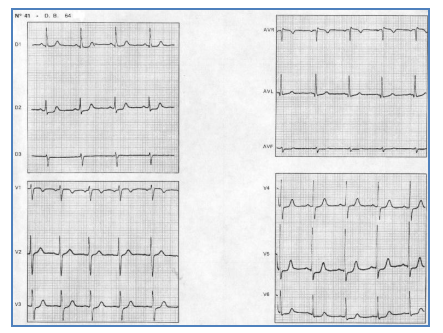
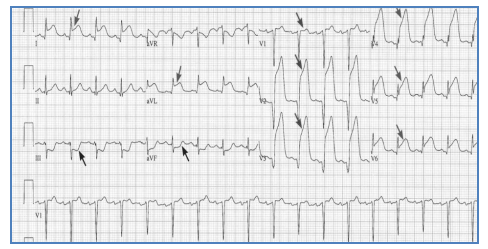
Hình 2.14. Điện tâm đồ của bệnh nhân có cơn đau ngực dữ dội, mới xuất hiện. Nhịp xoang nhanh 100 ck/ph; ST chênh xuống nhiều hầu hết các chuyển đạo ngoại trừ khả năng ở aVR gợi tổn thương thiếu máu cấp tính nhiều vùng cơ tim liên quan đến hẹp thân chung hoặc hẹp nhiều nhánh động mạch vành.
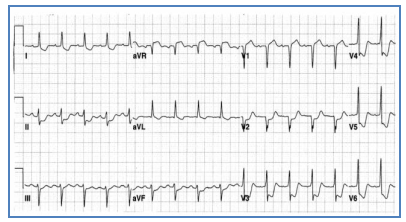
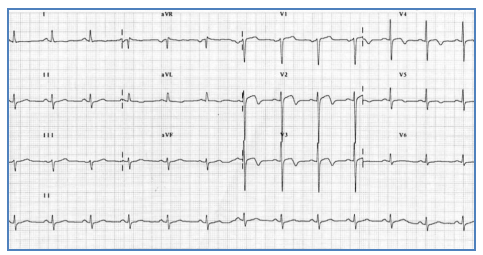
Hình 2.15. Điện tâm đồ của một bệnh nhân đau thắt ngực khi gắng sức do hẹp động mạch vành phải. Nhịp xoang 83 ck/ph, ST chênh xuống rất nhẹ (0,5 mm) nhưng thẳng đuỗn và đi ngang ở DII, DIII, aVF.
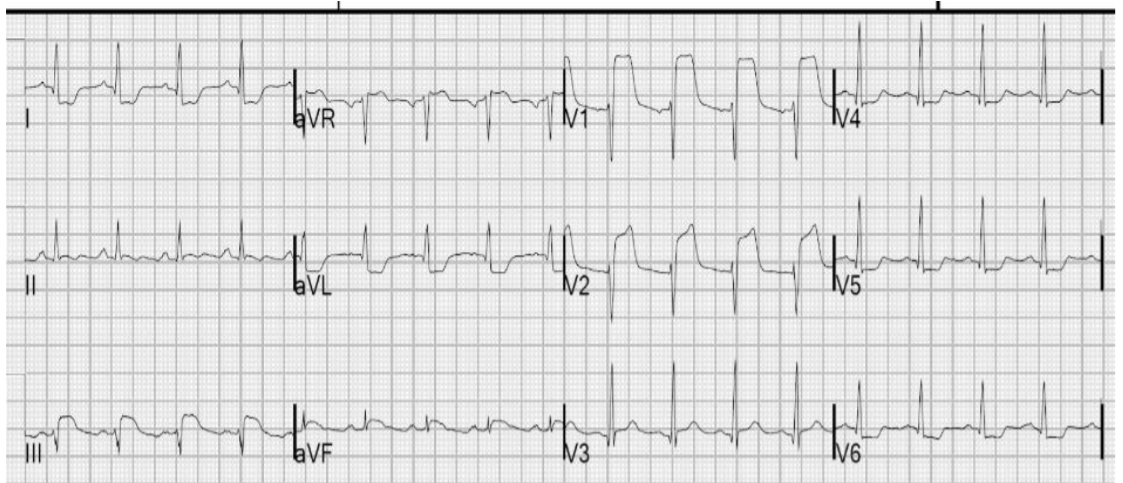
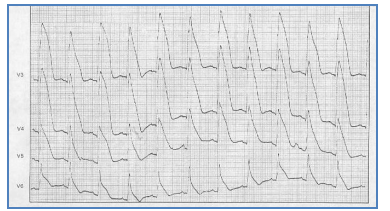
Hình 2.16. ST khả năng cao, phủ trùm cả sóng R sau đó lại trở về bình thường ở một bệnh nhân đau ngực kiểu Prinzmetal.
Hình 2.17. ST khả năng ở các chuyển đạo từ V1 đến V5 ở một bệnh nhân nhồi máu cơ tim trước rộng cấp. Đoạn ST V2, V3, V4 khả năng ở cao hơn cả sóng R tạo ra hình ảnh “bia mộ” (Tombstone ST elevation).
Biến đổi sóng T
Sóng T bình thường uốn lượn mềm mại với sườn lên thoai thoải hơn và sườn xuống dốc hơn. Sóng T luôn dương ở DI, DII, V3 đến V6 và luôn âm ở aVR. Sóng T ở các chuyển đạo còn lại có thể dương hoặc âm. Biên độ sóng T thường không cao quá 2/3 sóng R cùng chuyển đạo.
Biến đổi trong thiếu máu cục bộ cơ tim thường là sự đảo hướng của sóng T. Ngoài ra sóng T sẽ mất đi tính chất thoai thoải của sườn lên và dốc xuống của sườn xuống trở nên nhọn và đối xứng.
Hình 2.18. Điện tâm đồ gần như bình thường của một bệnh nhân ghi ở ngoài cơn đau thắt ngực.
Hình 2.19. Cũng BN nói trên, điện tâm đồ này ghi ở trong cơn đau thắt ngực với sự đảo hướng của sóng T từ V2 đến V6. Sóng T ở V2, V3, V4 tr nên âm, nhọn và đối xứng.
Hình 2.20. Sóng T biến đổi trung gian, trở nên dạng “hai pha” V2, V3, V4 trên một bệnh nhân nhồi máu cơ tim cấp đã được can thiệp động mạch vành qua da.
Sóng Q bệnh lý hay sóng Q “hoại tử”
Sóng Q bình thường có thể thấy ở một số chuyển đạo điện tâm đồ và được cho là liên quan đến hoạt động khử cực của các sợi cơ tim vùng vách liên thất bên trái. Sóng Q sinh lý thường sâu không quá 2mm, và có thời gian
Sóng Q bệnh lý được hình thành khi có một vùng cơ tim bị hoại tử gây ra một “lỗ hổng” điện học trên thành tim, khiến cho chuyển đạo điện tâm đồ đặt trên vùng cơ tim đó ghi được sóng R của thành tim bên đối diện theo chiều ngược lại (sóng âm). Sóng Q bệnh lý hay “hoại tử” là khi có độ sâu > 2mm và độ rộng > 0,04s. Sóng Q “hoại tử” là dấu hiệu muộn của nhồi máu cơ tim. Sóng Q hoại tử thường xuất hiện sau 8 – 12 giờ sau nhồi máu cơ tim cấp.
Hình 2.21. Sóng Q hoại tử kèm theo ST khả năng ở V2 và V3 trong một ca nhồi máu cơ tim vùng trước rộng, cấp tính.
Hình 2.22. Sóng Q hoại tử ở các chuyển đạo V2-V5 trên một bệnh nhân có tiền sử nhồi máu cơ tim cũ.
Chẩn đoán định khu nhồi máu cơ tim cấp
Điện tâm đồ là một phương tiện chẩn đoán nhanh và thiết yếu để chẩn đoán bệnh lý động mạch vành. Đặc biệt trong những trường hợp nhồi máu cơ tim cấp.
Theo hướng dẫn chẩn đoán nhồi máu cơ tim cấp của Hội Tim mạch Châu Âu năm 2017, các biểu hiện điện tâm đồ gợi ý NMCT cấp :
Đoạn ST khả năng/chênh xuống điển hình.
Block nhánh trái/phải mới xuất hiện.
Trường hợp block nhánh trái từ trước: Đoạn ST khả năng ≥ 1mm đồng hướng ở các chuyển đạo mà phức bộ QRS dương, hoặc ST chênh xuống đồng hướng ≥ 1mm ở chuyển đạo từ V1 – V3, hoặc ST khả năng ngược hướng ≥ 5 mm ở các chuyển đạo phức bộ QRS âm.
Block nhánh phải từ trước có thể làm che lấp biểu hiện NMCT trên điện tâm đồ.
Bệnh nhân có máy tạo nhịp tim: khi máy tạo nhịp, điện tâm đồ có dạng block nhánh trái, do đó có thể áp dụng tiêu chuẩn ở trên tuy nhiên kết quả thường ít đặc hiệu hơn.
ST chênh xuống ≥ 0.5 mm ở V1 – V3 và khả năng ≥ 0.5 mm tại V7 – V9 gợi ý NMCT vùng thành dưới đơn độc.
Điện tâm đồ gợi ý tổn thương thân chung ĐMV trái hoặc bệnh nhiều thân ĐMV: ST chênh xuống ≥ 1mm từ 8 chuyển đạo trở lên, hoặc ST khả năng ở aVR và/hoặc V1.
Hình 2.23. NMCT cấp với dạng block nhánh phải tại V1. Đoạn ST khả năng ở các chuyển đạo trước tim gợi tổn thương thân chung ĐMV trái.
Hình 2.24. Điện tâm đồ có đoạn ST chênh xuống trên nhi u chuyển đạo kèm theo ST khả năng ở aVR gợi tổn thương nhiều thân ĐMV hoặc thân chung ĐMV trái.
Định khu vùng thiếu máu cơ tim và ĐMV thủ phạm trong nhồi máu cơ tim cấp có ST khả năng phụ thuộc vào giải phẫu cấp máu của hệ ĐMV đã nhắc ở trên
Hình 2.25. Định khu vùng NMCT trên điện tâm đồ.
Lateral: Bên; Inferior: Dưới; Ant – Anterior: Trước; Septal: vách
Nhồi máu cơ tim ở vùng nào thì ST khả năng và có thể có sóng Q hoại tử ở các miền chuyển đạo tương ứng. Do vậy, điện tâm đồ có thể giúp dự đoán khá chính xác các nhánh động mạch vành thủ phạm gây nhồi máu cơ tim.
V1, V2: NMCT vùng vách
V3, V4: NMCT vùng trước
V1, V2, V3, V4: NMCT trước vách
V5, V6: NMCT thành bên thấp (mỏm)
DI, aVL: NMCT thành bên cao
V5, V6, D1, aVL: NMCT thành bên
V3, V4, V5, V6: NMCT trước bên
Từ V1 đến V6, kèm D1, aVL: NMCT trước rộng
DII, DIII, aVF: NMCT thành dưới (vùng cơ tim nằm trên cơ hoành)
V7, V8, V9: NMCT thành sau thực (vùng cơ tim “tựa” vào cột sống)
DII, DIII, aVF kèm V7, V8, V9: NMCT sau dưới
V3R, V4R: NMCT thất phải
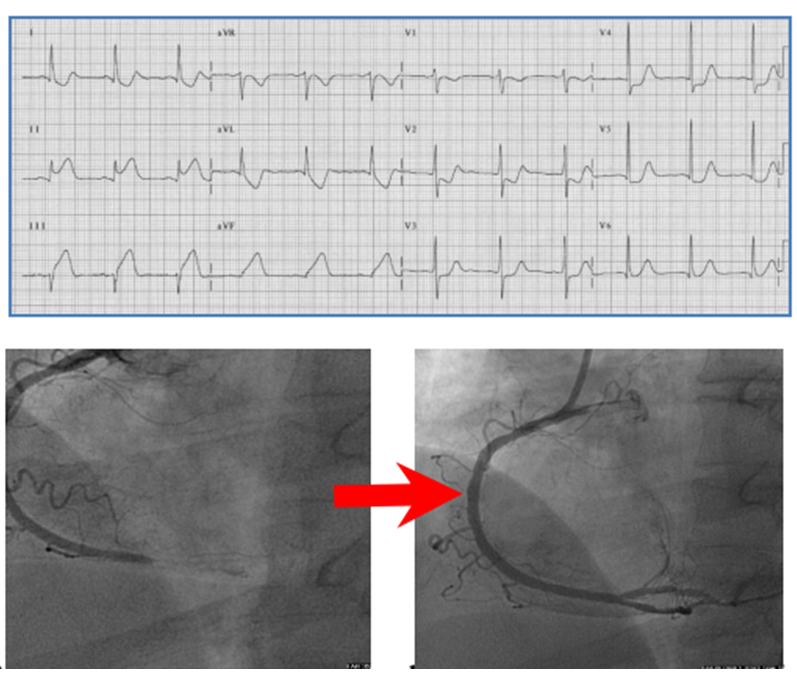
Hình 2.26 và 2.27. Minh họa một trộng hợp nhồi máu cơ tim trước rộng với ST khả năng ở từ V2-V6 và ST chênh xuống soi gương ở DIII, aVF do tắc hoàn toàn động mạch liên thất trước đoạn 1, động mạch bị tắc sau đó đã được tái thông bằng can thiệp qua da.
Hình 2.28 và 2.29. Minh họa một trộng hợp nhồi máu cơ tim thành dưới với ST khả năng ở DII, DIII, aVF và ST chênh xuống soi gương V1-V5 do tắc hoàn toàn động mạch vành phải đoạn xa, động mạch bị tắc sau đó đã được tái thông bằng can thiệp qua da.
Hình 2.30 và 2.31. Minh họa một trộng hợp nhồi máu cơ tim với ST khả năng ở DII, DIII, aVF và ST chênh xuống soi gương ở V1-V2, ST đồng thời cũng khả năng ở V5, V6. Lưu V1, V2 có sóng R cao chiếm ưu thế. Kết quả chụp động mạch vành cho thấy tắc hoàn toàn động mạch mũ đoạn gần, động mạch bị tắc sau đó đã được tái thông bằng can thiệp qua da. Trộng hợp này cần làm thêm các chuyển đạo thành sau (V7, V8, V9) để có thể thấy rõ hơn tổn thương.
Hình 2.32 và 2.33. Minh họa một trộng hợp nhồi máu cơ tim với ST khả năng ở V1, aVR và ST chênh xuống hầu hết các chuyển đạo. Kết quả chụp động mạch vành cho thấy hình ảnh tắc hoàn toàn thân chung động mạch vành trái.
Siêu âm tim trong bệnh động mạch vành
Giải phẫu và chức năng động mạch vành ứng dụng trong siêu âm tim
Giải phẫu và chức năng động mạch vành
Động mạch vành gồm ĐMV trái và ĐMV phải xuất phát từ gốc ĐM chủ qua trung gian là xoang vành.
ĐMV trái: xuất phát từ xoang vành, tương ứng với lá vành trái. Đoạn thân chung dài khoảng 15 mm rồi chia thành hai nhánh động mạch liên thất trước và động mạch mũ.
Động mạch liên thất trước (ĐMLTT) chạy dọc rãnh liên thất trước xuống mỏm tim và nối với ĐMV phải ở rãnh liên thất sau. ĐMLTT cung cấp máu cho vách liên thất, thành trước bên thất trái, mỏm tim và các nhánh nhỏ cấp máu cho mặt trước thất phải.
Động mạch mũ (LCx) tách từ ĐMV trái chạy dọc rãnh nhĩ thất. ĐM mũ kêt thúc bằng nhánh rìa và nhánh nhĩ. Nhánh rìa chung cấp máu cho mặt bên và mặt sau bên thất trái. Nhánh mũ nhĩ trái cung cấp máu cho nhĩ trái.
ĐMV phải: xuất phát từ gốc ĐM chủ tương ứng với lá vành phải. ĐMV phải có các nhánh:
Nhánh nón (conus branch): chạy phía trước trên vòng quanh đường ra thất phải ở ngang mức van động mạch phổi
Nhánh động mạch nút xoang
Nhánh động mạch vách trên phải
Động mạch xuống sau (PD= posterior descending)
Động mạch nút nhĩ thất (Atrioventricular node)
Nhánh sau thất trái (posterior left ventricular): cấp máu cho hầu hết thành sau sát cơ hoành và một phần cho thành sau bên thất trái.
Sinh lý tuần hoàn vành
Tuần hoàn vành là tuần hoàn dinh dưỡng cơ tim. ĐMV bị hẹp làm hạn chế dòng máu nuôi quả tim. Nghiệm pháp gắng sức thể lực làm tăng nhịp tim, tăng co bóp cơ tim, tăng độ dày thành tim thì tâm thu và tăng nhu cầu oxy cơ tim. Khi hẹp ĐMV, nhu cầu oxy cơ tim tăng không đáp ứng đủ với nhu cầu tăng dòng máu tưới ĐMV. Sự mất cân bằng giữa tăng nhu cầu oxy và cung cấp oxy làm gây ra tình trạng thiếu máu cơ tim.
Hậu quả tức thời là khởi phát thiếu máu thường được gọi là các giai đoạn thiếu máu “ischemic cascade” bao gồm rối loạn chức năng tâm trương (giảm giãn và tăng co cứng tâm trương), biến đổi điện tâm đồ, rối loạn chức năng tâm thu và cuối cùng là đau ngực. Quá trình này được mô tả trên lâm sàng bởi độ nhạy của các marker đánh giá thiếu máu khác nhau. Rối loạn vận động vùng xảy ra ngay khi giảm tưới máu cơ tim. Do vậy, đánh giá thiếu máu cơ tim bằng siêu âm tim gắng sức là rất quan trọng trong chẩn đoán bệnh ĐMV.
Những biến đổi sớm nhất của thiếu máu có thể là sự xuất hiện hay biến mất của dày thành tim thì tâm thu mà đôi khi không phát hiện được bằng mắt thường mà chỉ có thể phát hiện bằng các phương tiện như phân tích biến dạng cơ tim. Gần đây, Reant và cộng sự mô tả trên động vật hẹp ĐMV có hạn chế dòng chảy và không hạn chế dòng chảy là bất thường chức năng tâm thu theo chiều dọc và chu vi (chức năng nội mạc) thường xảy ra trước khi giảm sức căng (sự biến dạng) theo chiều bán kính ( biểu hiện bằng độ dày thành tim). Điều này được giải thích bởi sự sắp xếp chủ yếu theo chiều dọc của các sợi cơ ở nội tâm mạc thường nhạy với thiếu máu và vì vậy bị ảnh hưởng đầu tiên trong quá trình thiếu máu “ischemic cascade”
Khi thiếu máu cơ tim, những vùng không thiếu máu có thể tăng co bóp bù, duy trì chức năng tâm thu thất trái toàn bộ. Khi có bệnh ĐMV khi không có tăng co bóp toàn bộ tâm thu trong gắng sức thường liên quan đến giãn buồng thất trái và đây là một dấu hiệu chỉ điểm hẹp mạch vành nặng gợi ý tổn thương nhiều thân. Giảm chức năng thất trái toàn bộ khi gắng sức, có thể do những nguyên nhân khác như THA, bệnh cơ tim. Trong đa số các trường hợp, khi ngừng gắng sức, thiếu máu cơ tim được hồi phục và vận động vùng hồi phục lại rất nhanh. Đôi khi, rối loạn co bóp cơ tim có thể kéo dài hơn 30 phút gợi ý tổn thương mạch vành nặng nề.
Siêu âm tim trong chẩn đoán bệnh động mạch vành
Đánh giá vận động vùng thành tim
Các bước làm siêu âm
Trên lâm sàng, đánh giá bằng mắt (eye ball) dựa trên hình ảnh siêu âm 2D đưa ra những nhận định nhanh nhất về vận động vùng thành tim hay chức năng tâm thu theo vùng. Buồng thất trái được chia thành nhiều vùng khác nhau và mỗi vùng được tính điểm dựa trên mức độ co bóp thành tim. Hội tim mạch Hoa Kỳ khuyến cáo chia thất trái thành 17 vùng. Vị trí của các vùng thành tim tương ứng với vùng tưới máu của ĐMV.
Điểm vận động vùng thành tim được đánh giá bằng mắt dựa trên mức độ co bóp như sau: 1điểm : bình thường; 2 điểm : giảm vận động, 3 điểm: không vận động, 4 điểm: vận động nghịch thường, 5 điểm: phình thành tim. Chỉ số vận động vùng thành tim được tính bằng tổng số điểm chia cho tổng số vùng. Thất trái vận động bình thường có chỉ số vận động vùng thành tim (WMSI) bằng 1 và chỉ số này tăng lên khi rối loạn vận động vùng càng tăng. Có mối tương quan khá tốt giữa chỉ số vận động vùng thành tim và chức năng co bóp: chỉ số vận động vùng thành tim 1.1-1,9 có thể dự đoán vùng nhồi máu nhỏ và chỉ số lớn hơn hoặc bằng 2 có thể dự báo các biến chứng.
Độ chính xác của đánh giá vận động vùng phụ thuộc nhiều vào chất lượng hình ảnh và kinh nghiệm của người làm siêu âm. Vận động vùng thành tim theo vùng có thể đánh giá bằng sức căng. Sức căng cơ tim mô tả sự biến dạng và có nhiều thông số. Giá trị sức căng có thể phân biệt vận động bình thường và bất thường ở vùng thiếu máu. Sức căng cơ tim có thể đánh giá bằng Doppler mô nhưng Doppler mô phụ thuộc góc. Siêu âm tim đánh dấu mô (speckle tracking echo) là đánh giá sức căng dựa trên hình ảnh 2D và đánh giá chức năng vùng ở mặt cắt trục ngắn và trục trục dọc.
Định khu vùng nhồi máu
Giá trị của siêu âm 2D là một phương tiện chẩn đoán ở NMCT cấp đã được sử dụng từ rất lâu và nhiều nghiên cứu đã chỉ ra độ nhạy của phương pháp này trong định khu vùng nhồi máu.
Dựa trên nguyên tắc chung là so sánh vận động vùng cơ tim bình thường với vùng nhồi máu, sự thay đổi độ dày thành tim. NMCT xuyên thành được phát hiện tối ưu hơn NMCT dưới nội tâm mạc bởi liên quan đến độ dày thành tim dưới 20%. Hơn nữa, siêu âm 2D cũng chính xác trong định khu vùng nhồi máu loại trừ những trường hợp tổn thương nhiều nhánh ĐMV, NMCT cũ và những vùng tưới máu đan xen giữa những vùng tưới máu của ĐMV phải và ĐM mũ. Độ rộng của vùng nhồi máu và chức năng co bóp cơ tim có mối tương quan khá chặt.
Động mạch liên thất trước cấp máu cho vách liên thất, thành trước và vùng mỏm. Những vùng này quan sát rõ ở mặt cắt trục dọc cạnh ức trái, 2 buồng, 3 buồng và 4 buồng từ mỏm. Vị trí tắc hẹp ĐMV đoạn gần hay xa cũng ảnh hưởng đến độ nặng và mức độ rối loạn vận động vùng. Động mạch liên thất trước cấp máu cho phần lớn mỏm thất trái. Tắc động mạch liên thất trước có thể dẫn tới rối loạn vận động vùng phần xa của thành dưới và vùng sau bên.
Động mạch mũ: điển hình ảnh hưởng tới vùng tưới máu của thành trước bên và dưới bên. Hình ảnh mặt cắt trục dọc cạnh ức (thành sau bên) và 4 buồng từ mỏm, 3 buồng từ mỏm (thành dưới bên). Khoảng 20% bệnh nhân động mạch mũ cấp máu cho nhánh PDA (ưu năng) và khi tắc nghẽn dòng chảy của động mạch mũ có thể gây rối loạn vận động vùng lan rộng và có thể bao gồm phần dưới vách liên thất và thành tự do thất trái.
Động mạch vành phải: thành sau dưới thất trái, toàn bộ thành dưới thất trái. Mặt cắt trục ngắn qua vùng đáy và phần giữa của vách liên thất và mặt cắt 2 buồng từ mỏm. Đánh giá kỹ kích thước và chức năng của thất phải là rất quan trọng trong NMCT thành dưới cấp.
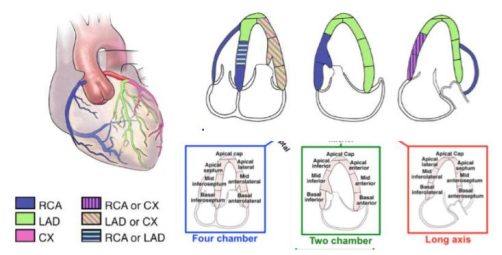
Hình 2.34. Phân vùng tưới máu cơ tim. Giải phẫu mạch vành có thể khác nhau giữa các bệnh nhân. Sự cấp máu của động mạch vành cho một số vùng cũng khác nhau.
Đánh giá chức năng thất trái theo vùng
Để đánh giá chức năng từng vùng, tâm thất trái được chia thành các vùng khác nhau. Mô hình phân chia thất trái làm 17 vùng được sử dụng phổ biến nhất. Bắt đầu từ điểm nối vách liên thất phía trước với thành tự do của tâm thất phải, đi ngược chiều kim đồng hồ, các đoạn đáy và giữa thất trái được phân thành vùng trước vách, dưới vách, dưới, dưới bên, trước bên, và vùng trước. Mỏm tim được chia làm năm vùng: vách, dưới, bên, trước mỏm, và “đỉnh mỏm”(apical cap) là vùng cơ tim ở vị trí kết thúc của buồng thất trái. Mô hình 17 vùng có thể được áp dụng trong các nghiên cứu về tưới máu cơ tim, hoặc để so sánh các phương pháp chẩn đoán hình ảnh khác nhau như chụp cắt lớp xạ hình đơn dòng, chụp cắt lớp xạ hình positron và cộng hưởng từ hạt nhân. Khi sử dụng mô hình này để đánh giá vận động thành hoặc sức căng từng vùng, vùng thứ 17 (đỉnh mỏm) không được tính đến. Một số mô hình phân vùng khác được sử dụng: Mô hình 16 vùng phân chia toàn bộ mỏm tim làm 4 vùng (vách, dưới, bên, trước) hoặc mô hình 18 vùng, phân chia mỏm tim làm 6 vùng, tương tự như với phần đáy và giữa thất trái tuy đơn giản nhưng hơi chia nhỏ quá mức vùng cơ tim ở xa khi tính điểm. Tất cả các phân vùng đều có thể quan sát được bằng siêu âm 2D.
Hình 2.35. Sơ đồ của mô hình phân vùng thất trái khác nhau: mô hình 16 vùng, 17 vùng và 18 vùng. Trong tất cả các sơ đồ, vòng ngoài thể hiện các vùng đáy, vòng giữa là các vùng mức cơ nhú và vòng trong cho vùng xa. Vị trí nối phía trước của thành tự do thất phải vào thất trái xác định ranh giới giữa vùng trước và trước vách. Từ vị trí này, cơ tim bị chia thành 6 vùng bằng nhau theo góc 60 đ .
Chẩn đoán phân biệt với các nguyên nhân gây rối loạn vận động vùng khác
Siêu âm tim là phương tiện chẩn đoán hình ảnh không xâm nhập cung cấp những thông tin về chức năng tim và huyết động. Siêu âm tim giúp loại trừ những nguyên nhân đau ngực khác dựa trên đánh giá chức năng thất và sự xuất hiện rối loạn vận động vùng thành tim.
Các nguyên nhân khác gây rối loạn vận động vùng trên siêu âm tim có thể là:
Takotsubo
Viêm cơ tim
Máy tạo nhịp hay block nhánh
Giãn thất phải gây VLT đi động về bên trái
Giả rối loạn vận động vùng
Siêu âm tim bình thường là không đủ để loại trừ chẩn đoán bệnh ĐMV. Hình ảnh rối loạn vận động vùng phải đánh giá dựa trên nhiều mặt cắt trục dọc cạnh ức, trục ngắn, 4 buồng, 2 buồng, 3 buồng từ mỏm. Mặt cắt dưới mũi ức cũng có giá trị đặc biệt khi chất lượng hình ảnh siêu âm tim trên thành ngực mờ. Phải lưu ý tránh gây cắt ngắn mỏm tim sẽ đánh giá không chính xác vận động vùng.
Đánh giá các biến chứng của nhồi máu cơ tim
Vỡ tim
Vỡ thành tự do: tràn dịch màng tim hay giả phình thành tim.
Là biến chứng cơ học phổ biến nhất sau NMCT
Tỷ lệ vỡ thành tự do giảm đi trong kỷ nguyên của thuốc tiêu huyết khối
Yếu tố nguy cơ: NMCT cấp tắc hoàn toàn động mạch vành. Giới nữ, tuổi >70.
Nếu bệnh nhân không có tiền sử NMCT trước đó ít khi có tràn dịch màng ngoài tim.
Nếu có tiền sử NMCT hay viêm màng ngoài tim trước đó: vỡ cấp có thể gặp, gây ra giả phình thành tim.
Ngoài ra có thể gặp tình trạng vỡ bán cấp
Phân biệt giả phình và phình thành tim
Bảng 2.1. Phân biệt giả phình thành tim và phình thành tim
|
Giả phình thành tim |
Phình thành tim |
|
Thường không ở mỏm Cổ túi phình thường hẹp hơn phần thân túi phình Không có sự liên tục phần cơ với tổ chức phình Dòng chảy ĐMP trong thì tâm thu thường có vận tốc cao Bệnh nhân có yếu tố nguy cơ vỡ cao |
Thường ở vùng mỏm Cổ túi phình thường rộng hơn thân phình Vùng cơ mỏng nhưng liên tục Khả năng vỡ thấp |
Hình 2.36. A.Giả phình thành tim B.Phình thành tim
Hình 2.37. Giả phình thành tim tại vị trí thành sau bên thất trái trên mặt cắt 4 buồng từ mỏm (A) và trục dọc cạnh ức (B)
Hình 2.38. Phình thành sau thất trái
Thủng vách liên thất:
Nguy cơ tương tự như vỡ thành tự do
Tần số gặp ở tổn thương ĐM liên thất trước và ĐMV phải là như nhau
Thường xảy ra ngày thứ năm của bệnh
Có tiếng thổi lớn và mới ở tim
Thủng có thể ở vùng cơ tim nhồi máu hoặc ranh giới giữa vùng cơ tim nhồi máu và vùng cơ tim bình thường.
Siêu âm 2D có thể phát hiện được lỗ thủng trong 60% – 80% các trường hợp.
Thủng vách liên thất có thể thấy ở mặt cắt 4 buồng, mặt cắt trục dọc dưới mũi ức.
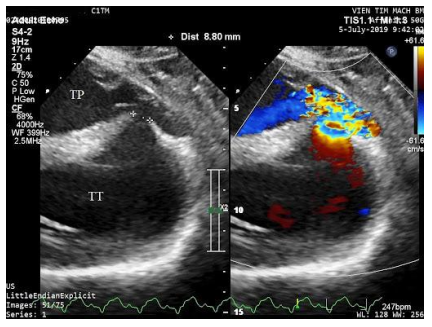
Hình 2.39. Thông liên thất sau nhồi máu cơ tim
Hở hai lá cấp do suy chức năng cơ nhú hay đứt cơ nhú
Hở hai lá cấp có thể thứ phát do suy chức năng cơ nhú.
Thường gặp lá sau van hai lá bị tổn thương
Đứt cơ nhú hoặc dây chằng: có thể đứt cơ nhú một phần hoặc toàn phần. Nếu đứt toàn phần bệnh nhân có thể tử vong rất nhanh. Biểu hiện lâm sàng là tiếng thổi toàn tâm thu ở mỏm, lan về phía đáy tim (dễ nhầm với thông liên thất).
Suy chức năng cơ nhú: giai đoạn sớm có thể thấy là rối loạn vận động của cơ nhú ở mặt cắt trục ngắn cắt qua cơ nhú. Hay gặp nhất là suy chức năng cơ nhú sau giữa.
Hở hai lá cấp có thể xảy ra với vùng nhồi máu rất nhỏ.
Giãn vòng van thứ phát do giãn thất trái.
Huyết khối trong buồng tim
Trước kỷ nguyên tái tưới máu, huyết khối buồng thất được báo cáo từ 25-40% sau NMCT thành trước. Huyết khối thường ở NMCT thành trước mỏm và liên quan đến rối loạn vận động vùng rộng. Huyết khối thất trái xảy ra ở vùng thành tim không vận động, thường gặp nhất ở vùng mỏm tim nhưng cũng có thể gặp ở những vùng khác phình thành tim ở thành bên và thành dưới.
Hình ảnh đặc trưng của huyết khối là một cấu trúc siêu âm bất thường trong buồng tim trái, thường là một một cấu trúc đậm âm, thường khác biệt với các cấu trúc cơ tim bên cạnh.
Khi làm siêu âm phải quan sát được huyết khối trên nhiều mặt cắt và xuất hiện trong cả chu chuyển tim.
Hình ảnh siêu âm tim mờ đôi khi phải dùng chất cản âm thất trái để nhìn rõ bờ nội mạc của tim đặc biệt ở những bệnh nhân nghi ngờ có huyết khối và có hình ảnh siêu âm không rõ và cũng loại trừ các nguyên nhân khác của đau ngực như bệnh cơ tim phì đại.
Huyết khối có thể hình thành rất sớm, trong 36 giờ đầu, trung bình hay gặp là ngày thứ 5 của bệnh.
Tiến triển của huyết khối trên siêu âm: huyết khối có thể tổ chức hóa, nhỏ đi hay tự ly giải. Biến chứng của huyết khối là gây tắc mạch, đặc biệt là nhồi máu não.
Hình 2.40. Huyết khối mỏm tim (LV: thất trái, L : nhĩ trái)
Suy tim
Khi chức năng thất trái khi >15% vùng cơ tim bị tổn thương
Khó thở và sốc liên quan tới suy chức năng thất trái cấp
Trên lâm sàng biểu hiện suy tim khi > 25% cơ tim bị tổn thương
Shock tim xảy ra khi > 40% vùng cơ tim bị ảnh hưởng
Tái cấu trúc thất trái sau nhồi máu cơ tim
Sau NMCT, thất trái phải thích nghi với tình trạng giảm chức năng theo vùng bằng việc tăng co bóp của những vùng cơ tim còn sống. Tái cấu trúc thất trái được đặc trưng bằng việc thay đổi kích thước, hình dạng, và chức năng như hậu quả của tổn thương cơ tim hay tình trạng tăng gánh. Mức độ nặng của suy chức năng theo vùng (kích thước vùng nhồi máu, chức năng của những vùng còn lại, hoạt hóa hệ thần kinh thể dịch và sự tồn tại những bệnh lý van tim khác kèm theo đặc biệt là hở hai lá xác định độ lớn của tái cấu trúc thất trái.
Quá trình này thường bắt đầu trong vòng vài giờ sau nhồi máu và tiến triển theo thời gian. Sự mỏng và giãn ra của vùng nhồi máu sau NMCT được định nghĩa như vùng nhồi máu lan rộng và thường dẫn đến thay đổi hình dạng và thể tích thất trái và mất dần chức năng. Khi tái cấu trúc, thất trái giãn ra có dạng hình cầu hơn và giảm chức năng. Sự thay đổi hình dạng thất trái dẫn đến hở hai lá do thiếu máu cơ tim, tăng thể tích thất trái, hoạt hóa hệ thần kinh thể dịch và giảm co bóp cơ tim vì vậy dẫn đến vòng xoắn bệnh lý và hở hai lá. Mối liên quan giữa giảm chức năng thất trái và hở hai lá được phản ánh tỷ lệ sống còn thấp ở những bệnh nhân sau NMCT có cả hở hai lá nặng và chức năng thất trái kém.
Siêu âm tim đánh giá trái cấu trúc thất trái sau NMCT bao gồm đánh giá phân số tống máu, kích thước, hình dạng và thể tích thất trái cuối tâm thu và tâm trương và mức độ hở hai lá.
Nhồi máu cơ tim thất phải
Siêu âm là phương tiện chẩn đoán hình ảnh được lựa chọn trong chẩn đoán NMCT thất phải. Siêu âm tim rất hữu ích trong loại trừ tràn dịch màng tim, nguyên nhân có thể chẩn đoán nhầm với NMCT thất phải. NMCT thất phải cấp đôi khi chẩn đoán nhồi máu phổi khi không có các biến cố về thiếu máu.
Siêu âm NMCT thất phải bao gồm:
Giãn thất phải
Suy chức năng tâm thu thất phải
Rối loạn vận động vùng và vận động nghịch thường của vách liên thất: không hay giảm vận động thành sau dưới.
Lâm sàng:
Tụt áp
Phổi không rales
Đáp ứng với truyền dịch
Điện tâm đồ có hình ảnh NMCT sau dưới
Vai trò của siêu âm tim gắng sức
Siêu âm tim gắng sức lần đầu tiên được giới thiệu năm 1979 đánh giá thiếu máu cơ tim. Đến ngày nay, vai trò của nó càng rõ rệt trong đánh giá thiếu máu cơ tim và sống còn cơ tim.
Sử dụng phần mềm số hóa và kỹ thuật second harmonic
Khi từ hai vùng trở lên không quan sát được sử dụng chất cản âm để quan sát vận động vùng rõ hơn.
Nguyên tắc cơ bản và định nghĩa
Thiếu máu cơ tim được đặc trưng bởi giảm tưới máu đến các tế bào cơ tim và có thể xảy ra lúc nghỉ hay gắng sức. Vùng cơ tim còn sống có thể phát hiện dễ dàng khi co bóp bình thường. Sự phân biệt giữa vùng cơ tim giảm chức năng nhưng vẫn còn sống với cơ tim hoại tử là ứng dụng phổ biến trên lâm sàng. Thiếu máu cơ tim gây rối loạn vận động vùng thành tim trong vòng vài giây. Nhiều nghiên cứu đã chỉ ra rằng thời gian và mức độ nặng của thiếu máu là nguyên nhân chính quyết định hồi phục chức năng và chuyển hóa cơ tim. Rối loạn chức năng thất trái theo vùng nặng gây ra suy giảm chức năng tâm thu thất trái ở BN bệnh ĐMV có thể từ mức độ hoại tử cơ tim, đờ cơ tim hay đông miên cơ tim.
Đờ cơ tim là tình trạng suy chức năng co bóp ở cơ tim còn sống và là hậu quả của thiếu máu cơ tim thoáng qua sau tái tưới máu.
Đông miên cơ tim là tình trạng cơ tim giảm chức năng co bóp kéo dài do thiếu máu cơ tim mạn tính. Đông miên cơ tim được mô tả như tình trạng thích nghi với thiếu máu nặng và mạn tính và tăng nguy cơ đột tử ngay cả khi không nhồi máu cơ tim.
Phân tích kết quả siêu âm tim gắng sức
Ở bệnh nhân thiếu máu cơ tim, gắng sức làm rối loạn vận động vùng mới xuất hiện. Tăng khả năng co bóp của vùng cơ tim mà trước đó vận động bất thường bằng thuốc tăng co bóp để đánh giá cơ tim còn sống nhưng suy giảm chức năng. Vùng cơ tim suy chức năng có thể nằm trong các tình huống sau:
Tăng cường khả năng co bóp mà tăng với kích thích tối đa
Không cải thiện (vùng cơ tim không còn sống)
Chức năng tim kém hơn (thiếu máu)
Liều thấp Dobutamin tăng vận động nhưng liều cao lại giảm vận động. Đáp ứng hai pha này được đặc trưng bằng vùng cơ tim còn sống và thiếu máu ở liều gắng sức cao hơn.
Các phương pháp siêu âm tim gắng sức
Phân tích hình ảnh gắng sức dựa trên so sánh vận động vùng khi nghỉ và trong quá trình gắng sức. Đánh giá bán định lượng bằng chỉ số vận động vùng thành tim. Phương pháp mới trong đánh giá vận động vùng bằng Doppler mô và đánh dấu mô cơ tim (speckle tracking) dựa trên sức căng và tốc độ căng cơ tim. Bởi rối loạn vận động vùng xảy ra trong vòng vài giây của thiếu máu cấp tính và giai đoạn hồi phục xảy ra trong vòng 2 đến 3 phút. Hình ảnh phải được ghi khẩn trương trong hay ngay sau gắng sức.
Chỉ số vận động vùng thành tim (WMSI)
Được tính bằng tổng số điểm chia cho số vùng
Dựa trên đánh giá ASE về vùng cơ tim bao gồm cả vùng mỏm
Bình thường WMSI = 1
Bất kỳ vùng nào có điểm số >1 ở ít nhất một vùng là có vận động bất thường
Các hình thức siêu âm tim gắng sức: Siêu âm gắng sức có thể bằng thể lực hoặc bằng thuốc phụ thuộc vào khả năng gắng sức của bệnh nhân, trang thiết bị và trình độ của cơ sở y tế và mục đích của siêu âm gắng sức. Độ nhạy của siêu âm gắng sức phụ thuộc vào chất lượng hình ảnh và trình độ kinh nghiệm của người làm siêu âm.
Siêu âm tim gắng sức bằng thể lực: giúp phát hiện bệnh ĐMV và có giá trị tiên lượng.
Những lưu ý khi làm gắng sức thể lực:
Định nghĩa tổn thương có ý nghĩa trên chụp mạch là ĐMV hẹp từ 50% trở lên được coi là tổn thương có ý nghĩa.
Hồi phục tần số tim nhanh có thể che dấu kết quả dương tính
Những triệu chứng làm hạn chế gắng sức có thể bộc phần lớn các tổn thương nặng nề nhưng không phải tất cả các trường hợp hẹp mạch.
Đáp ứng tăng huyết áp có thể làm dương tính giả, đặc biệt với siêu âm gắng sức bằng xe đạp nằm ngửa.
Siêu âm tim gắng sức có thể cung cấp đầy đủ các thông tin gắng sức: rối loạn vận động vùng, các biến đổi trên điện tâm đồ và các đáp ứng về huyết động khi gắng sức, các triệu chứng đau ngực hay khó thở khi gắng sức.
Chỉ định ngừng gắng sức:
Chỉ định tuyệt đối:
Xuất hiện ST khả năng ở >1 mm
Tụt huyết áp tâm thu >10 mmHg và có dấu hiệu thiếu máu
Đau ngực vừa đến nặng, khó thở
Bệnh nhân yêu cầu ngừng gắng sức
Chỉ định tương đối:
Rối loạn nhịp (trừ nhịp nhanh thất là tuyệt đối)
ST chênh xuống >2 mm
Tăng mức độ đau ngực
Tụt huyết áp >10 mmHg mà không có triệu chứng
Huyết áp tâm thu >250 mmHg hay HA tâm trương >115 mmHg
Siêu âm tim gắng sức bằng xe đạp nằm ngửa
Cho phép thu được hình ảnh liên tục tại đỉnh gắng sức ngay cả giai đoạn trung gian của gắng sức
Tần số tim tối đa cao hơn với gắng sức bằng thảm chạy
Hình thức gắng sức xe đạp có đáp ứng huyết áp cao hơn.
Một số nghiên cứu so sánh: siêu âm gắng sức bằng xe đạp phát hiện thiếu máu lan rộng nhiều hơn.
Siêu âm gắng sức xe đạp không thực hiện được ở một số bệnh nhân như đau khớp gối, tai biến, mất khả năng vận động…
Một số lưu ý khi làm siêu âm tim gắng sức bằng thể lực:
Bệnh nhân phải có khả năng gắng sức chạy trên thảm chạy hay đạp xe.
Phòng siêu âm gắng sức phải thuận lợi cho việc thay đổi nhanh tư thế để lấy hình ảnh siêu âm sau gắng sức
Điều dưỡng phải chuẩn bị sẵn sàng tiêm cản âm nếu cần thiết.
Sử dụng phác đồ Bruce là phổ biến nhất
Với các hình thức gắng sức bằng thể lực, hình ảnh phải được ghi trong vòng một phút sau gắng sức.
Siêu âm tim gắng sức bằng thuốc
Siêu âm gắng sức với Dobutamin:
Chỉ định:
Những bệnh nhân không có khả năng gắng sức
Protocol cơ bản của siêu âm gắng sức với Dobutamin ở những bệnh nhân không có khả năng gắng sức
Protocol tiêu chuẩn: mỗi giai đoạn 3 phút và tăng liều 5, 10, 20, 30 mcg/kg/phút (bắt đầu ở giai đoạn 30 mcg/kg/phút, tiêm Atropin tới 2 mg)
Ngừng gắng sức khi có triệu chứng không dung nạp được, tụt huyết áp và tăng huyết áp.
Nhồi máu cơ tim hay rối loạn nhịp thất bền bỉ gặp
Siêu âm gắng sức với Dobutamin đánh giá sống còn cơ tim:
Khi nghỉ, có hình ảnh giảm vận động vùng thành tim. Với Dobutamin liều thấp, vận động những vùng này cải thiện. Đây có thể là đờ cơ tim hay cơ tim đông miên.
Siêu âm với Dobutamin có thể đánh giá đáp ứng hai pha: liều thấp tăng vận động nhưng với Dobutamin liều cao gây giảm vận động. Có thể là cơ tim đông miên. Đáp ứng hai pha dự đoán khả năng hồi phục sau tái tưới máu.
Chỉ số vận động vùng phụ thuộc nhiều vào chủ quan, đặc biệt là kinh nghiệm của người làm siêu âm.
Đánh giá chức năng vùng phải dựa vào phân tích hình ảnh siêu âm. Vì thế, chất lượng hình ảnh đóng vai trò quan trọng.
Tốc độ căng cơ tim (strain rate) có thể làm tăng độ chính xác của siêu âm gắng sức với Dobutamin.
Giá trị của test gắng sức âm tính
Nguy cơ rất thấp: tỷ lệ NMCT hay tử vong tim mạch
Nguy cơ thấp (tần số tim gần tối ưu hoặc EF
Một số thăm dò không xâm lấn khác trong chẩn đoán bệnh lý động mạch vành
Điện tâm đồ gắng sức
Giới thiệu
Là nghiệm pháp thường được sử dụng trong thực hành tim mạch. Hệ thống thiết bị làm nghiệm pháp bao gồm thảm chạy/xe đạp, máy đo huyết áp (HA) và máy ghi điện tâm đồ liên tục. Độ nhạy của phương pháp trong chẩn đoán bệnh mạch vành là 68%, độ đặc hiệu 77%. Ngoài giá trị chẩn đoán, nghiệm pháp điện tâm đồ (ĐTĐ) gắng sức còn có giá trị phân tầng nguy cơ các trường hợp hội chứng động mạch vành mạn tính. Phương pháp này có khả năng dự đoán chính xác trên 90% ở nhóm bệnh nhân nguy cơ tim mạch trung bình đến cao (ví dụ: Nam giới cao tuổi có các triệu chứng thiếu máu cơ tim), tuy nhiên gặp hạn chế trong việc đánh giá nhóm bệnh nhân có nguy cơ thấp mắc bệnh thiếu máu cơ tim, (ví dụ: Nữ giới trung niên không có triệu chứng, độ nhạy của điện tâm đồ gắng sức
Chỉ định
Chẩn đoán thiếu máu cục bộ cơ tim ở các đối tượng có nguy cơ mắc bệnh từ trung bình đến cao, đau thắt ngực do co thắt mạch vành.
Sau nhồi máu cơ tim: Trước khi ra viện (đánh giá mức độ gắng sức tối đa của bệnh nhân vào ngày thứ 4 – 7 để tiên lượng, quyết định các chương trình luyện tập và đánh giá điều trị), giai đoạn muộn sau ra viện (3 – 6 tuần).
Trước và sau can thiệp mạch vành (cần chú ý chống chỉ định).
Đánh giá rối loạn nhịp: Đánh giá và tối ưu hoá đáp ứng tần số của máy tạo nhịp, đánh giá các rối loạn nhịp gây ra do luyện tập đã biết hoặc nghi ngờ, và đánh giá tác dụng của thuốc chống loạn nhịp.
Chống chỉ định
Sốt do virus hoặc nhiễm virus cấp tính gây mệt mỏi.
Viêm cơ tim/viêm màng ngoài tim.
Hẹp khít van động mạch chủ.
Tách thành động mạch chủ.
Tăng huyết áp khó kiểm soát.
Suy tim mất bù.
Đau thắt ngực không ổn định hoặc nhồi máu cơ tim cấp.
Rối loạn nhịp nghiêm trọng khi nghỉ (ví dụ: Rung nhĩ không kiểm soát hoặc block dẫn truyền hoàn toàn).
Tổn thương nặng thân chung động mạch vành trái đã biết hoặc tương đương.
Các trường hợp hạn chế khả năng vận động (bệnh xương khớp…).
Bất thường trên điện tâm đồ gây khó đánh giá ST (ví dụ: Block nhánh trái, phì đại thất trái do tăng gánh hoặc ST chênh xuống do ngộ độc digoxin).
Tiêu chuẩn ngừng nghiệm pháp
Đạt đến tần số tim mục tiêu (các test có độ nhạy độ đặc hiệu tốt hơn nếu đạt tới nhịp tim mục tiêu > 85% x [220 – tuổi] ở nam và > 85% x [210 – tuổi] ở nữ).
Đau thắt ngực tiến triển xấu hoặc khó thở mất bù.
Chóng mặt.
Mệt cần phải dừng hoặc theo yêu cầu của bệnh nhân.
Rối loạn nhịp nhĩ dai dẳng (trừ ngoại tâm thu nhĩ).
Ngoại tâm thu thất chu kỳ hoặc nhịp nhanh thất.
Biến đổi đoạn ST có ý nghĩa (khả năng ít nhất 2 mm hoặc chênh xuống ít nhất 5 mm).
Tụt huyết áp hoặc huyết áp không tăng khi tăng mức gắng sức.
Tăng huyết áp quá mức (huyết áp tâm thu >220 mmHg).
Block nhĩ thất độ cao hoặc block nhánh mới xuất hiện.
Tiêu chuẩn nghiệm pháp gắng sức dương tính
Hình 2.41: Các dạng biến đổi ST trên điện tâm đồ gắng sức
ST chênh xuống đi ngang hoặc đi xuống ít nhất 1 mm và 80 ms sau điểm J (điểm nối giữa phức bộ QRS và đoạn ST).
ST khả năng.*
Tăng biên độ phức bộ QRS (giãn thất trái do thiếu máu).
Không tăng được huyết áp khi gắng sức (rối loạn chức năng thất trái do thiếu máu cơ tim).*
Rối loạn nhịp thất.*
Triệu chứng thiếu máu điển hình.
Không có khả năng tăng tần số tim.
* Các tình trạng này có chỉ định chụp mạch vành cấp.
Nguyên nhân dương tính giả
Các bệnh cơ tim.
Tăng huyết áp.
Hẹp đường ra thất trái.
Sa van hai lá.
Tăng thông khí.
Bất thường điện tâm đồ lúc nghỉ (LBBB, tiền kích thích, dấu hiệu ngộ độc digoxin).
Rối loạn điện giải (hạ kali máu).
Tác dụng của các thuốc chống trầm cảm 3 vòng.
Hội chứng X.
Co thắt mạch vành.
Cường giao cảm.
Hướng dẫn về điện tâm đồ gắng sức của hiện nay theo khuyến cáo của Hội Tim Mạch Châu Âu (ESC) 2019
Trong lịch sử, điện tâm đồ gắng sức đã trở thành nền tảng để chẩn đoán các bệnh nhân có biểu hiện của hội chứng động vành mạn tính. Tuy nhiên, độ nhạy và độ đặc hiệu thấp hơn khi so sánh với các phương pháp khác. ESC hiện nay không khuyến cáo điện tâm đồ gắng sức ở các bệnh nhân chưa được chẩn đoán bệnh mạch vành trước đây.
Thay vào đó, ESC khuyến cáo sử dụng chụp cắt lớp vi tính ở các bệnh nhân có nguy cơ bị bệnh mạch vành thấp; các phương pháp đánh giá chức năng như siêu âm tim gắng sức với Dobutamin với bệnh nhân nguy cơ trung bình; và chụp mạch vành qua da với các bệnh nhân nguy cơ cao.
Chụp cắt lớp vi tính tim
Cắt lớp vi tính (CLVT) là biện pháp thăm dò không xâm lấn hữu hiệu trong đánh giá tổn thương động mạch vành.
Đánh giá điểm vôi hóa mạch vành
Mảng xơ vữa vôi hóa chiếm khoảng 20% gánh nặng xơ vữa toàn bộ mạch vành. Do vậy có thể đánh giá tổng thể mức độ xơ vữa mạch vành gián tiếp qua việc cho điểm mức độ canxi hóa mạch vành. Điểm vôi hóa có thể được đo thông qua chụp bức xạ thấp không đối quang (ví dụ không sử dụng thuốc cản quang chứa iod). Mức độ canxi hóa của mỗi động mạch vành được thể hiện bằng một con số và tính tổng là điểm vôi hóa chung của cả hệ mạch vành, thường là sử dụng thang điểm Agatston:
0 điểm: không mảng vôi hóa
1 – 99 điểm: vôi hóa nhẹ (nguy cơ thấp, tỷ lệ tử vong hoặc nhồi máu cơ tim hàng năm
100 – 399: vôi hóa trung bình (nguy cơ trung bình, tỷ lệ tử vong hoặc nhồi máu cơ tim hàng năm 1 – 3%)
≥ 400 điểm: vôi hóa nặng (nguy cơ cao, tỷ lệ tử vong hoặc nhồi máu cơ tim hàng năm > 3%).
Các nghiên cứu lâm sàng đã chứng minh đánh giá điểm vôi hóa mạch vành cung cấp thêm các thông tin cho phân tầng nguy cơ tim mạch ngoài các yếu tố nguy cơ cơ bản như tuổi, giới, tăng huyết áp, tiền sử gia đình, tăng lipid máu và đái tháo đường.
Kỹ thuật chụp CLVT động mạch vành
Chụp CLVT động mạch vành được thực hiện bằng cách tiêm thuốc cản quang chứa iod vào tĩnh mạch ngoại biên. Khi nồng độ thuốc cản quang trong động mạch chủ đạt đến mức độ nhất định, máy sẽ quét và hình ảnh được ghi nhận. Các hình ảnh được phân tích bằng phần mềm máy tính, cho phép tái tạo hình ảnh 2D và dựng hình ảnh 3D của động mạch vành, các buồng tim, cũng như cho biết các thông số thể tích .
Lưu ý về kỹ thuật
Độ phân giải theo thời gian: Thách thức cơ bản của việc dựng hình động mạch vành bằng CLVT là đạt được độ phân giải thời gian cao. Độ phân giải thời gian được định nghĩa là thời gian cần thiết để ghi được một ảnh. Do tim đập nên cần có thời gian tim “đông cứng” để thu nhận hình ảnh. Sự di động là lớn nhất trong thì tâm thu và tương đối tĩnh trong thì tâm trương, do vậy lấy hình ảnh được ghi trong thì tâm trương cho chất lượng cao hơn và chẩn đoán chính xác hơn. Do đó máy CLVT yêu cầu phải có khả năng thu được hình ảnh nhanh trong thì tâm trương khi quả tim ít chuyển động.
Độ phân giải theo không gian: Hình ảnh của các cấu trúc nhỏ như động mạch vành có yêu cầu cao về độ phân giải không gian. Độ phân giải không gian định nghĩa là khoảng cách nhỏ nhất giữa 2 phần mà có thể phát hiện được bởi đầu dò. Độ phân giải không gian của chụp CLVT được quyết định bởi kích thước điểm ảnh (ví dụ điểm ảnh 3D).
Kiểm soát nhịp tim:
Thời gian tâm thu tương đối như nhau ở bệnh nhân có tần số tim khác nhau, nhưng thời gian tâm trương thay đổi rất lớn. Tần số tim thấp (tức là là thích hợp và đảm bảo ghi hình ảnh không bị ảnh hưởng bởi chuyển động của động mạch vành).
Bệnh nhân thường được uống thuốc chẹn beta giao cảm 1 – 2 giờ trước khi chụp CLVT. Ngoài ra, tiêm tĩnh mạch thuốc chẹn beta giao cảm (metoprolol) bổ sung nhiều lần cho bệnh nhân đang trong máy chụp là một phương pháp an toàn, nhanh và hiệu quả để kiểm soát nhịp tim. Uống thuốc chẹn beta giao cảm trong 2 ngày (ngày chụp CLVT và ngày trước đó) cũng hiệu quả và hạn chế phải truyền metoprolol tĩnh mạch trong thời gian chụp.
Thuốc chẹn kênh canxi, thuốc chẹn kênh If (ivabradine) có thể được chọn thay thế ở các bệnh nhân có chống chỉ định với chẹn beta.
Với các máy chụp cắt lớp thế hệ mới: 256, 320, 512 dãy, không yêu cầu bắt buộc tần số tim thấp, tuy nhiên, chất lượng hình ảnh càng gia tăng khi tần số tim giảm.
Chiến lược để giảm liều phóng xạ
Một số chiến lược đã được áp dụng để giảm liều hiệu quả của phóng xạ ion hóa trong mỗi lần chụp:
Giảm trường quan sát (từ mỏm tim đến đáy tim).
Giảm điện áp ở các bệnh nhân không béo phì (từ 120 kV giảm xuống 100 kV).
Điều chỉnh dòng điện bằng điện tâm đồ (dòng điện giảm trong thì tâm thu và tăng trong thì tâm trương).
Điều chỉnh cổng chụp bằng điện tâm đồ (ống chỉ bật lên trong các thì cố định của chu kỳ tim, thường là giữa kỳ tâm trương hoặc 75% khoảng R – R).
Bằng cách kết hợp các kỹ thuật này, liều hiệu quả chụp CLVT động mạch vành gần đây đã đạt tới 1 mSv (milli – Sievert).
Độ nhạy và độ đặc hiệu
CLVT từ 64 dãy trở lên có độ nhạy cao (95%) và độ đặc hiệu cao (83%). Vì thế, CLVT động mạch vành có giá trị dự báo âm tính rất cao (lên tới 95%). Ứng dụng chính của CLVT động mạch vành là để loại trừ các bệnh động mạch vành nặng ở các bệnh nhân nguy cơ tim mạch thấp đến trung bình.
Ứng dụng lâm sàng của chụp CLVT
So sánh với chụp động mạch vành (ĐMV) qua da: Chụp ĐMV qua da vẫn là tiêu chuẩn vàng trong chẩn đoán các bệnh lý ĐMV do có độ phân giải vượt trội. Hơn nữa, chụp ĐMV qua da cho phép tiến hành can thiệp ĐMV nếu tổn thương có ý nghĩa. Tuy nhiên, đây vẫn là một thăm dò xâm lấn và tiềm ẩn nguy cơ bị các biến chứng mạch máu bao gồm nhồi máu cơ tim, đột quỵ não và các biến chứng tại mạch máu đường vào. Máy chụp CLVT 256 – 512 dãy có thể gia tăng độ bao phủ đồng thời giảm thời gian quét xuống dưới 0,5 giây, cho phép ghi hình toàn bộ tim trong một nhát bóp. So với chụp mạch truyền thống, chụp CLVT có độ phân giải không gian thấp hơn (0,4 – 0,6 mm so với 0,2 mm) và độ phân giải thời gian thấp hơn (60 – 220 ms so với 8 ms).
So sánh với các nghiệm pháp thăm dò chức năng: Trong lịch sử, các nghiệm pháp thăm dò chức năng không xâm nhập (ví dụ như nghiệm pháp gắng sức, siêu âm tim gắng sức, hình ảnh học hạt nhân, chụp cộng hưởng từ đánh giá tưới máu) đã được sử dụng để chọn lọc những bệnh nhân có nguy cơ trung bình, hay nói cách khác là những đối tượng có thể cần phải chụp và can thiệp động mạch vành qua da. Tuy nhiên, đa số thăm dò trên đòi hỏi nhiều công sức để thực hiện và không sẵn có tại nhiều bệnh viện. Hơn nữa, hạn chế chính của các thăm dò này là tỷ lệ dương tính giả dẫn tới một số bệnh nhân phải thông tim chẩn đoán không cần thiết.
Chỉ định chụp cắt lớp vi tính tim
Chỉ định
Chỉ định chính của chụp CLVT tim trong các khuyến cáo thực hành hiện nay là loại trừ hoặc phát hiện tổn thương động mạch vành. Chụp CLVT đặc biệt hiệu quả để đánh giá các bất thường giải phẫu động mạch vành cũng như cầu nối chủ vành.
Ưu tiên CLVT động mạch vành trong hội chứng động mạch vành mạn tính, các trường hợp có khả năng mắc bệnh động mạch vành thấp và trung bình (ESC 2019).
Các chỉ định bổ sung bao gồm
Tầm soát bệnh lý động mạch vành (ví dụ: Điểm vôi hóa).
Đánh giá cầu nối chủ vành.
Đánh giá các bất thường giải phẫu động mạch vành.
Lập bản đồ các tĩnh mạch phổi trước các thăm dò điện sinh lý và triệt đốt.
Đánh giá giải phẫu trong các bệnh lý tim bẩm sinh.
Đánh giá các khối bất thường trong lòng động mạch vành.
Đánh giá động mạch chủ trong trường hợp theo dõi tách thành ĐMC.
Đánh giá stent động mạch vành.
Đánh giá hình thái mảng xơ vữa – mềm/vôi hóa/hỗn hợp.
Ưu điểm và nhược điểm của chụp cắt lớp vi tính tim
Ưu điểm:
Nhanh chóng.
Không xâm nhập (tránh được các biến cố mạch máu do chụp mạch xâm nhập).
Không quá đắt tiền.
Đánh giá chi tiết cầu nối chủ vành điểm đầu/điểm cuối/cầu nối.
Đánh giá đặc điểm của mảng xơ vữa – CLVT có khả năng đánh giá mảng xơ vữa không chỉ trong lòng mạch mà cả thành mạch (xơ vữa mềm/vôi hóa/hỗn hợp).
Nhược điểm:
Phơi nhiễm với bức xạ ion hóa.
Khó đánh giá mức độ hẹp mạch nếu mức độ vôi hóa mạch vành đáng kể.
Khó đánh giá trong lòng stent cũng như mức độ thông thoáng của stent.
Khó đánh giá mức độ hẹp cầu nối chủ vành tại vị trí miệng nối.
Đòi hỏi bệnh nhân có nhịp tim chậm và đều.
Ứng dụng mới của chụp cắt lớp vi tính tim
Chụp cắt lớp vi tính tưới máu:
Các kỹ thuật mới của chụp CLVT cho phép khảo sát giải phẫu hệ động mạch vành cùng với thông số chức năng. Thuốc cản quang được tiêm tĩnh mạch và cơ tim được quét nhiều lần trong một thời khoảng. Thuốc cản quang ngay khi đi qua vùng cơ tim cần đánh giá sẽ được đánh dấu và ghi thành đường cong thời gian – tỷ trọng, rồi sau đó được phiên giải để xác định tưới máu mô. Tuy nhiên, với công nghệ chụp CLVT hiện tại, rào cản chính của việc áp dụng chụp CLVT tưới máu một cách thường quy là liều phóng xạ cao.
Các kỹ thuật chẩn đoán hình ảnh đa phương thức (hybrid):
Một kỹ thuật thay thế cho chụp CLVT tưới máu là phiên giải các thông tin giải phẫu từ chụp cắt lớp vi tính mạch máu cùng những thông tin về chức năng từ siêu âm tim gắng sức, chụp cắt lớp bằng bức xạ đơn photon (SPECT), PET hoặc chụp cộng hưởng từ tưới máu.
Các nghiên cứu lâm sàng chỉ ra rằng phối hợp thông tin về mặt giải phẫu và chức năng sẽ làm nâng cao độ nhạy và độ đặc hiệu so với từng kỹ thuật chẩn đoán riêng lẻ.
Xạ hình tưới máu cơ tim
Tổng quan
Trong trường hợp hẹp mạch vành có dòng chảy giới hạn, tưới máu cơ tim khi nghỉ thường vẫn bình thường do giãn động mạch. Khi gắng sức, có ít dự trữ chất giãn mạch, và tưới máu hạ lưu sẽ thấp hơn so với hạ lưu của mạch máu không bị tắc nghẽn.
Trong nghiệm pháp gắng sức, sử dụng một chất đánh dấu tưới máu phóng xạ, chất này được bắt giữ bởi các tế bào cơ tim, mức độ tùy thuộc lưu lượng máu.
Hình ảnh SPECT sau đó được ghi lại và sự phân phối hạt nhân phóng xạ phản ánh khả năng sống còn và tưới máu tại thời điểm làm nghiệm pháp gắng sức. Một hình ảnh riêng biệt được ghi sau khi tiêm chất đánh dấu ở trạng thái nghỉ (chất đánh dấu gắn technetium- 99m) hoặc sau khi thuốc được phân phối lại khi làm nghiệm pháp gắng sức (thallium-201), và sự phân phối của hạt nhân phóng xạ phản ánh sống còn của cơ tim.
Nghiệm pháp gắng sức trên xạ hình tưới máu cơ tim
Nghiệm pháp gắng sức bằng thể lực (máy chạy bộ hoặc xe đạp) là dạng gắng sức sinh lý nhất, cung cấp thông tin lâm sàng quan trọng có thể bổ sung cho các thăm dò hình ảnh. Những bệnh nhân phù hợp hơn với phương pháp xạ hình tưới máu cơ tim nhưng không đạt được nhịp tim mục tiêu khi vận động sẽ được làm nghiệm pháp gắng sức bằng thuốc. Các loại thuốc được sử dụng thuộc hai loại:
Thuốc giãn mạch chính (dipyridamole hoặc adenosine): Lựa chọn đầu tiên, trừ khi có chống chỉ định (bệnh hô hấp hoặc block nhĩ thất). Adenosine gây giãn mạch vành trực tiếp thông qua thụ thể A-2a. Dipyridamole hoạt động gián tiếp, làm tăng adenosine nội sinh bằng cách ức chế sự phân hủy và tái hấp thu của nó.
Thuốc tăng co (dobutamine): Dobutamine là chất chủ vận beta tổng hợp, làm tăng nhu cầu oxy của cơ tim, gây ra giãn mạch vành thứ phát.
Chất đánh dấu phóng xạ
Chất đánh dấu phóng xạ trong xạ hình tưới máu cơ tim được sử dụng trong lâm sàng là thallium-201 (201Tl) và các chất mới dựa trên Technetium-99m (99mTc) là sestamibi và tetrofosmin.
Thallium-201
201Tl dưới dạng clorua thallous, là một đồng vị được tạo ra từ cyclotron, đi vào tế bào cơ tim theo gradient điện hóa theo cách tương tự như kali. Sau khi thuốc đạt nồng độ cao nhất sẽ dần cân bằng giữa các khoang nội bào và nội mạch, và do đó cần phải ghi ngay hình ảnh. Sau 4 giờ cần ghi lại hình ảnh phân bố thuốc để đánh giá tưới máu cơ tim khi nghỉ.
Chất đánh dấu gắn Technetium-99m
99mTc được sản xuất từ một máy phát điện và được tạo phức với một phân tử hữu cơ (sestamibi hoặc tetrofosmin). 99mTc-sestamibi và 99mTc-tetrofosmin khuếch tán thụ động vào tế bào cơ, là nơi chúng liên kết với ty thể.
Hình ảnh có thể được thực hiện sau khi tiêm 30 – 60 phút, nhưng cần phải tiêm riêng 2 lần khi gắng sức và khi nghỉ ngơi cách nhau 1 hoặc 2 ngày. Có thể tiêm nitrat trước khi tiêm thuốc lúc nghỉ để tối đa hóa sự hấp thu thuốc vào cơ tim.
So sánh các bộ đếm
201Tl là một chất đánh dấu tưới máu vượt trội về mặt sinh lý, nhưng 99mTc có một số lợi thế về ứng dụng thực tế. Các hình ảnh được tạo ra có chất lượng cao hơn vì các photon có năng lượng cao hơn và có thể được kiểm soát để cho phép đánh giá chức năng tâm thất trái. Ngoài ra, thời gian bán hủy ngắn hơn (6 giờ so với 73 giờ) làm giảm phơi nhiễm bức xạ cho bệnh nhân.
Ứng dụng xạ hình tưới máu cơ tim trên lâm sàng
Chỉ định
Đánh giá chẩn đoán và tiên lượng trong nghi ngờ bệnh mạch vành khi điện tâm đồ gắng sức có thể không đáng tin cậy:
Phụ nữ.
Bệnh nhân không đạt mục tiêu khi làm nghiệm pháp gắng sức.
Bệnh nhân có điện tâm đồ nghỉ ngơi bất thường đáng kể.
Hướng dẫn quản lý trong bệnh mạch vành đã biết:
Sau nhồi máu cơ tim.
Sau chụp động mạch vành.
Sau tái thông mạch vành.
Đánh giá khả năng sống còn, sự thiếu máu và chức năng cơ tim trong rối loạn chức năng thất trái do thiếu máu cục bộ.
Giải thích hình ảnh
Khiếm khuyết tưới máu:
Cố định (trên gắng sức và nghỉ ngơi): Gợi ý sẹo sau nhồi máu cơ tim.
Đảo ngược (chỉ trên gắng sức): Gợi ý giảm tưới máu cơ tim đoạn xa tương ứng mạch vành bị hẹp có hạn chế dòng chảy.
Xác định vị trí (vùng tưới máu của mạch vành), diện tích và mức độ nghiêm trọng (vai trò tiên lượng).
Có thể cần được phân biệt với các hình giả, ví dụ: Mô mềm ở phía trước ở phụ nữ, phía sau ở nam giới.
Dấu hiệu nguy cơ cao, ví dụ:
Phổi tăng hấp thu Tl-201.
Giãn cơ tim do thiếu máu cục bộ thoáng qua (TID): Tăng thể tích thất trái sau gắng sức so với lúc nghỉ.
Chức năng thất trái trên ghi hình có gắn điện tâm đồ.
Giá trị lâm sàng của xạ hình tưới máu cơ tim
Chẩn đoán hoặc loại trừ bệnh mạch vành: Để phát hiện hẹp mạch vành, độ nhạy của xạ hình tưới máu cơ tim là khoảng 90%. Độ đặc hiệu thường thấp hơn, khoảng 75%, nhưng có thể bị đánh giá thấp do diễn giải quá mức các hình giả và do sai số xác định. Trong thực tế, tỷ lệ chuẩn tắc có ý nghĩa hơn độ đặc hiệu, đó là tỷ lệ các xét nghiệm bình thường trong dân số có xác suất thấp và tỷ lệ này thường là 90% trở lên.
Tiên lượng: Xạ hình tưới máu cơ tim là một thăm dò đánh giá chức năng, và do đó không thể dự đoán giải phẫu mạch vành với độ chính xác hoàn hảo. Tuy nhiên, phương pháp này cung cấp thông tin với khả năng tiên lượng mạnh mẽ độc lập với dữ liệu lâm sàng và thậm chí cả dữ liệu chụp động mạch.
Xạ hình tưới máu cơ tim bình thường dự đoán tỷ lệ tử vong do tim hoặc nhồi máu cơ tim hàng năm là khoảng 0,6%.
Nguy cơ tử vong thấp duy trì tới 5 năm ở những bệnh nhân không có bệnh mạch vành biết trước, khoảng thời gian này ngắn hơn ở bệnh nhân tiểu đường và những người mắc bệnh mạch vành đã được chẩn đoán.
Nguy cơ tử vong tăng tỷ lệ thuận với mức độ bất thường trên kết quả xạ hình.
Tử vong do tim chủ yếu liên quan đến chức năng tâm thu thất trái, trong khi nhồi máu cơ tim không tử vong chủ yếu được dự đoán theo phạm vi vùng giảm tưới máu.
Tiên lượng về lợi ích từ tái thông mạch vành có thể hạn chế ở bệnh nhân có phạm vi giảm tưới máu chiếm > 10% khối cơ thất trái.
Rối loạn chức năng thất trái: Xạ hình tưới máu cơ tim có giá trị trong đánh giá bệnh nhân bị rối loạn chức năng thất trái do thiếu máu cục bộ để xác định mức độ đông miên của cơ tim và khả năng phục hồi chức năng sau khi tái thông mạch.
Cộng hưởng từ đánh giá thiếu máu cục bộ và sống còn cơ tim trong bệnh lý động mạch vành
Chụp Cộng hưởng từ trong đánh giá thiếu máu cơ tim
Để phát hiện thiếu máu cơ tim có thể sử dụng các chất đối quang từ gadolinium ghi hình ảnh tưới máu cơ tim thì đầu cùng với các tác nhân giãn mạch, hoặc đánh giá vận động vùng thành tim với dobutamine, tương tự như siêu âm tim gắng sức.
Coi chụp động mạch vành là tiêu chuẩn vàng, CHT đánh giá tưới máu cơ tim thì đều có độ nhạy 91%, độ đặc hiệu 81% và được ưa chuộng hơn so với kỹ thuật chụp SPECT bởi không phụ thuộc vào các yếu tố nhiễu khi làm với SPECT và không liên quan đến bất kỳ bức xạ ion hóa nào. Đồng thời CHT lại có độ phân giải không gian tốt hơn và tương tự như PET, có thể định lượng mức độ tưới máu mô, mặc dù phương tiện khá cồng kềnh và hiện mới chỉ được sử dụng trong nghiên cứu.
Nghiệm pháp gắng sức dùng thuốc giãn mạch bằng cách truyền adenosine với tốc độ 140 μg/kg/min (3 mg/mL) đến khi có bằng chứng về sự đáp ứng huyết động (thường là 3 phút), tiếp theo truyền nhanh chất đối quang gadolinium và nhanh chóng ghi hình các mặt cắt trục ngắn ở các mức đáy, giữa tâm thất và mỏm tim khi chất đối quang đi vào cơ tim. Quy trình chụp yêu cầu bệnh nhân phải nín thở lâu. Có thể ghi được hình ảnh rõ nét bằng cách hít thở nhẹ nhàng sau khi hít sâu và nín thở tối đa.
Khi sử dụng adenosine trong nghiệm pháp gắng sức sử dụng tác nhân giãn mạch bệnh nhân được yêu cầu không sử dụng các thức ăn và đồ uống có chứa cafein (VD: Cà phê, chè, socola, Coca-Cola…) lý tưởng là trong vòng 24 giờ trước khi thực hiện nghiệm pháp. Chống chỉ định trong trường hợp bệnh nhân có block nhĩ thất độ cao và hen phế quản nặng. Trong nghiệm pháp gắng sức Dobutamine phải ngừng sử dụng thuốc chẹn β giao cảm và các thuốc chẹn kênh canxi trong vòng 48 giờ nhưng không cần ngừng những thuốc trên với nghiệm pháp sử dụng chất giãn mạch. Adenosine không nên sử dụng cùng với dipyridamole vì dipyridamole kéo dài đáng kể thời gian bán hủy của adenosine và bản thân nó cũng có thể được dùng như là một thuốc để test gắng sức.
Lưu ý trong thực hành: Để có hình ảnh tưới máu cơ tim trong nghiệm pháp gắng sức, nên đặt hai đường truyền tĩnh mạch riêng biệt, một đường lớn (18G hoặc lớn hơn) để tạo thuận lợi cho truyền nhanh chất đối quang và một đường truyền khác để truyền adenosine. Theo dõi huyết áp động mạch nên được thực hiện ở tay với đường truyền chất đối quang bởi sử dụng băng đo huyết áp có thể làm gián đoạn quá trình truyền adenosine.
Hạn chế đáng kể của hình ảnh CHT tưới máu cơ tim 1,5 Tesla là sự tồn tại của khoảng tối giả có thể làm giảm độ đặc hiệu trong phát hiện giảm tưới máu lớp dưới nội mạc. Hình ảnh với bước sóng dài hơn (3 tesla) có thể nâng cao hơn tỷ số tương phản trên sóng âm và làm giảm nguy cơ của yếu tố nhiễu này giúp cải thiện độ đặc hiệu của chẩn đoán.
Hiện tượng giả này có thể được xác định bằng hình ảnh tưới máu được ghi lại lúc nghỉ và được củng cố rõ hơn bằng hình ảnh chụp ở thì muộn. Kỹ thuật chụp thì muộn có thể phát hiện xơ hóa giúp cho phân biệt giữa thiếu máu và nhồi máu.
Điểm hạn chế của chụp CHT tim là hạn chế không gian bên trong máy quét và sự thiếu trang thiết bị hồi sức đảm bảo an toàn trong phòng chụp, cũng như các lượng tử hidro có thể ảnh hưởng làm nhiễu hình ảnh điện tâm đồ và làm việc sử dụng máy monitor theo dõi biến đổi ST trên điện tâm đồ không thực hiện được. Tuy nhiên, sự biến đổi ST trên điện tâm đồ là giai đoạn muộn trong quá trình thiếu máu, và theo dõi nhịp tim, khám lâm sàng và giao tiếp với người bệnh có thể thay thế cho sự theo dõi đoạn ST.
Mặc dù có những hạn chế nhất định, một hình ảnh cộng hưởng từ tưới máu cơ tim bình thường có thể đảm bảo > 99% không có biến cố trong 3 năm tiếp theo.
Cộng hưởng từ trong Đánh giá sống còn cơ tim và cơ tim đông miên
Bệnh tim thiếu máu cục bộ là nguyên nhân của hơn 60% bệnh nhân suy tim.
Tế bào cơ tim có khả năng sống còn được định nghĩa là vùng cơ tim được cấp máu bởi động mạch vành bị hẹp gây giảm khả năng co bóp của cơ tim nhưng chưa sẹo hóa và có thể phục hồi khả năng co bóp nếu được tái tưới máu thành công. Đông miên cơ tim là vùng cơ tim bị giảm co bóp do thiếu máu cơ tim phục hồi chức năng sau khi được tái tưới máu.
Tái tưới máu thành công ở những bệnh nhân bị thiếu máu vành đáng kể (> 4 vùng cơ tim) nhưng tế bào cơ tim có khả năng sống giúp cải thiện phân suất tống máu và tiên lượng tương quan với mức độ suy giảm chức năng thất trái. Theo phân tích kết quả dữ liệu từ nhiều nghiên cứu hồi cứu và sổ bộ (nghiên cứu tiến cứu để đánh giá vấn đề này đang được tiến hành và từ các báo cáo ngắn tạm thời). Tuy nhiên, tái tưới máu ở những bệnh nhân không có những tế bào cơ tim có khả năng sống dường như không mang lại lợi ích mà có thể còn gây hại, bởi vì những rủi ro cao hơn trong trường hợp suy chức năng tâm thu thất trái đáng kể.
Hình ảnh CHT tim thì ngấm thuốc đối quang muộn cho phép xác định vùng xơ hóa cơ tim khi nguyên nhân là thiếu máu lan rộng từ lớp dưới nội mạc hướng ra thượng tâm mạc.
CHT có độ phân giải về không gian tốt hơn, nó vượt trội hơn cả PET và SPECT trong xác định xơ hóa. Khả năng sống còn tỷ lệ với độ xơ hóa xuyên thành với vùng xơ hóa > 50% được định nghĩa là vùng cơ tim không có khả năng sống. Độ đặc hiệu có thể cải thiện bằng cách kết hợp kỹ thuật với gắng sức dobutamine liều thấp đánh giá rối loạn vận động vùng. Kỹ thuật này đặc biệt hữu ích với vùng nhồi máu xuyên thành và có độ nhạy 95% và độ đặc hiệu 85% khi kết hợp với hình ảnh ở thì ngấm thuốc muộn.
CHT thể hiện rằng, khi không có xơ hóa, chức năng cơ tim có thể phục hồi đáng kể ngay cả vùng cơ tim mỏng (và tái cấu trúc cơ tim mà trước giờ vẫn được coi là cơ tim không còn sống. Hơn thế nữa, sự ngấm thuốc muộn là một yếu tố tiên lượng độc lập có giá trị trong dự đoán tử vong.
Chụp động mạch vành và một số thăm dò xâm lấn khảo sát bệnh động mạch vành
Kỹ thuật chụp động mạch vành
Ống thông chụp động mạch vành
Các ống thông dùng trong chụp động mạch vành để chẩn đoán và điều trị có nhiều hình dạng khác nhau. Ở Anh, thường dùng nhiều nhất là ống thông Judkins Left 4 và Judkins Right 4 (JL4 và JR4) để chụp động mạch vành trái và phải, ống thông đuôi lợn (pigtail) dùng để chụp buồng thất trái. Đường kính của ống thông được tính bằng đơn vị French (Fr), 6 Fr tương ứng 2 cm, ống thông thường dùng có đường kính dao động từ 4 – 8 Fr.
Hình dạng của các ống thông thông dụng
Hình 2.42: Hình dạng của các loại ống thông hay sử dụng
Kỹ thuật luồn ống thông và sử dụng bộ phận manifold
Dây dẫn đầu cong (J- tipped) đường kính 0.035 inch luồn qua ống thông rồi kết nối với van một chiều và bơm nước cả hệ thống để đảm bảo không có khí trong ống thông.
Dưới màn tăng sáng, dây dẫn được đẩy theo đường đi của động mạch, theo sau là ống thông cho tới gốc động mạch chủ ngay phía trên van động mạch chủ. Rút dây dẫn sau khi ống thông được đẩy đến vị trí này.
Để đảm bảo không có khí hay cục máu đông trong lòng ống thông, dùng xilanh kết nối với van một chiều và hút khoảng 5 mL máu ra rồi bỏ đi. Sau đó, ống thông được kết nối với bộ phận manifold để theo dõi áp lực, bơm nước, bơm cản quang tạo thành một hệ thống khép kín.
Kỹ thuật bơm thuốc cản quang
Một điểm lưu ý lớn nhất trong toàn bộ quá trình chụp mạch vành là phải đảm bảo không được bơm khí vào hệ mạch vành. Sau khi hút đầy thuốc cản quang vào xilanh, cần dựng thẳng xilanh lên sao cho các bọt khí đi hết lên phía trên. Sau đó, bơm thuốc cản quang đều tay để nhìn rõ toàn bộ giải phẫu hệ mạch vành.
Chú ý theo dõi đường áp lực trước khi bơm thuốc cản quang: Đường cong áp lực giảm xuống gợi ý hẹp lỗ vào hoặc đưa ống thông chụp vào quá sâu, hoặc đi vào nhánh bên.
Chụp động mạch vành/buồng thất trái
Động mạch vành trái
Tư thế nghiêng trái 50o (LAO 50) là tư thế tốt nhất để luồn ống thông vào cả lỗ vành phải và lỗ vành trái.
Tuy nhiên trong thực tế, có thể dùng tư thế thẳng mặt (AP) để luồn sonde chụp vào mạch vành trái.
Sonde JL4 gần như tự trôi vào động mạch vành trái mà không cần xoay chỉnh sonde nhiều.
Ở bệnh nhân bị giãn gốc động mạch chủ (THA, bệnh van ĐM chủ), có thể cần phải dùng sonde JL5 (với độ cong lớn hơn) để chụp. Trong trường hợp ngược lại, nếu gốc ĐM chủ hẹp thì dùng JL3.5.
Động mạch vành phải
Tư thế nghiêng trái 50 độ (LAO 50) là tư thế tốt nhất để luồn ống thông vào lỗ vành phải.
Sonde chụp JR4 được đưa tới gốc động mạch chủ cho đến khi đầu sonde nằm trên van ĐM chủ khoảng 1 – 2 cm.
Xoay sonde chụp cùng chiều kim đồng hồ, khi đó đầu sonde sẽ xoay và hướng vào lỗ động mạch vành phải. Đôi khi cần phải giảm lực xoay để phòng sonde chụp bị lệch ra khỏi lỗ vành phải.
Thường bác sĩ sẽ cảm nhận được có sự di lệch nhẹ sang bên khi sonde chụp vào trong lỗ vành phải.
Trước khi bơm thuốc cản quang, phải đảm bảo không có hiện tượng giảm đường cong áp lực sau khi đầu sonde chụp vào trong lỗ mạch vành.
Chú ý: Khi có giảm đường cong áp lực gợi ý sonde chụp chọn lọc vào nhánh Conus, và nếu bơm cản quang vào nhánh này có thể gây ra rối loạn nhịp nguy hiểm, cần rút lại nhẹ sonde đến khi thấy áp lực tăng lên.
Chụp buồng thất trái
Đưa ống thông đuôi lợn (sonde pigtail) vào gốc ĐM chủ, cách van khoảng vài cm rồi rút dây dẫn vào trong sonde cách đầu sonde 5 – 10 cm rồi nhẹ nhàng đẩy sonde xuống buồng thất trái.
Nếu không đẩy qua được van ĐM chủ, rút nhẹ sonde về đồng thời xoay nhẹ sonde.
Nếu không thành công, sử dụng dây dẫn mềm đầu thẳng và một sonde chụp với hình dạng đặc biệt có thể “hướng” về van ĐM chủ (như AL hoặc JR) sẽ làm tăng khả năng đưa được sonde xuống buồng thất trái.
Khi sonde chụp được đưa xuống giữa buồng thất trái và ổn định (không gây ra ngoại tâm thu), kết nối với bộ phận manifold để theo dõi áp lực.
Ngắt kết nối với manifold và kết nối sonde chụp với máy chụp buồng tim, đảm bảo không có khí trong hệ thống.
Cài đặt thể tích cản quang và tốc độ bơm thuốc: Thông thường từ 25 – 30 mL với tốc độ 10 mL/s.
Sau khi chụp xong buồng tim, kết nối sonde chụp với bộ phận manifold để theo dõi áp lực khi kéo sonde chụp từ buồng thất ra ngoài phía động mạch chủ.
Phân tích kết quả chụp mạch vành
Các tư thế và hình chiếu tương ứng chụp động mạch vành trái (LC )
Có 4 tư thế cơ bản:
Tư thế nghiêng Phải (RAO) 10o và chếch chân (CAU) 30o cho phép quan sát rõ thân chung ĐMV trái (LM), đoạn 1 LAD và toàn bộ LCx.
Tư thế nghiêng trái (LAO) 30 – 40o và chếch chân (CAU) 30 – 40o (còn gọi là tư thế Spider View), cho phép quan sát rõ LM, chỗ chia nhánh và đoạn 1 của LAD và LCx.
Tư thế nghiêng phải (RAO) 0 – 10o và chếch đầu (CRA) 35 – 40o, cho phép quan sát rõ đoạn 2, 3 của LAD và các nhánh Diagonal.
Tư thế nghiêng trái (LAO) 30o và chếch đầu (CRA) 30o, cho phép quan sát LM và toàn bộ LAD, các nhánh Diagonal.
Hình 2.43: Các tư thế chụp động mạch vành trái cho các hình chiếu tương ứng
Nguồn: Theo Heart Disease: A textbook of cardiovascular medicine. 5th ed. Philadelphia: WB Saunders – 2001
Chú thích: LAO cranial: Nghiêng trái chếch đầu, LAO caudal: Nghiêng trái chếch chân, AP caudal: Thẳng chân; AP cranial: Thẳng đầu; RAO cranial: Nghiêng phải chếch đầu; RAO caudal: Nghiêng phải chếch chân; LMCA: left main coronary artery (Nhánh chính động mạch vành trái); LCx: left circumflex artery (Nhánh mũ động mạch vành trái); LAD Left Anterior Descending (Nhánh liên thất trước); OMB: Obtuse Marginal Branches (Nhánh bờ).
Các tư thế chụp động mạch vành phải
Có 3 tư thế cơ bản:
Nghiêng trái (LAO) 30o sẽ thấy rõ toàn bộ đường đi ĐMV phải.
Nghiêng trái (LAO) 30o và chếch đầu (CRA) 30o sẽ thấy rõ toàn đoạn 3, hai nhánh PDA và PLV của ĐMV phải.
Nghiêng phải (RAO) 30o sẽ thấy rõ đoạn 2 ĐMV phải.
Hình 2.44: Các tư thế chụp động mạch vành phải
Nguồn: Theo Heart Disease: a textbook of cardiovascular medicine. 5th ed. Philadelphia: WB Saunders – 2001
Chú thích: LAO straight: Nghiêng trái; LAO cranial: Nghiêng trái chếch đầu; RAO straight: Nghiêng phải; RCA: Động mạch vành phải; PDA: Động mạch liên thất sau; AMP: Acute marginal artery (Nhánh bờ); PLV: Posterior Left Ventricular (Nhánh sau thất trái); Conus branch: Nhánh nón
Chụp cầu nối động mạch vành
Trong chụp cầu nối động mạch vành, điều quan trọng là xem lại biên bản phẫu thuật trước đó, hoặc nếu không có thường chúng ta có thể chụp MSCT động mạch vành trước khi chụp qua da để trả lời các câu hỏi: Có bao nhiêu cầu nối? Thời điểm mổ? Vị trí xuất phát của các cầu nối? Thông thường, tư thế bóng thích hợp để tìm cầu nối phía bên trái tim là nghiêng phải (RAO) 50 độ và cầu nối phía bên phải là nghiêng trái (LAO) 50 độ. Đôi khi cần chụp gốc động mạch chủ để nhìn được vị trí lỗ vào các cầu nối. Một số loại ống thông đặc biệt được thiết kế chuyên dụng để chụp cầu nối (ví dụ: LCB – Left Coronary Bypass – chụp cầu nối cho động mạch vành trái).
Trên thực tế, luôn có những định hướng về giải phẫu để tìm cầu nối.
Cầu nối cho nhánh PDA xuất phát từ phía trước, bên phải động mạch chủ và chạy thẳng hướng xuống mặt trước quả tim.
Cầu nối cho nhánh OM xuất phát từ phía trước bên trái động mạch chủ và chạy vòng ra mặt sau bên của tim.
Cầu nối cho động mạch liên thất trước (LAD) và nhánh Diagonal xuất phát từ vị trí ở giữa và chạy ra bên rồi xuống phía trước rãnh liên thất.
Hiện nay, sử dụng các cầu nối bằng động mạch có độ bền hơn và được ưu tiên sử dụng trong mổ bắc cầu nối chủ vành. Động mạch vú trong trái (LIMA) thường được chụp qua đường động mạch đùi, cũng có thể chụp được qua đường quay. Động mạch vú trong phải (ít được sử dụng làm cầu nối) có thể chụp qua đường động mạch quay hoặc động mạch đùi phải.
Động mạch dưới đòn trái thường được chụp bằng sonde JR hoặc MP. Cần thận trọng khi đưa sonde chụp lên động mạch dưới đòn. Sonde chụp JR có thể chụp chọn lọc trực tiếp động mạch vú trong, nhưng đôi khi cần phải sử dụng dây dẫn dài hơn để thay sonde JR bằng sonde chụp động mạch vú trong chuyên dụng.
Bơm một ít thuốc cản quang để phát hiện lỗ vào của động mạch LIMA.
Bơm thuốc cản quang qua LIMA để chụp ĐMV: Cần phải chụp ở nhiều tư thế khác nhau để quan sát đầy đủ LIMA và vùng diện tích được tưới máu, đặc biệt là vị trí miệng nối.
Rút sonde chụp ra khỏi cầu nối dưới màn tăng sáng và luồn dây dẫn vào để rút ra khỏi lòng mạch.
Vị trí thông thường của các cầu nối tĩnh mạch ở động mạch chủ lên (Hình 3.45)
Hình 2.45: Các vị trí thông thường của cầu nối tĩnh mạch
Cách đánh giá kết quả
Đánh giá tổng quan giải phẫu hệ động mạch vành, bên phải hay trái trội hơn (căn cứ vào nhánh PDA bên phải có nuôi dưỡng bù sang trái nhiều không).
Đánh giá các bất thường về giải phẫu, vị trí xuất phát, đường đi động mạch vành…
Đánh giá tổn thương động mạch vành:
Vị trí tổn thương (hẹp).
Số lượng nhánh bị hẹp.
Mức độ hẹp: Đo theo % đường kính chỗ hẹp nhất so với chỗ lành tham chiếu trước chỗ hẹp (nhẹ 70%; tắc hoàn toàn).
Tính chất hẹp: Lệch tâm, vôi hóa, dài, huyết khối.
Dòng chảy phía sau.
Tuần hoàn bàng hệ.
Tính toán các thang điểm theo AHA/ACC; SYNTAX…
Các đánh giá khác: Cầu cơ động mạch vành…
Các biến chứng có thể xảy ra trong thủ thuật chụp động mạch vành
Biến chứng ở tại vị trí chọc động mạch đùi
Khối máu tụ: Mức độ hình thành khối máu tụ liên quan đến các yếu tố sau:
Thời gian ống mở đường vào lưu lại trong lòng mạch.
Độ lớn của ống mở đường vào dùng trong thủ thuật.
Có sử dụng các thuốc chống đông.
Yếu tố nguy cơ: Tăng huyết áp, béo phì, bệnh lý động mạch ngoại biên có từ trước.
Kỹ thuật rút ống mở đường vào.
Khối máu tụ có các đặc điểm sau cần được theo dõi và đánh giá kỹ lưỡng: Kích thước lớn, lan rộng và nhanh.
Giả phình (Hình 20.11)
Khối giả phình xuất hiện khi có rách thành động mạch ở vị trí chọc mạch, với sự hình thành lòng giả có lớp áo giữa và áo ngoài. Giả phình được đánh giá tốt nhất bằng siêu âm Doppler mạch. Nếu giả phình nhỏ có thể được điều trị bằng băng ép trực tiếp, tuy nhiên khối giả phình lớn cần tiêm thrombin vào trong túi phình hoặc phẫu thuật.
Chảy máu
Nếu chảy máu còn tiếp diễn, cần băng ép trực tiếp vào vị trí chảy máu (băng ép bằng tay hoặc dụng cụ kẹp cầm máu). Đồng thời trung hoà heparin bằng protamine.
Thiếu máu chi cấp tính
Tỷ lệ hiếm gặp và thường xảy ra trên bệnh nhân bị bệnh động mạch ngoại biên từ trước. Nếu nghi ngờ có thiếu máu chi cấp, cần nhanh chóng mời bác sĩ chuyên khoa phẫu thuật mạch máu đánh giá và xử trí kịp thời.
Hình 2.46: Giải phẫu khối giả phình
(a) Dòng máu chảy qua một đường rò và đọng lại ở mô cạnh mạch máu. Băng ép bằng tay không thể loại bỏ được đường rò (b) và khối máu tụ vẫn tồn tại. Dòng máu từ mạch chính tiếp tục chảy vào khối phình và không hình thành được máu đông trong túi phình tạo ra khối giả phình (c). Có thể thấy được khối giả phình bằng siêu âm mạch.
Biến chứng tại đường vào động mạch quay
Một ưu điểm của đường vào từ động mạch quay là làm giảm được biến chứng tại vị trí chọc mạch.
Chảy máu
Có thể xử trí bằng băng ép trực tiếp tại chỗ dễ dàng hơn nhiều so với chảy máu ở động mạch đùi.
Hội chứng khoang
Rất hiếm gặp nhưng để lại hậu quả nặng nề, cần phẫu thuật giải chèn ép.
Giả phình
Hiếm gặp. Cách xử trí giống như đối với giả phình động mạch đùi.
Tắc mạch chi cấp
Tỷ lệ tắc mạch chi cấp sau khi chụp mạch vành qua đường vào động mạch quay cũng không rõ ràng, thường dao động từ 1 – 5%. Tỷ lệ tắc mạch cấp sẽ giảm nếu dùng ống mở đường vào nhỏ, ngậm nước, và được dùng heparin đầy đủ trong thủ thuật.
Biến chứng toàn thân
Phản vệ với thuốc cản quang
Phản vệ với thuốc cản quang khá thường gặp. Triệu chứng có thể từ mức độ nhẹ như ngứa, phát ban, nổi mề đay, rét run đến mức độ nguy kịch như khó thở, tụt áp, rối loạn ý thức. Các triệu chứng có thể nặng lên rất nhanh đến mức nguy kịch. Phản vệ nhẹ xử trí bằng methylprednisolon và diphenhydramin. Trong phản vệ nặng, Adrenalin là thuốc quan trọng hàng đầu trong xử trí phản vệ. Khi phản vệ xảy ra cần được xử trí theo phác đồ.
Cường phế vị
Hay xảy ra trong khi chụp mạch vành và khi rút ống mở đường vào, với triệu chứng nhịp chậm và tụt huyết áp. Có thể xử trí bằng tiêm tĩnh mạch Atropin, giảm đau đầy đủ và bù dịch.
Rối loạn nhịp
Nhịp nhanh trên thất ngắn xuất hiện khá thường xuyên và thường thoáng qua. Ngoại tâm thu thất và nhịp nhanh thất có thể xuất hiện khi xoay sonde chụp, nhất là khi đưa sonde vào buồng thất trái. Rung thất có thể xảy ra khi bơm thuốc cản quang vào mạch vành, đòi hỏi cần phải sốc điện phá rung cấp cứu.
Siêu âm trong lòng mạch
Siêu âm trong lòng mạch (IVUS) là một thăm dò xâm nhập cho phép quan sát trực tiếp mảng xơ vữa và đường kính lòng mạch, cho phép chúng ta có cái nhìn đầy đủ hơn về hình ảnh mô học của mảng xơ vữa với những cải tiến về phương tiện siêu âm gần đây. Những hình ảnh trên siêu âm trong lòng mạch được tạo ra bằng phát và nhận sóng âm sinh ra do sự kích thích điện bởi một tinh thể áp điện trong đầu dò siêu âm. Những sóng âm phản hồi lại từ các cấu trúc sẽ quay trở lại đầu dò siêu âm để tạo nên các xung động điện và có thể biểu diễn thành hình ảnh học. Một dãy tinh thể (thường là 64) được kích hoạt tuần tự để tạo ra các hình ảnh của lòng mạch. Thiết bị cần thiết để tiến hành IVUS bao gồm : Đầu dò siêu âm thu nhỏ được gắn trên ống thông (thường kích thước 2,6 – 3,5Fr), và máy tính để thực hiện tái tạo hình ảnh.
Chỉ định
Khảo sát chính xác và chi tiết các tổn thương ĐMV giúp đưa ra chỉ định can thiệp đúng trong các trường hợp mà chỉ hình ảnh chụp ĐMV khó đưa ra quyết định như:
Tổn thương thân chung ĐMV trái.
Tổn thương hẹp mức độ vừa trên chụp mạch (hẹp từ 40-70% đường kính lòng ĐMV).
Tổn thương chỗ phân nhánh; tổn thương dài lan tỏa.
Khảo sát tình hình tái hẹp sau khi đã đặt stent trước đây.
Khi hình ảnh tổn thương trên chụp ĐMV khó đánh giá, mờ nhạt.
Tổn thương tắc mạn tính ĐMV: Giúp tìm hiểu lòng thật để đưa dây dẫn qua.
Đánh giá kết quả can thiệp/đặt stent động mạch vành đã tối ưu chưa.
Đánh giá tổn thương, mảng xơ vữa và một số dị thường đặc biệt khác của ĐMV.
Chống chỉ định
Không có chống chỉ định tuyệt đối.
Thận trọng khi tiến hành IVUS: Hẹp quá nặng, vôi hóa nhiều, mạch gập góc, nhiều huyết khối, đoạn mạch xa quá nhỏ.
Quy trình kỹ thuật
Sau khi tiến hành chụp ĐMV xác định vị trí hẹp, luồn dây dẫn lái qua chỗ hẹp và đưa đến đoạn xa ĐMV.
Kết nối đầu dò siêu âm với máy IVUS, đuổi khí, test đầu dò siêu âm xem có hoạt động bình thường hay không, với hình ảnh tròn và đều trên màn hình ở chế độ test.
Đưa đầu dò siêu âm vào trong lòng mạch, trượt trên dây dẫn, đi qua chỗ tổn thương ít nhất > 10 mm, ra phía đầu xa tổn thương.
Lựa chọn chế độ kéo ngược đầu dò từ phía xa qua chỗ tổn thương về phía đầu gần tùy thuộc tổn thương:
Sử dụng chế độ kéo tự động (auto pullback): Kết nối đầu dò với hệ thống pullback và cài đặt chế độ kéo ngược với tốc độ định sẵn 0,5 mm/s.
Sử dụng chế độ manual: Kéo ngược bằng tay khi cần thiết.
Đánh giá tổn thương ĐMV: Mức độ hẹp, hình thái lòng mạch, mảng xơ vữa, mức độ vôi hóa, chiều dài tổn thương, mức độ áp thành của stent… và các thông số cần thiết.
Rút đầu dò siêu âm ra khỏi lòng mạch vành.
Bơm nitroglycerin với liều 100 – 200 µg qua ống thông làm giãn ĐMV.
Chụp lại động mạch vành, hoàn tất quy trình.
Ưu điểm của siêu âm trong lòng mạch:
Có thể nhìn rõ hình ảnh chu vi của thành mạch máu, không chỉ là hình ảnh hai chiều giống như trong chụp mạch qua da, mà đây còn là phương pháp đánh giá chính xác kích thước của lòng mạch.
Ngoài ra IVUS còn rất hữu ích khi đánh giá các tổn thương không rõ ràng như:
Các tổn thương trung gian khó đánh giá chính xác được mức độ hẹp trên chụp động mạch vành qua da
Mức độ hẹp lỗ vào
Tổn thương thân chung động mạch vành trái
Tổn thương chỗ chia đôi
Hình ảnh tổn thương mảng xơ vữa bên cạnh hình ảnh trong lòng mạch.
Cho phép tối ưu hóa hiệu quả của nong và đặt stent ĐMV.
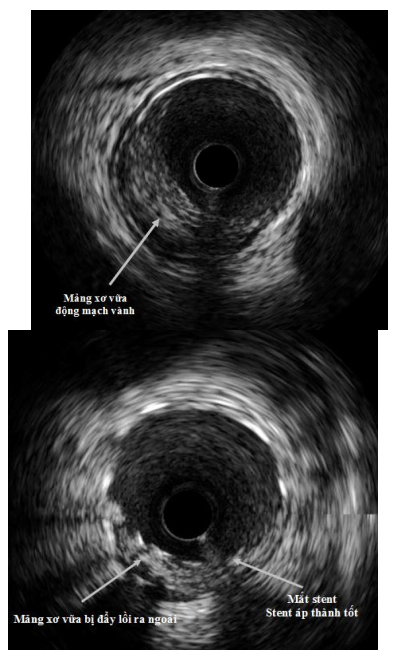
Hình 2.47: Minh họa về siêu âm trong lòng mạch
Hình 2.48: Ví dụ về siêu âm trong lòng mạch
Nguồn: Viện tim mạch Việt Nam
Hình 2.49: Hình ảnh siêu âm trong lòng mạch trước và sau đặt stent
Nguồn: Viện tim mạch Việt Nam
Theo dõi
Theo dõi tình trạng đau ngực trên lâm sàng và các thông số mạch, huyết áp, điện tâm đồ của người bệnh trong quá trình thực hiện đo IVUS để phát hiện sớm các biến chứng và xử trí.
Biến chứng và xử trí
Tách thành ĐMV do quá trình đưa đầu dò siêu âm vào lòng ĐMV: Phát hiện sớm và đặt stent nếu cần.
Co thắt ĐMV: Khá hay gặp, nên cho nitroglycerin đều đặn.
Dòng chảy chậm trong lòng ĐMV.
Tắc mạch đoạn xa, huyết khối…
Đứt đầu dò siêu âm trong lòng mạch: Giữ nguyên dây dẫn, có thể dùng mini snare gắp ra hoặc đưa thêm dây dẫn khác bên cạnh và dùng bóng bơm căng rồi kéo ra.
Các biến chứng khác liên quan đến chỗ chọc mạch (huyết khối, tắc mạch); liên quan đến thủ thuật can thiệp ĐMV.
Đo phân suất dự trữ lưu lượng vành (ffr)
Chụp ĐMV không đánh giá được sinh lý dòng chảy ĐMV bị hẹp. Siêu âm nội mạch có thể cung cấp những thông tin về kích thước lòng mạch và thành phần của mảng xơ vữa, tuy nhiên lại không cung cấp thông tin nào về ảnh hưởng của mảng xơ vữa lên huyết động dòng chảy mạch vành. Hiểu rõ những tác động sinh lý lên dòng chảy tại vùng tổn thương quan sát được trên chụp ĐMV có ý nghĩa hướng dẫn trong can thiệp ĐMV qua da.
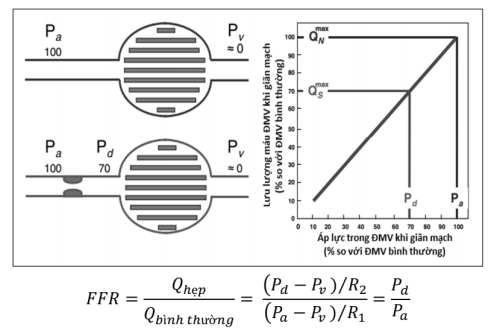
Phân suất dự trữ lưu lượng mạch vành (FFR) có tương quan với áp lực tưới máu cơ tim đoạn xa của mạch vành khi giãn tối đa (sử dụng adenosin hoặc papaverin). FFR là tỷ số giữa lưu lượng lúc giãn mạch tối đa qua ĐMV bị hẹp với lưu lượng tối đa lý thuyết (Hình 20.15).
Do đó những thông tin thu được từ FFR cho phép chẩn đoán xem tại chỗ hẹp mạch vành có gây thiếu máu cơ tim (và triệu chứng đau ngực), từ đó có thể quyết định việc tái tưới máu. Hiện nay, chỉ định tối ưu cho việc sử dụng FFR là công cụ để chẩn đoán, đánh giá hẹp động mạch vành “nặng”, có độ nhạy rất cao với giá trị cut – off là 0,8. Kỹ thuật này còn được sử dụng để tối ưu kết quả đặt stent mạch vành.
Hai kỹ thuật hiện nay có khả năng cung cấp thông tin về huyết động thu được từ kết quả FFR là sử dụng dây dẫn áp lực (bao gồm một bộ chuyển đổi áp lực gắn trên dây dẫn đường kính 0.014 inch), và dây dẫn dòng chảy Doppler (thăm dò vận tốc dòng chảy mạch vành bằng phương pháp phân tích quang phổ).
Dây dẫn áp lực (Ví dụ: Dây dẫn PressureWireTM của hãng Radi Medical Systems)
Bộ phận chuyển đổi áp lực nằm ở vị trí nối giữa đầu dây dẫn cản quang với đoạn gốc không cản quang.
Hệ thống phân tích hiển thị đồng thời áp lực trong động mạch chủ và áp lực trong ĐMV, cũng như giá trị FFR tức thời.
Dây dẫn Doppler (Ví dụ: Dây dẫn FlowWireTM của hãng Endosonics)
Thu nhận thông tin về vận tốc dòng chảy tại vùng trung tâm của lòng mạch.
Kết hợp thông tin về dòng chảy và điện tâm đồ, tính toán giá trị cơ sở các thành phần trong thì tâm thu và tâm trương của vận tốc dòng máu.
Sau truyền các thuốc giãn mạch, hệ thống có thể tính toán vận tốc dòng chảy dự trữ.
Hình 2.50: Mô tả cách tính phân suất dự trữ lưu lượng vành.
Dựa trên định luật Ohm, lưu lượng ĐMV bằng áp lực ĐMV chia cho kháng lực ĐMV. Áp lực ĐMV là hiệu số giữa áp lực trong ĐMV và áp lực trong tĩnh mạch (Pv). Khi không có hẹp ĐMV, áp lực ĐMV bằng hiệu số giữa áp lực động mạch chủ (Pa) và áp lực tĩnh mạch (Pv). Do đó, khi không có hẹp ĐMV thì áp lực tưới máu ĐMV là (Pa-Pv). Lưu lượng máu tưới ĐMV bình thường là tỷ số của áp lực tưới máu ĐMV và kháng lực mao mạch (Pa – Pv)/R1. Trong trường hợp hẹp ĐMV thì áp lực tưới máu ĐMV bị hẹp là hiệu số giữa áp lực đoạn xa ĐMV bị hẹp (Pd) với áp lực tĩnh mạch (Pd-Pv). Lưu lượng tưới máu ĐMV bị hẹp là tỷ số của áp lực tưới máu ĐMV bị hẹp và kháng lực mao mạch (Pd-Pv)/R2. Áp lực tĩnh mạch vành (Pv) luôn luôn rất thấp, ảnh hưởng không đáng kể và gần bằng 0. Khi mạch vành triệt tiêu được trở kháng tối đa bằng thuốc thì kháng lực R1,R2 là rất thấp và xem là bằng nhau. Điều này dẫn đến chỉ số FFR lâm sàng đơn giản hóa bằng áp lực ĐMV trung bình đoạn xa chia áp lực động mạch chủ trung bình (FFR = Pd/Pa). Giá trị FFR bình thường là 1.0
Chỉ định
Người bệnh hẹp động mạch vành mức độ vừa (hẹp từ 40-70%) trên hình ảnh chụp mạch qua đường ống thông, tính cả những trường hợp tái hẹp trong stent cũ động mạch vành.
Người bệnh có hẹp nhiều nhánh động mạch vành mà không thể xác định được nhánh nào là thủ phạm gây thiếu máu cơ tim.
Người bệnh hẹp lan tỏa nhiều vị trí trên cùng một nhánh động mạch vành, nhằm xác định vị trí nào là hẹp đáng kể nhất.
Người bệnh có hẹp tại chỗ phân nhánh và cần quyết định có can thiệp vào nhánh bên hay không.
Theo dõi sau khi can thiệp nong/stent động mạch vành để đánh giá kết quả và đánh giá ảnh hưởng tới nhánh bên.
Chống chỉ định
Không có các chống chỉ định tuyệt đối, nên cân nhắc chống chỉ định tương đối ở một số trường hợp sau:
Những tổn thương hẹp ở phía quá xa không thích hợp về mặt giải phẫu để đo FFR.
Nhồi máu cơ tim cấp, bệnh cơ tim phì đại, có nhiều tuần hoàn bàng hệ, cầu cơ động mạch vành… do khó đánh giá chính xác được mức độ ảnh hưởng huyết động.
Quy trình kỹ thuật:
Sát trùng da rộng rãi khu vực tạo đường vào mạch máu.
Mở đường vào động mạch: Thường là động mạch quay, có thể sử dụng đường vào là động mạch đùi.
Chụp ĐMV qua đường ống thông, thấy tổn thương cần được khảo sát FFR.
Xác định vị trí, nhánh ĐMV cần khảo sát FFR (theo chỉ định).
Kết nối máy đo FFR với hệ thống đo áp lực thực tế qua đường ống thông, đây là đường áp lực phản ánh áp lực thực tế.
Đưa ống thông can thiệp (guiding catheter) vào ĐMV tùy theo vị trí cần khảo sát FFR.
Kết nối dây dẫn áp lực (pressure wire) với máy đo.
Đưa dây dẫn áp lực qua ống thông can thiệp vào lòng ĐMV.
Khi dây dẫn áp lực đi vào lòng mạch được 30 mm (đồng nghĩa với cảm biến áp lực ở sát đầu ống thông can thiệp), tiến hành cân bằng áp lực (equalize) để đảm bảo áp lực ở dây dẫn tương đương áp lực ở đầu ống thông can thiệp.
Lái/đưa dây dẫn áp lực qua tổn thương xuống đoạn xa ĐMV (đảm bảo đầu cảm biến áp lực đến đoạn mạch vành lành sau chỗ tổn thương 10 – 20 mm).
Tiêm trực tiếp vào mạch vành 200 µg nitroglycerin để gây giãn ĐMV, loại bỏ yếu tố co thắt.
Gây tình trạng giãn mạch cường huyết động tối đa (hyperemic) bằng thuốc adenosine với 2 cách:
Tiêm adenosin trực tiếp vào lòng mạch vành để tạo tình trạng gắng sức huyết động. Liều adenosin sử dụng là 60 µg với ĐMV trái, 40 µg với ĐMV phải (tăng liều nếu nghi ngờ chưa đạt giãn mạch tối đa).
Truyền adenosin liên tục qua một ống siêu nhỏ (micro-catheter) được đưa đến đoạn đầu của nhánh ĐMV định khảo sát FFR, tốc độ truyền bắt đầu 360 µg/min.
Đo FFR trong lúc giãn mạch tối đa (sau khi tiêm adenosin hoặc truyền adenosin vào lòng ĐMV). FFR được máy tính tự động và hiện lên liên tục trên màn hình. Lấy chỉ số thấp nhất và ngay khi nhịp tim ổn định.
Để đảm bảo tính chính xác và hằng định của kết quả, cần đo lại ít nhất 2 lần cho mỗi tổn thương cần xác định.
Sau đó, kéo dây dẫn áp lực về đầu ống thông can thiệp, đảm bảo FFR khi đó bằng 1,0 để loại bỏ các sai số.
Can thiệp mạch vành nếu FFR
Liều heparin sử dụng tương tự các ca can thiệp ĐMV thông thường.
Theo dõi:
Theo dõi toàn trạng, huyết áp và nhịp tim của người bệnh trong quá trình đo FFR để phát hiện kịp thời các biến chứng nếu có.
Biến chứng và xử trí:
Các biến chứng nhẹ thoáng qua của quá trình đo FFR, gồm: Khó thở, đau ngực, co thắt mạch vành, block nhĩ thất, ngưng xoang (do thuốc adenosin),… Các biến chứng này thường thoáng qua và không gây nguy hại gì. Cần phải phát hiện kịp thời, cho các thuốc giãn mạch khi bị co thắt động mạch vành. Trong trường hợp nhịp chậm do thuốc, người bệnh được thông báo ho vài tiếng hoặc nếu cần cho tiêm atropin tĩnh mạch.
Các biến chứng nặng (hiếm gặp, do động tác thô bạo): Tách thành động mạch vành, thủng động mạch vành do pressure wire. Cần phát hiện sớm, bơm bóng kéo dài hoặc stent có màng bọc (cover stent) để chặn. Nếu biến chứng nặng có thể xem xét khả năng phẫu thuật.