Advanced magnetic resonance imaging in evaluation of glioma
Lê Văn Phước*
*Khoa Chẩn đoán hình ảnh Bệnh viện Chợ Rẫy
Mở đầu
U sao bào não là u não trong trục nguyên phát thường gặp nhất. Có hai nhóm mô học chính u sao bào độ ác thấp và nhóm độ ác cao. U sao bào chiếm khoảng 24,7% các u não nguyên phát. Với các u ác tính, u sao bào độ ác cao chiếm 74,6% [3].Trong nhiều trường hợp u gây tổn thương thực thể và chức năng não nặng nề, tỉ lệ tử vong cao. Vấn đề điều trị dựa vào chẩn đoán chính xác tổn thương, đặc biệt mô bệnh học. MRI thường qui (cMRI) dựa trên hình ảnh giải phẫu kết hợp dùng thuốc tương phản là kỹ thuật hình ảnh xem như tiêu chuẩn vàng trong chẩn đoán u não hiện nay. Tuy nhiên, cMRI có nhiều hạn chế: không đánh giá hết các tính chất sinh lý, cấu trúc bên trong phức tạp của u sao bào; hạn chế trong chẩn đoán, chẩn đoán phân biệt với các bệnh lý không do u, phân độ mô học u,… Nhiều tiến bộ kỹ thuật MRI hiện nay như: kỹ thuật khuếch tán (DWI), khuếch tán theo hướng (DTI), bó sợi thần kinh (DTT), tưới máu (PMR), phổ (MRS) và chức năng (fMRI) đã phát triển và đang được ứng dụng lâm sàng ngày càng rộng rãi, một số trở nên khảo sát thường qui. Các kỹ thuật mới này đã đi sâu đánh giá u sao bào ở mức độ phân tử, thay đổi mật độ tế bào, chuyển hóa, huyết động, liên quan u với các cấu trúc giải phẫu, vùng chức năng ở não. Các kỹ thuật mới đã bổ sung các thông tin quan trọng, cần thiết cho cMRI trong đánh giá u về: chẩn đoán, lập kế hoạch phẫu thuật, sinh thiết, theo dõi sau điều trị. Bài viết giới thiệu một cách cập nhật các vấn đề cơ bản về nguyên lý và ứng dụng lâm sàng các tiến bộ kỹ thuật MRI trong u sao bào ở não.
Các tiến bộ kỹ thuật mri
Nguyên lý cơ bản kỹ thuật
MRI phổ
MRI phổ (MRS) là kỹ thuật đánh giá các thay đổi chuyển hóa tại vùng u. Mỗi chất chuyển hóa có mỗi vị trí tương ứng tùy vào tần số chuyển động, được biểu diễn bằng đường cong với đỉnh là nồng độ chất chuyển hóa. Các chất chuyển hóa thường dùng đánh giá trong u gồm: Cho, NAA, Cr, Lactate, Lipid. Mỗi chất chuyển hóa là dấu ấn chỉ điểm cho mỗi quá trình sinh hóa tại u. Ví dụ, Cho tượng trưng cho tăng sinh màng tế bào, tăng cao trong u; NAA là dấu chỉ điểm cho hoạt động bình thường tế bào thần kinh, giảm trong u do tổn thương tế bào.
Kỹ thuật MRScó thể lấy vùng đo đơn thể tích (SVS) hoặc đa thể tích (MVS). Hai chuỗi xung thường sử dụng là STEAM và PRESS. Mỗi kỹ thuật có các ưu nhược điểm khác nhau. Các vùng đo kích thước nhỏ, cần thời gian ngắn thường dùng SVS. Đánh giá tổng thể bản đồ phổ dùng MVS.
MRI tưới máu
MRI tưới máu (PMR) là kỹ thuật dùng đánh giá thay đổi huyết động, tính thấm thành mạch ở u. Ở u não có sự tạo thành các chất gây tăng sinh mạch, các mạch máu này thường có bất thường cấu trúc, thay đổi tính thấm thành mạch, dòng chảy.
Kỹ thuật PMR dựa trên hai phương pháp: dùng thuốc tương phản (dựa trên hiệu ứng T2*(DSC) hoặc dùng hiệu ứng T1 (DCE) hoặc không dùng thuốc tương phản (ASL). Kỹ thuật DSC thường hay sử dụng lâm sàng. DSC đánh giá giảm tín hiệu của Gd do hiệu ứng T2. Các thay đổi này được đánh giá bằng đường cong thời gian – cường độ tăng quang. Các thông số thu được là: CBV, CBF, MTT, TTP. CBV là diện tích dưới đường cong, biểu hiện thể tích máu tại một vùng não. Giá trị rCBV được đo bằng tỉ số CBV vùng u và bình thường. ASL là kỹ thuật không sử dụng thuốc tương phản ngoài, thời gian khảo sát ngắn, có giá trị, hiện được nghiên cứu gần đây.
MRI khuếch tán
MRI khuếch tán thường qui (DWI) là kỹ thuật hình ảnh khảo sát chuyển động tự do của phân tử nước trong cơ thể. Khuếch tán của các phân tử nước trong cơ thể thay đổi tùy theo cấu trúc, mật độ tế bào, tình trạng bệnh lý. Có tương quan nghịch giữa mật độ tế bào u với hệ số khuếch tán biểu kiến (ADC). ADC giúp phân biệt các loại u, phân độ mô học u. Các kỹ thuật mới liên quan DWI hiện nay là: hình ảnh khuếch tán Kurtosis (DKI), bản đồ khuếch tán chức năng (fDM), hình ảnh phổ hạn chế (RSI), DTI, DTT.
MRI khuếch tán theo hướng (DTI): Các sợi chất trắng trong não có tính không đẳng hướng do myelin và màng của sợi trục thần kinh tác dụng như hàng rào ngăn cản chuyển động các phân tử nước theo các hướng không song song với sợi trục. Khuếch tán trong não thường không đẳng hướng. Kỹ thuật khuếch tán theo hướng (DTI)giúp đánh giá khuếch tán không đẳng hướng của chuyển động các phân tử nước này.
Hình bó sợi thần kinh (DTT): Hình các bó sợi thần kinh (DTT)được tạo ra bằng cách chọn các khối thể tích cạnh nhau có hướng khuếch tán liên quan. Hướng của bó sợi thần kinh là hướng khuếch tán cao nhất của chuyển động do đó có thể vẽ hình các bó sợi thần kinh não.
Kỹ thuật chụp DIW, DTI, DTT thường liên quan sử dụng các chuỗi xung EPI, hình 3D. Để tính toán mức độ không đẳng hướng tốt, tối thiểu cần tính toán trên 6 hướng (trung bình trên 20 hướng). Mỗi giá trị khuếch tán theo mỗi hướng trên không gian sẽ biểu thị trên một hướng với giá trị gọi là phân suất không đẳng hướng (FA). Giá trị của FA từ 0 đến 1, với 0 cho giá trị khuếch tán đẳng hướng và 1 cho giá trị khuếch tán tối đa.Hướng khuếch tán tối đa có thể vẽ màu lại bằng cách mã màu: đỏ, xanh và tím tùy theo hướng của bó sợi thần kinh.
MRI chức năng
MRI chức năng (fMRI) là kỹ thuật dùng khảo sát các vùng não chức năng. Khi vùng não được kích thích, máu sẽ đến nhiều hơn, có sự thay đổi nồng độ Oxy tại chỗ, thay đổi mức độ oxy tại vùng não có thể ghi nhận bằng các thay đổi tín hiệu trên MRI, từ đó giúp đánh giá các vùng chức năng não. Các vùng chức năng não thường khảo sát trong u não gồm: vận động, ngôn ngữ, cảm giác, thị giác,…
Kỹ thuật fMRI liên quan đến đánh giá thay đổi tín hiệu dựa trên kỹ thuật BOLD. Thường sử dụng hai pha: kích thích và nghỉ. Các tác vụ kích thích tùy theo vùng chức năng khác nhau. Ví dụ: vùng vận động thường kích thích bằng các cử động liên quan: bấm đầu các ngón tay trong vùng vận động bàn tay, gập duỗi bàn chân trong vùng vận động bàn chân. Phức tạp hơn là các vùng ngôn ngữ Broca, Werknicke trong xác định bán cầu ưu thế. Hướng mới hiện nay của fMRI liên quan dùng các máy từ trường siêu cao (>3T), khảo sát đơn thuần pha nghỉ,…
Ứng dụng trong u sao bào
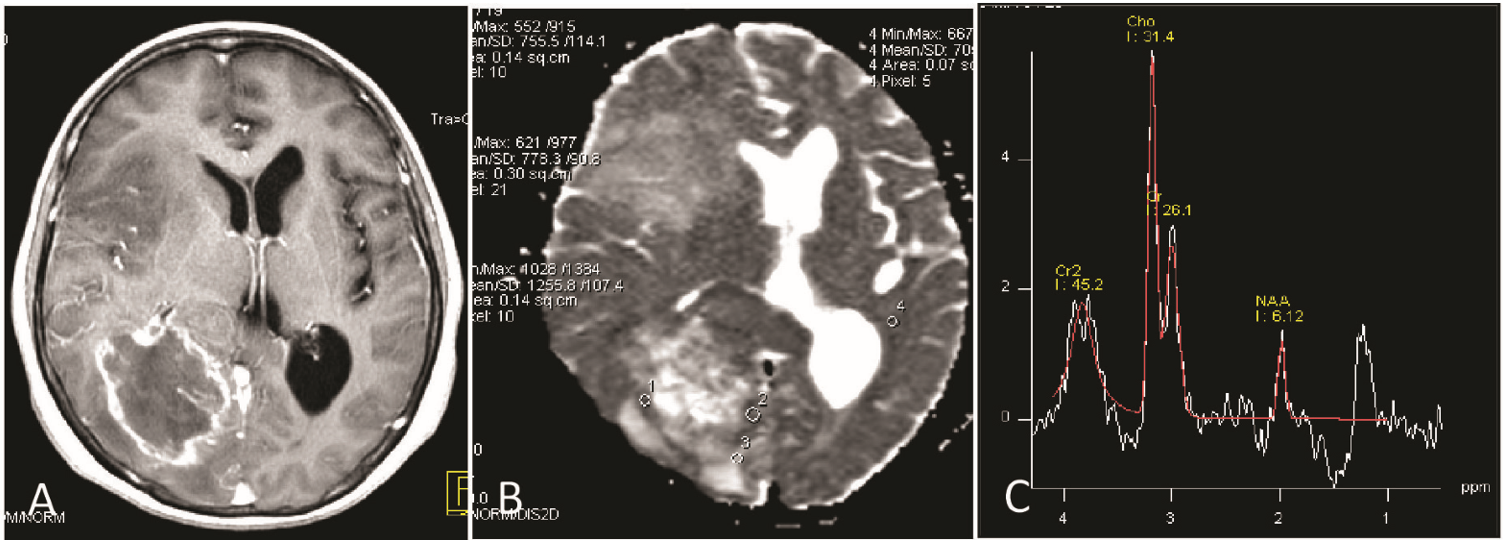
MRS thường được dùng phân biệt: u hay không u, phân độ mô học, xác định vùng xâm nhiễm u, loại u, phân biệt u tái phát, còn sót hay hoại tử sau xạ, hướng dẫn sinh thiết, đánh giá đáp ứng điều trị,… (Hình 1). Ví dụ: u tế bào đệm độ ác cao có tỉ số Cho/NAA, Cho/Cr cao. Giá trị tỉ số Cho/NAA bằng 2.2là ngưỡng dùng phân biệt u độ ác cao và thấp cũng như các bệnh lý không do u [9]. Các vùng có tỉ số Cho/NAA cao gợi ý vùng độ ác cao, MRS có giá trị trong lựa chọn vị trí sinh thiết, góp phần chẩn đoán chính xác hơn độ mô học u sao bào, loại u có thành phần mô học không đồng nhất [4].
Hình 1. BN Trần Th.H. Nam, 58t, u sao bào grade IV. Hình DWI (B) gía trị ADC: 0,755x103mm2s-1, hình MRS (C) : Cho/NAA: 5,13; hình T1W + Gd (A)
PMR thường được chỉ định dùng phân biệt: u hay không u, phân độ mô học, xác định vùng xâm nhiễm u, phân biệt u tái phát, còn sót hay hoại tử sau xạ, hướng dẫn sinh thiết, đánh giá đáp ứng điều trị,… Giá trị rCBV thường tăng cao ở u so với các bệnh lý không phải u, vùng u tái phát so với vùng hoại tử, u độ ác cao so với thấp. Ví dụ: giá trị rCBV bằng 1.75 là ngưỡng dùng phân biệt u độ ác cao và thấp [8]. Tỉ số rCBV > 2,6 gợi ý u tái phát, trong lúc đó
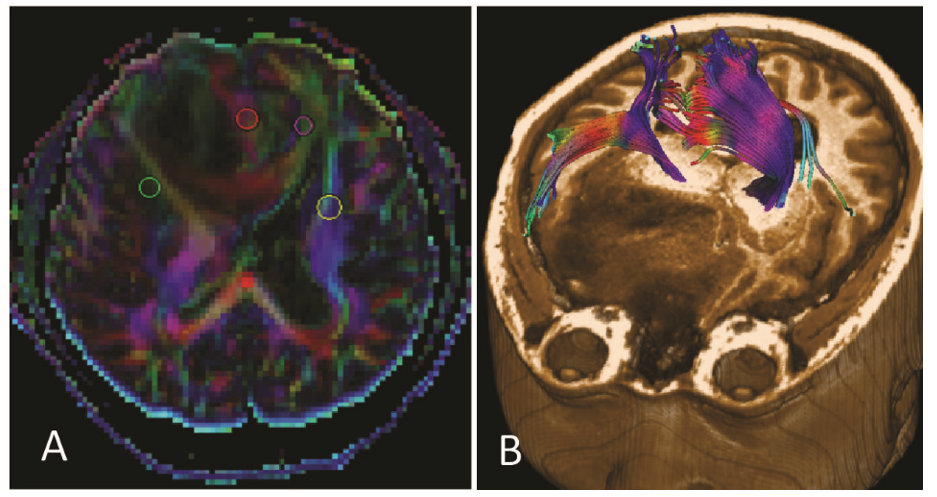
DWI, DTI, DTT thường chỉ định trong u sao bào trong đánh giá thành phần mô u (đặc, hoại tử), phân biệt các u, u và áp-xe, phân độ ác tính, đánh giá xâm lấn các sợi thần kinh, liên quan u và các sợi chất trắng trong lập kế hoạch tiền phẫu,…(Hình 2). Kỹ thuật bó sợi thần kinh giúp đánh giá liên quan u và các bó sợi thần kinh, hỗ trợ việc lập kế hoạch phẫu thuật. ADC, FA giúp phân biệt độ ác u sao bào. ADC trung bình của u sao bào độ ác cao thấp hơn độ ác thấp (0,92 so với 1,28 x103mm2s-1). Ngưỡng giá trị FA giúp phân biệt u độ ác cao và thấp là 0,188, với u độ ác cao có FA cao hơn u độ ác thấp[7]. Các vùng quanh u, các u độ ác cao có FA thấp hơn u độ ác thấp do phù, mô u xâm lấn,… DTTkết hợp fMRI giúp lập kế hoạch tiền phẫu, hạn chế tổn thương vùng chức năng liên quan u.
Hình 2. BN Nguyễn Tr H. Nam, 41t, u sao bào grade IV. Hình DTI (A): thâm nhiễm chất trắng: FA mô u/ đối bên 0.44/0.17. Hình DTT(B): chèn đẩy và xâm lấn các bó sợi chất trắng.
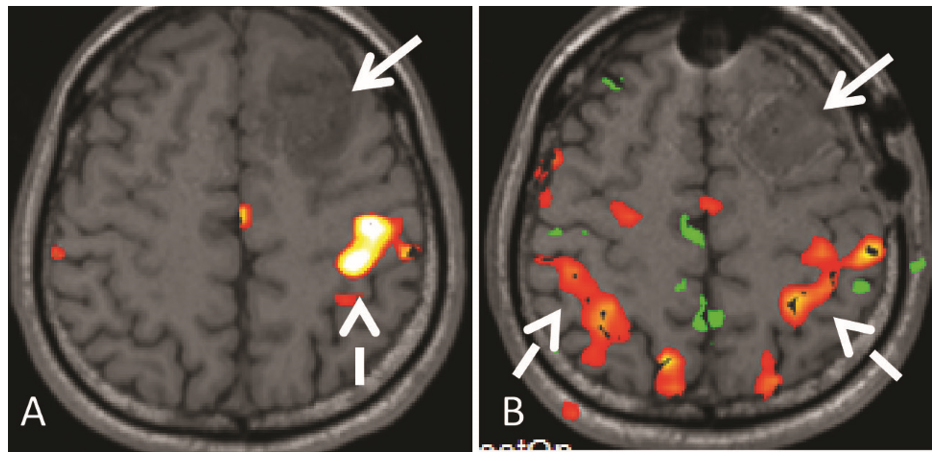
fMRI chỉ định trong u sao bào nhằm đánh giá liên quan u với vùng chức năng giúp lập kế hoạch phẫu thuật: xác định và đánh giá các vùng chức năng, chọn phương án tối ưu, xác định các nguy cơ phẫu thuật; đánh giá sau phẫu thuật [5] (Hình 3). fMRI có thể thay thế nghiệm pháp Wada và kích thích điện trực tiếp trong phẫu thuật [1]. fMRI giúp nhà phẫu thuật thần kinh lấy
tối đa mô u, hạn chế tổn thương mô não lành, giảm ít nhất tổn thương chức năng não, giúp cải thiện chất lượng sống bệnh nhân.
Các tiến bộ kỹ thuật MRIđược ứng dụng trong u sao bào tùy ưu điểm và hạn chế mỗi kỹ thuật. Sự phối hợp nhiều kỹ thuật giúp gia tăng độ chính xác của MRI. Các ứng dụng kỹ thuật hình ảnh mới tập trung các lĩnh vực sau: đánh giá tiền phẫu u gồm: thông tin cấu trúc, vị trí không gian, loại u, vị trí sinh thiết, phân độ mô học, phân biệt các bệnh lý ‘giống u’, tiên lượng điều trị; đánh giá đáp ứng điều trị: đặc biệt trong phân biệt ‘giả tiến triển’ và ‘tiến triển thật sự’ của u não, đáp ứng sau điều trị, (kháng tân sinh mạch, điều trị thuốc miễn dịch); và theo dõi tiến triển u não [6].
Hình 3. BN Ng. Th. N, 20t, u sao bào grade II. Hình fMRI trước (A) và sau phẫu thuật (B). U não ở trán trái (mũi tên liên tục), vùng vận động bàn tay (mũi tên không liên tục)
Ứng dụng các kỹ thuật MRI như đã giới thiệu trên ngày càng chứng minh giá trị trên lâm sàng. Ngoài phân tích thông thường, sự phát triển công nghệ máy tính với ứng dụng thông minh nhân tạo (AI) trong phân tích hình ảnh MRI, hoặc kỹ thuật xử lý dữ liệu hình ảnh kết hợp dữ liệu lâm sàng, kiểu hình hoặc ngay cả kiểu gen (radiomics/radiogenemics) đang được phát triển gần đây giúp gia tăng khả năng ứng dụng của MRI. Tuy nhiên, một số kỹ thuật MRI mới trên đòi hỏi có tính chính xác cao hơn, thống nhất thông số chụp hình, chuẩn hóa các thông số trong đánh giá, giữa các hệ thống máy và giữa các trung tâm [2].
Kết luận
Các tiến bộ kỹ thuật MRI hiện nay đã bổ sung cho MRI thường qui, cung cấp thêm nhiều thông tin về cấu trúc phân tử, chuyển hóa mức độ tế bào, liên quan uvới các bó sợi thần kinh, vùng chức năng thần kinh. Các tiến bộ kỹ thuật này giúp MRI trở nên phương tiện không xâm lấn rất có giá trị trong chẩn đoán, lập kế hoạch phẫu thuật, đánh giá sau điều trị u sao bào, cải thiện chất lượng sống của bệnh nhân đáng kể. Ứng dụng và triển khai các kỹ thuật mới của MRI trong đánh giá u sao bào ngày càng rộng rãi, một số đã trở thành thường qui ở các trung tâm trên thế giới cũng như các bệnh viện lớn ở nước ta hiện nay.
Tài liệu tham khảo
American College of Radiology. ACR Appropriateness Criteria®, 2017.
Benjamin M.Ellingson, Consensus recommendations for a standardized brain tumor imaging protocol in clinical trials, Neurooncology, 2015.
CBTRUS 2018.
Chen CY, Proton magnetic resonance spectroscopy-guided biopsy for cerebral glial tumors. J Formos Med Assoc, 2004.
European Commission, fMRI, 2013.
Inoue T, Ogasawara K, Beppu T, Diffusion tensor imaging for preoperative evaluation of tumor grade in gliomas. Clinical Neurology and Neurosurgery,2005
Hari Nandu, Imaging in neuro-oncology, Therapeutic advences in neurological Disorders, 2018.
Law M, Yang S, Wang H, Glioma grading: sensitivity, specificity, and predictive values of perfusion MR imaging and proton MR spectroscopic imaging compared with conventional MR imaging. Am J Neuroradiol 2003.