The Use of the Anticoagulant Heparin and Corticosteroid Dexamethasone as Prominent Treatments for COVID-19
Heloísa Antoniella Braz-de-Melo, Sara Socorro Faria , Gabriel Pasquarelli-do-Nascimento , Igor de Oliveira Santos, Gary P Kobinger, Kelly Grace Magalhães
Frontiers in Medicine | 1 April 2021 | Volume 8 | Article 615333
Dịch bởi: BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Tóm tắt
COVID-19 đang lan rộng trên toàn thế giới với tốc độ đáng lo ngại, áp đảo ngành y tế toàn cầu. Việc gắn kết các trường hợp tử vong do biến chứng của bệnh làm nổi bật sự cần thiết của việc mô tả các chiến lược điều trị bằng thuốc hiệu quả cho bệnh nhân nặng. Mức độ nghiêm trọng của COVID-19 liên quan đến tăng đông máu và tình trạng viêm trầm trọng hơn, cả hai đều bị ảnh hưởng bởi sự giảm điều hòa ACE2 và sự xuất hiện của cơn bão cytokine. Trong tổng quan này, chúng tôi thảo luận về khả năng áp dụng của heparin chống đông máu và corticosteroid dexamethasone chống viêm để quản lý bệnh nhân COVID-19 nặng. Tình trạng viêm và đông máu được điều chỉnh có thể được giảm thiểu bằng cách sử dụng heparin và các dẫn xuất của nó. Heparin tăng cường đặc tính chống đông máu của anti-thrombin (AT) và có thể hữu ích khi kết hợp với thuốc tiêu sợi huyết cho bệnh nhân COVID-19 nặng. Bên cạnh đó, heparin cũng có thể điều chỉnh phản ứng miễn dịch, làm giảm viêm qua trung gian TNF-α, làm suy giảm sản xuất và bài tiết IL-6, đồng thời liên kết với protein bổ sung và leukotriene B4 (LTB4). Hơn nữa, heparin có thể thể hiện tiềm năng chống SARS-CoV-2 một khi nó có thể tác động đến khả năng lây nhiễm của virus và làm thay đổi cấu trúc protein SARS-CoV-2 Spike. Một cách tiếp cận khả thi khác là sử dụng glucocorticoid dexamethasone. Mặc dù việc sử dụng glucocorticoid để kiểm soát nhiễm virus còn gây tranh cãi, ngày càng có nhiều bằng chứng chứng minh rằng điều trị bằng dexamethasone có khả năng làm giảm đáng kể tỷ lệ tử vong ở những bệnh nhân mắc Hội chứng nguy kịch hô hấp cấp tính (ARDS) yêu cầu thở máy xâm lấn. Quan trọng là, dexamethasone có thể gây bất lợi bằng cách làm giảm sự thanh thải của virus và gây tăng đường huyết và giữ natri, do đó có thể gây hại cho bệnh nhân tiểu đường và bệnh nhân tăng huyết áp, hai nhóm nguy cơ COVID-19 chính. Do đó, trong khi khả năng đa mục tiêu của heparin tỏ ra có lợi cho bệnh nhân COVID-19 nặng, dexamethasone nên được sử dụng cẩn thận có cân nhắc đến các tình trạng bệnh lý cơ bản và mức độ nghiêm trọng của bệnh COVID-19. Do đó, chúng tôi đề xuất rằng tác động đa mục tiêu của heparin như một loại thuốc chống vi rút, chống huyết khối và chống viêm trong giai đoạn đầu của COVID-19 có thể làm giảm đáng kể nhu cầu điều trị bằng dexamethasone trong giai đoạn đầu của bệnh này. Nếu điều trị tiêu chuẩn của heparin không bảo vệ được khỏi bệnh nặng, dexamethasone phải được áp dụng như một chất chống viêm mạnh để ngăn chặn tình trạng viêm không kiểm soát và trầm trọng hơn.
Giới thiệu
Hội chứng hô hấp cấp tính nghiêm trọng coronavirus 2 (SARS-CoV-2), tác nhân gây bệnh do coronavirus (COVID-19), đang nhanh chóng lây lan trên toàn thế giới, là nguyên nhân gây ra cái chết của hơn hai triệu người trên toàn cầu vào tháng 3 năm 2021 [Tổ chức Y tế Thế giới (WHO), 2020]. COVID-19 nghiêm trọng xảy ra do các biến chứng, chủ yếu ảnh hưởng đến phổi (1), tim (2) và thận (3), tác động thường xuyên hơn đến người già và bệnh nhân mắc một số bệnh đi kèm, như bệnh tim và tăng huyết áp, và thường tương quan với mức độ nặng nhập viện đơn vị chăm sóc (ICU), yêu cầu thở máy và tử vong (4). Số lượng bệnh nhân bệnh và qua đời tăng cao do COVID-19 đặt nó như một trường hợp khẩn cấp về chăm sóc sức khỏe và nêu bật tính cấp thiết của việc thiết lập các chiến lược điều trị bằng thuốc hiệu quả để quản lý đại dịch.
Bệnh nhân COVID-19 nặng có xu hướng cho thấy lượng tuần hoàn tăng cao của các chất trung gian tiền viêm Interleukin-6 (IL-6), IL-8, IL-1β, và Monocyte Chemoattractant Protein-1 (MCP-1) (5). Mặc dù nồng độ IL-6, IL-8, và yếu tố hoại tử khối u-α (TNF-α) trong huyết tương ở những bệnh nhân COVID-19 nặng có thể thấp hơn so với những đối tượng bị sốc nhiễm trùng và tương tự như ở những bệnh nhân khác trong trạng thái nguy kịch (6), kiểu hình bị viêm tương quan với tiên lượng COVID-19 kém và được tạo ra bởi cơn bão cytokine, một tình trạng đặc trưng bởi hội chứng hoạt hóa đại thực bào, giảm bạch huyết và thâm nhiễm tế bào đơn nhân nội tạng (7). Bên cạnh đó, nhiễm trùng SARSCoV-2 dẫn đến tổn thương nội mô (8) và giảm điều hòa thụ thể xâm nhập tế bào ACE2 (9), làm tăng thêm phản ứng viêm và tác động đến quá trình đông máu. Trong bối cảnh này, những bệnh nhân bị bệnh nặng có thể được hưởng lợi từ các liệu pháp chống viêm, bao gồm dexamethasone.
Đặc điểm trạng thái tăng đông của mức độ nghiêm trọng COVID-19 được minh họa bằng nồng độ Ddimer tăng liên tục (10), đông máu nội mạch lan tỏa (DIC) và rối loạn đông máu tiêu thụ tiếp theo (11) biểu hiện ở những người bị ảnh hưởng. Những thay đổi này giải thích nguy cơ gia tăng phát triển các biến chứng đe dọa tính mạng, chẳng hạn như thuyên tắc phổi (PE) (12) và nhồi máu cơ tim (13), bởi nhóm này. Do đó, sử dụng thuốc chống đông máu heparin cũng có thể hữu ích để cải thiện kết quả trong những trường hợp nặng.
Các quá trình viêm và đông máu ảnh hưởng mật thiết với nhau theo nhiều cách, bao gồm thông qua Yếu tố mô (TF), hoạt hóa PAR phụ thuộc vào thrombin, Cơ quan thụ cảm giống như Toll (TLR) và hệ thống bổ thể (14). Mức độ tăng cao của các dấu hiệu tiền viêm COVID-19, chẳng hạn như IL-6 và IL-8, cũng làm tăng nguy cơ hình thành huyết khối (15). Mức độ cao của IL-6 phá vỡ sự cân bằng chất chống đông máu bằng cách tăng sự biểu hiện của các yếu tố đông máu và giảm mức độ của các chất ức chế hình thành huyết khối (16). IL-8 cũng tác động đến quá trình cầm máu, thay đổi đáng kể lượng fibrin và thrombin, và kích hoạt tiểu cầu (17). Một khi cường độ của các phản ứng viêm và quá trình đông máu ảnh hưởng đến tiên lượng của bệnh nhân COVID-19 nặng, việc điều tra hiệu quả của các thuốc chống viêm và chống đông máu có thể rất quan trọng trong việc giảm tỷ lệ mắc bệnh và tử vong do đại dịch COVID-19 gây ra. Trong tổng quan này, chúng tôi thảo luận về việc sử dụng heparin chống đông máu và dexamethasone chống viêm như những công cụ đầy hứa hẹn để quản lý bệnh nhân COVID-19 nặng.
Thuốc chống đông heparin
Mối liên quan mới nổi giữa các sự kiện huyết khối tắc mạch và COVID-19 đã nâng cao hiểu biết mới về sinh lý bệnh của bệnh đại dịch. Vô số mục tiêu điều trị đã được đề xuất thông qua kiến thức về các yếu tố chống đông / chống đông máu không cân bằng dẫn đến suy giảm hoạt động chống huyết khối nội sinh trong quá trình nhiễm SARS-CoV-2 (18–20). Giả thuyết tuyệt vời liên quan đến việc sử dụng các thuốc chống đông máu có thể khôi phục cân bằng nội môi huyết động và bảo vệ chống lại rối loạn đông máu được quan sát thấy. Dựa trên cơ sở đó, nghiên cứu về các loại thuốc chống đông máu được sử dụng thường xuyên, đặc biệt là heparin, đã gia tăng trên toàn thế giới và dữ liệu sơ bộ cho thấy hiệu quả đầy hứa hẹn trong y học lâm sàng.
Heparin là một polysaccharide ban đầu được phân lập từ mô động vật có vú vào năm 1916 (21). Sau khi phát hiện ra, nghiên cứu ngày càng tăng về cấu trúc hóa học phân tử và cơ chế hoạt động đã mang lại các dẫn xuất mới giúp cải thiện hiệu quả hoạt động chống huyết khối và giảm tác dụng phụ liên quan đến dạng heparin không phân đoạn (UFH) (22). UFH có liên quan đến tăng nguy cơ giảm tiểu cầu và loãng xương, gây ra nhu cầu theo dõi bệnh nhân nhiều hơn trong quá trình điều trị (23, 24). Qua đó, sự phát triển của heparin trọng lượng phân tử thấp (LMWH) đã đạt được những quan điểm mới và hiện đang là thuốc chống đông máu được lựa chọn để điều trị và phòng ngừa các chứng rối loạn đông máu.
Cả UFH và LMWH đều có khả năng liên kết với glycoprotein kháng thrombin (AT), tăng cường sự bất hoạt AT của các enzym mạnh trong con đường đông máu, chẳng hạn như Yếu tố Xa và Yếu tố IIa (Thrombin). Sự phụ thuộc vào heparin của AT để ngăn chặn sự hình thành cục máu đông làm cho thuốc trở thành một chất chống huyết khối gián tiếp và sự vắng mặt của hoạt tính tiêu sợi huyết nội tại làm giảm sự phân hủy huyết khối khi chúng đã được hình thành (25, 26). Bên cạnh đó, heparin cũng thể hiện một hoạt động điều hòa miễn dịch thú vị (27). Một trong những cơ chế được đề xuất là ức chế các phản ứng viêm khác nhau qua trung gian yếu tố hoại tử-α (TNF-α), một cytokine chống viêm mạnh (28, 29). Kết quả là, hoạt động nhanh chóng và hiệu quả của heparin làm cho thuốc có khả năng chống lại chứng viêm, ngoài đặc tính chống đông máu của nó. Do đó, các báo cáo khác nhau đã khám phá khả năng này chống lại nhiễm trùng SARS-CoV-2, trong đó cả sự gián đoạn viêm và đông máu đều có thể dẫn đến một biến chứng trong quá trình tiến triển của bệnh.
Các báo cáo đã chỉ ra rằng bệnh nhân COVID-19 có mức độ tăng của dấu ấn sinh học đông máu và rối loạn chức năng miễn dịch nghiêm trọng có thể dẫn đến đông máu nội mạch lan tỏa (DIC), tăng nguy cơ huyết khối tĩnh mạch (VTE) và suy nội tạng, phản ánh tỷ lệ tử vong tại bệnh viện cao. là 1:31 với khoảng tin cậy (CI) là 95% (30–32). Sử dụng mô hình động vật, sự lắng đọng tăng lên của collagen, fibrin và yếu tố von Willebrand có liên quan đến việc tăng cường hình thành huyết khối và thành lập nội mô trong COVID-19 (33). Hơn nữa, sự xuất hiện của các thay đổi thần kinh do huyết khối tĩnh mạch não cũng đã được báo cáo (34, 35). Trong bối cảnh này, điều trị chống đông máu sớm đã được áp dụng và đã quan sát thấy sự giảm nồng độ D dimer, thở máy cấp cứu và giảm 24,2% tỷ lệ tử vong ở những bệnh nhân có rối loạn đông máu do nhiễm trùng huyết (30, 32, 36, 37) . Việc sử dụng liều UFH cao, chẳng hạn như 5.000 U, cho thấy khả năng bảo vệ quan trọng chống lại VTE do nhiễm trùng huyết, một biến chứng có ảnh hưởng lớn đến tiên lượng của bệnh nhân (32). Bên cạnh đó, các thử nghiệm lâm sàng đang diễn ra đang tập trung vào điều trị bằng heparin hít cho bệnh nhân nhập viện có hoặc không cần thở máy, đặc biệt là do một số báo cáo đã đề cập đến vai trò bảo vệ của UFH khí dung chống lại sự lắng đọng fibrin trong phổi và tổn thương phổi (38, 39).
Bảng 1 Các nghiên cứu về điều trị bằng heparin đối với COVID-19.
|
Tác giả, năm, nghiên cứu thiết kế, quốc gia |
Số bệnh nhân |
Điều trị |
Đặc điểm bệnh nhân |
Kết quả |
|
Ranuci và cộng sự, 2020; Nhóm thuần tập tiềm năng; Ý |
16 |
Sử dụng phác đồ điều trị dự phòng huyết khối chuyên sâu với LMWH, antithrombin và clopidogrel |
Bệnh kèm theo: 5% – béo phì (BMI> 30 kg / m2); 20% bệnh tiểu đường; 16% CDV |
56,3% với tiến triển về hồ sơ đông máu bình thường, sau khi tăng dự phòng huyết khối ở ngày thứ 14 |
|
Tang và cộng sự, 2020; Đoàn hệ hồi cứu; Trung Quốc |
449 |
Sử dụng dự phòng huyết khối UFH hoặc LMWH |
Bệnh kèm theo: tăng huyết áp 40%; 21% bệnh tiểu đường và 9,1% CDV |
Giảm 20% tỷ lệ tử vong khi bệnh nhân có D-dimer vượt quá 3,0 μg / mL và được điều trị bằng heparin |
|
Zhang và cộng sự, 2020; Đoàn hệ hồi cứu; Trung Quốc |
143 |
Dự phòng bằng LMWH |
Tuổi: 63 y; Bệnh đi kèm: béo phì: 24,9 kg / m2 – 35,8%; 39,2% tăng huyết áp; 18,2% bệnh tiểu đường |
8,8% DVT (tất cả bệnh viện) |
|
Middeldorp và cộng sự, 2020; Đoàn hệ hồi cứu; Hà Lan |
198 |
Dự phòng LMWH tiêu chuẩn và gấp đôi |
Tuổi: 61 y; BMI: 27 kg / m2 |
GW: PE 6,6%, DVT 13% ICU: PE 15%, DVT 32% |
|
Llitjos và cộng sự, 2020; Đoàn hệ hồi cứu; Pháp |
26 ICU |
31% LMWH dự phòng, 69% điều trị |
Tuổi: 68 y; Cơ địa: Tăng huyết áp: 85% |
|
|
Helms và cộng sự, 2020; Đoàn hệ tương lai đa trung tâm; Pháp |
150 ICU |
70% LMWH dự phòng, 30% điều trị |
Tuổi: 63 y; Bệnh kèm theo: Tiểu đường: 22,1% |
16,7% PE; 2,6% ATE |
|
Fauvel và cộng sự, 2020; Đoàn hệ hồi cứu Muticentric; Pháp |
1,240 nonICU |
8,4% LMWH dự phòng; 11% UFH dự phòng |
Tuổi: 64 y; Bệnh đi kèm: tăng huyết áp 45,4%; 21,7% tiểu đường; |
8,3% VTE |
|
Lodigiani và cộng sự, đoàn hệ hồi cứu; Ý |
327 |
40,7% LMWH dự phòng; 22,6% UFH dự phòng |
Tuổi: 68 y; Bệnh đi kèm: 29,8% BMI> 30 kg / m2; Tăng huyết áp 44,3%; 18% bệnh tiểu đường |
6,4% VTE |
|
Klok và cộng sự, 2020; Đoàn hệ hồi cứu; Hà Lan |
184 ICU |
Nadroparin (2.850 IUod * tăng một số lên 5.700 IUbd) |
Tuổi: 64 y; Bệnh kèm theo: béo phì |
31% VTE |
|
Van Haren và cộng sự, 2020; Nhóm thuần tập tiềm năng; Úc, Anh, Argentina, Brazil và Ai Cập |
712 |
UFH khí dung hít vào (và liều chăm sóc tiêu chuẩn 25.000 IU) |
Tuổi: 18 tuổi trở lên không cần thở máy ngay lập tức |
|
|
Van Haren và cộng sự, 2020; Nhóm thuần tập tiềm năng; Úc, Ireland, Mỹ, Tây Ban Nha và Vương quốc Anh |
202 ICU |
UFH khí dung (25.000 IU) |
Tuổi: 18 tuổi trở lên có biểu hiện giảm oxy máu và mờ phổi cấp tính |
|
ATE, arterial thromboembolic events; DVT, deep vein thrombosis; ICU, intensive care unit; MWH, low molecular weight heparin; PE, pulmonary embolism; VTE, venous thromboembolism; UEDVT, upper extremity deep vein thrombosis. *5,700 IUod for patients >100 kg.
Việc sử dụng đường dùng này có thể cung cấp trực tiếp UFH đến vi môi trường phổi, là một cơ chế tiềm năng để làm mềm quá trình tăng đông cục bộ và quá trình viêm nhiễm, ngăn ngừa tác hại toàn thân của việc điều trị bằng thuốc chống đông máu. Các thử nghiệm lâm sàng đang tiến hành và các thử nghiệm chính đang được đề cập ở trên được tóm tắt trong Bảng 1.
Cần nhấn mạnh tầm quan trọng của việc chỉ định LMWH và UFH cho cả dự phòng và điều trị sớm, một khi các thuốc này không có khả năng thúc đẩy quá trình tiêu sợi huyết của huyết khối đã hình thành từ trước trong mô. Nhận thức được thực tế này, sự kết hợp giữa heparin và thuốc tiêu sợi huyết có thể có hiệu quả trong điều trị các trường hợp nặng, một khi tiêu huyết khối cũng mang lại lợi ích lâm sàng chống lại thuyên tắc phổi nặng (40).
Ngoài tác dụng dự kiến của heparin trong việc ngăn ngừa sự hình thành cục máu đông thông qua việc ức chế gián tiếp con đường đông máu, các đặc tính khác do các thuốc này cung cấp có thể là chìa khóa cho dữ liệu tích cực về hiệu quả của chúng so với các thuốc nhắm mục tiêu đơn lẻ. Tình trạng viêm trầm trọng hơn cũng được tìm thấy trong các trường hợp COVID-19 nghiêm trọng, đặc biệt là qua trung gian sản xuất không kiểm soát của các cytokine tiền viêm như interleukin-6 (IL-6), interleukin-8, protein-1 hóa trị đơn bào (MCP-1) , và TNF-α trong hội chứng giải phóng cytokine (41, 42). Nghiên cứu đã nhấn mạnh việc nhắm mục tiêu TNF-α quan trọng như thế nào để có tiên lượng tốt hơn chống lại rối loạn chức năng cytokine do COVID-19 gây ra, một khi sự phong tỏa của nó có thể làm giảm cả dấu ấn sinh học viêm và huyết khối (43). Trong bối cảnh này, các báo cáo đã chỉ ra rằng cả LMWH và UFH đều làm mềm các phản ứng viêm do TNF-α gây ra, chẳng hạn như sản xuất IL-6 và IL-8 thích hợp (28, 44, 45). Hiệu ứng này có thể xảy ra thông qua sự ức chế UFH của yếu tố phiên mã hạt nhân-κB (NF-κB) liên kết với DNA, đây là một quá trình quan trọng đối với một loạt các con đường tín hiệu cytokine (44). Bên cạnh đó, một phần không chống đông máu của enoxaparin được báo cáo là chất ức chế một phần giải phóng IL-6, cho thấy rằng phạm vi tín hiệu được chỉ định cho cytokine này có thể được giảm thiểu khi có LMWH (46). Thật vậy, một tổng quan hồi cứu đã chứng minh rằng điều trị các trường hợp COVID-19 bằng LMWH làm giảm sản xuất quá mức IL-6, do đó là một lựa chọn điều trị quan trọng cần được xem xét, một khi tình trạng viêm và rối loạn đông máu có liên quan chặt chẽ với nhau (37). Các nghiên cứu cũng đã thảo luận rằng những xáo trộn về các tác nhân gây viêm tạo thành dòng bổ thể có thể được điều chỉnh trong thời gian bị bệnh COVID-19 (47, 48). Nó đã được chứng minh rằng hệ thống bổ thể đóng một vai trò trong tổn thương nội mô do SARS-CoV-2 gây ra ở khỉ rhesus (33). Do đó, điều quan trọng cần làm nổi bật là UFH và LMWH cũng liên kết với các protein bổ sung và làm giảm hoạt động của dòng cổ điển, do đó là những tác nhân gây ra các phản ứng chống viêm thông qua con đường này (49, 50).
Các chất trung gian lipid eicosanoid đã được xác định là tác nhân quan trọng trong quá trình viêm đường hô hấp do vi rút gây ra (51), như được quan sát thấy trong bệnh Cúm (52) và nhiễm trùng tiểu phế quản do vi rút hợp bào hô hấp nặng cấp tính (53). Tế bào biểu mô phế quản ở người và bạch cầu thường trú của phổi là nguồn quan trọng của leukotriene B4 (LTB4), một chất trung gian tiền viêm mạnh có liên quan chặt chẽ đến hoạt hóa bạch cầu trung tính (54). Một đánh giá gần đây đã nhấn mạnh mối liên hệ giữa căng thẳng lưới nội chất do SARS-CoV-2 gây ra với sự kích hoạt con đường eicosanoid, có thể làm tăng cơn bão tiền viêm liên quan đến COVID-19 (55). Trong bối cảnh này, các báo cáo trước đây đã chỉ ra rằng heparin có khả năng ức chế tín hiệu LBT4, do đó làm dịu phản ứng viêm được gán cho phân tử này (56). Bên cạnh đó, sự co thắt phế quản do tăng thông khí đã được giảm bớt thông qua việc ức chế sản xuất eicosanoids bởi heparin ở mô hình động vật (57). Xem xét tổn thương đa cơ quan do COVID-19 gây ra thông qua quá trình viêm siêu vi, vô số tác dụng điều hòa miễn dịch của heparin ngoài đặc tính chống đông máu còn cải thiện khả năng chống lại bệnh đại dịch này.
Một cách tiếp cận khác đang được thảo luận rộng rãi là tiềm năng kháng vi-rút do heparin cung cấp. Trước đại dịch COVID-19, hoạt tính kháng vi rút của thuốc hiện tại đã được quan sát thấy trong các mô hình thử nghiệm và vi rút khác nhau, chẳng hạn như vi rút suy giảm miễn dịch ở người (HIV) và vi rút Herpes Simplex (HSV) (58, 59). Tác dụng kháng vi rút này của heparin có thể liên quan đến sự cạnh tranh trực tiếp để liên kết với các thụ thể glycoprotein của tế bào hoặc thông qua việc làm dịu các tác dụng có hại do nhiễm trùng, như đã được chứng minh đối với virus Zika (60). Ngày càng có nhiều bằng chứng cho thấy heparin cũng có tác dụng kháng virus đối với SARS-CoV-2. Một báo cáo đã chỉ ra rằng khả năng xâm nhập tế bào của vi rút có thể bị ảnh hưởng khi có mặt của heparin (61). Trong nghiên cứu này, người ta nhận thấy rằng các dẫn xuất heparan sulfat (HS), như UFH và LMWH, ở nồng độ khả thi cho ứng dụng lâm sàng, gây ra sự thay đổi cấu trúc của protein SARS-CoV-2 Spike, một phân tử trung tâm cho sự xâm nhập tế bào của vật chủ. Một bản in trước khác đã chứng minh rằng UFH cũng có khả năng ảnh hưởng đến sự xâm nhập của SARS-CoV-2 vào tế bào chủ, tác động đến các thông số lây nhiễm của nó (62). Hơn nữa, một phân tích so sánh trong ống nghiệm cho thấy UFH có tiềm năng kháng virus cao hơn đối với SARS-CoV2, cho thấy rằng nó có thể có lợi hơn LMWH (63, 64). Người ta cũng nhận thấy vai trò quan trọng của liên kết HS tế bào với SARS-CoV-2, thúc đẩy sự thay đổi cấu trúc protein S và liên kết với thụ thể ACE-2, cho thấy rằng HS có thể là thụ thể cốt lõi cho sự xâm nhập của virus (65). Trong bối cảnh này, UFH cũng được báo cáo là tác nhân ngăn chặn sự tương tác này giữa phân tử HS tế bào với SARS-CoV-2, củng cố hoạt tính kháng vi-rút của nó.
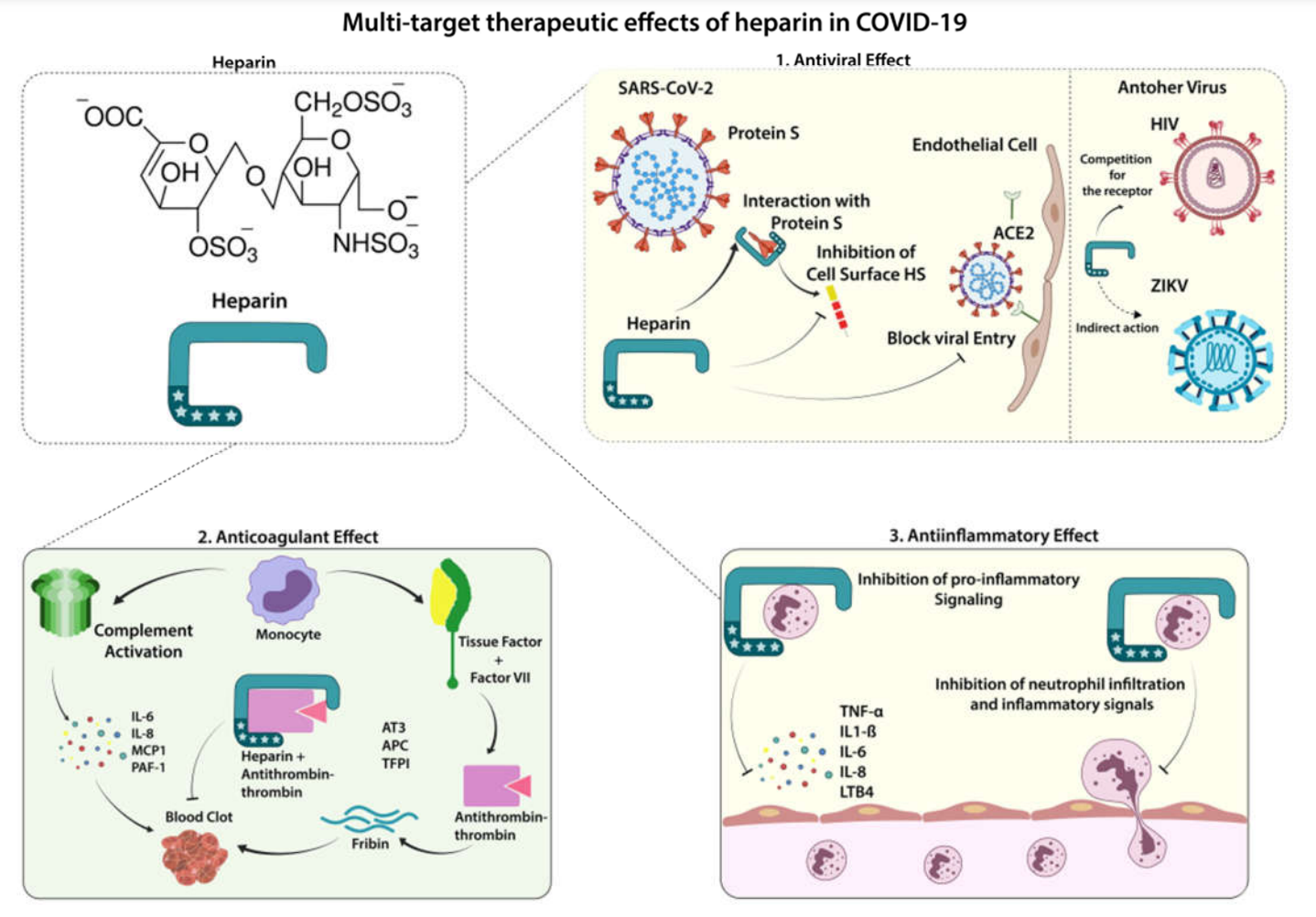
Mặc dù bằng chứng kháng vi-rút của cả LMWH và UFH chống lại SARS-CoV-2 vẫn còn sơ khai, các hoạt động bảo vệ khác chống lại các biến chứng COVID-19 đã rõ ràng. Phương pháp trị liệu lý tưởng để điều trị những căn bệnh phức tạp như vậy cũng là sử dụng một phân tử đa đích có khả năng phục hồi các con đường khác nhau bị ảnh hưởng bởi SARS-CoV-2. Tác dụng chống đông máu, chống viêm và kháng vi-rút do heparin cung cấp làm tăng quan điểm của việc sử dụng các loại thuốc này để tạo ra tiên lượng tốt hơn cho những người bị ảnh hưởng bởi COVID-19 (Hình 1). Xem xét các phát hiện rằng tác dụng kháng vi rút của UFH có thể mạnh hơn LMWH, liều lượng lựa chọn phải được quyết định cẩn thận, một khi UFH có nguy cơ chảy máu cao hơn LMWH. Để tránh nguy cơ gia tăng, liều lượng phù hợp nhất cho cả UFH và LMWH là chế độ chăm sóc tiêu chuẩn, có thể được điều chỉnh theo chỉ số khối cơ thể (BMI) và chức năng thận (66). Bên cạnh đó, các yếu tố nguy cơ gây chảy máu phải được xem xét trước khi kê đơn thuốc chống đông máu làm thuốc dự phòng. Hơn nữa, UFH khí dung là một khả năng tuyệt vời để cải thiện hiệu suất của thuốc hiện tại bằng cách hướng tác dụng đến vị trí cần thiết nhất và giảm nguy cơ tác động không mong muốn lên đường đông máu toàn thân.
Corticosteroid dexamethasone
Dựa trên dữ liệu lâm sàng hiện có, khoảng 20% bệnh nhân nhiễm SARS-CoV-2 phát triển Hội chứng suy hô hấp cấp (ARDS), đặc trưng bởi các thay đổi bệnh lý phổi như tăng không gian chết và giảm oxy (67–69). Sự giải phóng ồ ạt các cytokine tiền viêm và chemokine (5), rối loạn đông máu và huyết khối vi mạch (5, 10), hình thành màng hyalin (68, 70), và bẫy ngoại bào bạch cầu trung tính DNA nội mạch (NETs) (71) hiện được mô tả là những yếu tố góp phần gây ra tổn thương phế nang lan tỏa thường được hiển thị trong ARDS liên quan đến COVID-19.
Hình 1 Tác dụng điều trị của Heparin trong COVID-19. Nhiễm trùng phổi do SARS-CoV-2 có thể kích hoạt quá trình viêm toàn thân, quá trình này cũng liên quan đến sự gia tăng các yếu tố gây đông máu được tìm thấy trong các trường hợp nghiêm trọng của COVID-19. Heparin trọng lượng phân tử thấp (LMWH) cho thấy tác dụng theo 3 cách chính: 1. Tác dụng kháng virus: sự xâm nhập của SARS-CoV-2 trong tế bào nội mô và biểu mô phụ thuộc vào sự tương tác của nó với bề mặt tế bào heparan sulfat; do đó, sự gắn kết của heparin với protein đột biến của virus có thể ức chế sự tương tác này, làm giảm sự xâm nhập của tế bào virus. Heparin đã cho thấy tác dụng kháng vi-rút của nó đối với các vi-rút khác như HIV (cạnh tranh cho thụ thể) và ZIKV (tác động gián tiếp, loại bỏ tác dụng gây độc tế bào do vi-rút gây ra). 2. Tác dụng chống đông máu: sự hình thành cục máu đông không kiểm soát được có thể được kiểm soát bởi chức năng chống đông máu vốn có của heparin, qua trung gian tương tác của heparin và glycoprotein chống thrombin-3 (AT3), tăng cường sự bất hoạt AT3 của thrombin, một yếu tố cần thiết cho hình thành huyết khối. 3. Tác dụng chống viêm: heparin có tác dụng chống viêm được biết đến rộng rãi, chủ yếu hủy bỏ các chất trung gian gây viêm, chẳng hạn như TNF-α, IL-6, và LTB4, làm giảm sự di chuyển và kích hoạt các tế bào miễn dịch, ngăn ngừa phản ứng viêm toàn thân. ACE2, Angiotensin-converting enzyme 2; APC, activated protein C; AT3, Antithrombin-III; CK, creatine kinase; CRP, C-reactive protein; ESR, erythrocyte sedimentation rate; HS, heparan sulfate; IL, interleukin; LDH, lactate dehydrogenase; PAI-1, Plasminogen activator inhibitor 1, TF, Tissue factor, TFPI, Tissue factor pathway inhibitor; TNF, Tumor necrosis factor; VII, Factor VII.
Biểu hiện nhất quán ở bệnh nhân ARDS, sự hình thành màng hyalin ở phổi làm cản trở sự trao đổi khí, hạn chế hoạt động bề mặt, gây xơ hóa phổi và gây ra huyết khối vi mạch phổi (72, 73). Các yếu tố khác đối phó với sự hình thành huyết khối và tình trạng viêm khi khởi phát ARDS là bẫy ngoại bào bạch cầu trung tính DNA nội mạch (NET) và NETosis (71, 74). Ngoài bạch cầu trung tính, các yếu tố nguy cơ liên quan đến việc hình thành ARDS ở bệnh nhân COVID-19 là tuổi lớn hơn, rối loạn chức năng cơ quan và rối loạn đông máu (75). Việc quản lý cơn bão cytokine và chemokine trong COVID-19 đại diện cho một điểm quan trọng và gây tranh cãi (76), xem xét rằng việc sử dụng các loại thuốc chống viêm toàn thân có thể ức chế tổn thương mô hoặc hạn chế miễn dịch qua trung gian tế bào (77, 78) .
Glucocorticoids (GCs) là hormone steroid có nguồn gốc từ quá trình chuyển hóa cholesterol. Cả hai dạng GC nội sinh và tổng hợp đều có chung một cấu trúc hóa học ưa béo cho phép phân tử này thực hiện một loạt các tác động nội tiết trong cơ thể sinh vật (79). Hiện tại, các GC tổng hợp, chẳng hạn như dexamethasone, đã bị thay đổi để cải thiện đáng kể tính đặc hiệu, sinh khả dụng và hiệu lực, dẫn đến hiệu quả cao hơn so với con đường tín hiệu nội sinh (80). Tiềm năng ức chế miễn dịch được biết đến của dexamethasone đã làm cho phân tử chống viêm này trở thành liệu pháp hàng đầu cho một số bệnh viêm nhiễm, chẳng hạn như rối loạn tự miễn dịch và nhiễm trùng đường hô hấp (81).
Cơ chế hoạt động của dexamethasone được đặc trưng bởi sự gắn kết độc quyền với thụ thể GC tế bào cổ điển (cGCR), cung cấp phần lớn các tác dụng chống viêm (82). Thuốc có thể làm giảm quá trình viêm bằng cách kiểm soát phiên mã của nhiều gen gây viêm mã hóa cytokine, các phân tử kết dính tế bào và các thụ thể liên quan đến viêm (83). Dexamethasone có liên quan đến việc giảm tính thấm của mao mạch, ngoài ra còn làm giảm sự di chuyển của bạch cầu trung tính và tế bào lympho vào các vị trí viêm (84–86). Một ưu điểm quan trọng của thuốc hiện tại là thời gian bán hủy kéo dài trong cơ thể, có thể làm giảm thời gian điều trị so với các GC thay thế (74). Liều lựa chọn dựa trên hiệu quả mong muốn, một khi liều thấp có liên quan đến điều biến chống viêm và liều cao hơn có liên quan đến hoạt động ức chế miễn dịch (87).
Như đã thảo luận trước đây, GC nội sinh là trung tâm của cân bằng nội môi chuyển hóa và các hiện tượng viêm hệ thống trong quá trình sửa chữa mô và loại bỏ mầm bệnh (88). Do thực tế này, việc hấp thụ GC tổng hợp ngoại sinh trong thời gian dài có thể gây ra các tác dụng phụ, chẳng hạn như cực kỳ ngừng phản ứng viêm, dẫn đến khả năng bị nhiễm trùng thứ phát cao hơn (87, 89). Bên cạnh đó, GC đóng một vai trò trong quá trình chuyển hóa glucose thông qua sự thay đổi tín hiệu insulin, dẫn đến giảm hấp thu và tăng nồng độ glucose plasmatic (90). Sự can thiệp vào quá trình trao đổi chất này làm phát sinh tình trạng kháng insulin (IR) do dùng thuốc GCs tổng hợp quá mức hoặc kéo dài, có thể tiến triển thành bệnh tiểu đường loại 2 (T2D) và các rối loạn chuyển hóa khác (91, 92). Vì lý do này, thuốc GCs tổng hợp cần được xử lý cẩn thận, tránh các biến chứng hơn là tác dụng điều trị.
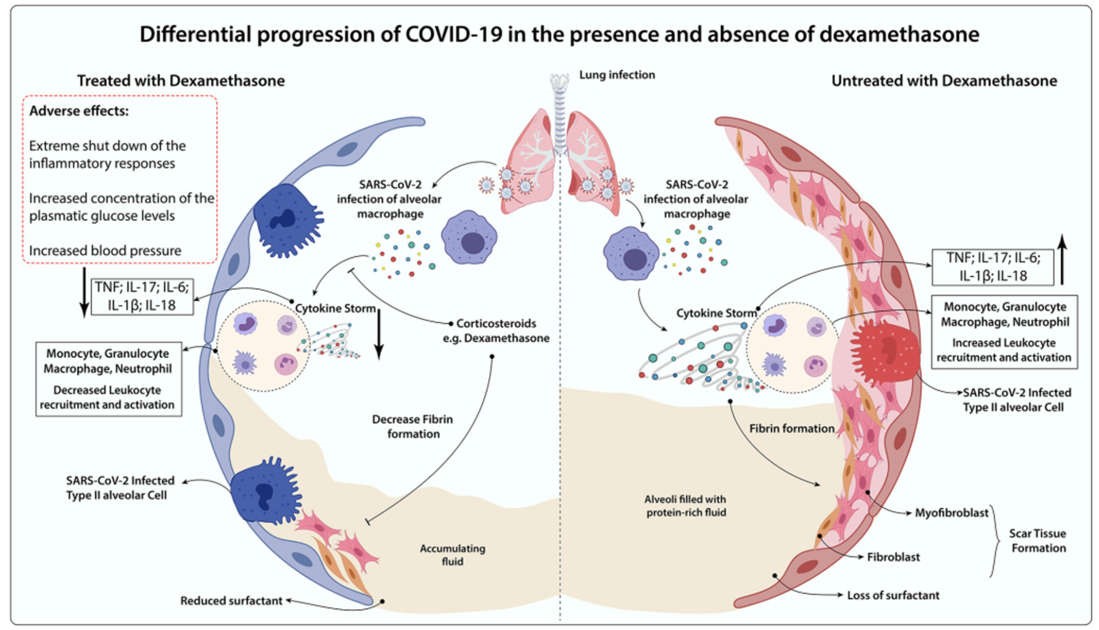
Lúc đầu, không rõ liệu những bệnh nhân được chẩn đoán mắc COVID-19 có thể tận dụng lợi thế của việc sử dụng dexamethasone hay không, đặc biệt là khi lưu ý đến các điểm nêu trên (93). Các báo cáo đã chỉ ra rằng thuốc dexamethasone chống lại bệnh viêm phổi do cúm, SARS-CoV-1 và coronavirus hội chứng hô hấp Trung Đông (MERS-CoV) gây ra những tác hại có thể ảnh hưởng tiêu cực đến tiên lượng bệnh (94-97). Tuy nhiên, đặc biệt ở những bệnh nhân phát triển ARDS trong thời gian dùng COVID-19, điều trị bằng dexamethasone cho thấy có hiệu quả trong việc điều chỉnh giảm viêm toàn thân và phổi, phục hồi cân bằng nội môi mô bằng cách tăng tốc độ phân giải tổn thương phế nang lan tỏa, dẫn đến bảo vệ chống lại rối loạn chức năng cơ quan ngoài phổi (98, 99). Bên cạnh đó, các nghiên cứu thực nghiệm và lâm sàng đã chứng minh rằng sự biểu hiện GR-α trong tế bào tủy của dịch rửa phế quản phế nang có liên quan đến việc bảo vệ đáng kể chống lại các triệu chứng COVID-19 nghiêm trọng, đặc biệt là thông qua việc giảm NETosis và viêm bạch cầu trung tính ở phổi (100). Lưu ý, khi phổi đã bị tổn thương, tỷ lệ tử vong trong trường hợp COVID-19 là cao (101). Nếu dexamethasone có thể làm giảm bớt tiến triển lâm sàng ở giai đoạn này, thì liệu pháp có thể làm giảm các trường hợp bệnh nặng và do đó giảm tỷ lệ tử vong trong trường hợp của COVID-19 (102). Một kịch bản so sánh về sự tiến triển của COVID-19 khi có và không có dexamethasone đã được tóm tắt (Hình 2).
Hình 2 Sự tiến triển khác biệt của COVID-19 khi có và không có dexamethasone. Trong trường hợp không có phương pháp điều trị chống viêm, rối loạn chức năng phổi do COVID-19 gây ra sẽ được kích hoạt bởi sự tăng cường hoạt động của các đại thực bào phế nang bị nhiễm SARS-CoV-2 và các tế bào miễn dịch (Bạch cầu đơn nhân, Bạch cầu hạt, Đại thực bào, Bạch cầu trung tính) đến môi trường xung quanh phổi, điều này dẫn đến sự bài tiết ồ ạt của các chất trung gian gây viêm (TNF, IL-17, IL-6, IL-1b, IL-18) trong quá trình giải phóng cơn bão cytokine. Quá trình viêm kéo dài làm tăng sự xâm nhập của nguyên bào sợi và nguyên bào sợi trong suốt quá trình hình thành mô sẹo, làm mất chất hoạt động bề mặt phổi tự nhiên và tăng dịch phế nang. Dùng dexamethasone có thể có lợi thông qua việc làm giảm sự xuất hiện của bão cytokine và sự thâm nhập vào phổi của bạch cầu, làm giảm xơ hóa mô và tích tụ dịch phế nang. Tuy nhiên, glucocorticoid này có liên quan đến ức chế miễn dịch, tăng huyết áp và đường huyết là những tác dụng phụ chính. Do đó, nó có thể gây bất lợi cho một số nhóm, bao gồm các trường hợp COVID-19 không nghiêm trọng, bệnh nhân tiểu đường và các đối tượng tăng huyết áp.
Đối mặt với kịch bản phức tạp của những bệnh nhân bị bệnh nặng với COVID-19, các phác đồ đa dạng sử dụng các phương pháp điều trị bổ sung (94) đã được phát triển, một số trong số họ sử dụng GC để điều trị bệnh nhân nhập viện với COVID-19 (103). Các thành viên của WHO và Hiệp hội Lồng ngực Trung Quốc có ý kiến trái ngược nhau về việc sử dụng corticosteroid trong COVID-19 (104). Theo hướng dẫn của WHO, dexamethasone chỉ nên được sử dụng trong điều kiện thử nghiệm lâm sàng (105). Russell và các đồng nghiệp kết luận rằng không có lý do gì để mong đợi rằng những người bị COVID19 sẽ được lợi khi điều trị bằng corticosteroid, dựa trên việc tăng tỷ lệ tử vong và nguy cơ nhiễm trùng thứ phát trong bệnh cúm, suy giảm khả năng thanh thải SARS-CoV và MERS-CoV (93). Tuy nhiên, tiềm năng cao của dexamethasone trong việc giảm thiểu cơn bão cytokine đã mang lại các đề xuất để khắc phục tình trạng suy giảm khả năng thanh thải của virus và tăng nguy cơ phát triển các bệnh nhiễm trùng thứ phát, và các thử nghiệm lâm sàng chính đang tiến hành được tóm tắt trong Bảng 2.
Bảng 2 Các nghiên cứu về dexamethasone đối với COVID-19.
|
Tác giả, năm, nghiên cứu thiết kế, quốc gia |
Số bệnh nhân |
Điều trị |
Đặc điểm bệnh nhân |
Kết quả |
|
Selvaraj và cộng sự, Chuỗi trường hợp; Hoa Kỳ |
23 |
Dexamethasone: 4 mg |
Tuổi: 60 tuổi; Bệnh đi kèm: tăng huyết áp 38,09%; 61,9% tiểu đường; BMI: 28,68 kg / m2 |
CS ngăn chặn sự tiến triển của suy hô hấp do thiếu oxy ở những bệnh nhân bị bệnh từ trung bình đến nặng |
|
Nhóm phục hồi 2020; Đa tâm; Thử nghiệm nhãn mở có kiểm soát; Vương quốc Anh |
6,425 |
Dexamethasone (6 mg 1 lần/ngày – 10 ngày) |
Tuổi: 66,1 tuổi; Bệnh đi kèm: 24% đái tháo đường; 27% CĐV; 21% phổi mãn tính 56% mắc bệnh đồng thời |
Trong nhóm dexamethasone, tỷ lệ tử vong thấp hơn ở nhóm chăm sóc thông thường ở bệnh nhân được IMV |
|
Tomazini và cộng sự, 2020; Thử nghiệm lâm sàng đa tâm, ngẫu nhiên, nhãn mở, thử nghiệm lâm sàng; Brazil |
299 |
Dexamethasone (10 mg – 5 ngày) |
Tuổi: 61 tuổi: Bệnh đi kèm: 60,3% tăng huyết áp; 37,8% tiểu đường; 30,5% béo phì |
Việc sử dụng dịch vụ chăm sóc tiêu chuẩn so với chỉ chăm sóc tiêu chuẩn đã làm tăng đáng kể số ngày không có máy thở trong hơn 28 ngày. |
AKI, acute kidney injury; ARDS, acute respiratory distress syndrome; CDV, cardiovascular diseases; CS, corticosteroids; ICU, intensive care unit; IMV, invasive mechanic ventilation; MTP, methylprednisolone; NIV, non-invasive ventilation; Pts, patients; UK, United Kingdom; USA, United States America; y, years.
Kết quả sơ bộ của một thử nghiệm nhãn mở, ngẫu nhiên, có đối chứng, được tiến hành ở Vương quốc Anh ủng hộ việc sử dụng dexamethasone. Trong thử nghiệm này, nhánh Dexamethasone bao gồm 2.104 bệnh nhân nhận 6 mg dexamethasone (uống hoặc tiêm tĩnh mạch) một lần mỗi ngày trong tối đa 10 ngày và 4.321 bệnh nhân được chăm sóc tiêu chuẩn. Dexamethasone làm giảm 35% tỷ lệ tử vong ở bệnh nhân thở máy xâm nhập. Bên cạnh đó, phân tích tổng hợp tiềm năng từ Nhóm công tác Đánh giá bằng chứng nhanh của WHO cho Liệu pháp COVID-19 (REACT) đã khuyến nghị việc sử dụng độc lập corticosteroid ở bệnh nhân COVID-19. Một mối tương quan quan trọng giữa việc sử dụng GC toàn thân và giảm tỷ lệ tử vong đã được tìm thấy ở những bệnh nhân bị bệnh nặng với COVID-19 (106). Selvaraj và cộng sự. báo cáo rằng việc sử dụng dexamethasone trong thời gian ngắn của bệnh nhân nhập viện với COVID-19 được dung nạp tốt và làm tăng tiên lượng của bệnh nhân (107).
Mặc dù dexamethasone hứa hẹn hiệu quả đối với COVID-19 nghiêm trọng, vẫn có những lo ngại về việc kê đơn thuốc chống viêm này cho các trường hợp bừa bãi. Cho đến nay, các dữ liệu có sẵn cho thấy vai trò có lợi của việc điều trị bằng dexamethasone trên bệnh nhân nhập viện, đặc biệt là đối với những người được điều trị bằng oxy tích cực (108, 109). Một lời giải thích khả thi có thể dựa trên mối liên hệ giữa quá phát viêm và sự phát triển của tổn thương phổi, làm tăng tính cấp thiết cho ICU. Tình trạng viêm quá mức cần được xử lý bằng cách điều trị kháng viêm mạnh, có thể tiếp cận bằng liệu pháp dexamethasone. Trong trường hợp không xảy ra quá trình viêm không cân bằng như trong giai đoạn đầu của bệnh, điều trị bằng dexamethasone có thể làm rối loạn sự phát triển miễn dịch tự nhiên của vật chủ và làm giảm phản ứng chống vi rút, điều này có thể dẫn đến chậm thanh thải vi rút.
Bên cạnh sự suy giảm khả năng thanh thải virus đã được thảo luận trước đây khi áp dụng trong giai đoạn đầu của bệnh (95), nguy cơ nhiễm trùng thứ cấp ngày càng tăng liên quan đến liều cao GC toàn thân đã được nhận thấy (87, 89). Một báo cáo liên quan đến bệnh siêu nhiễm giun lươn, một bệnh do tuyến trùng bị bỏ quên, đã đưa ra mối quan tâm hiện nay về việc sử dụng dexamethasone mà không sử dụng đồng thời vermifuge (110).
Bên cạnh đó, việc điều chỉnh chuyển hóa glucose của GCs dẫn đến việc chăm sóc tích cực cho bệnh nhân đái tháo đường trong quá trình điều trị (92). Như đã thảo luận trên toàn thế giới, bệnh tiểu đường là một yếu tố nguy cơ chính đối với điều trị COVID-19 nghiêm trọng và dexamethasone ở những người này có thể liên quan đến sự phát triển của tình trạng tăng đường huyết (111–113). Nồng độ glucose trong máu tăng lên có thể liên quan đến tiên lượng xấu của bệnh, xem xét phát hiện gần đây về sự phụ thuộc của SARS-CoV-2 của glucose đối với sự nhân lên của virus trong ống nghiệm (114). Khi tăng nồng độ glucose, tải lượng vi rút tăng đồng thời, có lợi cho nhiễm trùng và mức độ nghiêm trọng của bệnh (114). Bên cạnh đó, bệnh nhân tăng huyết áp, những người cũng có nguy cơ bị COVID19 mức độ nghiêm trọng, nên được theo dõi liên tục trong khi điều trị bằng dexamethasone, một khi thường xuyên quan sát thấy tăng huyết áp do GCs (115). Liều dexamethasone cao có liên quan đến việc tăng giữ natri, dẫn đến tăng huyết áp, ngoài ra còn làm thay đổi cân bằng nội môi dây thần kinh ngoại vi (87, 116, 117). Hiệu ứng này có thể dẫn đến các biến chứng hơn là điều trị bằng COVID-19, làm tăng nguy cơ tử vong liên quan của những người bị ảnh hưởng.
Kết luận
Các trường hợp nghiêm trọng của COVID-19 được đánh dấu bằng tình trạng viêm dữ dội và sự hiện diện của các biến cố huyết khối. Tình trạng viêm trầm trọng hơn làm trung gian cho cơn bão cytokine đặc trưng được quan sát thấy trong COVID-19 nghiêm trọng, và các cục máu đông trong phổi có thể làm ảnh hưởng đến quá trình oxy hóa, dẫn đến kết quả lâm sàng của nhiễm SARS-CoV-2 trở nên tồi tệ hơn. Một số báo cáo gần đây đã chứng minh tác dụng có lợi của việc sử dụng heparin / heparin trọng lượng phân tử thấp và corticosteroid, chẳng hạn như dexamethasone, đối với tỷ lệ tử vong ở COVID-19.
Tác dụng thuận lợi và thành công của việc điều trị cơ bản bằng heparin đối với bệnh nhân COVID-19 có thể được giải thích không chỉ bởi đặc tính chống đông máu của nó mà còn do cơ chế không chống đông máu của nó, bao gồm các hoạt động chống vi rút và chống viêm như (I) giảm Sự xâm nhập tế bào chủ của SARS-CoV-2, (II) ức chế cytokine và chemokine gây viêm, (III) ức chế tính thấm thành mạch và sự di chuyển của bạch cầu.
Bất chấp vai trò gây tranh cãi của corticosteroid trong điều trị các bệnh truyền nhiễm nặng, một số nghiên cứu lâm sàng đã cung cấp ngày càng nhiều bằng chứng cho thấy dexamethasone có thể hoạt động rộng rãi như một phương pháp điều trị sẵn có cho những bệnh nhân bị bệnh nặng nhất với COVID-19. Tuy nhiên, nhiều câu hỏi quan trọng về mặt lâm sàng vẫn còn bỏ ngỏ và việc xác định thời gian bắt đầu điều trị tối ưu, liều lượng và thời gian điều trị dexamethasone có thể được xem xét để tránh các tác dụng phụ nghiêm trọng trong quá trình quản lý COVID-19.
Trong khi UFH hoặc LMWH được chỉ định làm thuốc dự phòng cho giai đoạn đầu của bệnh, có thể làm giảm sự hình thành cục máu đông bên cạnh việc loại bỏ sự xâm nhập của tế bào vi rút, dexamethasone chỉ được kê đơn cho những trường hợp nặng, khi bệnh đạt đến trạng thái viêm nặng.
Có tính đến điều này, chúng tôi gợi ý rằng tác động đa mục tiêu của heparin như một loại thuốc chống vi rút, chống huyết khối và chống viêm trong giai đoạn đầu của COVID-19 có thể làm giảm đáng kể nhu cầu điều trị dexamethasone trong giai đoạn đầu của bệnh này. Nếu điều trị tiêu chuẩn của heparin không bảo vệ được khỏi bệnh nặng, dexamethasone phải được áp dụng như một chất chống viêm mạnh để ngăn chặn tình trạng viêm không kiểm soát và trầm trọng hơn.
Nhìn chung, sự kết hợp giữa heparin chống đông máu và corticosteroid dexamethasone có thể là một công cụ điều trị rất hiệu quả và đầy hứa hẹn trong việc tránh các biến chứng COVID-19 khi sử dụng cho bệnh nhân bị bệnh nặng.